AI驱动的深度视觉蛋白组学揭示胰腺癌前驱病变的关键分子转变
胰腺导管腺癌(PDAC)是预后极差的恶性肿瘤之一,五年生存率不足10%,主要归因于晚期发现、治疗耐药和快速转移。经典进展模型显示,PDAC从组织学正常的导管上皮逐步演变为胰腺上皮内瘤变(PanIN),最终发展为浸润性癌,驱动因素包括KRAS基因的顺序激活以及CDKN2A、TP53和SMAD4的失活。然而,前驱病变阶段的蛋白水平分子变化仍不清晰。
2026年4月21日,纽约大学医学院和Resolute Bio研究团队合作在Cancer Discovery(IF:33.3)发表题为《AI-powered Deep Visual Proteomics reveals critical molecular transitions in pancreatic cancer precursors》的研究,通过整合计算病理学、激光显微切割和质谱分析技术,系统描绘了从正常导管、腺泡-导管化生(ADM)、低级别和高级别胰腺上皮内瘤变(PanIN)到浸润性癌的蛋白组学图谱。研究揭示了癌症相关”场效应”的存在,并识别出四个与病变进展相关的分子模式,为胰腺癌的早期检测和干预提供了新的候选靶点。

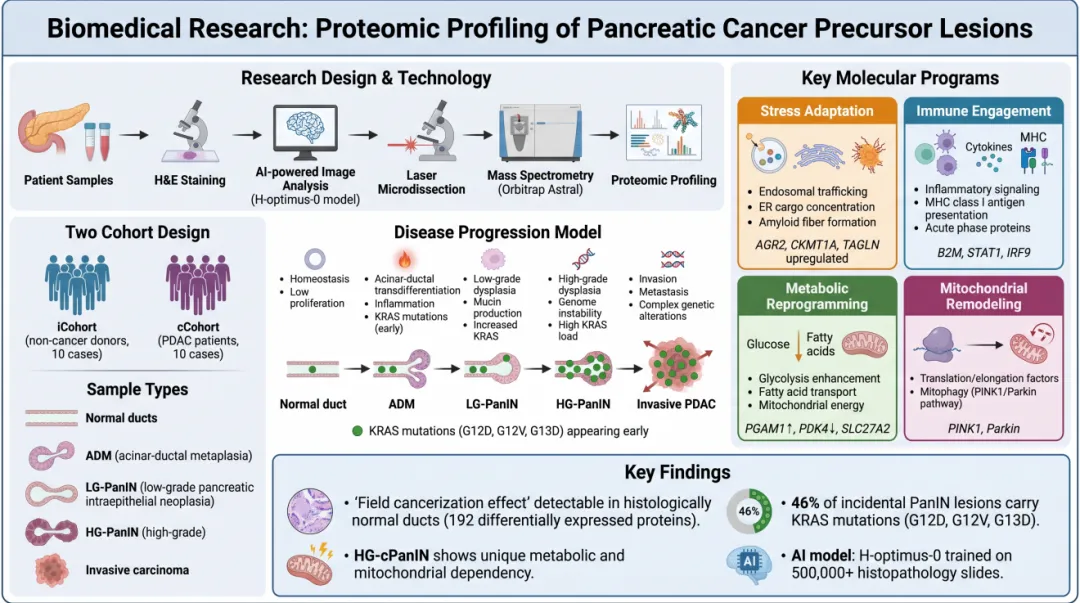 队列设计与技术方法
本研究采用深度视觉蛋白组学(DVP)技术平台,整合了多项前沿技术。
在样本层面,研究纳入20例个体(10例无癌器官捐献者和10例PDAC患者)的115个离散组织区域。获得的样本类型涵盖正常导管、ADM病变、低级别PanIN(LG-PanIN)、高级别PanIN(HG-PanIN)和浸润性癌组织。所有病变均经资深胰腺病理学家复核确认。
在技术层面,首先对福尔马林固定石蜡包埋(FFPE)组织进行苏木精-伊红(H&E)染色和高分辨率成像。随后采用H-optimus-0病理学基础模型(基于超过50万张组织病理学切片训练)进行AI驱动的表型聚类分析,精确区分形态学相似但生物学意义不同的组织区域。在病理学家引导下,使用Leica LMD7激光显微切割系统对包含了约100个表型匹配细胞的区域进行蛋白质组学分析。质谱检测采用Orbitrap Astral质谱仪,最终量化了9,181种蛋白质和117,178种独特肽段。
研究结果
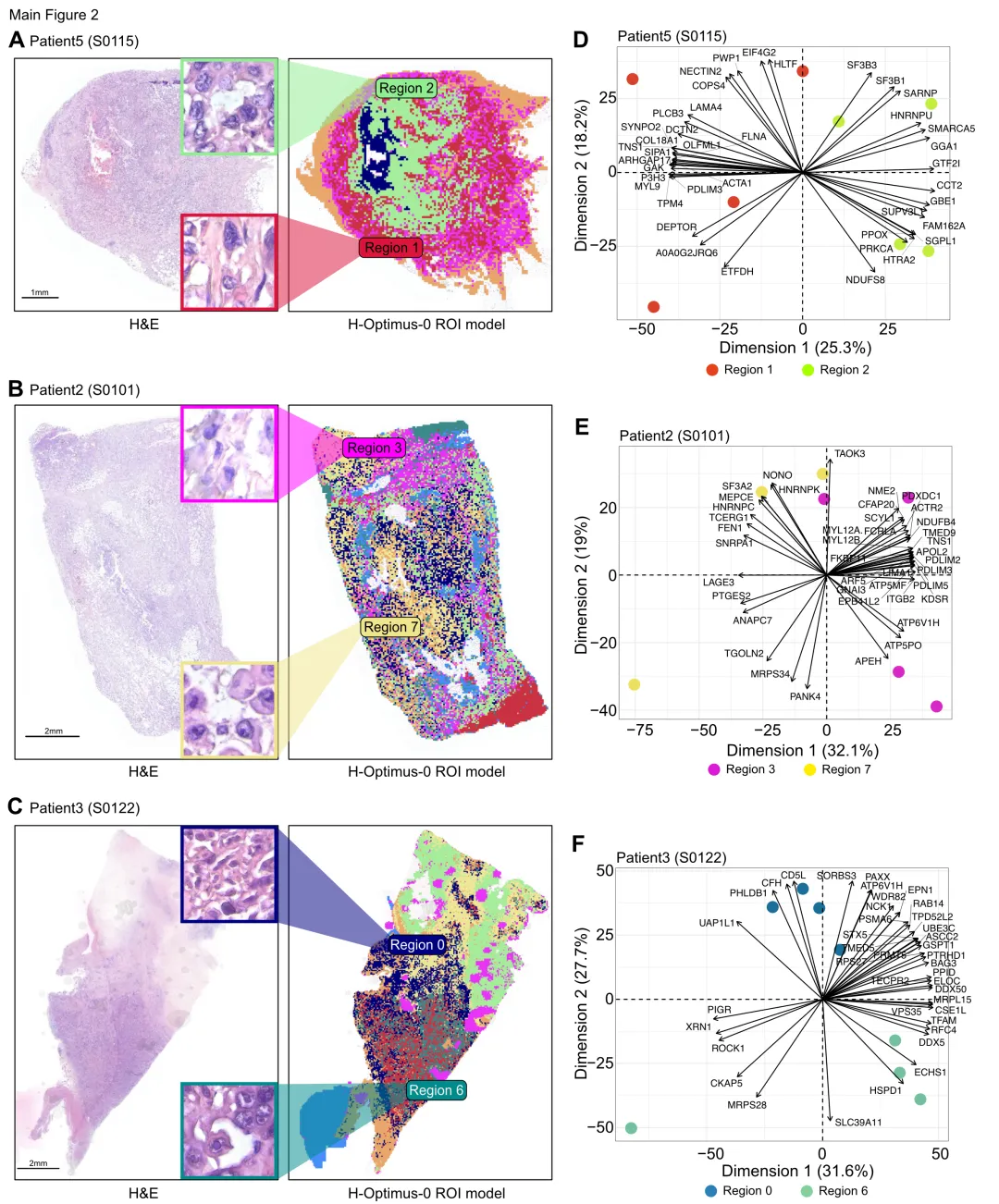
为解析PDAC肿瘤内异质性,对3例PDAC患者的肿瘤及其匹配LG-cPanIN病变区域进行蛋白质组学采样分析。主成分分析显示,同一患者不同区域间存在显著的分子差异,且差异不仅限于胞外基质蛋白,还延伸至细胞内应激、RNA调控和线粒体程序。
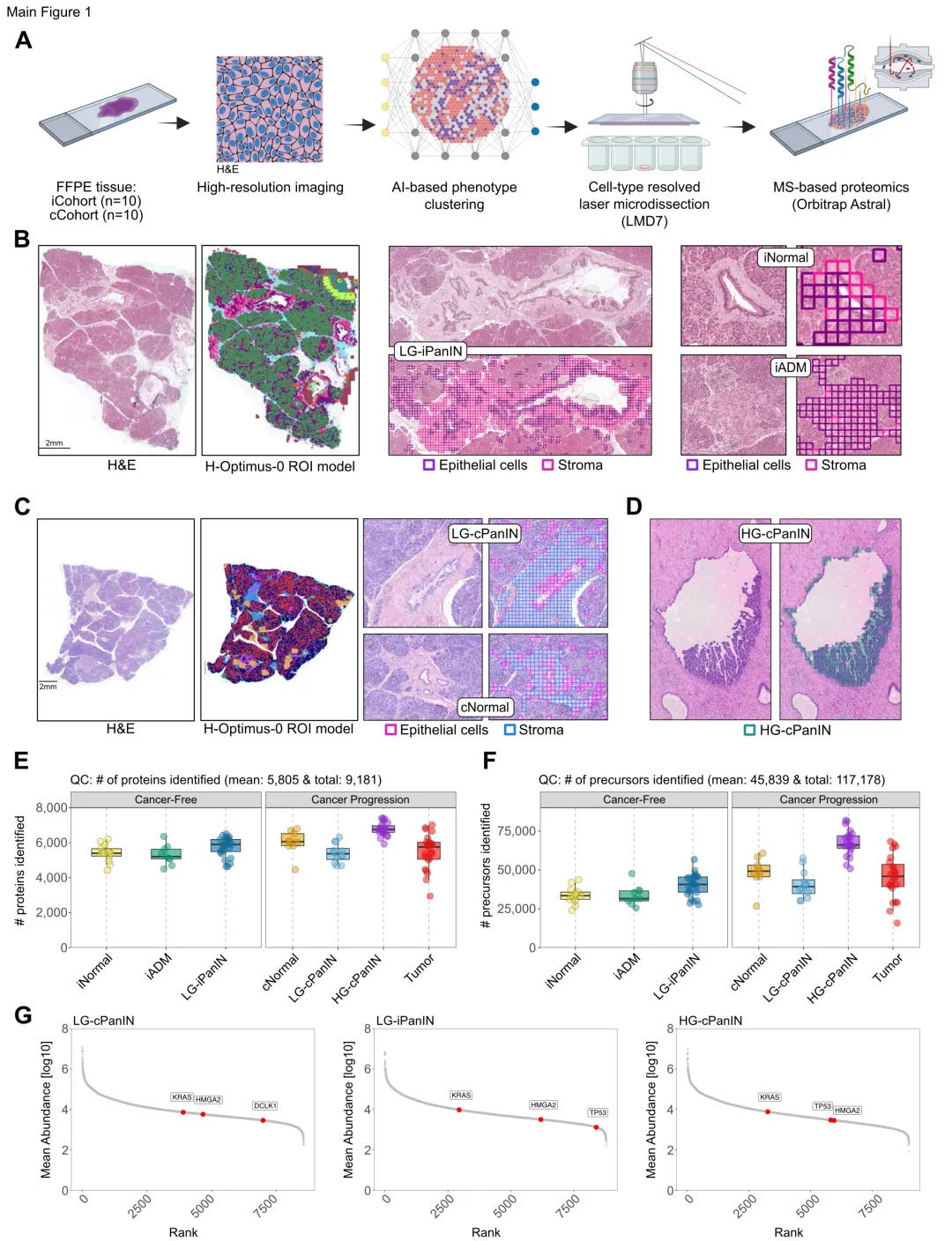
队列设计与技术方法
本研究采用深度视觉蛋白组学(DVP)技术平台,整合了多项前沿技术。
在样本层面,研究纳入20例个体(10例无癌器官捐献者和10例PDAC患者)的115个离散组织区域。获得的样本类型涵盖正常导管、ADM病变、低级别PanIN(LG-PanIN)、高级别PanIN(HG-PanIN)和浸润性癌组织。所有病变均经资深胰腺病理学家复核确认。
在技术层面,首先对福尔马林固定石蜡包埋(FFPE)组织进行苏木精-伊红(H&E)染色和高分辨率成像。随后采用H-optimus-0病理学基础模型(基于超过50万张组织病理学切片训练)进行AI驱动的表型聚类分析,精确区分形态学相似但生物学意义不同的组织区域。在病理学家引导下,使用Leica LMD7激光显微切割系统对包含了约100个表型匹配细胞的区域进行蛋白质组学分析。质谱检测采用Orbitrap Astral质谱仪,最终量化了9,181种蛋白质和117,178种独特肽段。
研究结果
为解析PDAC肿瘤内异质性,对3例PDAC患者的肿瘤及其匹配LG-cPanIN病变区域进行蛋白质组学采样分析。主成分分析显示,同一患者不同区域间存在显著的分子差异,且差异不仅限于胞外基质蛋白,还延伸至细胞内应激、RNA调控和线粒体程序。
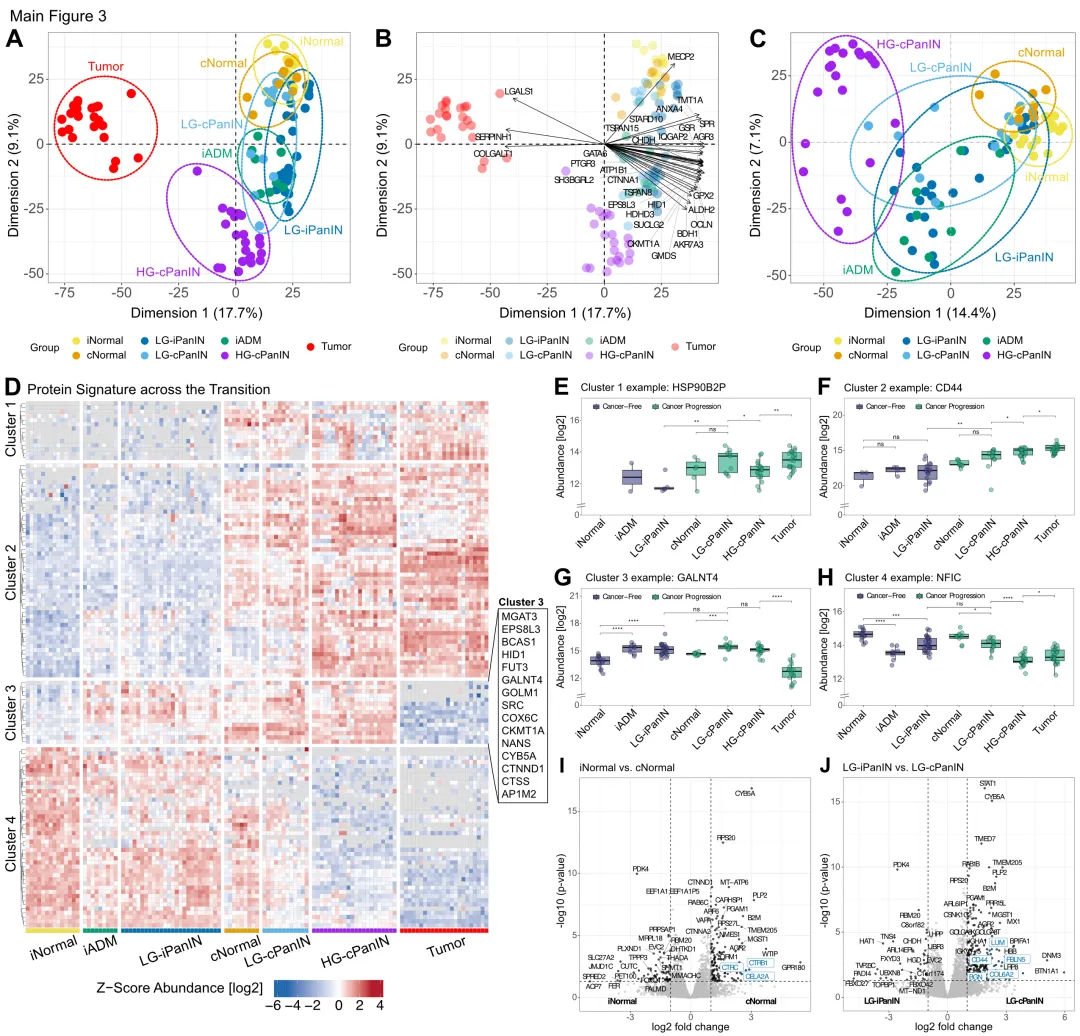
 对所有区域数据的PCA分析揭示了肿瘤蛋白质组与正常导管、ADM及PanIN的明显分离。值得注意的是,HG-cPanIN占据介于LG-cPanIN和肿瘤之间的独特位置,提示高级别病变是不同于肿瘤的分子状态,而非简单的”导管癌化”。
关键发现之一是,尽管组织学表现完全正常,形态学正常的胰腺导管上皮细胞,在癌症患者(cNormal)与无癌个体(iNormal)之间存在192 个蛋白质组差异,提示”场癌化”效应的存在:即使在组织学正常的组织中,癌症相关微环境也已诱导了可检测的分子改变。
对所有区域数据的PCA分析揭示了肿瘤蛋白质组与正常导管、ADM及PanIN的明显分离。值得注意的是,HG-cPanIN占据介于LG-cPanIN和肿瘤之间的独特位置,提示高级别病变是不同于肿瘤的分子状态,而非简单的”导管癌化”。
关键发现之一是,尽管组织学表现完全正常,形态学正常的胰腺导管上皮细胞,在癌症患者(cNormal)与无癌个体(iNormal)之间存在192 个蛋白质组差异,提示”场癌化”效应的存在:即使在组织学正常的组织中,癌症相关微环境也已诱导了可检测的分子改变。
 03. 高级别cPanIN呈现独特的代谢和线粒体依赖特征
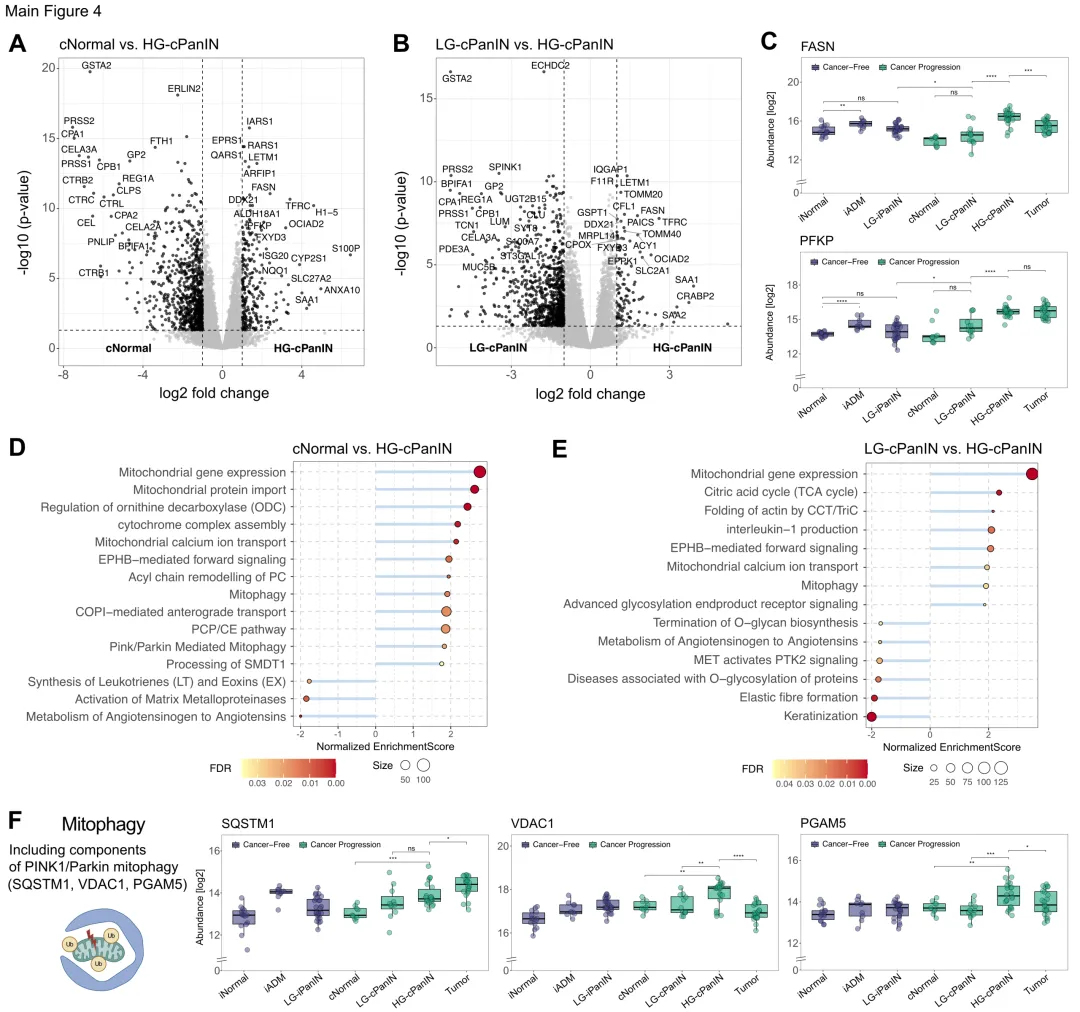
HG-cPanIN代表了介于癌前与浸润性癌之间的关键过渡状态。与cNormal相比,HG-cPanIN显示1,075个差异蛋白;与LG-cPanIN相比,则有951个差异蛋白。
代谢重编程主导了HG-cPanIN的蛋白质组学特征。脂肪酸合成酶(FASN)和磷酸果糖激酶(PFKP)在HG-cPanIN中显著上调,说明糖酵解活性增强。转铁蛋白受体(TFRC)升高进一步提示营养获取需求的增加。通路富集分析发现,线粒体基因表达和翻译模块的异常强烈激活,包括线粒体翻译起始/延伸/终止和呼吸链电子传递。PINK1/Parkin线粒体自噬通路组分(如SQSTM1/p62、VDAC1、PGAM5)在HG-cPanIN阶段显著升高。这些结果表明,HG-cPanIN依赖线粒体功能维持其异常增殖状态,可能是一个可干预的潜在靶点。
04. 四个阶段相关的分子程序贯穿胰腺癌变全过程
研究定义了四个与癌症“场效应”和PDAC进展相关的分子变化:
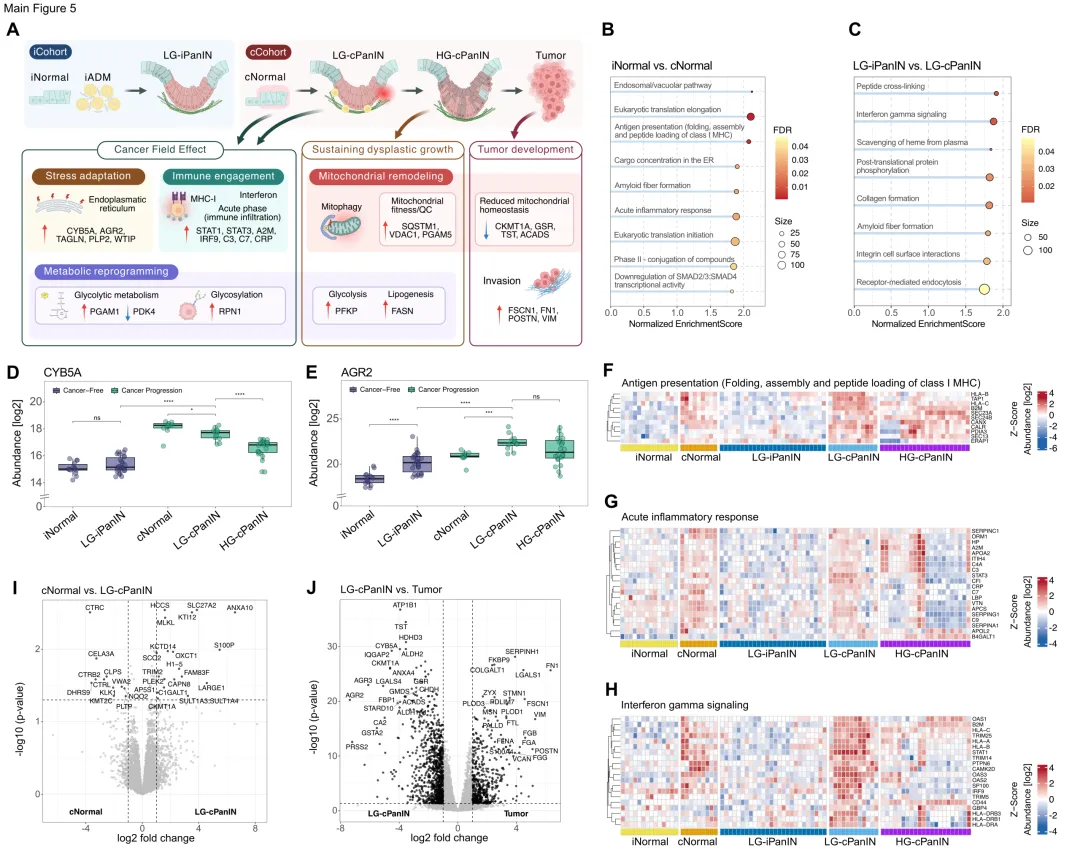
应激适应:与无癌组织相比,cNormal和LG-cPanIN中可见内体/空泡运输、内质网货物浓缩和淀粉样纤维形成通路的激活。CkB5A、WTIP、TAGLN等应激应答蛋白以及AGR2、PLP2等ER/分泌转运因子均呈上调趋势。
免疫参与:cNormal中观察到炎症信号网络激活和MHC I类抗原提呈增强。急性期蛋白(如CRP、补体、触珠蛋白HP、α2-巨球蛋白A2M)水平升高,STAT信号通路蛋白增加。干扰素γ信号通路在LG-cPanIN中尤为显著。
代谢重编程:cNormal和LG-cPanIN呈现免疫代谢转换,表现为PGAM1升高和PDK4降低,提示糖酵解通量增强和丙酮酸进入TCA循环的调控改变。cNormal向LG-cPanIN的转变伴随脂肪酸转运和β-氧化调节因子(如SLC27A2、OXCT1)以及线粒体能量和氧化还原酶(如CKMT1A、HCCS、SCO2)的协调上调。
线粒体重塑:从LG-cPanIN向浸润性PDAC的转变伴随多种线粒体蛋白(如TST、GSR、ACADS、CKMT1A)的下降,而侵袭促进蛋白如FSCN1、STMN1和S100A4则呈上升趋势。肿瘤组织还表现出强烈的促结缔组织增生ECM和间质标记物富集(如FN1、POSTN、VIM)。
图6 癌症相关高级别PanIN病变的蛋白质组学特征
05. 人类腺泡-导管化生的蛋白质组学景观
尽管小鼠ADM已被单细胞技术广泛研究,人类ADM及其与低级别PanIN病变的关系仍不清楚。
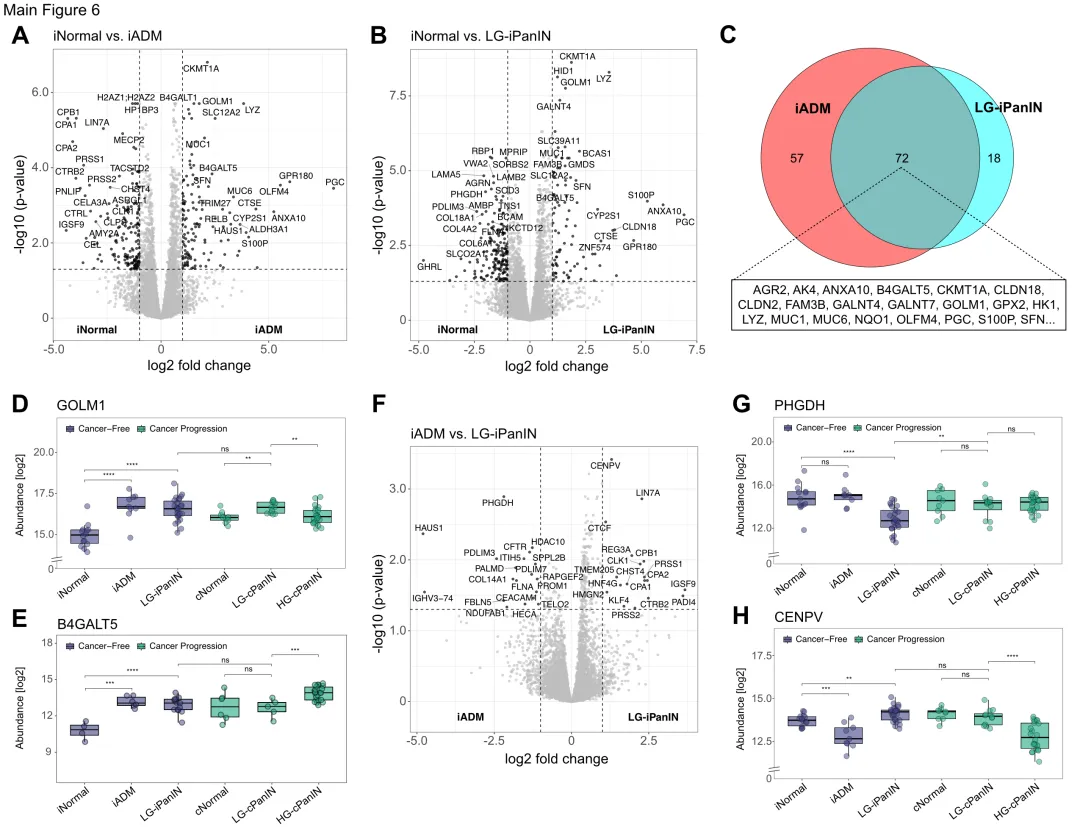
比较无癌个体的正常导管(iNormal)、ADM和LG-iPanIN,研究发现129个蛋白在iADM中上调,90个蛋白在LG-iPanIN中上调,两者共享72个核心蛋白。CKMT1A是诱导最显著的蛋白之一,提示线粒体能量处理的改变是导管重编程的早期特征。GOLM1和B4GALT5等分泌轴蛋白在两种病变中均一致上调。
直接比较iADM和LG-iPanIN发现37个蛋白呈差异化表达。iADM优先表达代谢重编程和导管/祖细胞相关标记物,如PHGDH;而LG-iPanIN选择性上调染色质调控和上皮结构蛋白,如CENPV和LIN7A。这些差异与稳定前驱病变建立结构化上皮程序的特征相一致。
06. KRAS突变肽在偶发性前驱病变中的检测
既往研究表明,PDAC患者的PanIN即使组织学低级别也常携带致癌KRAS热点突变。本研究进一步探索无癌个体偶发性前驱病变中是否存在类似突变。
通过质谱的靶向突变特异性搜索,在iADM和LG-iPanIN中检测到KRAS热点突变肽(主要为G12D和G12V,偶见G13D),而iNormal导管中基本未检测到。数字微滴PCR(ddPCR)正交验证进一步证实了这些发现。
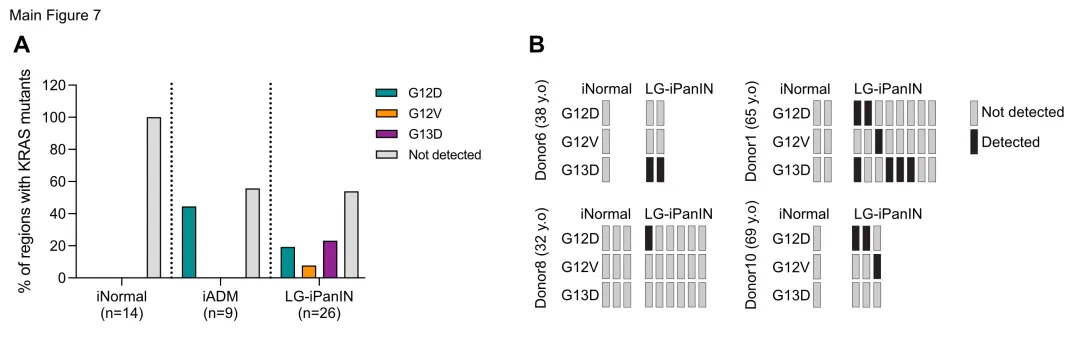
总体而言,46%的LG-iPanIN(26个病变中的12个,来自8个供体中的4个)携带KRAS突变,包括G12D(41.7%)、G12V(16.7%)和G13D(50%)。值得注意的是,部分携带KRAS突变的个体年龄小于40岁(如G13D在38岁供体6中,G12D在32岁供体8中),提示KRAS突变可能在生命早期就已获得。
图8 偶发性前驱病变中KRAS突变肽的蛋白质组学检测
该研究通过AI驱动的深度视觉蛋白组学技术,首次在蛋白质水平系统描绘了胰腺癌前驱病变的多阶段分子演变图谱。
核心发现包括:癌症相关”场效应”在组织学完全正常的导管中即可检测到,表现为应激适应、免疫参与和代谢重编程程序的激活;其次,尽管组织学相似,偶发性PanIN(LG-iPanIN)与癌症相关PanIN(LG-cPanIN)之间存在显著的蛋白质组学差异;第三,HG-cPanIN代表了一个分子上独特的中间状态,具有肿瘤样代谢程序和线粒体质量控制依赖性,而非低级别程序的简单数量增强;最后,KRAS热点突变在无癌个体的偶发性前驱病变中普遍存在。
03. 高级别cPanIN呈现独特的代谢和线粒体依赖特征
HG-cPanIN代表了介于癌前与浸润性癌之间的关键过渡状态。与cNormal相比,HG-cPanIN显示1,075个差异蛋白;与LG-cPanIN相比,则有951个差异蛋白。
代谢重编程主导了HG-cPanIN的蛋白质组学特征。脂肪酸合成酶(FASN)和磷酸果糖激酶(PFKP)在HG-cPanIN中显著上调,说明糖酵解活性增强。转铁蛋白受体(TFRC)升高进一步提示营养获取需求的增加。通路富集分析发现,线粒体基因表达和翻译模块的异常强烈激活,包括线粒体翻译起始/延伸/终止和呼吸链电子传递。PINK1/Parkin线粒体自噬通路组分(如SQSTM1/p62、VDAC1、PGAM5)在HG-cPanIN阶段显著升高。这些结果表明,HG-cPanIN依赖线粒体功能维持其异常增殖状态,可能是一个可干预的潜在靶点。
04. 四个阶段相关的分子程序贯穿胰腺癌变全过程
研究定义了四个与癌症“场效应”和PDAC进展相关的分子变化:
应激适应:与无癌组织相比,cNormal和LG-cPanIN中可见内体/空泡运输、内质网货物浓缩和淀粉样纤维形成通路的激活。CkB5A、WTIP、TAGLN等应激应答蛋白以及AGR2、PLP2等ER/分泌转运因子均呈上调趋势。
免疫参与:cNormal中观察到炎症信号网络激活和MHC I类抗原提呈增强。急性期蛋白(如CRP、补体、触珠蛋白HP、α2-巨球蛋白A2M)水平升高,STAT信号通路蛋白增加。干扰素γ信号通路在LG-cPanIN中尤为显著。
代谢重编程:cNormal和LG-cPanIN呈现免疫代谢转换,表现为PGAM1升高和PDK4降低,提示糖酵解通量增强和丙酮酸进入TCA循环的调控改变。cNormal向LG-cPanIN的转变伴随脂肪酸转运和β-氧化调节因子(如SLC27A2、OXCT1)以及线粒体能量和氧化还原酶(如CKMT1A、HCCS、SCO2)的协调上调。
线粒体重塑:从LG-cPanIN向浸润性PDAC的转变伴随多种线粒体蛋白(如TST、GSR、ACADS、CKMT1A)的下降,而侵袭促进蛋白如FSCN1、STMN1和S100A4则呈上升趋势。肿瘤组织还表现出强烈的促结缔组织增生ECM和间质标记物富集(如FN1、POSTN、VIM)。
图6 癌症相关高级别PanIN病变的蛋白质组学特征
05. 人类腺泡-导管化生的蛋白质组学景观
尽管小鼠ADM已被单细胞技术广泛研究,人类ADM及其与低级别PanIN病变的关系仍不清楚。
比较无癌个体的正常导管(iNormal)、ADM和LG-iPanIN,研究发现129个蛋白在iADM中上调,90个蛋白在LG-iPanIN中上调,两者共享72个核心蛋白。CKMT1A是诱导最显著的蛋白之一,提示线粒体能量处理的改变是导管重编程的早期特征。GOLM1和B4GALT5等分泌轴蛋白在两种病变中均一致上调。
直接比较iADM和LG-iPanIN发现37个蛋白呈差异化表达。iADM优先表达代谢重编程和导管/祖细胞相关标记物,如PHGDH;而LG-iPanIN选择性上调染色质调控和上皮结构蛋白,如CENPV和LIN7A。这些差异与稳定前驱病变建立结构化上皮程序的特征相一致。
06. KRAS突变肽在偶发性前驱病变中的检测
既往研究表明,PDAC患者的PanIN即使组织学低级别也常携带致癌KRAS热点突变。本研究进一步探索无癌个体偶发性前驱病变中是否存在类似突变。
通过质谱的靶向突变特异性搜索,在iADM和LG-iPanIN中检测到KRAS热点突变肽(主要为G12D和G12V,偶见G13D),而iNormal导管中基本未检测到。数字微滴PCR(ddPCR)正交验证进一步证实了这些发现。
总体而言,46%的LG-iPanIN(26个病变中的12个,来自8个供体中的4个)携带KRAS突变,包括G12D(41.7%)、G12V(16.7%)和G13D(50%)。值得注意的是,部分携带KRAS突变的个体年龄小于40岁(如G13D在38岁供体6中,G12D在32岁供体8中),提示KRAS突变可能在生命早期就已获得。
图8 偶发性前驱病变中KRAS突变肽的蛋白质组学检测
该研究通过AI驱动的深度视觉蛋白组学技术,首次在蛋白质水平系统描绘了胰腺癌前驱病变的多阶段分子演变图谱。
核心发现包括:癌症相关”场效应”在组织学完全正常的导管中即可检测到,表现为应激适应、免疫参与和代谢重编程程序的激活;其次,尽管组织学相似,偶发性PanIN(LG-iPanIN)与癌症相关PanIN(LG-cPanIN)之间存在显著的蛋白质组学差异;第三,HG-cPanIN代表了一个分子上独特的中间状态,具有肿瘤样代谢程序和线粒体质量控制依赖性,而非低级别程序的简单数量增强;最后,KRAS热点突变在无癌个体的偶发性前驱病变中普遍存在。
原文链接:https://aacrjournals.org/cancerdiscovery/article/doi/10.1158/2159-8290.CD-25-1119/782738/AI-powered-Deep-Visual-Proteomics-reveals-critical
推荐阅读:
👉细胞外囊泡蛋白质组学揭示结肠腺癌诊断生物标志物
👉【Cell子刊】脑脊液蛋白组解锁SOD1-ALS靶向治疗的关键生物标志物
👉Blood | 血栓空间蛋白组学发现急性缺血性卒中预后标志物和治疗靶点
👉早期活化的细胞外基质蛋白塑造了肾脏纤维化微环境的代谢与空间动态
👉从系统免疫到肿瘤微环境:多维解析 EBV⁺DLBCL 的免疫生物学
👉Cell | Matthias Mann等基于大规模、深入的脑脊液蛋白质组学分析揭示多发性硬化症生物标志物和靶点
👉不挑亚型、不限背景!IL-4Rα阻断对慢性手部湿疹普遍有效
👉多组学整合揭示了致命性 Group 3 髓母细胞瘤中脂质依赖性的肿瘤异质性
👉多模态深度学习在肝内胆管癌术后风险分层中的创新应用与深度解析
👉肝细胞癌进展中的N-糖基化动态:为早期检测开辟新途径
👉破解“胆囊癌之王”的致命密码:多组学研究揭示精准治疗新策略
👉项目文章|Science开年重磅:SPARK-seq破局核酸适体筛选,通量与动力学兼得
注:本文封面图由 AI 技术生成,仅作示意参考,如有不准确之处欢迎指正,相关内容不作为结论依据。
西湖欧米是一家专注于AI赋能的微观世界数据公司,致力于多组学驱动的精准医学的转化落地,目前专注于基于蛋白质谱技术的 AI+proteomics 的疾病生物标记物IVD试剂盒的开发。
欧米的科研服务包括高深度血液蛋白质组学、空间蛋白质组学、微量组织蛋白质组学、宏蛋白质组学等特色业务。截至目前,已和合作者在 Cell、Immunity、Cell Discovery、Molecular Cell、Cell Reports、Nature Communications、Cell Reports Medicine、Nature Protocols 等多种杂志上发表多篇高质量蛋白质组学相关的研究论文。
service@westlakeomics.com
ivd@westlakeomics.com







































 夜雨聆风
夜雨聆风




