文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(六)探究水的组成及变化
实验深度突破
一、实验基础:电解水的本质
1.实验原理
化学反应:2H O 通电 2H ↑+O ↑
2 2 2
科学依据:
化学反应中元素种类不变,通过产物推断反应物组成。
水由水分子构成,通电时分子分裂为氢原子(H)和氧原子(O),原子重新组合成氢分
子(H )和氧分子(O )。
2 2
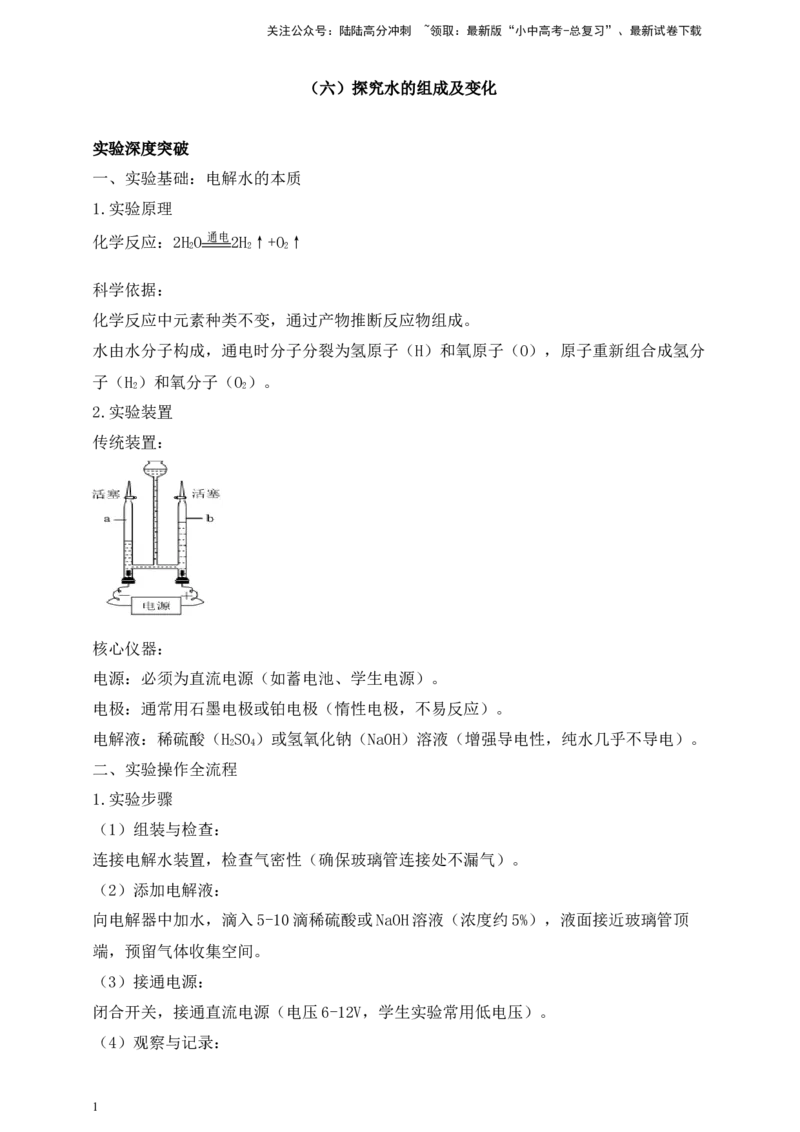
2.实验装置
传统装置:
核心仪器:
电源:必须为直流电源(如蓄电池、学生电源)。
电极:通常用石墨电极或铂电极(惰性电极,不易反应)。
电解液:稀硫酸(H SO )或氢氧化钠(NaOH)溶液(增强导电性,纯水几乎不导电)。
2 4
二、实验操作全流程
1.实验步骤
(1)组装与检查:
连接电解水装置,检查气密性(确保玻璃管连接处不漏气)。
(2)添加电解液:
向电解器中加水,滴入5-10滴稀硫酸或NaOH溶液(浓度约5%),液面接近玻璃管顶
端,预留气体收集空间。
(3)接通电源:
闭合开关,接通直流电源(电压6-12V,学生实验常用低电压)。
(4)观察与记录:
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
记录通电时间,观察电极处气泡产生速率及玻璃管内液面变化。
待气体收集到一定体积(如玻璃管容积的1/2),断开电源。
(5)气体检验:
正极气体(氧气):用燃烧的木条靠近玻璃管尖嘴,缓慢打开活塞,木条燃烧更旺则为
氧气。
负极气体(氢气):用燃烧的木条靠近玻璃管尖嘴,缓慢打开活塞,产生淡蓝色火焰,
说明是氢气。
2.关键现象
通电阶段:
(1)两极均产生气泡,负极(与电源负极相连)气泡速率更快。
(2)玻璃管内液面下降,气体体积逐渐增大。
气体体积比:
(1)理论值:负极气体体积∶正极气体体积=2∶1。
(2)实际观察:初始阶段体积比可能略大于2∶1(氧气在水中溶解度略高于氢气,或
电极消耗部分氧气)。
(简单概括:正氧负氢,氢二氧一)
三、实验结论与科学推理
1.核心结论
宏观层面:水由氢元素(H)和氧元素(O)组成。
微观层面:
(1)水分子由氢原子和氧原子构成;
(2)1个水分子含2个氢原子和1个氧原子。
(3)化学反应的本质是分子分裂为原子,原子重新组合成新分子(化学变化中原子种
类、数目不变)。
定量关系:生成氢气和氧气的体积比为2∶1,质量比为1∶8(可通过密度计算推
导)。
2.误差分析
误差类型 可能原因 改进方法
①氧气溶解度大于氢气; ①预先煮沸电解液排出溶
解气体;
体积比大于2∶1
②使用铂电极
②电极氧化消耗氧气
气体无法点燃或复 ①气体量不足; ①延长通电时间;
燃
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
②装置漏气 ②检查装置气密性
四、实验注意事项(安全与规范)
1、电源安全:
必须使用直流电源,且电压不超过12V(避免触电风险)。
2、电解液防护:
稀硫酸和NaOH溶液具有腐蚀性,避免接触皮肤和衣物,若不慎接触需立即用大量水冲
洗。
3、氢气验纯:
点燃氢气前必须验纯!若气体不纯,点燃可能发生爆炸(氢气爆炸极限:4%-74.2%)。
4、装置检查:
实验前确保玻璃管无裂纹,连接处密封良好,防止气体泄漏影响实验结果。
五、实验改进与创新装置
1.简易家庭版装置
材料:透明塑料瓶(去底)、回形针(电极)、电池、导线、食盐溶液(代替电解液,
需注意:电解食盐水会生成Cl ,需在通风处操作)。
2
优点:取材方便,适合课外探究。
2.刻度优化装置
改进点:在玻璃管外侧贴刻度贴纸,精确记录气体体积变化,直观对比2∶1比例。
优点:减少人为估算误差,适合课堂演示。
六、实验拓展与知识延伸
1.拓展实验:氢气燃烧验证水的生成
点燃
原理:2H +O 2H O
2 2 2
操作:
用干燥烧杯罩在氢气燃烧火焰上方,观察内壁出现无色液滴(证明生成水)。
意义:与电解水实验形成“分解-合成”闭环,双向验证水的组成。
2.跨学科联系
物理学视角:电能转化为化学能(电解过程),体现能量守恒定律。
环保应用:电解水制氢气可作为清洁能源(氢能源)的制备途径,但需消耗大量电能,
目前正研究太阳能电解等绿色方法。
3.科学史链接
卡文迪许实验:18世纪英国科学家卡文迪许通过氢气燃烧实验首次证明水是化合物,
推翻“水是单质”的传统观念。
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
拉瓦锡贡献:法国化学家拉瓦锡通过定量实验确定水的元素组成,奠定近代化学基础。
中考命题探秘
一、考情分析
在历年中考化学试卷中,电解水实验频繁出现,是重点考查内容。其考查的知识点涵盖
了实验现象、实验结论、气体检验、实验原理以及实验装置等多个方面。随着教育对学
生科学素养和探究能力的重视程度不断提高,对电解水实验的考查也更加深入和灵活,
不再局限于对基础知识的简单记忆,而是更注重考查学生对实验的理解和应用能力,以
及分析问题、解决问题的能力。
二、考查形式
1.选择题:常以四选一的形式出现,要求学生从多个选项中选择关于电解水实验描述正
确或错误的一项。选项内容可能涉及实验现象(如两极产生气体的状态、颜色、体积比
等)、实验结论(水的元素组成、分子构成等)、实验原理(化学反应方程式的书写及
含义)、实验条件(电源类型、电解液的作用等)以及气体的性质和检验方法等方面。
2.填空题:主要考查学生对电解水实验关键信息的准确记忆和书写。例如,要求填写实
验中两极产生的气体名称、气体的体积比;写出电解水的化学反应方程式;根据实验现
象推导水的组成元素等。有时也会让学生分析实验过程中出现某些现象或问题的原因。
3.实验探究题:这类题型综合性较强,通常会给出电解水的实验装置图或实验情境,然
后提出一系列问题。可能包括实验步骤的完善(如补充实验前的准备工作、实验操作的
具体顺序等);对实验现象的详细描述和解释;根据实验目的对实验装置进行改进或评
价;通过实验数据的分析得出结论;探究影响电解水速率或实验结果的因素等。此外,
还可能结合微观粒子的知识,让学生从微观角度解释电解水的过程。
三、中考所占分值或比例
电解水实验在中考化学中所占分值和比例因地区而异。在大多数地区,单独考查电解水
实验的分值一般在2-4分左右。如果与其他知识点综合考查,分值可能会有所增加,在
一些综合性较强的试卷中,与电解水实验相关的内容分值可能达到5-8分。整体来看,
其分值大约占中考化学总分的3%-6%。
四、中考预测
1.联系实际应用:未来中考可能会更多地将电解水实验与实际生活、科技发展相联系。
例如,以水电解制氢在新能源领域的应用为背景,考查学生对电解水实验原理、条件以
及产物性质的理解;或者探讨电解水技术在污水处理、海水淡化等方面的潜在应用,要
求学生分析其可行性和优势。
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
2.强化探究能力:实验探究题的比重可能会进一步加大,对学生的实验设计、操作、观
察、分析和评价能力提出更高要求。可能会出现一些开放性的探究问题,如让学生设计
实验验证电解水实验中气体体积比的理论值与实际值存在差异的原因,或者探究不同电
解液对电解水速率和产物纯度的影响等。
3.融合多学科知识:随着跨学科理念的推进,中考可能会将化学与物理、生物等学科知
识融合考查。比如,从物理角度考查电解水过程中的电能转化、电极材料的导电性;从
生物角度探讨电解水产生的氢气和氧气对生物生长和代谢的影响等。
4.考查微观本质:结合微观示意图或模型,考查学生对电解水过程中分子、原子变化的
理解,以及化学反应本质的认识。例如,通过给出电解水前后微观粒子的变化示意图,
让学生判断粒子的种类、数量变化,以及化学反应的微观实质。
五、备考建议
1.夯实基础知识:深入理解电解水实验的原理,牢记实验现象(正氧负氢,氢二氧
一)、实验结论(水由氢氧元素组成)以及气体的检验方法(氢气用燃着的木条,氧气
用带火星的木条)。熟练掌握电解水的化学反应方程式,并理解其含义。
2.注重实验操作细节:了解实验所需的仪器和装置,掌握实验操作步骤和注意事项。例
如,实验使用的是直流电;为增强水的导电性,常加入少量稀硫酸或氢氧化钠溶液;实
验前要检查装置的气密性等。有条件的话,亲自参与实验操作,通过实践加深对实验细
节的理解和记忆。
3.构建知识网络:将电解水实验与其他相关知识建立联系,形成完整的知识体系。比
如,将水的组成与物质的分类、元素的概念相联系;将电解水的化学反应与质量守恒定
律、化学方程式的书写和计算相结合;将氢气和氧气的性质与气体的制取、收集、检验
等知识串联起来。
4.加强练习与总结:通过做大量的练习题,熟悉各种考查形式和题型,总结解题方法和
技巧。对于做错的题目,要认真分析原因,找出自己的知识漏洞和薄弱环节,有针对性
地进行强化训练。同时,要注意对相似知识点的对比和辨析,避免混淆。
5.关注学科前沿和实际应用:平时多关注化学学科的前沿动态,了解电解水实验在实际
生产生活中的应用案例,拓宽知识面。这样不仅可以提高学习兴趣,还能在考试中更好
地应对与实际应用相关的题目,提高知识的迁移能力和应用能力。
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
6