Nature|AI与微电子交织,定义下一代智能给药装置
生物技术、AI、微电子与材料科学的深度耦合,正诱发体内药物递送系统的范式转移。智能化小型化药物递送装置(IMDDDs)的崛起,不仅攻克了传统给药体系在被动释药、剂量固定及靶向偏差上的局限,更确立了精准医疗时代的革新基准。近日,《Nature》刊发的综述“Towards intelligent and miniaturized drug delivery devices”系统剖析了该领域的底层架构与设计准则,深度解码了 AI 驱动的性能增益,并前瞻性地评估了其临床转化路径中的关键变量。

二元架构创新:定义IMDDDs的底层设计逻辑
IMDDDs 的核心创新在于突破了传统给药装置药物容器的单一属性,构建了控制模态 + 释放模块的二元核心架构。
1. 模块化组合范式
-
控制模态: 集成生物电子传感、数字化处理单元及响应性材料。 -
释放模块: 划分为可穿戴、可植入、原位作用、非接触四大场景。 -
材料矩阵: 覆盖金属、无机非金属、聚合物及复合材料。
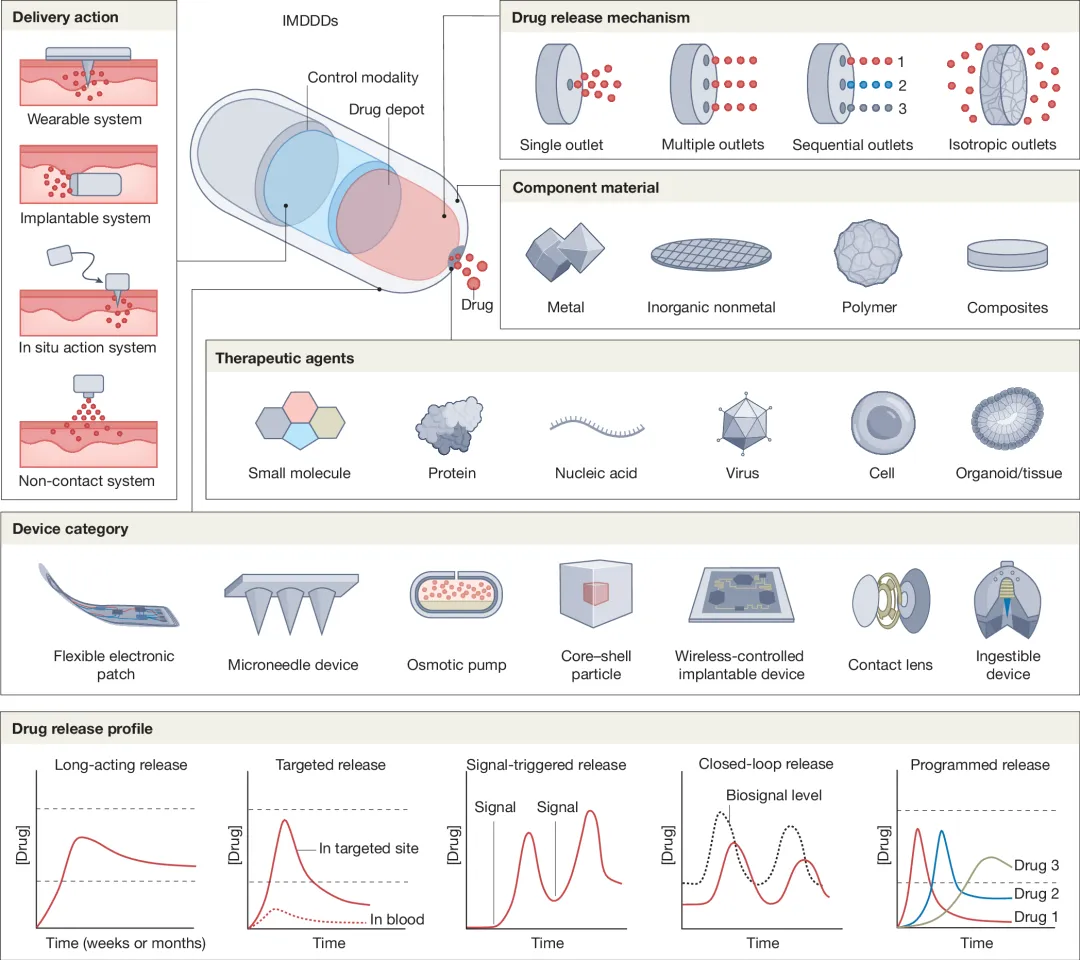 图1.IMDDDs组件及分类示意图。
图1.IMDDDs组件及分类示意图。
2. 四大差异化器件体系
-
生物电子治疗器: 构建传感-处理-释放闭环,典型代表如无线诊疗隐形眼镜与智能敷料。 -
物理触发致动器: 依靠磁、声等外场能量转换,实现毫米级给药器的定向推进。 -
理化响应型器件: 基于材料分子修饰,实现对pH、离子、葡萄糖浓度的自主感应。 -
活体器件: 将细菌、细胞或类器官集成于多孔膜(孔径 <0.8μm)腔室中,打造“体内细胞工厂”。
机制与效果解析:从数据看“按需给药”的精准度
IMDDDs 实现了从被动释药向长效、靶向、信号触发及闭环释放的升级。以下是核心释药机制的数据解读:
1. 闭环控制的临床优势
-
控糖效率: 商业化 MiniMed 780G 系统利用 AI 算法每 5 分钟 调整一次剂量。临床数据显示,其可使患者血糖达标时间(TIR)超过 80%。 -
创面愈合: 智能敷料通过监测电阻抗与 pH 值变化,按需释放生长因子,显著提升慢性创面的闭环管理效率。
2. 内源性响应的灵敏性
-
血栓干预: 利用凝血酶特异性剪切机制,抗凝贴片可在血栓形成部位 20 分钟内 快速释放肝素。相比全身给药,这种局部按需释放大幅降低了自发性出血风险。 -
pH响应: 针对肿瘤微环境,利用 pH 差异实现药物释放,提高局部药物浓度并减少全身毒性。
3. 外场触发的穿透力
-
磁控递送: 利用磁场的深层组织穿透性,可控释药深度可达体内深部病灶,在肿瘤局部化疗中展现出显著的时空可控性。
智能化全链条:AI驱动的自适应进化
AI 的介入使 IMDDDs 从单纯的硬件进化为具备“思维”的系统。
-
设计制造: 利用 AI 辅助生物相容性材料筛选与 4D 打印路径规划。 -
动态优化: 强化学习(RL)算法可根据患者实时生理数据,自主学习并生成最优治疗方案。 -
自适应导航: AI 导航微机器人通过深度学习实现复杂血流环境下的实时路径规划,极大提升了靶向递送的成功率。
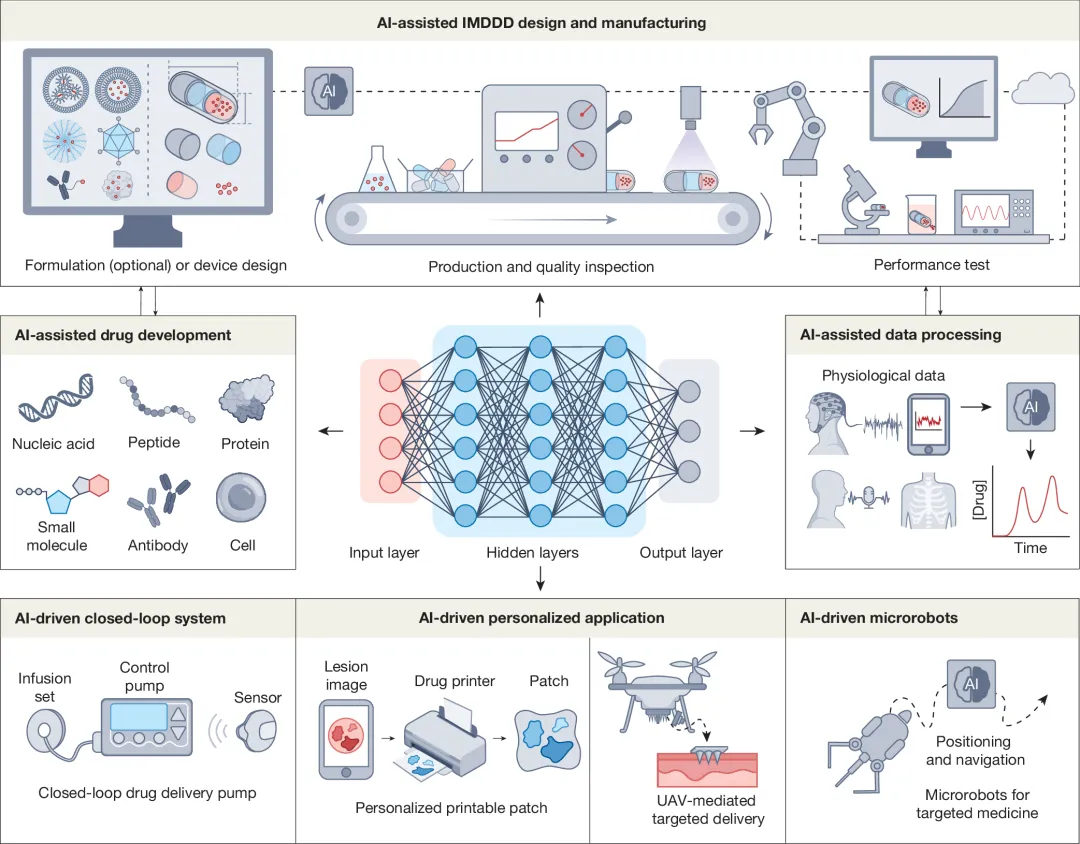 图2. AI增强IMDDDs。
图2. AI增强IMDDDs。生物相容性保障:长期植入的安全性基石
对于植入式器件,IMDDDs 通过全链条设计降低宿主异物反应:
材料选择:优先采用 PLGA 等可降解材料,避免二次手术取出。
结构工程:活体器件采用 孔径 <0.8μm 的多孔膜,既保证了营养物质与药物的交换,又实现了对宿主免疫细胞的物理屏蔽。
力学匹配:通过柔性电子与软材料集成,解决了刚性器件与软组织间的应力不匹配问题,降低了组织损伤与纤维化风险。
结语与前瞻:向“泛血管介入器械”的智能化演进
IMDDDs 的出现不仅是给药技术的革新,更是对未来植入介入医疗器械的一次深刻启示。
从心血管介入视角来看: 未来的冠脉支架或瓣膜将不再仅仅是机械支撑结构。借鉴 IMDDDs 的逻辑,智能化支架将集成微纳传感与 AI 算法:
主动抗栓:感知局部血流动力学与凝血因子浓度,在血栓形成初期按需释放抗凝药物。
抑制再狭窄:通过电触发或理化响应机制,精准控制抗增殖药物的脉冲式释放。
实时监测:实现支架内再狭窄与内皮化程度的远程数字化监控。
IMDDDs 所代表的微型化、智能化、集成化趋势,正驱动心血管介入器械从盲目植入向精准自适应跨越;而当这种微观层面的智能释药逻辑,与跨越 5200 公里的泛血管手术机器人辅助装置PANVIS深度联动,人类将真正构建起感知-决策-远程执行的全球化诊疗闭环,开启泛血管介入手术跨时空、全生命周期的智能新纪元。
 夜雨聆风
夜雨聆风




