文档内容
专练 28 分子空间结构与物质性质
授课提示:对应学生用书55页
一、选择题
1.[2024·吉林卷]如下反应相关元素中,W、X、Y、Z为原子序数依次增大的短周期
元素,基态X原子的核外电子有5种空间运动状态,基态Y、Z原子有两个未成对电子,Q
是ds区元素,焰色试验呈绿色。下列说法错误的是( )
QZY 溶液―――――――→QZX YW 溶液
4 4 4 12
A.单质沸点:Z>Y>W
B.简单氢化物键角:X>Y
C.反应过程中有蓝色沉淀产生
D.QZX YW 是配合物,配位原子是Y
4 4 12
答案:D
解析:常温下,单质S呈固态,O 、H 均呈气态,且相对分子质量O>H ,则分子间
2 2 2 2
作用力O>H ,故单质的沸点:S>O>H ,A正确;NH 、HO的中心原子N、O均采取sp3
2 2 2 2 3 2
杂化,但N、O上分别有1,2个孤电子对,孤电子对数越多,对成键电子对的斥力越大,
键角越小,故简单氢化物的键角:NH >H O,B正确;向CuSO 溶液中逐渐通入NH ,先
3 2 4 3
生成蓝色Cu(OH) 沉淀,当NH 过量时,Cu(OH) 沉淀溶解生成深蓝色的Cu(NH )
2 3 2 3
SO 溶液,C正确;配合物Cu(NH ) SO 中Cu2+提供空轨道,N原子提供孤电子对形
4 4 3 4 4
成配位键,即其中配位原子是N,D错误。
2.[2024·石家庄市质量检测]物质的结构决定其性质,下列事实与解释相符的是
( )
选项 事实 解释
C原子处在4个F原子所组成的正方形中心,键
A CF 是非极性分子
4 的极性的向量和为零
B Ge原子间难以形成π键 Ge的原子半径较大,未杂化的p轨道很难重叠
2个C===O键的键能之和小于4个Si—O键的键
C 干冰的熔点低于SiO
2 能之和
D 利用杯酚可分离C 和C 超分子具有自组装的特征
60 70
答案:B
解析:CF 中C与4个F形成4个σ键,孤对电子数为0,所以C原子采用sp3杂化,
4
则CF 为正四面体形结构,该分子正负电荷中心重合,为非极性分子,A项事实与解释不
4
相符;Ge的原子半径较大,未杂化的p轨道很难有效肩并肩重叠形成π键,B项事实与解
释相符;干冰(二氧化碳)为分子晶体、二氧化硅为共价晶体,共价晶体的熔沸点高于分
子晶体,C项事实与解释不相符;杯酚可分离C 与C 是由于杯酚能与C 形成超分子,而
60 70 60
不能与C 形成超分子,反映出超分子具有分子识别的特性,D项事实与解释不相符。
70
3.[2024·吉林卷]下列化学用语或表述正确的是( )
A.中子数为1的氦核素:He
B.SiO 的晶体类型:分子晶体
2
C.F 的共价键类型:p—p σ键
2
D.PCl 的空间结构:平面三角形
3
答案:C
3
解析:中子数为1的氦元素的质量数为3,表示为 He,A错误;二氧化硅为共价晶体,
2
B错误;F2中的共价键由2个F原子各提供1个未成对电子的2p原子轨道重叠形成,为pp
σ键,C正确; PCl 的中心P原子的价层电子对数为3+=4,有1个孤电子对,故PCl
3 3
的空间结构为三角锥形,D错误。
4.[2024·湖北卷]基本概念和理论是化学思维的基石。下列叙述错误的是( )A.VSEPR理论认为VSEPR模型与分子的空间结构相同
B.元素性质随着原子序数递增而呈周期性变化的规律称为元素周期律
C.泡利原理认为一个原子轨道内最多只能容纳两个自旋相反的电子
D.sp3杂化轨道由1个s轨道和3个p轨道混杂而成
答案:A
解析:中心原子含有孤电子对的分子,其空间结构与VSEPR模型不同,A错误。
5.[2024·安徽卷]下列有关物质结构或性质的比较中,正确的是( )
A.键角:NH >NO
3
B.熔点:NH OH>[NHOH]Cl
2 3
C.25 ℃同浓度水溶液的pH:[NH OH]Cl>NH Cl
3 4
D.羟胺分子间氢键的强弱:O—H…O>N—H…N
答案:D
解析:NH3中N为sp3杂化,NO-3中N为sp2杂化,则键角:NH N—H…N,D项正确。
6.[2023·湖北卷]价层电子对互斥理论可以预测某些微粒的空间结构。下列说法正确的
是( )
A.CH 和HO的VSEPR模型均为四面体
4 2
B.SO和CO的空间构型均为平面三角形
C.CF 和SF 均为非极性分子
4 4
D.XeF 与XeO 的键角相等
2 2
答案:A
解析:甲烷分子的中心原子的价层电子对数为4,水分子的中心原子价层电子对数也
为4,所以他们的VSEPR模型都是四面体,A正确;SO的孤电子对数为1,CO的孤电子
对数为0,所以SO的空间构型为三角锥形,CO的空间构型为平面三角形,B错误,CF 为
4
正四面体结构,为非极性分子,SF 中心原子有孤电子对,为极性分子,C错误;XeF 和
4 2
XeO 分子中,孤电子对数不相等,孤电子对数越多,排斥力越大,所以键角不等,D错误;
2
故选A。
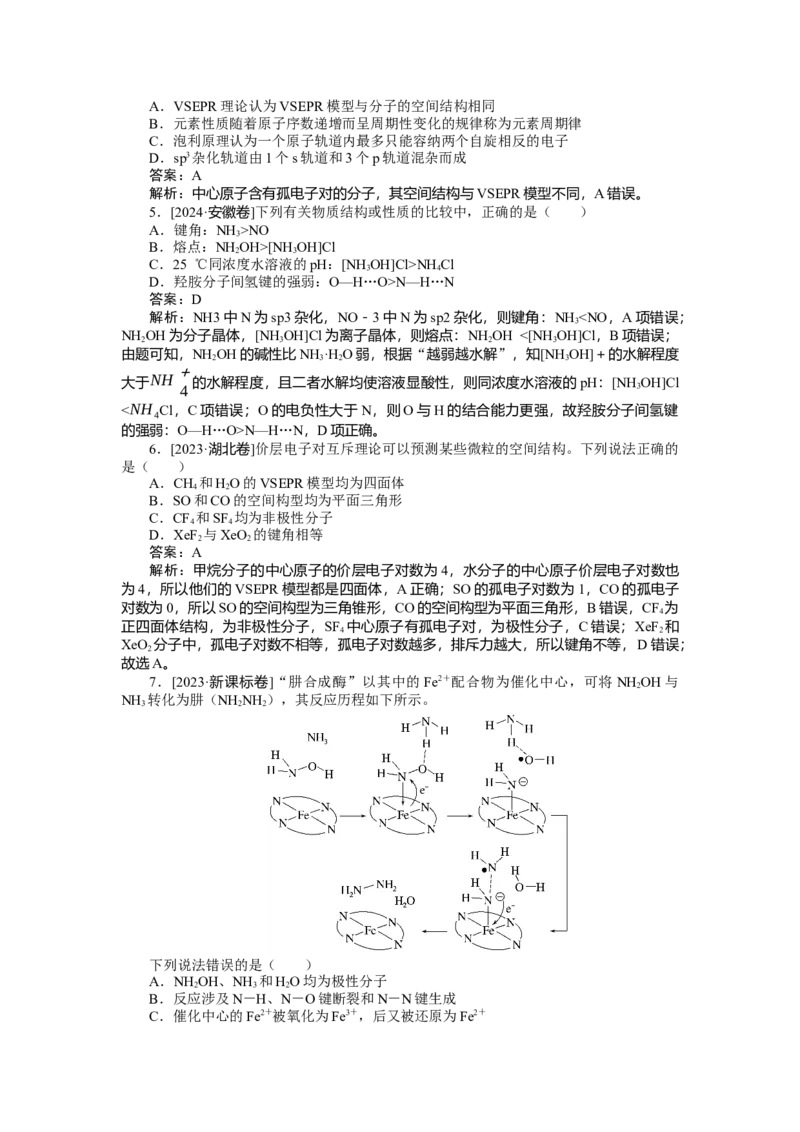
7.[2023·新课标卷]“肼合成酶”以其中的Fe2+配合物为催化中心,可将NH OH与
2
NH 转化为肼(NH NH ),其反应历程如下所示。
3 2 2
下列说法错误的是( )
A.NH OH、NH 和HO均为极性分子
2 3 2
B.反应涉及N-H、N-O键断裂和N-N键生成
C.催化中心的Fe2+被氧化为Fe3+,后又被还原为Fe2+D.将NH OH替换为ND OD,反应可得ND ND
2 2 2 2
答案:D
解析:NH OH、NH 、HO的电荷分布都不均匀,不对称,为极性分子,A正确;由
2 3 2
反应历程可知,有N-H,N-O键断裂,还有N-H键的生成,B正确;由反应历程可知,
反应过程中,Fe2+先失去电子发生氧化反应生成Fe3+,后面又得到电子生成Fe2+,C正确;
由反应历程可知,反应过程中,生成的NH NH 有两个氢来源于NH ,所以将NH OH替换
2 2 3 2
为ND OD,不可能得到ND ND ,得到ND NH 和HDO,D错误;故选D。
2 2 2 2 2
8.[2024·北京清华附中阶段检测]已知SiCl 与N甲基咪唑( )反应可以得
4
到M2+,其结构如图所示,下列说法不正确的是( )
A.M2+中Si的配位数是6
B.1个M2+中含有42个σ键
C.SiF、SiCl 、SiBr 、SiI 的沸点依次升高
4 4 4 4
D.气态SiCl 分子的空间结构为正四面体形
4
答案:B
解析:由图可知,中心Si原子与Cl之间、与N原子之间均形成配位键,故其配位数
是6,A项正确;单键为σ键,双键为1个σ键和一个π键,配位键也为σ键,故1个M2+
中含有54个σ键,B项错误;由于SiF 、SiCl 、SiBr 、SiI 均为分子晶体,结构相似,随
4 4 4 4
着相对分子质量的增大,分子间作用力增大,沸点逐渐升高,故 SiF 、SiCl 、SiBr 、SiI
4 4 4 4
的沸点依次升高,C项正确;SiCl 的中心原子Si原子的价层电子对数为4+=4,无孤电子
4
对,故气态SiCl 分子的空间结构为正四面体形,D项正确。
4
9.[2024·兰州市高三诊断考试]化学用语是表述化学学科知识的专业语言符号。下列说
法不正确的是( )
A.基态Cr原子的价层电子排布式:3d54s1
B.ClO的电子式:Cl∶O∶Cl
2
C.OF 和ClO的VSEPR模型均为四面体形
2
D.ICl和NH 均为极性分子
3
答案:B
解析:Cr是24号元素,基态Cr原子的价层电子排布式为3d54s1,A项正确;ClO中
2
Cl原子的最外层电子数为7,Cl和O原子之间存在1对共用电子,各原子最外层均满足8
电子稳定结构,故其电子式为∶Cl∶O∶Cl∶,B项错误;OF 的中心O原子的价层电子对
2
数为2+×(6-2×1)=4,ClO的中心Cl原子的价层电子对数为2+×(7+1-2×2)=
4,故二者的VSEPR模型均为四面体形,C项正确;ICl中I原子和Cl原子之间形成1对共
用电子,其结构为I—Cl,结构不对称,为极性分子,NH 为三角锥形结构,正负电荷中心
3
不重合,为极性分子,D项正确。
10.[2024·浙江1月]X、Y、Z、M和Q五种主族元素,原子序数依次增大,X原子半
径最小,短周期中M电负性最小,Z与Y、Q相邻,基态Z原子的s能级与p能级的电子
数相等,下列说法不正确的是( )
A.沸点:XZ>X Q
2 2
B.M与Q可形成化合物MQ、MQ
2 2 2
C.化学键中离子键成分的百分数:MZ>M Q
2 2
D.YZ与QZ离子空间结构均为三角锥形
答案:D
解析:X、Y、Z、M和Q五种主族元素,原子序数依次增大,X原子半径最小,则X
为H,短周期中M电负性最小,则M为Na,基态Z原子的s能级与p能级的电子数相等,
则 Z 为 O,Z 与 Y、Q 相邻,则 Y 为 N,Q 为 S。HO 可形成分子间氢键,故沸点:
2
HO>HS,A项正确;O与S同主族,其化学性质相似,Na与O可形成NaO、NaO ,故
2 2 2 2 2Na与S也可形成NaS、NaS ,B项正确;电负性差值越大,离子键成分的百分数越大,
2 2 2
同主族元素自上而下电负性依次降低,O的电负性大于 S,则离子键成分的百分数:
NaO>Na S,C项正确;NO的中心N原子的孤电子对数==0,为sp2杂化,则NO的空间
2 2
构型为平面三角形,D项错误。
11.[2022·湖北卷]磷酰三叠氮是一种高能分子,结构简式为O===P(N ) 。下列关于
3 3
该分子的说法正确的是( )
A.为非极性分子
B.立体构型为正四面体形
C.加热条件下会分解并放出N
2
D.分解产物NPO的电子式为N⋮⋮P∶O∶
答案:C
解析:从结构简式可知该分子正负电荷中心不重合,是极性分子,A项错误;P连接
的四个原子或原子团不完全相同,故立体构型不可能为正四面体形,B项错误;O===P
(N) 的分解产物为NPO(D项中提示),N元素化合价降低,由得失电子守恒知,其分
3 3
解还会产生N,C项正确;NPO的电子式是∶N⋮⋮P∶O∶,D项错误。
2
二、非选择题
12.[2022·全国甲卷(节选)]
2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现
了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH===CH )与四氟乙烯
2 2
(CF===CF )的共聚物(ETFE)制成。回答下列问题:
2 2
(1)基态F原子的价电子排布图(轨道表示式)为 。
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不
同)。第一电离能的变化图是 (填标号),判断的根据是___________________
________________________________________________________________________
________________________________________________________________________;
第三电离能的变化图是 (填标号)。
(3)固态氟化氢中存在(HF) 形式,画出(HF) 的链状结构 。
n 3
(4)CF===CF 和ETFE分子中C的杂化轨道类型分别为 和 ;聚四
2 2
氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因 。
答案:(1)
(2)a 同周期元素从左到右,第一电离能呈增大趋势,N原子的价电子排布式为
2s22p3,2p轨道是半充满稳定结构,第一电离能比O原子大 b
(3)H—F…H—F…H—F
(4)sp2 sp3 F的电负性比H大,C—F键的键能比C—H键的大
解析:(1)基态F原子的价电子排布式为2s22p5,故其价电子排布图(轨道表示式)
为
(2)C、N、O、F均位于第二周期,原子半径逐渐减小,原子核对最外层电子的吸引
能力增强,第一电离能逐渐增大,但N原子的价电子排布式为2s22p3,2p轨道是半充满稳
定结构,第一电离能比O原子大,故选a;C原子失去2个电子后达到2s2全满稳定结构,
再失去1个电子较难,故第三电离能比N原子大,故选b。(3)固态氟化氢分子间存在氢
键,故(HF) 的链状结构为H—F…H—F…H—F。(4) CF===CF 分子中C原子形成碳
3 2 2
碳双键,故C原子为sp2杂化;ETFE是乙烯与四氟乙烯的共聚物,可表示为CH—CH—
2 2CF—CF,故在ETFE分子中碳原子为sp3杂化;由于F的电负性比H大,C—F键的键能
2 2
比C—H键的大,故聚四氟乙烯比聚乙烯稳定。
13.[2024·浙江1月]氮和氧是构建化合物的常见元素。
已知:
请回答:
(1)某化合物的晶胞如图,其化学式是 ,晶体类型是 。
(2)下列说法正确的是 。
A.电负性:B>N>O
B.离子半径:P3-”“<”或
2 2 2 2
“=”),请说明理由
________________________________________________________________________
________________________________________________________________________。
②将HNO 与SO 按物质的量之比1∶2发生化合反应生成A,测得A由2种微粒构成,
3 3
其中之一是NO。比较氧化性强弱:NO HNO (填“>”“<”或“=”);写出A中
3
阴离子的结构式
________________________________________________________________________。
答案:(1)Cr(HO)Cl 或CrCl ·4H O 分子晶体
2 4 2 2 2
(2)CD
(3)①sp3 < —NH 中N有孤电子对,对成键电子对的斥力大,键角小
2
解析:(1)由晶胞结构可知,晶胞顶点和面心处原子团是一样的,均为CrCl ·4H O,
2 2
故该化合物的化学式为CrCl ·4H O,其晶体类型为分子晶体。(2)同一周期主族元素,从
2 2
左到右,电负性依次增大,故电负性顺序为O>N>B,A项错误;核外电子排布相同的离子,
核电荷数越大,半径越小,故离子半径顺序为P3->S2->Cl-,B项错误;同一周期元素从左
到右,第一电离能呈增大的趋势,但第ⅡA族和第ⅤA族元素例外,故第一电离能:
Ge HNO ;
3A中阴离子为HS O,根据题给已知信息可知其结构式为 。
2