文档内容
专练 39 化学反应速率及影响因素
授课提示:对应学生用书77页
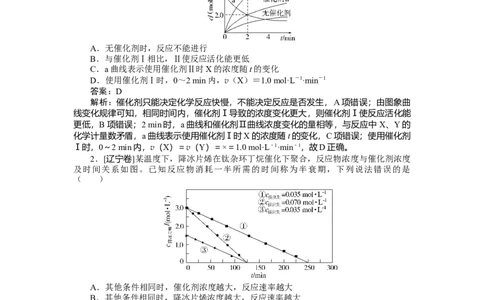
1.[2022·广东卷]在相同条件下研究催化剂Ⅰ、Ⅱ对反应X―→2Y的影响,各物质浓
度c随反应时间t的部分变化曲线如图,则( )
A.无催化剂时,反应不能进行
B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D.使用催化剂Ⅰ时,0~2 min内,v(X)=1.0 mol·L-1·min-1
答案:D
解析:催化剂只能决定化学反应快慢,不能决定反应是否发生,A项错误;由图象曲
线变化规律可知,相同时间内,催化剂Ⅰ导致的浓度变化更大,则催化剂Ⅰ使反应活化能
更低,B项错误;2 min时,a曲线和催化剂Ⅱ曲线浓度变化的量相等,与反应中 X、Y的
化学计量数矛盾,a曲线表示使用催化剂Ⅰ时X的浓度随t的变化,C项错误;使用催化剂
Ⅰ时,0~2 min内,v(X)=v(Y)=×=1.0 mol·L-1·min-1,故D正确。
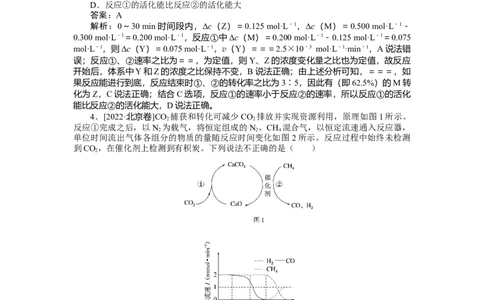
2.[辽宁卷]某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度与催化剂浓度
及时间关系如图。已知反应物消耗一半所需的时间称为半衰期,下列说法错误的是
( )
A.其他条件相同时,催化剂浓度越大,反应速率越大
B.其他条件相同时,降冰片烯浓度越大,反应速率越大
C.条件①,反应速率为0.012 mol·L-1·min-1
D.条件②,降冰片烯起始浓度为3.0 mol·L-1时,半衰期为62.5 min
答案:B
解析:通过图像对比①②可知,②的反应速率比①大,则说明其他条件相同时,催化
剂浓度越大,反应速率越大,A正确;①和③催化剂浓度相同,降冰片烯浓度③小于①,
但③的反应速率与①相等,不能说明其他条件相同时,降冰片烯浓度越大,反应速率越大
B错误;根据化学反应速率的计算公式 v=可知,条件①时,反应速率为=0.012 mol·L-
1·min-1,C正确;已知反应物消耗一半所需的时间称为半衰期,条件②,降冰片烯的起始
浓度为3.0 mol·L-1时,半衰期为62.5 min,D正确。
3.[河北卷]室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反
应:①M+N===X+Y;②M+N===X+Z。反应①的速率可表示为v =kc2(M),反应
1 1②的速率可表示为v =kc2(M)(k 、k 为速率常数)。反应体系中组分M、Z的浓度随
2 2 1 2
时间变化情况如图。下列说法错误的是( )
A.0~30 min时间段内,Y的平均反应速率为6.67×10-3 mol·L-1·min-1
B.反应开始后,体系中Y和Z的浓度之比保持不变
C.如果反应能进行到底,反应结束时62.5%的M转化为Z
D.反应①的活化能比反应②的活化能大
答案:A
解析:0~30 min时间段内,Δc(Z)=0.125 mol·L-1,Δc(M)=0.500 mol·L-1-
0.300 mol·L-1=0.200 mol·L-1,反应①中Δc(M)=0.200 mol·L-1-0.125 mol·L-1=0.075
mol·L-1,则Δc(Y)=0.075 mol·L-1,v(Y)===2.5×10-3 mol·L-1·min-1,A说法错
误;反应①、②速率之比为==,为定值,则Y、Z的浓度变化量之比也为定值,故反应
开始后,体系中Y和Z的浓度之比保持不变,B说法正确;由上述分析可知,===,如
果反应能进行到底,反应结束时①、②的转化率之比为3∶5,因此有(即62.5%)的M转
化为Z,C说法正确;结合C选项,反应①的速率小于反应②的速率,所以反应①的活化
能比反应②的活化能大,D说法正确。
4.[2022·北京卷]CO 捕获和转化可减少CO 排放并实现资源利用,原理如图1所示。
2 2
反应①完成之后,以N 为载气,将恒定组成的N 、CH 混合气,以恒定流速通入反应器,
2 2 4
单位时间流出气体各组分的物质的量随反应时间变化如图 2所示。反应过程中始终未检测
到CO,在催化剂上检测到有积炭。下列说法不正确的是( )
2
A.反应①为CaO+CO===CaCO ;反应②为CaCO +CH=====CaO+2CO+2H
2 3 3 4 2
B.t min~t min,n(H )比n(CO)多,且生成H 的速率不变,推测有副反应
1 3 2 2
CH=====C+2H
4 2
C.t min时刻,副反应生成H 的速率大于反应②生成H 的速率
2 2 2
D.t min之后,生成CO的速率为0,是因为反应②不再发生
3
答案:C
解析:根据图示知,A项正确;若只发生反应②,则n(H )=n(CO),而t ~t
2 1 3
min,n(H )比n(CO)多,且生成H 的速率不变,结合反应过程中始终未检测到CO ,
2 2 2
催化剂上有积炭,可推测有副反应,且反应②和副反应中CH 和H 的化学计量数之比均为
4 21∶2,B 项正确;t min 时,H 的流出速率为 2 mmol·min-1,CO的流出速率约为 1.5
2 2
mmol·min-1,<2,说明副反应生成H 的速率小于反应②生成H 的速率,C项错误;根据
2 2
图 2 知,t min 后,CO 的生成速率为 0,CH 的流出速率逐渐增大,最终恢复到 1
3 4
mmol·min-1,H 的生成速率逐渐减小至0,说明t min后反应②不再发生,副反应逐渐停
2 3
止,D项正确。
5.可逆反应mA(g)+nB(g) ⇌pC(g)+qD(g)的vt图像如图甲所示,若其他
条件都不变,只是在反应前加入合适的催化剂,则其 vt图像如图乙所示。①a =a ;②a
1 2 1
<a ;③b =b ;④b <b ;⑤t >t ;⑥t =t ;⑦两图中阴影部分面积相等;⑧图乙中阴
2 1 2 1 2 1 2 1 2
影部分面积更大。以上所述正确的为( )
A.②④⑤⑦ B.②④⑤⑧
C.②③⑤⑦ D.②③⑥⑧
答案:A
解析:加入催化剂的结果:一是正、逆反应速率都增大,二是缩短了达到平衡的时间;
由此可得:a <a 、b <b 、t >t ,但不能使平衡发生移动,由此推知,阴影面积为反应物
1 2 1 2 1 2
浓度的变化,由于催化剂不影响平衡移动,则两图中阴影部分面积相等,符合题意的选项
有②④⑤⑦;综上所述,本题选A。
6.一定温度下,10 mL 0.40 mol·L-1 HO 溶液发生催化分解。不同时刻测得生成 O
2 2 2
的体积(已折算为标准状况)如表所示。
t/min 0 2 4 6 8 10
V(O)/mL 0.0 9.9 17.2 22.4 26.5 29.9
2
下列叙述不正确的是(溶液体积变化忽略不计)( )
A.0~6 min的平均反应速率:v(HO)≈3.3×10-2 mol·L-1·min-1
2 2
B.6~10 min的平均反应速率:v(HO)<3.3×10-2 mol·L-1·min-1
2 2
C.反应至6 min时,c(HO)=0.30 mol·L-1
2 2
D.反应至6 min时,HO 分解了50%
2 2
答案:C
解析:根据题目信息可知,0~6 min,生成22.4 mL O (标准状况),消耗0.002 mol
2
HO ,则v(HO )≈3.3×10-2 mol·L-1·min-1,A项正确;随反应物浓度的减小,反应速
2 2 2 2
率逐渐降低,B项正确;反应至6 min时,剩余0.002 mol H O ,此时c(HO )=0.20
2 2 2 2
mol·L-1,C项错误;反应至6 min时,消耗0.002 mol HO,转化率为50%,D项正确。
2 2
7.[2024·石家庄市质量检测]某密闭容器中含有X和Y,同时发生以下两个反应:①X
+Y⇌M+Q;②X+Y⇌N+Q。反应①的正反应速率v
1(正)
=k
1
c(X)·c(Y),反应②的
正反应速率v
2(正)
=k
2
c(X)·c(Y),其中k
1
、k
2
为速率常数。某温度下,体系中生成物
浓度(c)随时间(t)变化的曲线如图所示。下列说法正确的是( )
A.反应①的活化能大于反应②B.升高温度,4 s时容器中c(N)∶c(M)的比值减小
C.0~6 s内,X的平均反应速率v(X)=0.5 mol·L-1·s-1
D.10 s时,正反应速率v
1(正)
>v
2(正)
答案:D
解析:由曲线图可知,初始生成M的速率大于N,说明反应①是快反应,则反应①的
活化能小于反应②,A项错误;4 s时反应未达到平衡,升高温度,反应速率加快,则c
(M)减小,c(N)增大,故容器中c(N)∶c(M)的比值变大,B项错误;由图可知,
6 s时,c(M)=c(N)=3 mol·L-1,则0~6 s内X的浓度变化量为6 mol·L-1,v(X)
==1 mol·L-1·s-1,C项错误;由曲线图可知,初始生成M的速率大于N,则k>k ,10 s
1 2
时两个反应均达到平衡状态,由于v =kc(X)c(Y),v =kc(X)c(Y),则
1(正) 1 2(正) 2
正反应速率v >v ,D项正确。
1(正) 2(正)
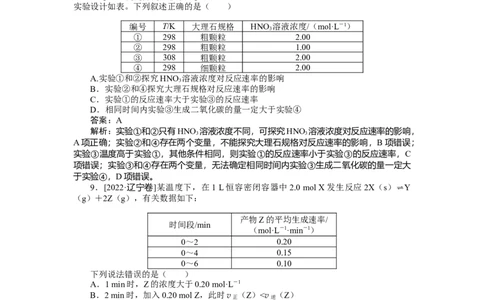
8.[2024·河南豫南九校联考]某探究小组利用如表四组实验来研究影响反应速率的因素,
实验设计如表。下列叙述正确的是( )
编号 T/K 大理石规格 HNO 溶液浓度/(mol·L-1)
3
① 298 粗颗粒 2.00
② 298 粗颗粒 1.00
③ 308 粗颗粒 2.00
④ 298 细颗粒 2.00
A.实验①和②探究HNO 溶液浓度对反应速率的影响
3
B.实验②和④探究大理石规格对反应速率的影响
C.实验①的反应速率大于实验③的反应速率
D.相同时间内实验③生成二氧化碳的量一定大于实验④
答案:A
解析:实验①和②只有HNO 溶液浓度不同,可探究HNO 溶液浓度对反应速率的影响,
3 3
A项正确;实验②和④存在两个变量,不能探究大理石规格对反应速率的影响,B项错误;
实验③温度高于实验①,其他条件相同,则实验①的反应速率小于实验③的反应速率,C
项错误;实验③和④存在两个变量,无法确定相同时间内实验③生成二氧化碳的量一定大
于实验④,D项错误。
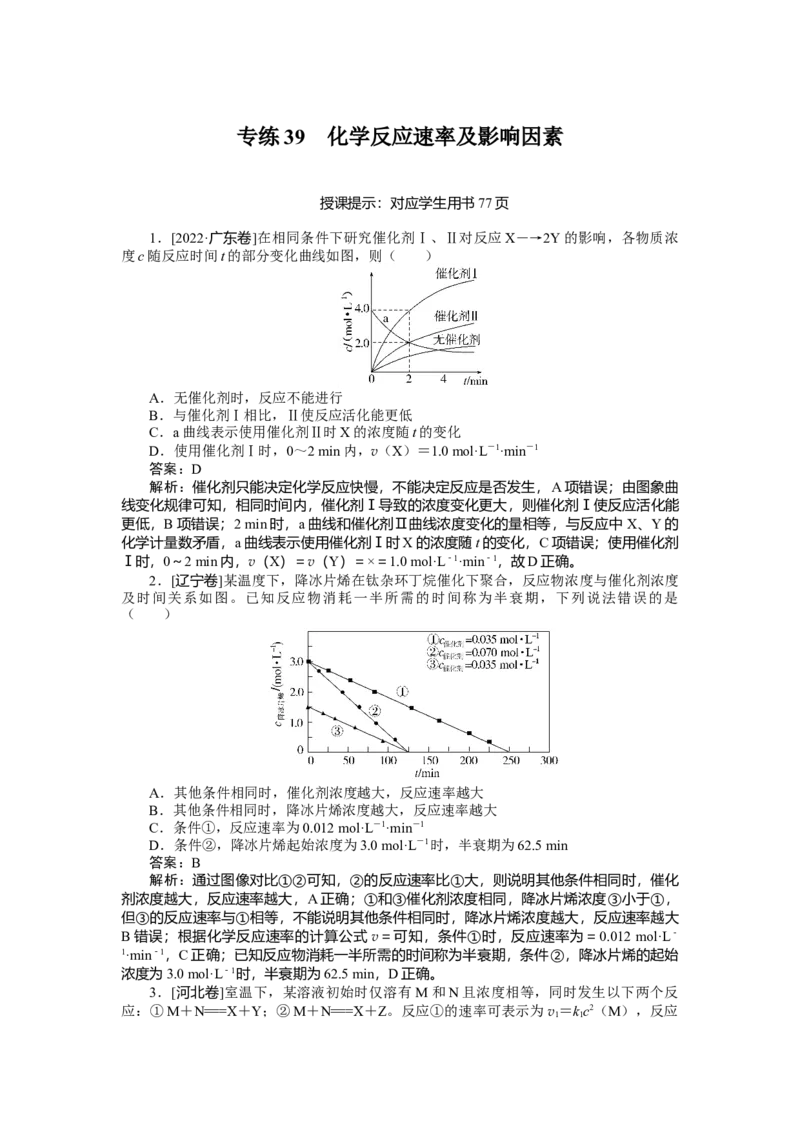
9.[2022·辽宁卷]某温度下,在1 L恒容密闭容器中2.0 mol X发生反应2X(s) ⇌Y
(g)+2Z(g),有关数据如下:
产物Z的平均生成速率/
时间段/min
(mol·L-1·min-1)
0~2 0.20
0~4 0.15
0~6 0.10
下列说法错误的是( )
A.1 min时,Z的浓度大于0.20 mol·L-1
B.2 min时,加入0.20 mol Z,此时v正 (Z)v (Z),B错误;反应生成的Y与Z的物质的量之比恒等于
正 逆
1∶2,反应体系中只有Y和Z为气体,相同条件下,体积之比等于物质的量之比,=,故
Y的体积分数始终约为33.3%,C正确;由B项分析可知5 min时反应处于平衡状态,此时
生成Z为0.6 mol,则X的转化量为0.6 mol,初始X的物质的量为2 mol,剩余X的物质的
量为1.4 mol,D正确。
10.CO(g)和HO(g)以1∶2体积比分别通入到体积为2 L的恒容密闭容器中进行
2
反应:CO(g)+H
2
O(g) ⇌CO
2
(g)+H
2
(g),得到如下三组数据:
起始时HO 平衡时CO 达到平衡所
实验组 温度/℃ 2 2
的量/mol 的量/mol 需时间/min
A 650 4.00 1.30 50
B 900 2.00 0.40 10
C 650 2.00 0.65 10
下列说法不正确的是( )
A.从实验数据分析,该反应的正反应是放热反应
B.实验A中,在0~10 min内,以v(H )表示的反应速率小于0.013 mol·(L·min)
2
-1
C.从生产效益分析,C组实验的条件最佳
D.比较实验B、C,说明C实验使用了更高效的催化剂
答案:B
解析:根据实验组B和C,升高温度,CO 的物质的量减少,说明升高温度,平衡向
2
逆反应方向移动,即正反应是放热反应,A正确;达到平衡时,v(CO)=mol·(L·min)
2
-1=0.013 mol·(L·min)-1,化学反应速率之比等于化学计量数之比,即 v(H )=v
2
(CO)=0.013 mol·(L·min)-1,随着反应的进行,反应物的浓度减小,化学反应速率降
2
低,0~10 min内,v(H )>0.013 mol·(L·min)-1,B错误;根据表格数据,实验C温度
2
低,投入量少,达到平衡时间短,因此从生产效益分析,C组实验的条件最佳,C正确;B
的温度高于C的温度,但达到平衡时间相等,说明C使用了比较高效的催化剂,D正确。