文档内容
2019 年长春中考化学
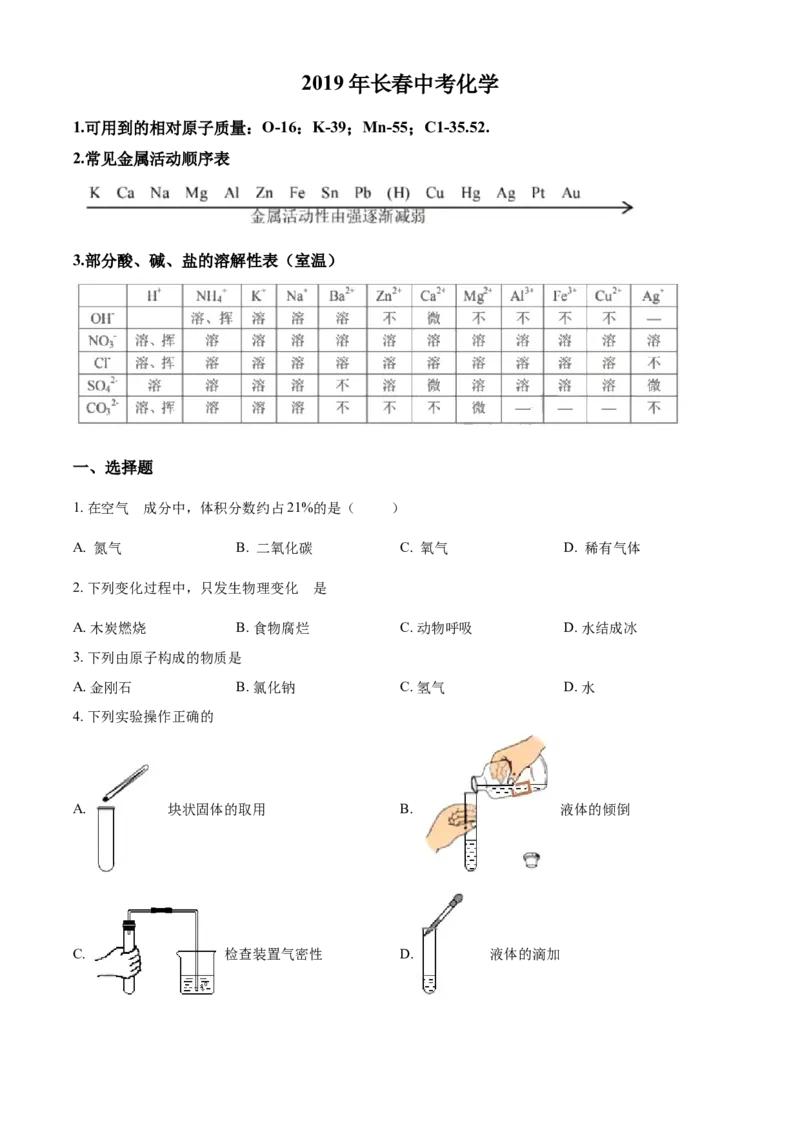
1.可用到的相对原子质量:O-16:K-39;Mn-55;C1-35.52.
2.常见金属活动顺序表
3.部分酸、碱、盐的溶解性表(室温)
一、选择题
的
1. 在空气 成分中,体积分数约占21%的是( )
A. 氮气 B. 二氧化碳 C. 氧气 D. 稀有气体
的
2. 下列变化过程中,只发生物理变化 是
A. 木炭燃烧 B. 食物腐烂 C. 动物呼吸 D. 水结成冰
3. 下列由原子构成的物质是
A. 金刚石 B. 氯化钠 C. 氢气 D. 水
4. 下列实验操作正确的
A. 块状固体的取用 B. 液体的倾倒
C. 检查装置气密性 D. 液体的滴加的
5. 下列说法中错误 是
A. 老年人缺钙容易引起骨质疏松
B. 用灼烧法可以区分羊毛和合成纤维
C. 煤、石油都是储量丰富的可再生能源
D. 工业废水排放前需做处理使之符合排放标准
6. ClO 是一种高效的水处理剂,其制备反应为:2NaClO+SO+H SO =2ClO +2X,下列说法错误的是
2 3 2 2 4 2
A. SO 的名称为二氧化硫 B. 该反应属于置换反应
2
C. X的化学式是NaHSO D. ClO 中氯、氧元素的质量比为71:64
4 2
7. 下列对有关事实的微观解释,不合理的是
A. 过氧化氢溶液是混合物——含有不同种分子
B. 水变为水蒸气时体积变大——水分子体积变大
C. 电解水属于化学反应——分子种类发生了改变
D. 水与过氧化氢的化学性质不同——分子构成不同
8. 下列有关物质用途的说法中正确的是
A. KNO 、NH Cl都能用作化肥 B. NaOH、CaO都能用作食品干燥剂
3 4
C. N、O 都能用作焊接金属的保护气 D. NaHCO 、Ca(OH) 都能用于治疗胃酸过多症
2 2 3 2
9. 下列说法中正确的是
A. 有发光放热现象的变化一定是燃烧 B. pH小于7的降雨一定是酸雨
C. 由同种元素组成的纯净物一定是单质 D. 生成盐和水的反应一定是中和反应
10. 下列实验中,能达到相应目的的是
A. 分离CaO和CaCO :将固体混合物高温煅烧
3
B. 制备CaCO :向CaCl₂溶液中通入足量的CO,过滤
3 2
C. 验证质量守恒定律:将锌粒与稀硫酸混合,比较混合前后溶液的质量
D. 除去CO 中混有的HCl和水蒸气:将气体依次通过足量的饱和NaHCO 溶液和浓硫酸
2 3
二、非选择题
11. 回答下列问题
(1)氢元素的符号是_____;
(2)3个钠离子可用符号表示为_____;
(3)水的化学式为_____;
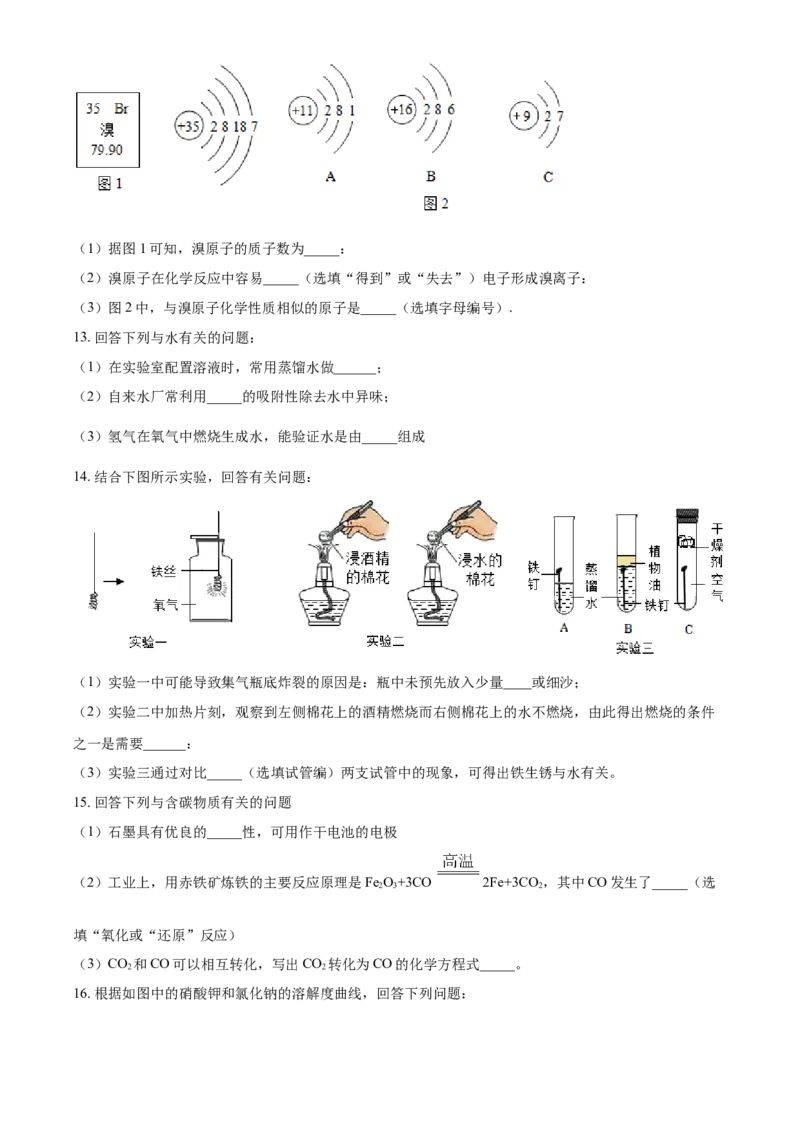
12. 根据下图信息,回答下列问题:(1)据图1可知,溴原子的质子数为_____:
(2)溴原子在化学反应中容易_____(选填“得到”或“失去”)电子形成溴离子:
(3)图2中,与溴原子化学性质相似的原子是_____(选填字母编号).
13. 回答下列与水有关的问题:
(1)在实验室配置溶液时,常用蒸馏水做______;
(2)自来水厂常利用_____的吸附性除去水中异味;
的
(3)氢气在氧气中燃烧生成水,能验证水是由_____组成
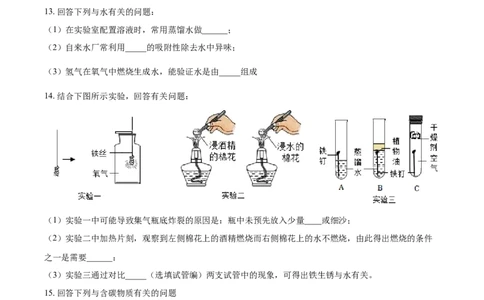
14. 结合下图所示实验,回答有关问题:
(1)实验一中可能导致集气瓶底炸裂的原因是:瓶中未预先放入少量____或细沙;
(2)实验二中加热片刻,观察到左侧棉花上的酒精燃烧而右侧棉花上的水不燃烧,由此得出燃烧的条件
之一是需要______:
(3)实验三通过对比_____(选填试管编)两支试管中的现象,可得出铁生锈与水有关。
15. 回答下列与含碳物质有关的问题
(1)石墨具有优良的_____性,可用作干电池的电极
(2)工业上,用赤铁矿炼铁的主要反应原理是Fe O+3CO 2Fe+3CO ,其中CO发生了_____(选
2 3 2
填“氧化或“还原”反应)
(3)CO 和CO可以相互转化,写出CO 转化为CO的化学方程式_____。
2 2
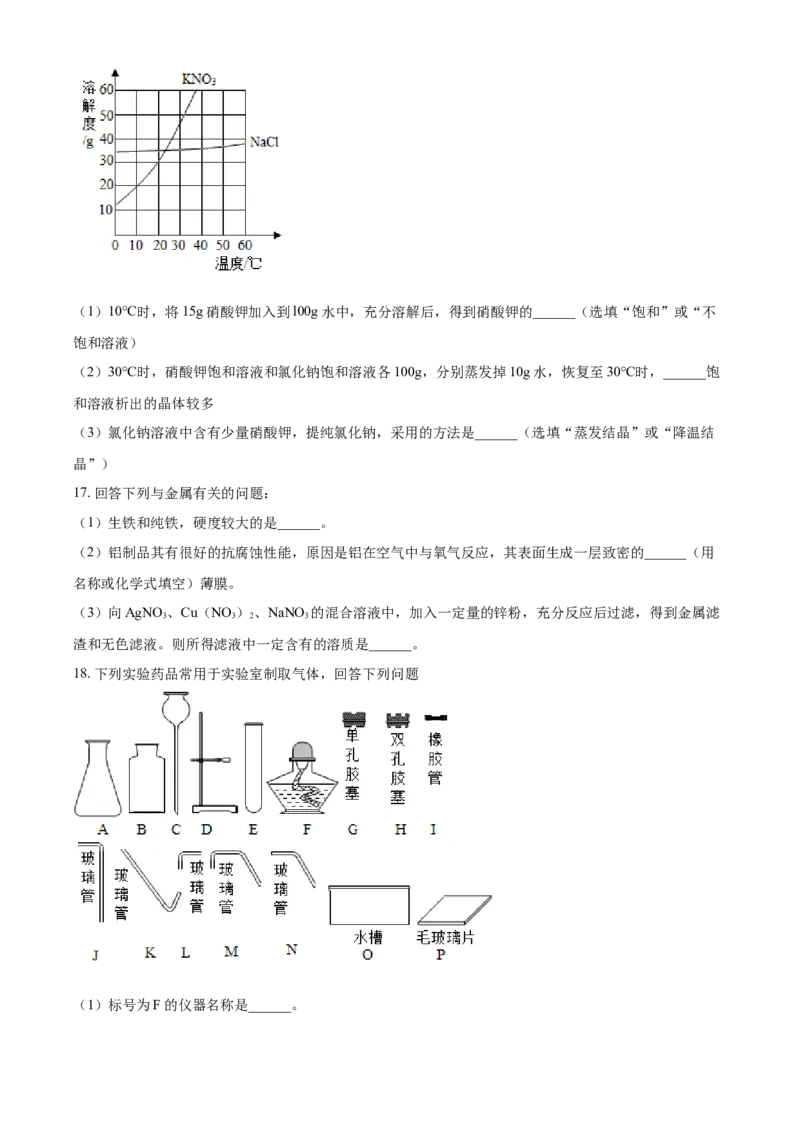
16. 根据如图中的硝酸钾和氯化钠的溶解度曲线,回答下列问题:(1)10℃时,将15g硝酸钾加入到l00g水中,充分溶解后,得到硝酸钾的______(选填“饱和”或“不
饱和溶液)
(2)30℃时,硝酸钾饱和溶液和氯化钠饱和溶液各100g,分别蒸发掉10g水,恢复至30℃时,______饱
和溶液析出的晶体较多
(3)氯化钠溶液中含有少量硝酸钾,提纯氯化钠,采用的方法是______(选填“蒸发结晶”或“降温结
晶”)
17. 回答下列与金属有关的问题:
(1)生铁和纯铁,硬度较大的是______。
(2)铝制品其有很好的抗腐蚀性能,原因是铝在空气中与氧气反应,其表面生成一层致密的______(用
名称或化学式填空)薄膜。
(3)向AgNO、Cu(NO )、NaNO 的混合溶液中,加入一定量的锌粉,充分反应后过滤,得到金属滤
3 3 2 3
渣和无色滤液。则所得滤液中一定含有的溶质是______。
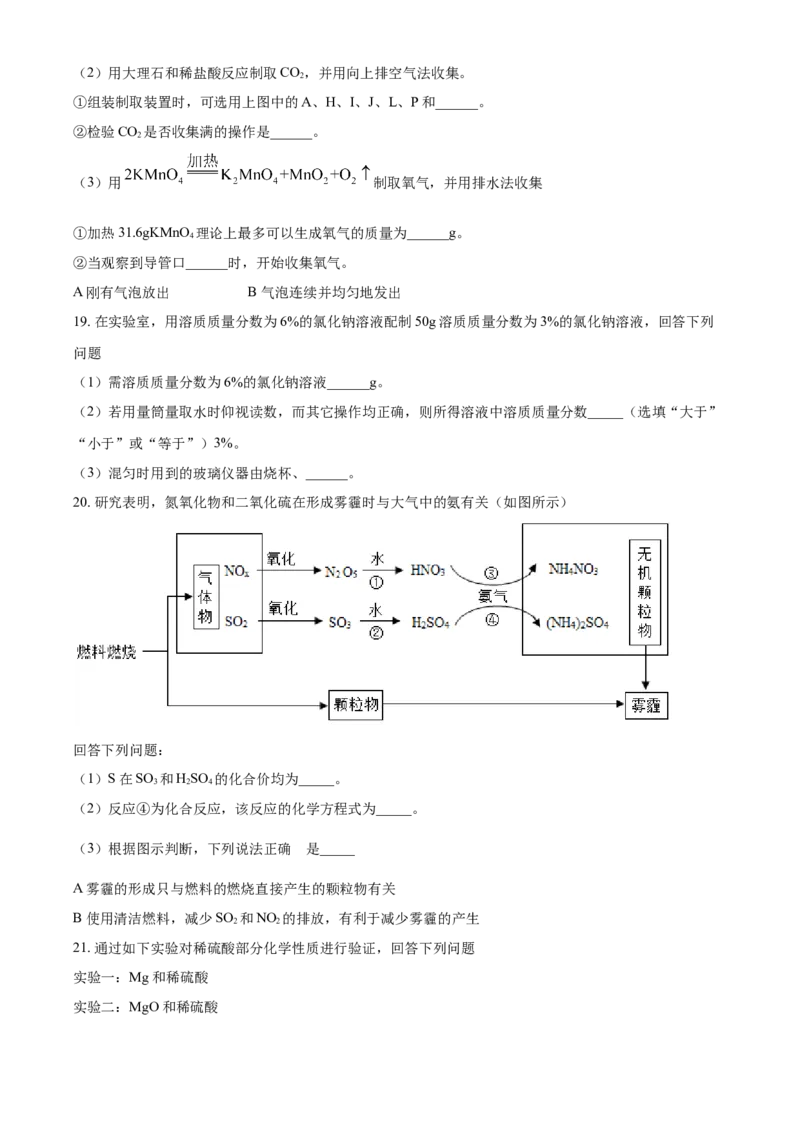
18. 下列实验药品常用于实验室制取气体,回答下列问题
(1)标号为F的仪器名称是______。(2)用大理石和稀盐酸反应制取CO,并用向上排空气法收集。
2
①组装制取装置时,可选用上图中的A、H、I、J、L、P和______。
②检验CO 是否收集满的操作是______。
2
(3)用 制取氧气,并用排水法收集
①加热31.6gKMnO 理论上最多可以生成氧气的质量为______g。
4
②当观察到导管口______时,开始收集氧气。
A 刚有气泡放出 B 气泡连续并均匀地发出
19. 在实验室,用溶质质量分数为6%的氯化钠溶液配制50g溶质质量分数为3%的氯化钠溶液,回答下列
问题
(1)需溶质质量分数为6%的氯化钠溶液______g。
(2)若用量筒量取水时仰视读数,而其它操作均正确,则所得溶液中溶质质量分数_____(选填“大于”
“小于”或“等于”)3%。
(3)混匀时用到的玻璃仪器由烧杯、______。
20. 研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如图所示)
回答下列问题:
(1)S在SO 和HSO 的化合价均为_____。
3 2 4
(2)反应④为化合反应,该反应的化学方程式为_____。
的
(3)根据图示判断,下列说法正确 是_____
A 雾霾的形成只与燃料的燃烧直接产生的颗粒物有关
B 使用清洁燃料,减少SO 和NO 的排放,有利于减少雾霾的产生
2 2
21. 通过如下实验对稀硫酸部分化学性质进行验证,回答下列问题
实验一:Mg和稀硫酸
实验二:MgO和稀硫酸实验三:Ba(NO ) 溶液和稀硫酸
3 2
实验四:KOH溶液和稀硫酸
(1)实验三中发生反应的化学方程式为_____。
(2)实验四无明显现象,再将打磨过的铁丝浸入该试验后的溶液中,仍无明显现象,据此_____(选填
“能”或“不能”)验证KOH溶液和H₂SO 发生反应
4
(3)将上述所有实验后的溶液混合,并进行如下实验:
①写出滤液a中所含溶质的所有可能情况_____。
②分析上述实验,下列说法正确的是_____
A 用白色沉淀A一定能除去MgC1 溶液中的少量盐酸
2
B 用白色沉淀B能检验CaCl 溶液中是否含有盐酸
2
C 用滤液b与适量的KSO 溶液混合,过滤,制备KNO 溶液
2 4 3
D 向溶液c中加入过量的NaOH溶液或过量的Na₂CO 溶液都有明显的现象
3
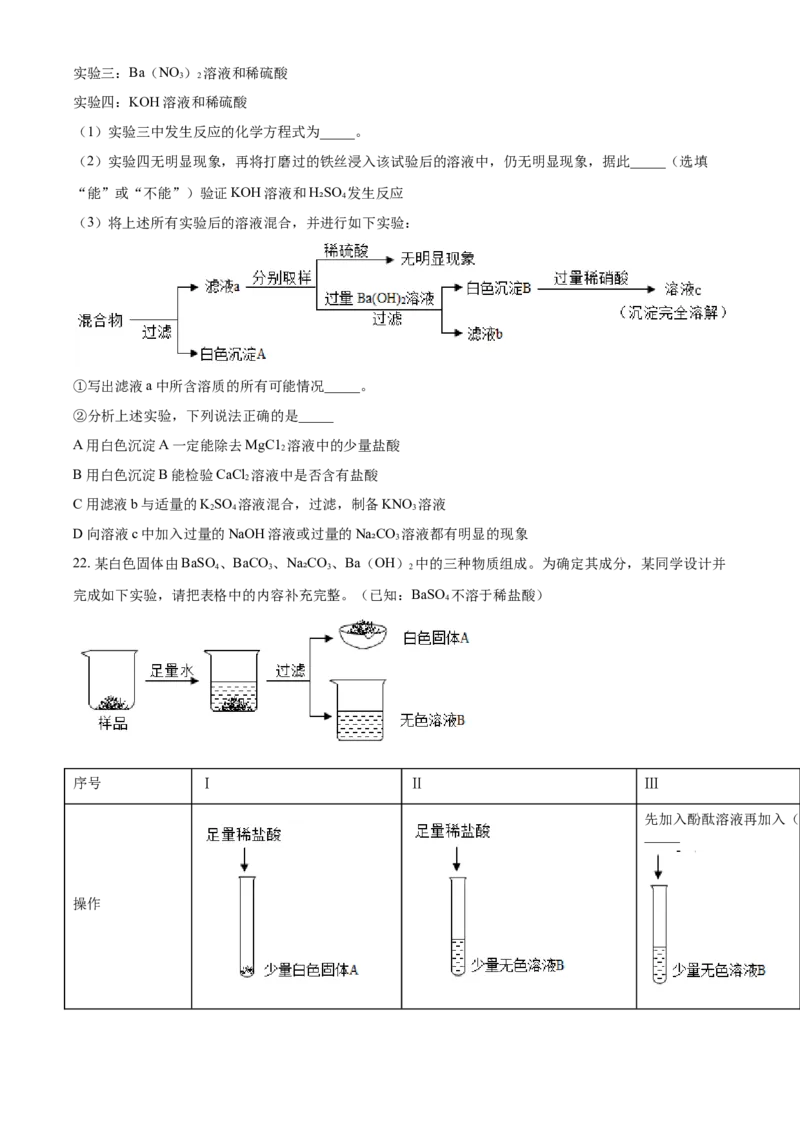
22. 某白色固体由BaSO、BaCO 、Na₂CO 、Ba(OH) 中的三种物质组成。为确定其成分,某同学设计并
4 3 3 2
完成如下实验,请把表格中的内容补充完整。(已知:BaSO 不溶于稀盐酸)
4
序号 Ⅰ Ⅱ Ⅲ
先加入酚酞溶液再加入(3
_____
操作产生白色沉淀,溶液最终显
现象 有气泡产生,固体有剩余 有气泡产生
(4)_____色
原白色固体中含有NaCO;生成气
结论或解释 原白色固体中含有(1)_____ 2 3 原白色固体中含有BaCO
体的化学方程式为(2)_____ 3