文档内容
《化学》三色速记手册
(四)影响 Ksp的因素
Ksp与其他化学平衡常数一样,只与难溶电解质的性质和温度有关,而与沉淀的量和溶液中
离子浓度的变化无关。
(五)溶度积规则
1.离子积Q:表示在难溶电解质溶液中,任意情况下各离子相对浓度幂的乘积。
Q > K 平衡向左移动,沉淀析出;
sp
Q = K 处于平衡状态,饱和溶液;
sp
Q < K 平衡向右移动,无沉淀析出;
sp
2.沉淀的溶解
沉淀溶解的必要条件:Q < K
sp
减小离子浓度的办法有下面几种:
①生成弱电解质使沉淀溶解
②氧化还原反应使沉淀溶解
③生成配合物使沉淀溶解
3.分级沉淀
如果溶液中含有两种或两种以上的离子,都能与同一种试剂生成难溶电解质沉淀,当向溶液
中加入这种沉淀剂时就会先后生成几种沉淀,这种先后沉淀的现象称为分级沉淀。
率先满足Q> K 的难溶电解质沉淀先析出。
sp
4.沉淀的转化
【考点八】氧化还原平衡
(一)原电池
1.电极反应
原电池中,电子流出的一极为负极,负极上发生氧化反应;电子流入的一极为正极,正极
上发生还原反应。
Zn负极:Zn=Zn2++2e(氧化反应)
Cu正极:Cu2++2e=Cu(还原反应)
将两个电极反应相加得到中反应,称为电池反应。
电池反应:Zn+Cu2+=Zn2++Cu
(二)电解池(外加电源的是电解池)
电解池:把电能转化为化学能的装置
阳极:2Cl--2e-=Cl↑
2
第 24 页《化学》三色速记手册
阴极:Cu2++2e-=Cu
移动方向
电子
原电池 负→正; 电解池 阳→阴
离子
原电池:正正负负; 电解池:阴阳相吸
(三)电池
1.一次电池—碱性锌锰干电池
干电池的电压通常约为1.5V,不能充电。负极是Zn,正极是MnO
2
负极反应:Zn+2OH--2e=Zn(OH)(负极质量增大)
2
正极反应:2MnO+2HO+2e-= 2MnOOH+2OH-
2 2
总反应:Zn+2MnO+2HO=Zn(OH)+2MnOOH
2 2 2
2.二次电池(或可充电电池)
铅蓄电池是最常见的二次电池,可以放电和充电,负极材料是Pb,正极材料是PbO,电解
2
质溶液是HSO 溶液。
2 4
①放电时的反应
负极:Pb+SO2-- 2e=PbSO(负极质量增大)
4 4
正极:PbO+4H++SO2-+2e=PbSO+2HO
2 4 4 2
电池总反应:Pb+PbO+2HSO=2PbSO+2HO
2 2 4 4 2
②充电时的反应
阴极:PbSO+2e-=Pb+SO2-
4 4
阳极:PbSO+2HO-2e=PbO+4H++SO2-
4 2 2 4
电池总反应:2PbSO+2HO=Pb+PbO+2HSO
4 2 2 2 4
(3)燃料电池
燃料电池由3个主要部分组成:
负极(燃料电极);
正极(氧气或空气电极);
电解质溶液。
两电极材料均为惰性电极,电极本身不发生反应,而是由引入到两电极上的燃料和氧化剂发
生反应。
第四章 金属及非金属化合物
【考点一】钠及其化合物
(一)钠的物理性质
导电、
颜色 状态 硬度 密度 熔点
导热性
银白色、有 小,可以用 р(水)>р(钠)
固体 97.8℃ 良好
金属光泽 小刀切割 >р(煤油)
(二)钠的化学性质
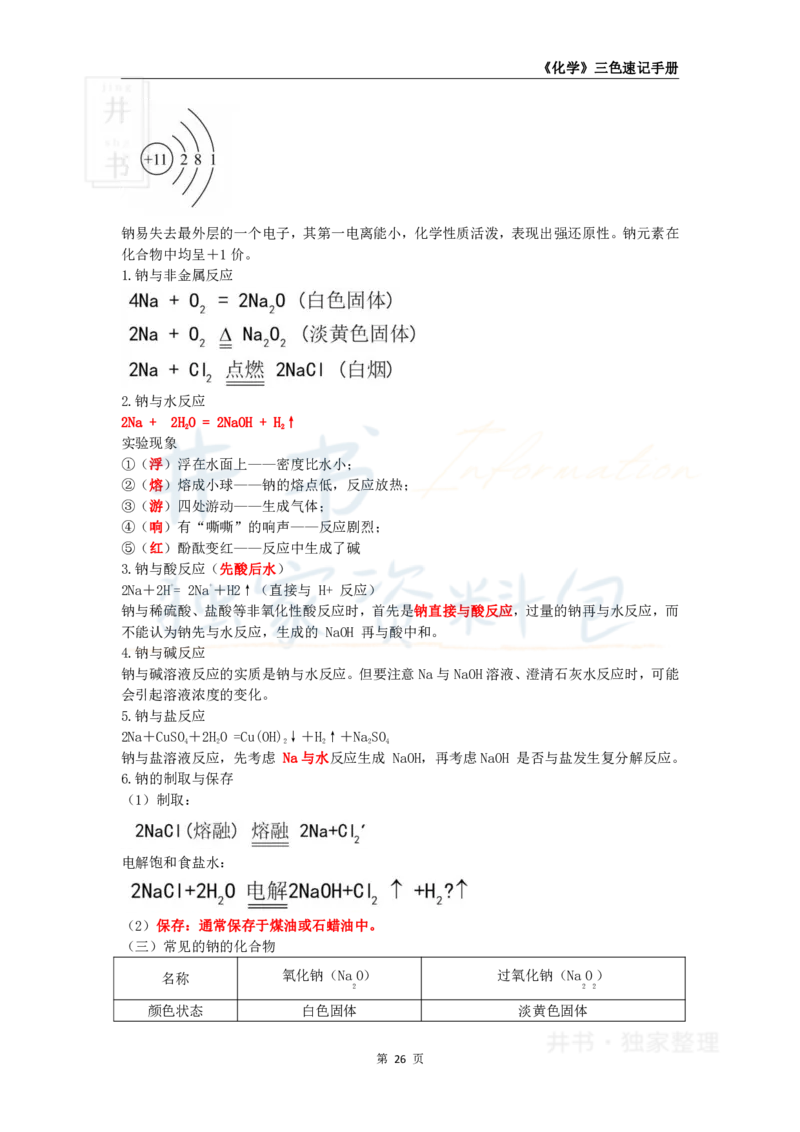
钠的原子结构
第 25 页《化学》三色速记手册
钠易失去最外层的一个电子,其第一电离能小,化学性质活泼,表现出强还原性。钠元素在
化合物中均呈+1价。
1.钠与非金属反应
2.钠与水反应
2Na + 2HO = 2NaOH + H↑
2 2
实验现象
①(浮)浮在水面上——密度比水小;
②(熔)熔成小球——钠的熔点低,反应放热;
③(游)四处游动——生成气体;
④(响)有“嘶嘶”的响声——反应剧烈;
⑤(红)酚酞变红——反应中生成了碱
3.钠与酸反应(先酸后水)
2Na+2H+= 2Na++H2↑(直接与 H+ 反应)
钠与稀硫酸、盐酸等非氧化性酸反应时,首先是钠直接与酸反应,过量的钠再与水反应,而
不能认为钠先与水反应,生成的 NaOH 再与酸中和。
4.钠与碱反应
钠与碱溶液反应的实质是钠与水反应。但要注意Na与NaOH溶液、澄清石灰水反应时,可能
会引起溶液浓度的变化。
5.钠与盐反应
2Na+CuSO+2HO =Cu(OH)↓+H↑+NaSO
4 2 2 2 2 4
钠与盐溶液反应,先考虑 Na与水反应生成 NaOH,再考虑NaOH 是否与盐发生复分解反应。
6.钠的制取与保存
(1)制取:
电解饱和食盐水:
(2)保存:通常保存于煤油或石蜡油中。
(三)常见的钠的化合物
名称 氧化钠(NaO) 过氧化钠(NaO)
2 2 2
颜色状态 白色固体 淡黄色固体
第 26 页《化学》三色速记手册
阴阳离子个数比 1:2 1:2
类型 碱性氧化物 金属氧化物
氧元素化合价 -2 -1
与水反应 NaO+HO=2NaOH 2NaO+2HO=4NaOH+O↑
2 2 2 2 2 2
与CO 反应 NaO+CO=NaCO 2NaO+2CO=2NaCO+O
2 2 2 2 3 2 2 2 2 3 2
与盐酸反应 NaO+2HCl=2NaCl+HO 2NaO+4HCl=4NaCl+O↑+2HO
2 2 2 2 2 2
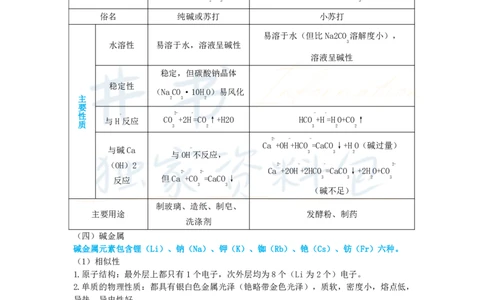
名称 碳酸钠(NaCO) 碳酸氢钠(NaHCO)
2 3 3
俗名 纯碱或苏打 小苏打
易溶于水(但比Na2CO 溶解度小),
水溶性 易溶于水,溶液呈碱性 3
溶液呈碱性
稳定,但碳酸钠晶体
稳定性
(NaCO·10HO)易风化
主 2 3 2
要
性 + 2- + - +
质 与H反应 CO +2H=CO↑+H2O HCO +H=HO+CO↑
3 2 3 2 2
2+ - -
Ca +OH+HCO =CaCO↓+HO(碱过量)
与碱Ca -
与OH不反应, 3 3 2
(OH)2 2+ - - 2-
Ca +2OH+2HCO =CaCO↓+2HO+CO
2+ 2-
反应 但Ca +CO =CaCO↓ 3 3 2 3
3 3
(碱不足)
制玻璃、造纸、制皂、
主要用途 发酵粉、制药
洗涤剂
(四)碱金属
碱金属元素包含锂(Li)、钠(Na)、钾(K)、铷(Rb)、铯(Cs)、钫(Fr)六种。
(1)相似性
1.原子结构:最外层上都只有1个电子,次外层均为8个(Li为2个)电子。
2.单质的物理性质:都具有银白色金属光泽(铯略带金色光泽),质软,密度小,熔点低,
导热、导电性好。
3.单质的化学性质:都能与氧气和水反应,生成物都是含R+(R为碱金属元素)的离子化
合物。
4.最高价氧化物对应的水化物(ROH)均是强碱,ROH 的碱性逐渐增强。
(2)特殊性
1.锂的密度比煤油小,不能保存在煤油中,通常密封在石蜡里。
2.碱金属 Li -Cs 的密度呈增大趋势,但 ρ(Na)>ρ(K)。
3.酸式盐的溶解度一般比相应的正盐大,但S(Na2CO3)>S(NaHCO3)。
4.锂易与氮气反应(生成Li3N)。
5.锂的熔点最高,金属性最弱,因而锂与水反应较慢且反应时锂并不熔化。
6.碱金属单质及其离子的焰色反应呈现不同的颜色。
第 27 页《化学》三色速记手册
7.试剂瓶中的药品取出后,一般不能放回原瓶,但金属Na、K等需立即放回原瓶。
(3)焰色反应
1.常见元素的焰色
钠:黄色
钾:紫色(透过蓝色钴玻璃)。
【考点二】镁、铝及其化合物
(一)镁、铝单质
镁 铝
银白色固体,较软,密度 2.70
3
银白色固体,质软,密度 1.738 g/cm,熔点
物理性质 g/cm3,熔点 660.4℃,沸点
645 ℃,沸点1090 ℃。
2467 ℃。
以化合态形式存在,主要以铝
存在 以化合态形式存在,主要存在于地壳和海水中
土矿存在
可用来制造合金、导线、电缆、
用途 可用来制造合金
防锈油漆、食品包装
1.与非金属反应
2.与酸反应
Mg + 2H+ = Mg2+ + H↑
2
与稀HNO 反应生成 Mg(NO)、NOx、HO
3 3 2 2
2Al+6H+=2Al3++3H↑
2
在冷的浓HSO 或浓HNO 中钝化
2 4 3
3.与氧化物反应
(二)氧化镁和氧化铝
氧化物 MgO AlO
2 3
工业制备 铝土矿→AlO
2 3
白色固体,熔点高,
重要物理性质 白色固体,熔点高,密度较小
密度小
第 28 页《化学》三色速记手册
HO MgO+HO=Mg(OH) 很慢 不溶解,也不反应
2 2 2,
主要
2+ + 3+
化学 H+ MgO+2H+=Mg +HO AlO+6H=2Al +3HO
2 2 3 2
性质
- - -
OH 不反应 AlO+2OH =2AlO +HO
2 3 2 2
制造耐火、耐高温器材;
重要用途 制造耐火、耐高温器材
工业冶炼铝
(三)氢氧化镁和氢氧化铝
1.氢氧化镁
Mg(OH) 是一种难溶于水的中强碱,其饱和溶液能使酚酞试液变为浅红色。
2
(1)与酸反应:Mg(OH)+2H+= Mg2++2HO
2 2
(2)热稳定性差:
(3)溶解平衡:可溶于浓NHCl等盐溶液中
4
Mg(OH)+2NH+ =Mg2++2NH·HO
2 4 3 2
2.氢氧化铝
Al(OH) 是难溶的白色胶体物质,不能使酚酞试液变色。
3
它是典型的两性氢氧化物,既能跟强酸反应,又能跟强碱反应。
(1)两性:
Al(OH)+3H+ =Al3++3HO
3 2
Al(OH)+OH- =AlO-+2HO 或 Al(OH)+OH- =[Al(OH)]-
3 2 2 3 4
(2)两式电离平衡:
AlO-+H++HO ⇌ Al(OH) ⇌ Al3++3OH-
2 2 3
酸式电离 碱式电离
(3)热稳定性:
(四)铝及其化合物之间的相互转化
(五)铝的其他化合物及铝合金
1.明矾
化学式:KAl(SO)·12HO
4 2 2
属类:复盐(由两种不同的金属阳离子和一种酸根阴离子构成的化合物)。
明矾净水原理:
KAl(SO)·12HO溶解于水后发生反应
4 2 2
Al3++3HO ⇋ Al(OH)(胶体)+3H+
2 3
形成的Al(OH) 胶体吸附能力强
3
2.铝合金及其制品
(1)合金指的是由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的
物质。
(2)合金有比它的成分金属更优良的性质。
如:
①合金的熔点一般比它的各成分金属的低;
第 29 页《化学》三色速记手册
②合金的硬度一般比它的各成分金属的大;
③合金的化学性质也因成分金属的不同而不同。
3.金属铝与镁、铜、硅等金属或非金属熔合形成铝合金。铝合金具有密度小、强度高、塑性
好、易于成型、制造工艺简单、成本低廉等特点,并且有一定的抗腐蚀能力。铝合金可用于
建筑业、容器、包装业、交通运输、电子行业,并广泛用于制造飞机构件等。
【考点三】铁、铜及其化合物
(一)铁、铜的物理性质
铁元素在周期表中位于第四周期第Ⅷ族,属于过渡金属。铁的粉末为黑色,纯净的铁块是银
白色金属,不仅有金属的通性(良好的导热性、延展性),而且易被磁铁吸引,也可被磁化。
铜元素在周期表中的位置是第四周期第IB族,属于过渡金属。铜是一种有金属光泽的紫红
色金属,质软,具有良好的导电导热性(仅次于银)、延展性。铜属于重金属、有色金属、
常见金属、不能被磁铁吸引
(二)铁、铜的化学性质
1.铁的化学性质
当铁与弱氧化剂(如盐酸、硫酸铜溶液等)反应时,只能失去2个电子形成Fe2+,当铁与强
氧化剂(如氯气、硝酸等)反应时,失去3个电子而形成Fe3+
(1)与非金属反应
由此可比较非金属单质的氧化性强弱:Cl、O 的氧化性比S强。
2 2
(2)与水蒸气反应(与冷、热水均不反应)
(3)与酸反应
与非氧化性酸:Fe+2H+=Fe2++H↑
2
与氧化性酸:
①在冷的浓HNO 或浓HSO 中钝化
3 2 4
②反应时,酸过量的产物为Fe3+
Fe+4HNO(稀)= Fe(NO)+NO↑+2HO
3 3 3 2
(4)与盐反应
Fe与CuSO 溶液反应的离子方程式:Fe+Cu2+ =Cu+Fe2+
4
Fe与FeCl 溶液反应的离子方程式:Fe+2Fe3+= 3Fe2+
3
2.铜的化学性质
(1)与非金属单质反应
(2)通入O 时,能与盐酸、硫酸反应
2
第 30 页《化学》三色速记手册
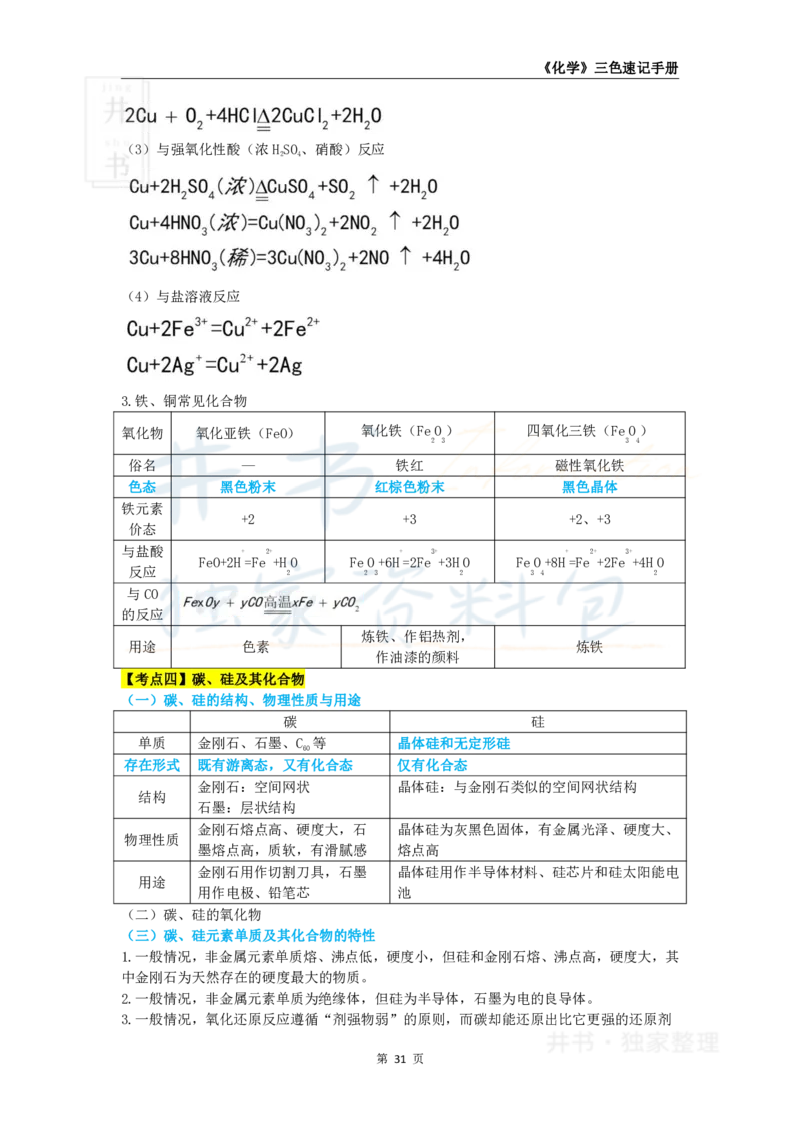
(3)与强氧化性酸(浓HSO、硝酸)反应
2 4
(4)与盐溶液反应
3.铁、铜常见化合物
氧化物 氧化亚铁(FeO) 氧化铁(FeO) 四氧化三铁(FeO)
2 3 3 4
俗名 — 铁红 磁性氧化铁
色态 黑色粉末 红棕色粉末 黑色晶体
铁元素
+2 +3 +2、+3
价态
与盐酸 + 2+ + 3+ + 2+ 3+
FeO+2H=Fe +HO FeO+6H=2Fe +3HO FeO+8H=Fe +2Fe +4HO
反应 2 2 3 2 3 4 2
与CO
的反应
炼铁、作铝热剂,
用途 色素 炼铁
作油漆的颜料
【考点四】碳、硅及其化合物
(一)碳、硅的结构、物理性质与用途
碳 硅
单质 金刚石、石墨、C 等 晶体硅和无定形硅
60
存在形式 既有游离态,又有化合态 仅有化合态
金刚石:空间网状 晶体硅:与金刚石类似的空间网状结构
结构
石墨:层状结构
金刚石熔点高、硬度大,石 晶体硅为灰黑色固体,有金属光泽、硬度大、
物理性质
墨熔点高,质软,有滑腻感 熔点高
金刚石用作切割刀具,石墨 晶体硅用作半导体材料、硅芯片和硅太阳能电
用途
用作电极、铅笔芯 池
(二)碳、硅的氧化物
(三)碳、硅元素单质及其化合物的特性
1.一般情况,非金属元素单质熔、沸点低,硬度小,但硅和金刚石熔、沸点高,硬度大,其
中金刚石为天然存在的硬度最大的物质。
2.一般情况,非金属元素单质为绝缘体,但硅为半导体,石墨为电的良导体。
3.一般情况,氧化还原反应遵循“剂强物弱”的原则,而碳却能还原出比它更强的还原剂
第 31 页《化学》三色速记手册
4.非金属单质一般不能生成H2,但C、Si均可:
5.一般情况,较活泼金属+酸 = 盐+氢气,然而Si是非金属,却能与氢氟酸发生反应:
6.一般情况,酸性氧化物+碱 = 盐+水,SiO 是酸性氧化物,却能与氢氟酸反应
2
SiO+4HF =SiF↑+2HO
2 4 2
7.无机酸一般能溶于水,而HSiO 却难溶于水。
2 3
8.HCO 的酸性强于HSiO 且生成的硅酸为沉淀,所以有 NaSiO+CO+HO=HSiO↓+NaCO,
2 3 2 3 2 3 2 2 2 3 2 3
【考点五】氯、溴、碘及其化合物
(一)氯气的性质和用途
1.物理性质
通常氯气为黄绿色、有刺激性气味,密度比空气大的有毒气体,易液化。
25 ℃时,1体积水约溶解 2 体积氯气,其水溶液俗称氯水,为淡黄绿色。
2.化学性质
氯气的化学性质很活泼,是一种活泼的非金属单质,是强氧化剂
(1)与金属反应(与变价金属反应,将金属氧化至高价态)
(2)与非金属反应
(3)与水反应
(4)与碱反应
Cl+2NaOH=NaCl+NaClO+HO
2 2
2Cl+2Ca(OH)=CaCl+Ca(ClO)+2HO
2 2 2 2 2
第 32 页