文档内容
成都市二00八年高中阶段教育学校统一招生考试试卷
(含成都市初三毕业会考)
化学
第Ⅰ卷(选择题,共36分)
一、选择题(本题包括12个小题,每小题3分,共36分。每小题只有一个选项符合题意。)化学
课上,每个学习小组各有一瓶无标签的无色透明液体。请你和同学们一起对此液体进行探究,
并完成下列1一4题。
1.某小组同学打开瓶盖后没有闻到特殊气味。可推测该液体不可能是( )
A.食盐水 B.纯净水 C.澄清石灰水 D.白醋
2. 从组成上看,这些液体不可能属于( )
A. 混合物 B.纯净物 C.含有Cu2+的盐溶液 D.氧化物
3.几组同学分别取少量液体进行如下实验,其中一定发生化学变化的是( )
A.加热——有水汽产生 B.通入CO ——产生白色沉淀
2
C.加入活性炭——振荡后变浑浊 D. 滴加植物油——静置后分层
4.若某小组的液体为只含有一种溶质的溶液,加入少量MnO 后产生能使带火星的木条复燃的
2
气体。则下列说法不正确的是( )
A.反应前后MnO 的化学性质不变
2
B.该反应的化学方程式为2H O ===H O+O
2 2 2 2
C.产生的气体高温时能与磷、硫等发生氧化反应
D.如果用右图装置收集该气体,则气体应从b端进入
5.比较煤与石油,下列说法正确的是( )
A.都是化石燃料 B.都是含有碳元素的有机物
C.综合利用的途径相同 D.都可直接用作家用燃料
6.丙氨酸的结构简式为 丙氨酸的说法不正确的是( )
A.含有C、H、O、N四种 元素 B.每个分子中含有三个碳原子
C.是一种离子化合物 D.化学式可表示为C H O N
3 7 2
7.硫离子的结构示意图如右图所示,与硫原子比较,二者( )
A.核内质子数相同 B.核外电子数相同
C.化合价相同 D.化学性质相同
8.通过化学课的学习,成语“细水长流”可理解为( )
A.在家用细细的长流水洗衣服或刷牙
B.节约每一滴水,形成“细水长流”的水资源C.地球淡水储量丰富,可供人类永久使用
D.水龙头漏水可让其“细水长流”,方便使用
9.某同学在实验室闻到类似碘酒的气味,寻“味”而去,发现实验台上棕色瓶内装有固体碘。据
此不能说明的是( )
A.碘易升华 B.分子在不断运到 C .分子间有间隙 D.分子可以再分
10.衣服上沾有碘极难洗净。有下表分析,在家庭去碘污渍最好选用( )
溶剂
溶质
水 酒精 苯(一种有机物,有毒) 汽油
碘 难溶 可溶 易溶 易溶
A.水 B.苯 C.汽油 D.碘酒
11.成都水陵出土的重要文物有白玉谥宝、玉带、银钵、铁猪及铁牛等,其中金属制品保存较好
的可能是( )
A. 玉带 B. 银钵 C. 铁猪 D. 铁牛
12.下表是某同学整理的实验报告。其中错误的是( )
实验内容 加入试剂或方法
A 鉴别羊毛纤维与涤纶 抽丝灼烧
B 除去O 中的CO 通过盛有CuO的硬质玻璃管,加热
2
C 区分硬水和软水 加肥皂液
D 分离沙子和NaCl的固体混合物 溶解、过滤、蒸发和结晶
第Ⅱ卷(非选择题,共54分)
总分人
题号 二 三 四 五 总分
编号
得分
可能用到的相对原子质量:H一1 C一12 N一14 O一16 S一32 Cl一35.5 Na一23
Ag一108 Ba一137
二、(本题包括2个小题,每空1分,共11分)
13.(5分)麻婆豆腐在清朝末年便被列为成都经 典名菜。其
配料见下表,此菜富含动植物蛋白质、钙、磷、铁、 维生素及碳
水化合物。具有温中益气、解毒润燥等功效。
⑴原料中提供蛋白质较多的是 等(填 一种即可)。
⑵此处钙、磷、铁主要指 (填“单质”“化合物”或“元素”),其中磷、铁的元素符
号是 、 。
⑶将生石膏 放进火中烙烧是制作石膏豆腐的一个关键工序。生石膏加热至163℃,失去结晶水变成熟石膏(CaSO )。该反应的化学方程式是
4
。
14(. 6分)2008年5月5日早上,上海某路公交车上发生自燃,当场死亡3人,据调查,造成火灾
的主要原因是乘客携有易燃物。
⑴乘客携带的易燃物可能是 (举出一种生活中常见易燃物名称)
⑵自燃是指可燃物在空气中没有外来火源的作用,靠自热或外热而发生燃烧的现象。因此,
造成此次火灾的另一原因可能是 。
⑶当汽车有焦味儿,冒出蓝色或黑色浓烟时,即是自燃的先兆。在①大声呼救 ②马上停车
③关闭电源 ④抢救车内财物 ⑤取出灭火器,给油箱和燃烧部分灭火,避免爆炸 ⑥尽快远
离 现 场 逃 生 等 项 措 施 中 , 你 认 为 司 机 此 时 最 应 该 做 的 三 件 事 是
(填代码)。
⑷灭火器是必须随车携带的装备。则车用灭火器最好使用 (填“泡沫”或
“干粉”)灭火器。
⑸作为目击者,发现火灾后,应及时拨打火警电话 (填电话号码)。
⑹ 灾 难 发 生 后 , 最 重 要 的 是 生 命 安 全 。 若 乘 车 人 员 衣 服 被 火 烧 着 , 可
。
三(本题只有1个小题,共10分)
15.(10分)“5.12汶川大地震”发生后,药品是灾区最急需的救助物资之一。如图是一种救
治伤员常用药品说明书的一部分,请仔细阅读并回答有关问题。
⑴不同规格的该药品中葡萄糖的含量 (填“相同”或“不同”)。(假设溶液
密度为1g/cm3)
⑵由【含量测定】数据,计算 1mL 硝酸银滴定液中硝酸银的质量。(滴定反应为
NaCl+AgNO ==AgCl↓+NaNO )
3 3⑶【药理】药品中, (填物质名称)是人体主要的能量来源之一;钠、氯
(填“分子”、“原子”或“离子”)对维持人体正常的血液和细胞外液的容量和渗透压起着
非常重要的作用。
取适量该药品,滴入紫色石蕊试液,则看到的现象是 。
四、(本题包括2个小题,方程式2分,其余每空1分,共22分)
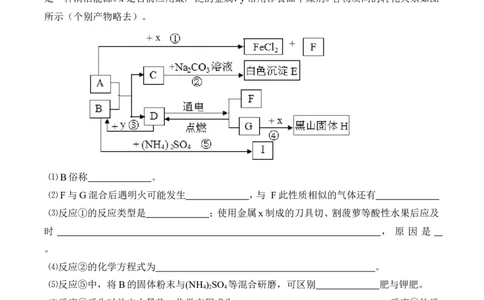
16(. 15分)A、B可发生中和反应,D是生活中最常见的液体。通常情况下,F、G、I为气体,且F
是一种清洁能源。x是目前应用最广泛的金属,y常用作食品干燥剂。各物质间的转化关系如图
所示(个别产物略去)。
⑴B俗称 。
⑵F与G混合后遇明火可能发生 ,与 F此性质相似的气体还有
⑶反应①的反应类型是 ;使用金属x制成的刀具切、割菠萝等酸性水果后应及
时 , 原 因 是
。
⑷反应②的化学方程式为 。
⑸反应⑤中,将B的固体粉末与(NH ) SO 等混合研磨,可区别 肥与钾肥。
4 2 4
⑹反应③反生时放出大量热,化学方程式为 。反应④的反
应条件是 ,实验现象是
。化学是研究物质及其变化的科学。比
较反③、④,你对化学变化的认识是:(写2条)
、
17.(7分)实验课上,同学们利用下列装置进行气体制备的学习。⑴反应原理:
用装置A制取
O 的化学方程
2
式为
。
⑵反应装置:
制取二氧化碳的反生装置是 (填“A”、“B”或“C”),其优点是
。
⑶除杂干燥:⑵中制得的CO 中含有少量的HCl和H O。某同学欲用氢氧化钠固体进行除杂
2 2
干燥,对此你的评价是 。
⑷气体收集:实验收集O 和CO 都能用的装置是 。(填序号)
2 2
⑸检验:类比O 和CO 的验满操作,检验氮气是否收集满的方法:
2 2
。
五、(本题只有1个小题,每空1分,共11分)
18(. 11分)某市热电厂使用的燃料是含硫较多的煤。该厂附近一所中学的同学经常闻到空气
有异味,且空气能见度差。学习化学后,同学们意识到这有可能是该厂排出的废气超标造成的,
于是在老师的指导下做了探究实验,请你填写下列空白。
【提出问题】该厂附近所降雨水是否是酸雨?空气里SO 是否超标呢?
2
【查阅资料】Ⅰ.我国关于SO 在风景区、居民区、工厂区的空气质量最高标准分别见下表:
2
级别 Ⅰ Ⅱ Ⅲ
SO 一小时测定平均含量(mg/m3) 0.15 0.5 0.7
2
Ⅱ.硫酸钡既不溶于水,也不溶于酸(如不与稀盐酸、稀硝酸等反应)。
【设计实验1】第一组同学取刚降到地面的雨水水样,用pH计(测pH的仪器)每隔几分钟测一
次pH,其数据如下表所示:
测定时刻 5:05 5:10 5:15 5:20 5:25 5:30 5:35
pH 4.95 4.94 4. 4.88 4.86 4.85 4.85
94
⑴ 所 降 雨 水 (填
“是”或“不是”)酸雨。
⑵在测定期间内,雨水的酸性 (填“增强”或“减弱”)。
【设计实验2】第二小组同学设计以下步骤来测定空气中SO 的含量。
2⑴用2L的空可乐瓶采集工厂附近的空气样品。采样的具体操作是:
。
⑵向取回的装有空气样品的可乐瓶中倒入NaOH溶液,盖紧瓶塞后充分振荡。仿照CO 与
2
NaOH溶液的反应,写出SO 与NaOH溶液反应的化学方程式:
2
。
⑶加入一定量氧化剂H O ,使其中Na SO 完全转化为Na SO 。向可乐瓶中加入过量的
2 2 2 3 2 4
BaCl 溶液。Na SO 和BaCl 反应的化学方程式为:
2 2 4 2
。
⑷经过过滤、洗涤、烘干,称量固体质量为1.165mg。
计算:1.165mg硫酸钡中硫元素的质量为 mg。
由质量守恒定律可知,2L空气样品中SO 的质量为 mg。
2
由空气质量标准可得出结论:该厂排放的SO 。
2
【发现新问题】考虑到空气中的各种气体成分,第一组认为第二组同学的SO 的含量偏大,其依
2
据是 ;
你提出的实验改进方案是 。
【反思与应用】为尽快改善该地区的空气质量,请你提出一条合理化建议:
。参考答案
序号 1 2 3 4 5 6 7 8 9 10 11 12
答案 D C B B A C A B D C B B
13. ⑴牛肉或嫩豆腐
⑵元素 P 、Fe
14. ⑴汽油(答案合理即可)
⑵可燃物缓慢氧化引起的自燃(答案合理即可)
⑶ ② ③ ⑤
⑷干粉
⑸119
⑹用水泼灭或尽快脱掉着火的衣服
15. ⑴不同
⑵17mg
⑶葡萄糖 离子 石蕊溶液变红
16. ⑴熟石灰或消石灰
⑵爆炸
⑶置换反应洗净,晾干 由于铁化学性质活泼 在酸性而潮湿的环境下更容易锈蚀
⑷CaCl +Na CO ==CaCO ↓+2NaCl
2 2 3 3
⑸铵态氮肥
⑹CaO+H O==Ca(OH) 剧烈燃烧,火星四射,生成黑山固体
2 2
17.
⑵C能控制反应随时反生和停止
⑶不能 因为二氧化碳也要和氢氧化钠反应
⑷F
⑸用燃着的木条放在集气瓶口
18. ⑴是⑵增强⑴可乐瓶装满水盖上瓶盖拿到工厂附近,然后倒掉水,再盖上瓶盖。
⑵SO +2NaOH==Na SO + H O
2 2 3 2
⑶BaCl +Na SO ==BaSO ↓+2NaCl
2 2 4 4
⑷0.16 0.32 严重超标 空气中的二氧化碳也要和氢氧化钠溶液反应,反应后生成的碳酸钠
要和BaCl 溶液反应,生成碳酸钡沉淀。 向沉淀中加入过量的稀硝酸后,再进行其余操作。 工厂
2
废气进行治理,达标后再排放。