文档内容
沈阳市 2015 年初中毕业升学统一考试
化学试卷
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cl-35.5
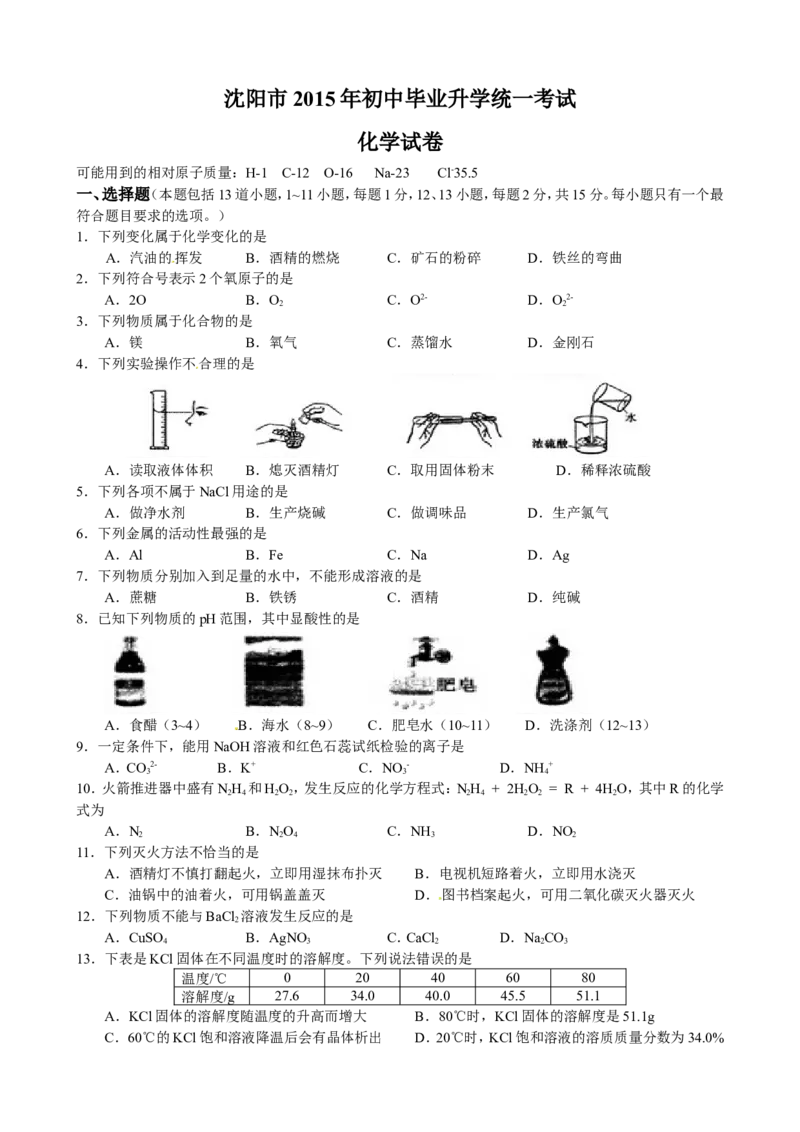
一、选择题(本题包括13道小题,1~11小题,每题1分,12、13小题,每题2分,共15分。每小题只有一个最
符合题目要求的选项。)
1.下列变化属于化学变化的是
A.汽油的挥发 B.酒精的燃烧 C.矿石的粉碎 D.铁丝的弯曲
2.下列符合号表示2个氧原子的是
A.2O B.O C.O2- D.O2-
2 2
3.下列物质属于化合物的是
A.镁 B.氧气 C.蒸馏水 D.金刚石
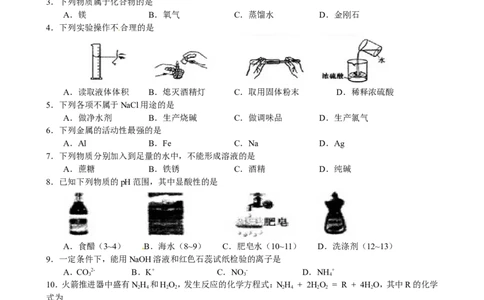
4.下列实验操作不合理的是
A.读取液体体积 B.熄灭酒精灯 C.取用固体粉末 D.稀释浓硫酸
5.下列各项不属于NaCl用途的是
A.做净水剂 B.生产烧碱 C.做调味品 D.生产氯气
6.下列金属的活动性最强的是
A.Al B.Fe C.Na D.Ag
7.下列物质分别加入到足量的水中,不能形成溶液的是
A.蔗糖 B.铁锈 C.酒精 D.纯碱
8.已知下列物质的pH范围,其中显酸性的是
A.食醋(3~4) B.海水(8~9) C.肥皂水(10~11) D.洗涤剂(12~13)
9.一定条件下,能用NaOH溶液和红色石蕊试纸检验的离子是
A.CO2- B.K+ C.NO - D.NH +
3 3 4
10.火箭推进器中盛有NH 和HO,发生反应的化学方程式:NH + 2HO = R + 4HO,其中R的化学
2 4 2 2 2 4 2 2 2
式为
A.N B.NO C.NH D.NO
2 2 4 3 2
11.下列灭火方法不恰当的是
A.酒精灯不慎打翻起火,立即用湿抹布扑灭 B.电视机短路着火,立即用水浇灭
C.油锅中的油着火,可用锅盖盖灭 D.图书档案起火,可用二氧化碳灭火器灭火
12.下列物质不能与BaCl 溶液发生反应的是
2
A.CuSO B.AgNO C.CaCl D.NaCO
4 3 2 2 3
13.下表是KCl固体在不同温度时的溶解度。下列说法错误的是
温度/℃ 0 20 40 60 80
溶解度/g 27.6 34.0 40.0 45.5 51.1
A.KCl固体的溶解度随温度的升高而增大 B.80℃时,KCl固体的溶解度是51.1g
C.60℃的KCl饱和溶液降温后会有晶体析出 D.20℃时,KCl饱和溶液的溶质质量分数为34.0%二、填空与简答题(本题包括4道小题,共20分)
14.(4分)酸雨主要是人工排放的二氧化硫酸、氮氧化物等酸性气体造成的。目前,酸雨正从硫酸型向硫酸
和硝酸复合型转化。化学在解决酸雨等环境问题中净发挥重要作用。请回答下列问题:
(1)氮元素的元素符号是 。
(2)二氧化硫酸的化学式是 。
(3)硫酸中氢元素(H)的化合价是 。
(4)写出防治酸雨的一种措施 。
15.(6分)有机化合物对人类的生活和社会发展具有极其重要的意义。请回答下列问题:
(1)下列有关有机化合物的说法,正确的是 。
A.有机化合物的种类繁多 B.葡萄糖、淀粉属于有机化合物
C.油脂、蛋白质属于有机化合物 D.硫酸、碳酸钙属于有机化合物
(2)中国是世界上最早利用天然气作燃料的国家。天然气的主要成分是甲烷(CH),请写出甲烷在氧气
4
中完全燃烧的化学方程式 。
(3)苹果中含有戊酸戊酯(C H O )是其有果香的主要原因。组成戊酸戊酯的元素有 种,其中
10 20 2
碳、氢元素的质量比为 。
(4)只用水来制取植物油是通过化学方法无法实现的。请从元素组成的角度说明原因
。
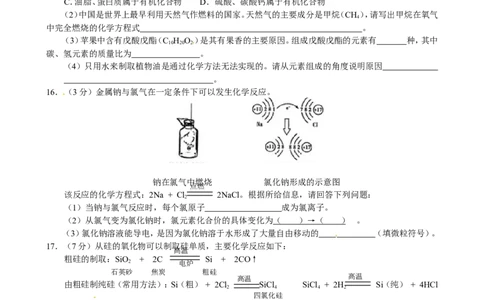
16.(3分)金属钠与氯气在一定条件下可以发生化学反应。
钠在氯气中燃烧 氯化钠形成的示意图
点燃
该反应的化A学方程式:2Na + C D l 2NaCl。根据所给信息,请回答下列问题:
2 [来源:学#科#网]
(1)当钠与氯气反应C时,每个氯原子 成为氯离子。
(2)从氯气变为氯化钠时,氯元素化合价的具体变化为( )→( ) 。
B E
(3)氯化钠溶液能导电,是因为氯化钠溶于水形成了大量自由移动的 (填微粒符号)。
17.(7分)从硅的氧化物可以制取硅单质,主要化学反应如下:
高温
粗硅的制取:SiO + 2C Si + 2CO↑
2 电炉
石英砂 焦炭 粗硅
高温 高温
由粗硅制纯硅(常用方法):Si(粗) + 2Cl SiCl SiCl + 2H Si(纯) + 4HCl
2 4 4 2
四氯化硅
(1)根据上述信息,请补全制取纯硅的简易流程图:
焦炭、高温 Cl 、高温 H、高温
石英砂 粗硅 2 2 纯硅
(2)根据已有知识和上述信息,进行总结归纳:
① 完成置换反应的通式:单质(I) + 化合物(I)= 单质(II) + 。
② 填写下表:
单质(I) 化合物(I) 相应的置换反应的化学方程式(各一例)
A 金属 非金属 Fe + 2HCl = FeCl + H↑
2 2 [来源:学_科_网Z_X_X_K]
B 金属 金属 [单质(I)为铜]
C
△D 金属 H + CuO Cu + HO
2 2
三、实验与探究题(本题包括3道小题,共24分)
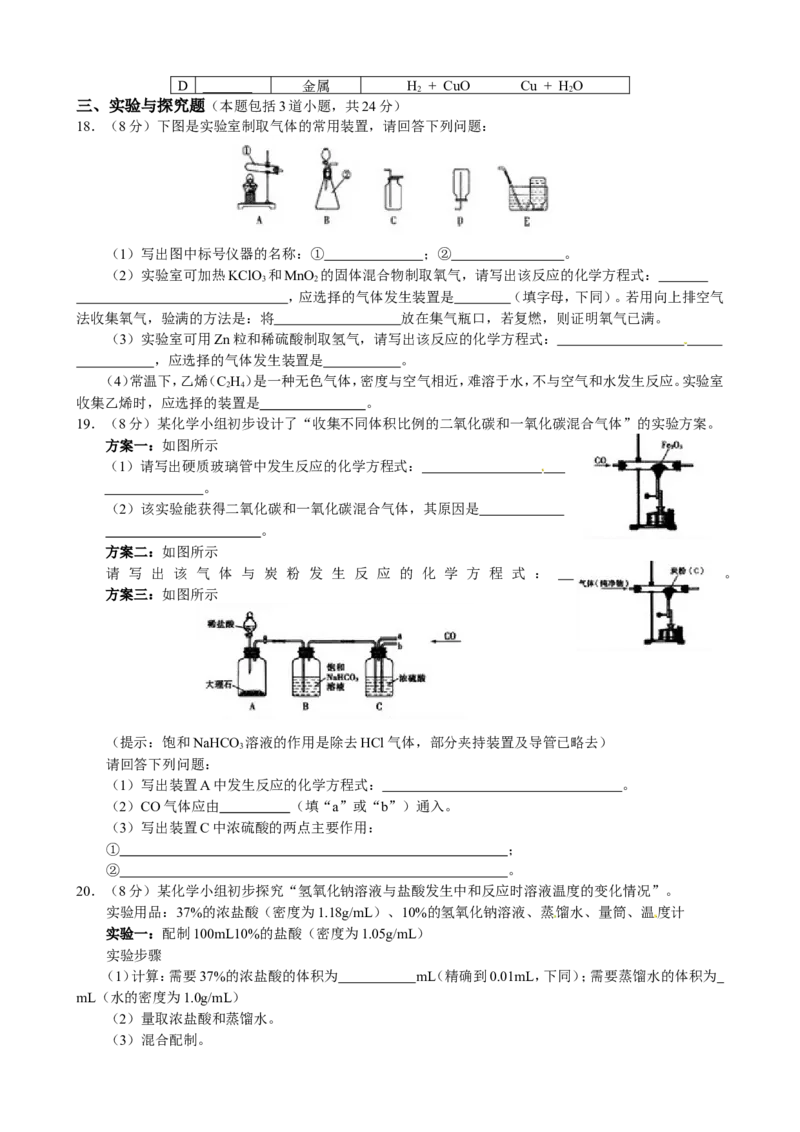
18.(8分)下图是实验室制取气体的常用装置,请回答下列问题:
(1)写出图中标号仪器的名称:① ;② 。
(2)实验室可加热KClO 和MnO 的固体混合物制取氧气,请写出该反应的化学方程式:
3 2
,应选择的气体发生装置是 (填字母,下同)。若用向上排空气
法收集氧气,验满的方法是:将 放在集气瓶口,若复燃,则证明氧气已满。
(3)实验室可用Zn粒和稀硫酸制取氢气,请写出该反应的化学方程式:
,应选择的气体发生装置是 。
(4)常温下,乙烯(C H)是一种无色气体,密度与空气相近,难溶于水,不与空气和水发生反应。实验室
2 4
收集乙烯时,应选择的装置是 。
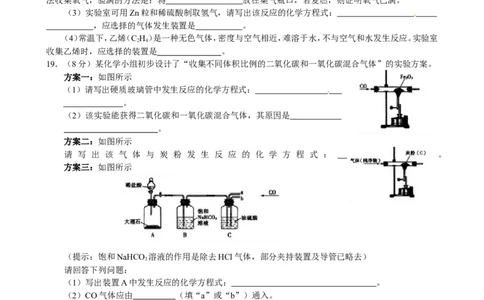
19.(8分)某化学小组初步设计了“收集不同体积比例的二氧化碳和一氧化碳混合气体”的实验方案。
方案一:如图所示
(1)请写出硬质玻璃管中发生反应的化学方程式:
。
[来源:学|科|网]
(2)该实验能获得二氧化碳和一氧化碳混合气体,其原因是
。
方案二:如图所示
请 写 出 该 气 体 与 炭 粉 发 生 反 应 的 化 学 方 程 式 : 。
方案三:如图所示
(提示:饱和NaHCO 溶液的作用是除去HCl气体,部分夹持装置及导管已略去)
3
请回答下列问题:
(1)写出装置A中发生反应的化学方程式: 。
(2)CO气体应由 (填“a”或“b”)通入。
(3)写出装置C中浓硫酸的两点主要作用:
[来源:Zxxk.Com]
① ;
② 。
20.(8分)某化学小组初步探究“氢氧化钠溶液与盐酸发生中和反应时溶液温度的变化情况”。
实验用品:37%的浓盐酸(密度为1.18g/mL)、10%的氢氧化钠溶液、蒸馏水、量筒、温度计
实验一:配制100mL10%的盐酸(密度为1.05g/mL)
实验步骤
(1)计算:需要37%的浓盐酸的体积为 mL(精确到0.01mL,下同);需要蒸馏水的体积为
mL(水的密度为1.0g/mL)
(2)量取浓盐酸和蒸馏水。
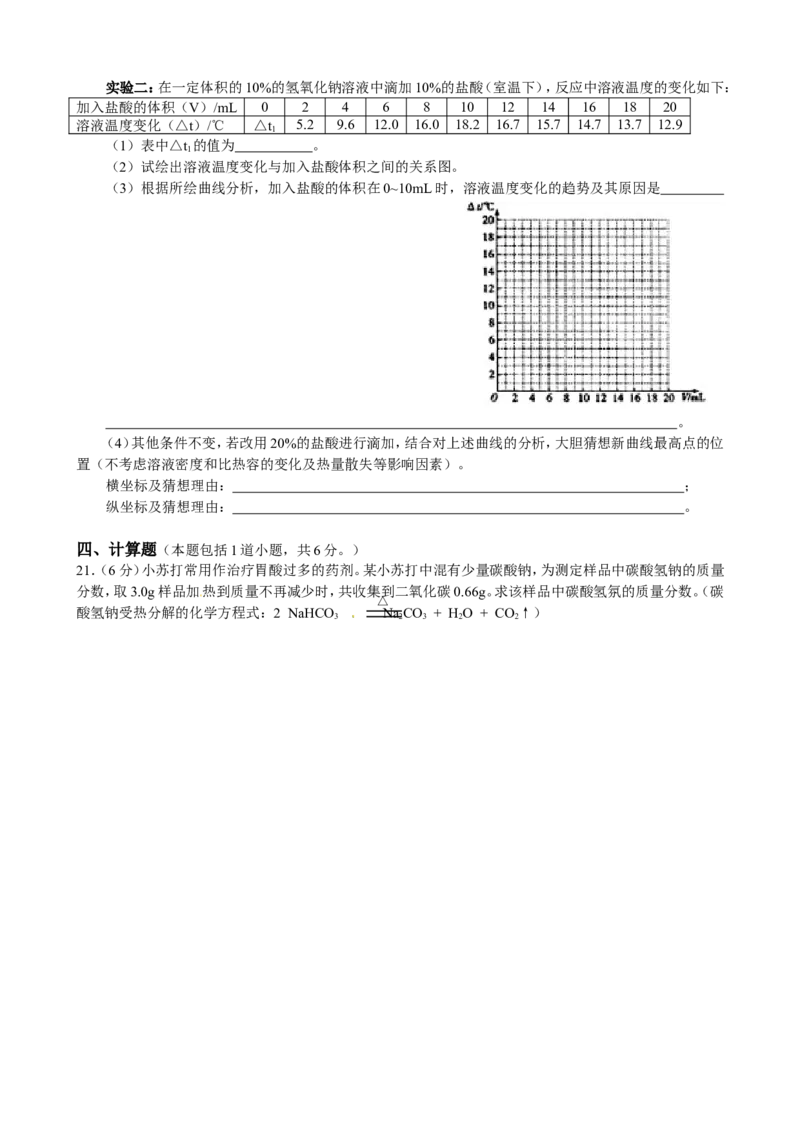
(3)混合配制。实验二:在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸(室温下),反应中溶液温度的变化如下:
加入盐酸的体积(V)/mL 0 2 4 6 8 10 12 14 16 18 20
溶液温度变化(△t)/℃ △t 5.2 9.6 12.0 16.0 18.2 16.7 15.7 14.7 13.7 12.9
1
(1)表中△t 的值为 。
1
(2)试绘出溶液温度变化与加入盐酸体积之间的关系图。
(3)根据所绘曲线分析,加入盐酸的体积在0~10mL时,溶液温度变化的趋势及其原因是
。
(4)其他条件不变,若改用20%的盐酸进行滴加,结合对上述曲线的分析,大胆猜想新曲线最高点的位
置(不考虑溶液密度和比热容的变化及热量散失等影响因素)。
横坐标及猜想理由: ;
纵坐标及猜想理由: 。
四、计算题(本题包括1道小题,共6分。)
21.(6分)小苏打常用作治疗胃酸过多的药剂。某小苏打中混有少量碳酸钠,为测定样品中碳酸氢钠的质量
分数,取3.0g样品加热到质量不再减少时,共收集到二氧化碳0.66g。求该样品中碳酸氢氛的质量分数。(碳
△
酸氢钠受热分解的化学方程式:2 NaHCO NaCO + HO + CO↑)
3 2 3 2 2[来源:学#科#网]