文档内容
2019年四川省绵阳市中考化学试卷
一、选择题(每小题3分,每个小题只有一个选项最符合题目要求)
1.(3分)化学对科技发展具有重要作用,下列说法错误的是( )
A.尖端技术采用液氮获得低温,利用了氮气的化学性质
B.用作新型电池电极材料的石墨烯与金刚石组成元素相同
C.中国具有自主知识产权的大飞机C919机身主体材料是铝合金
D.通过改变钢铁组成,表面覆盖保护层,可以确保港珠澳大桥使用寿命
2.(3分)冰毒是一种毒品。吸食初期有多语,对种种刺激过敏、焦躁、抑郁循环性病态。
继之,在幻听、幻视的错乱状态下,呈现被杀、被跟踪、嫉妒等多种妄想症,我们应该
远离毒品。某种冰毒的化学式为 C H NO Cl,下列关于该冰毒的说法正确的是
10 14 2
( )
A.是一种有机高分子化合物
B.相对分子质量为215.5 g
C.N、H两种元素的质量分数相同
D.在空气中燃烧只生成CO 和H O
2 2
3.(3分)下列关于资源、能源利用的说法正确的是( )
A.最理想的清洁、高能燃料是H
2
B.地球上水储量非常丰富,淡水资源取之不尽
C.我国稀土资源丰富,可随意开采
D.为快速提高人类生活质量,必须加速开采石油
4.(3分)大连物化所研究发现,利用催化剂在低温下可将甲烷转化为甲醇,其反应微观
示意图如图。下列说法错误的是( )
A.甲醇的化学式为CH O
4
B.图示物质中有3种氧化物
C.该反应中分子、原子个数均不变
第 1 页 / 共 6 页D.催化剂在反应前后质量不变
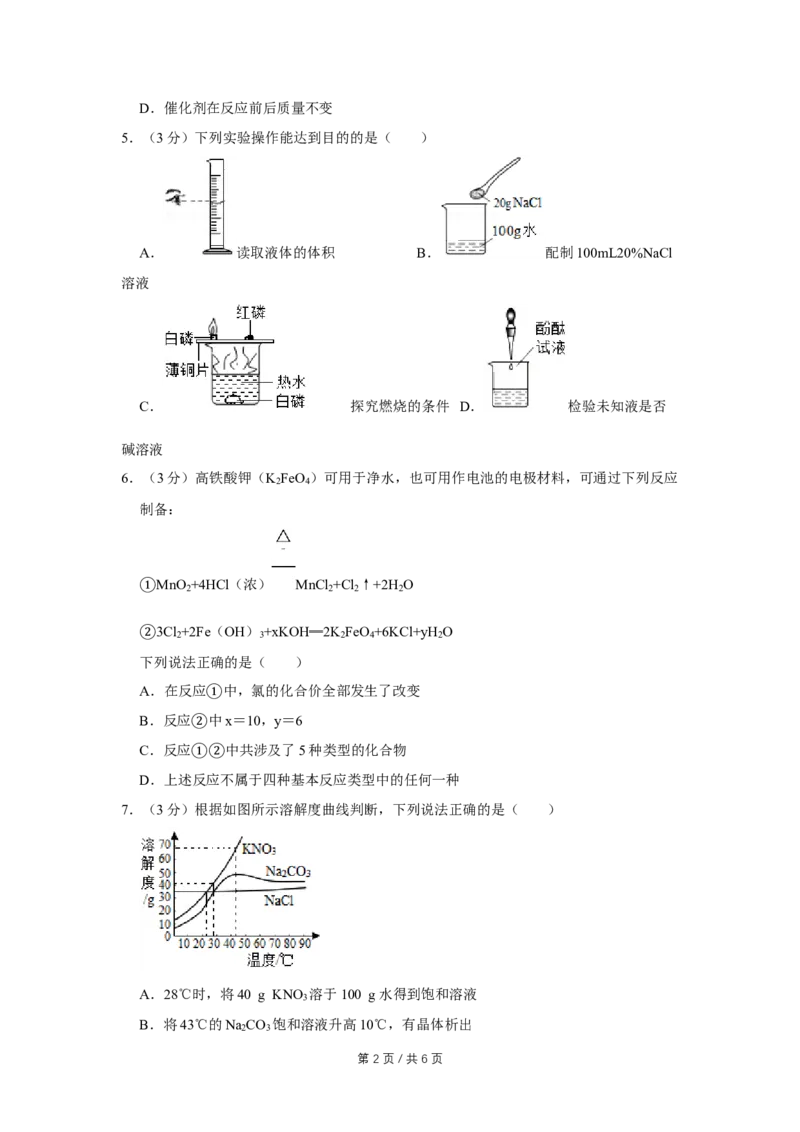
5.(3分)下列实验操作能达到目的的是( )
A. 读取液体的体积 B. 配制100mL20%NaCl
溶液
C. 探究燃烧的条件 D. 检验未知液是否
碱溶液
6.(3分)高铁酸钾(K FeO )可用于净水,也可用作电池的电极材料,可通过下列反应
2 4
制备:
MnO +4HCl(浓) MnCl +Cl ↑+2H O
2 2 2 2
①
3Cl +2Fe(OH) +xKOH═2K FeO +6KCl+yH O
2 3 2 4 2
②下列说法正确的是( )
A.在反应 中,氯的化合价全部发生了改变
B.反应 ①中x=10,y=6
C.反应② 中共涉及了5种类型的化合物
D.上述①反应②不属于四种基本反应类型中的任何一种
7.(3分)根据如图所示溶解度曲线判断,下列说法正确的是( )
A.28℃时,将40 g KNO 溶于100 g水得到饱和溶液
3
B.将43℃的Na CO 饱和溶液升高10℃,有晶体析出
2 3
第 2 页 / 共 6 页C.三种物质的饱和溶液由40℃降温至23℃,所得溶液中溶质质量:m(NaCl)=m
(KNO )>m(Na CO )
3 2 3
D.除去KNO 中混有的Na CO ,可在40℃配成饱和溶液,再降温结晶、过滤
3 2 3
8.(3分)向一定质量的AgNO 、Fe(NO ) 混合溶液中加入a g Zn粉,充分反应后过
3 3 2
滤,将滤渣洗涤、干燥、称量,所得质量仍为a g.下列说法正确的是( )
A.滤液一定呈无色
B.滤液中一定含Fe(NO ) 和Zn(NO )
3 2 3 2
C.滤渣中一定含Fe
D.滤渣滴加稀盐酸一定无气泡产生
9.(3分)我国古代将赤铜(Cu O)、炉甘石(ZnCO )和木炭混合加热到800℃得到黄
2 3
铜(铜锌合金)。若冶炼时所用Cu O与ZnCO 的质量比为26:25,则所得黄铜的含铜
2 3
量为( )
A.67.5% B.51% C.65% D.64%
二、(本题包括2小题,共15分)
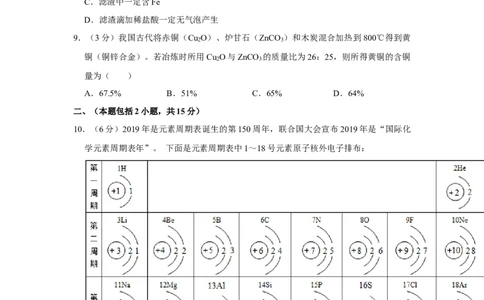
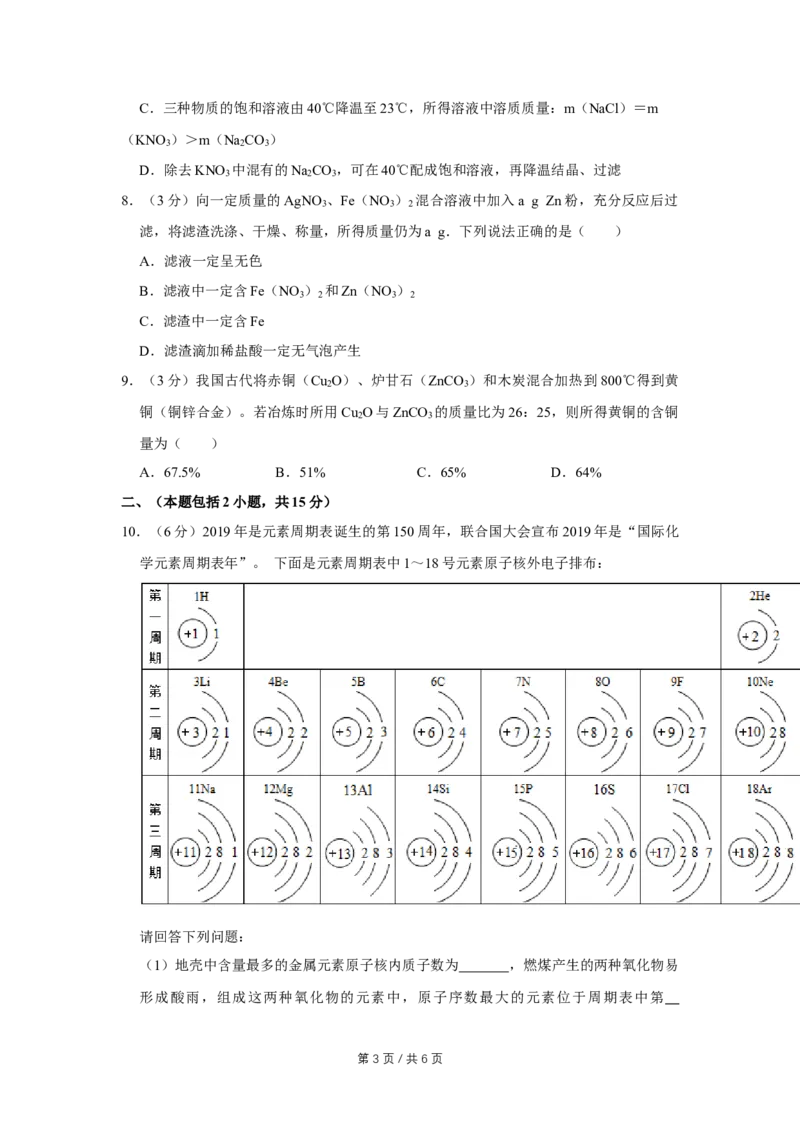
10.(6分)2019年是元素周期表诞生的第150周年,联合国大会宣布2019年是“国际化
学元素周期表年”。 下面是元素周期表中1~18号元素原子核外电子排布:
请回答下列问题:
(1)地壳中含量最多的金属元素原子核内质子数为 ,燃煤产生的两种氧化物易
形成酸雨,组成这两种氧化物的元素中,原子序数最大的元素位于周期表中第
第 3 页 / 共 6 页周期。
(2)第9号元素的钠盐常被添加到牙膏里以预防龋齿,该元素的离子结构示意图为
。元素X的原子核外电子总数为最外层电子数的3倍,单质X在空气中燃烧生成的化合
物化学式为 。
(3)在元素周期表中,19号元素钾与钠位于同一族,则钾原子的电子层数为 ,
金属钾与钠性质有许多相似之处,原因是 。
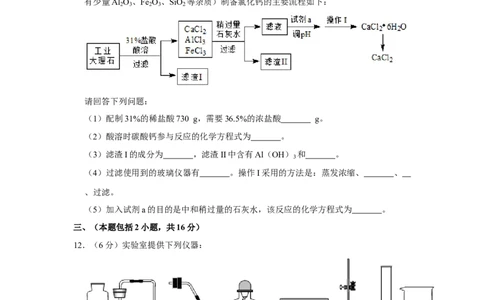
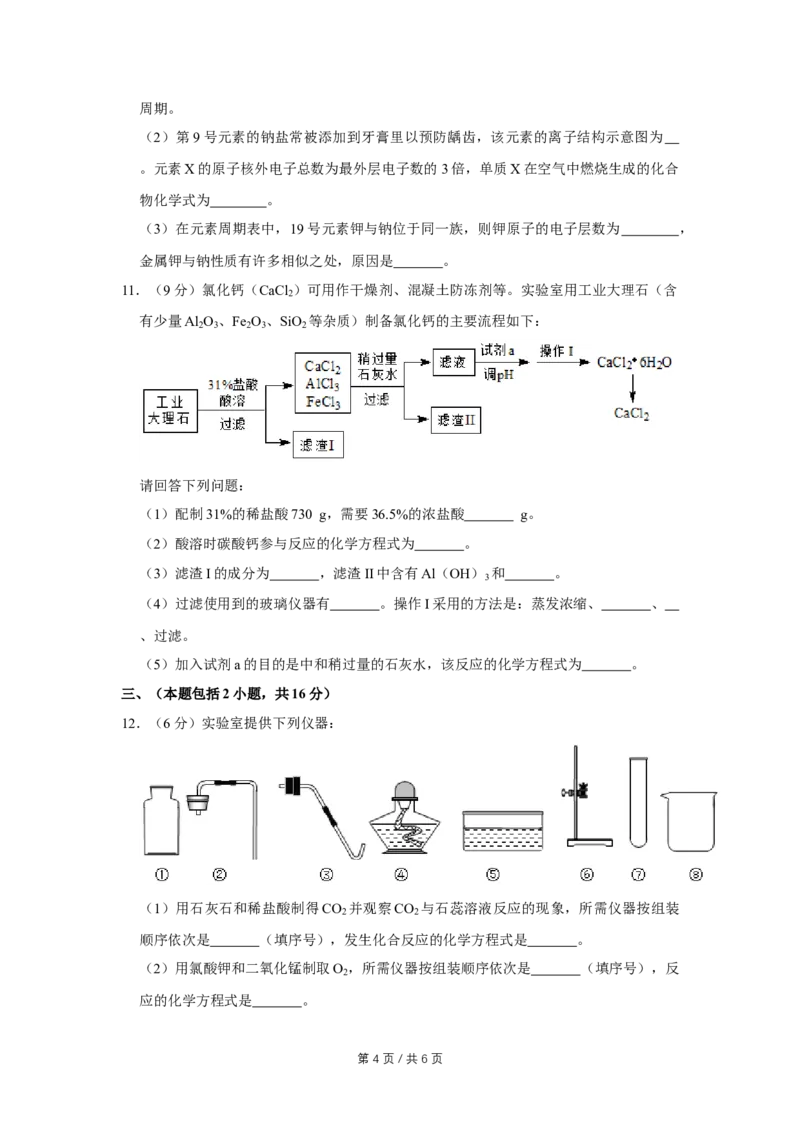
11.(9分)氯化钙(CaCl )可用作干燥剂、混凝土防冻剂等。实验室用工业大理石(含
2
有少量Al O 、Fe O 、SiO 等杂质)制备氯化钙的主要流程如下:
2 3 2 3 2
请回答下列问题:
(1)配制31%的稀盐酸730 g,需要36.5%的浓盐酸 g。
(2)酸溶时碳酸钙参与反应的化学方程式为 。
(3)滤渣I的成分为 ,滤渣II中含有Al(OH) 和 。
3
(4)过滤使用到的玻璃仪器有 。操作I采用的方法是:蒸发浓缩、 、
、过滤。
(5)加入试剂a的目的是中和稍过量的石灰水,该反应的化学方程式为 。
三、(本题包括2小题,共16分)
12.(6分)实验室提供下列仪器:
(1)用石灰石和稀盐酸制得CO 并观察CO 与石蕊溶液反应的现象,所需仪器按组装
2 2
顺序依次是 (填序号),发生化合反应的化学方程式是 。
(2)用氯酸钾和二氧化锰制取O ,所需仪器按组装顺序依次是 (填序号),反
2
应的化学方程式是 。
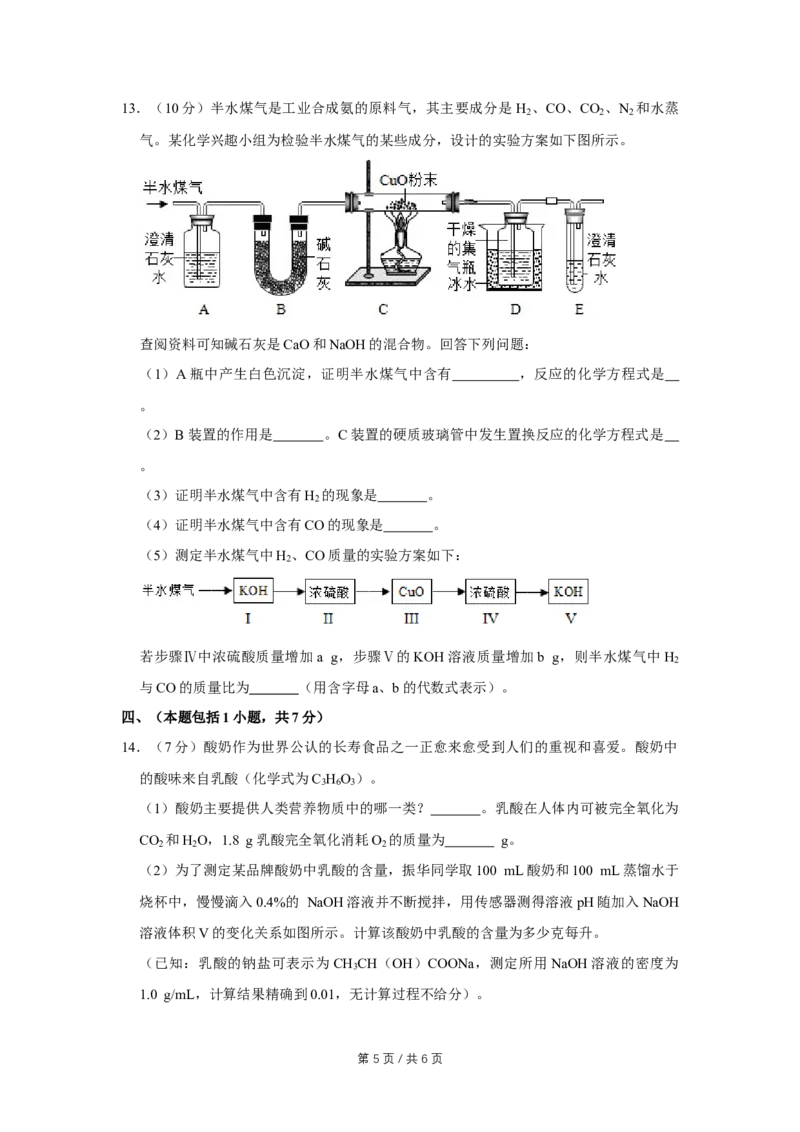
第 4 页 / 共 6 页13.(10分)半水煤气是工业合成氨的原料气,其主要成分是 H 、CO、CO 、N 和水蒸
2 2 2
气。某化学兴趣小组为检验半水煤气的某些成分,设计的实验方案如下图所示。
查阅资料可知碱石灰是CaO和NaOH的混合物。回答下列问题:
(1)A瓶中产生白色沉淀,证明半水煤气中含有 ,反应的化学方程式是
。
(2)B装置的作用是 。C装置的硬质玻璃管中发生置换反应的化学方程式是
。
(3)证明半水煤气中含有H 的现象是 。
2
(4)证明半水煤气中含有CO的现象是 。
(5)测定半水煤气中H 、CO质量的实验方案如下:
2
若步骤Ⅳ中浓硫酸质量增加a g,步骤Ⅴ的KOH溶液质量增加b g,则半水煤气中H
2
与CO的质量比为 (用含字母a、b的代数式表示)。
四、(本题包括1小题,共7分)
14.(7分)酸奶作为世界公认的长寿食品之一正愈来愈受到人们的重视和喜爱。酸奶中
的酸味来自乳酸(化学式为C H O )。
3 6 3
(1)酸奶主要提供人类营养物质中的哪一类? 。乳酸在人体内可被完全氧化为
CO 和H O,1.8 g乳酸完全氧化消耗O 的质量为 g。
2 2 2
(2)为了测定某品牌酸奶中乳酸的含量,振华同学取100 mL酸奶和100 mL蒸馏水于
烧杯中,慢慢滴入0.4%的 NaOH溶液并不断搅拌,用传感器测得溶液pH随加入NaOH
溶液体积V的变化关系如图所示。计算该酸奶中乳酸的含量为多少克每升。
(已知:乳酸的钠盐可表示为 CH CH(OH)COONa,测定所用NaOH溶液的密度为
3
1.0 g/mL,计算结果精确到0.01,无计算过程不给分)。
第 5 页 / 共 6 页第 6 页 / 共 6 页