文档内容
新高二开学摸底考试卷 02(新高考通用)
化 学
(考试时间:75分钟 试卷满分:100分)
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准
考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:人教版2019必修第一册+必修第二册。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5
第Ⅰ卷(选择题 共 42 分)
一、选择题:本题共14个小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.化学与生活密切相关,下列叙述正确的是
A.天然气、沼气和太阳能分别属于化石能源、可再生能源和二次能源
B.高纯度的硅单质广泛用于作光导纤维,光导纤维遇碱会“断路”
C.煤的气化和液化、石油的分馏,都属于物理变化
D.食品中添加适量的二氧化硫可以起到漂白、防腐和抗氧化等作用
2.在 反应中,表示该反应速率最慢的是
A. B.
C. D.
3.糖类、油脂和蛋白质是食物中的主要营养物质,它们对人类的生命活动有着极其重要的作用,下列有
关说法正确的是
A.淀粉水解的最终产物为葡萄糖,可用新制氢氧化铜悬浊液检验淀粉是否水解
B.淀粉和纤维素都属于多糖,两者的分子式均为 ,互为同分异构体
C.蛋白质被灼烧时,会产生类似烧纸的气味
D.糖类、油脂和蛋白质均能发生水解
4.下列金属中,通常用热还原法冶炼的是
A.钠 B.铁 C.铂 D.汞
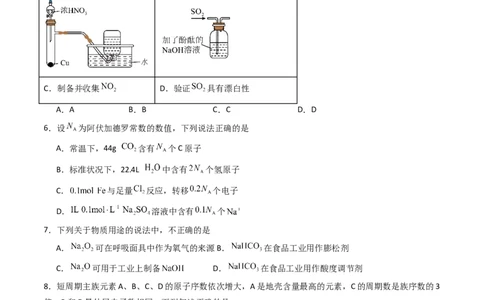
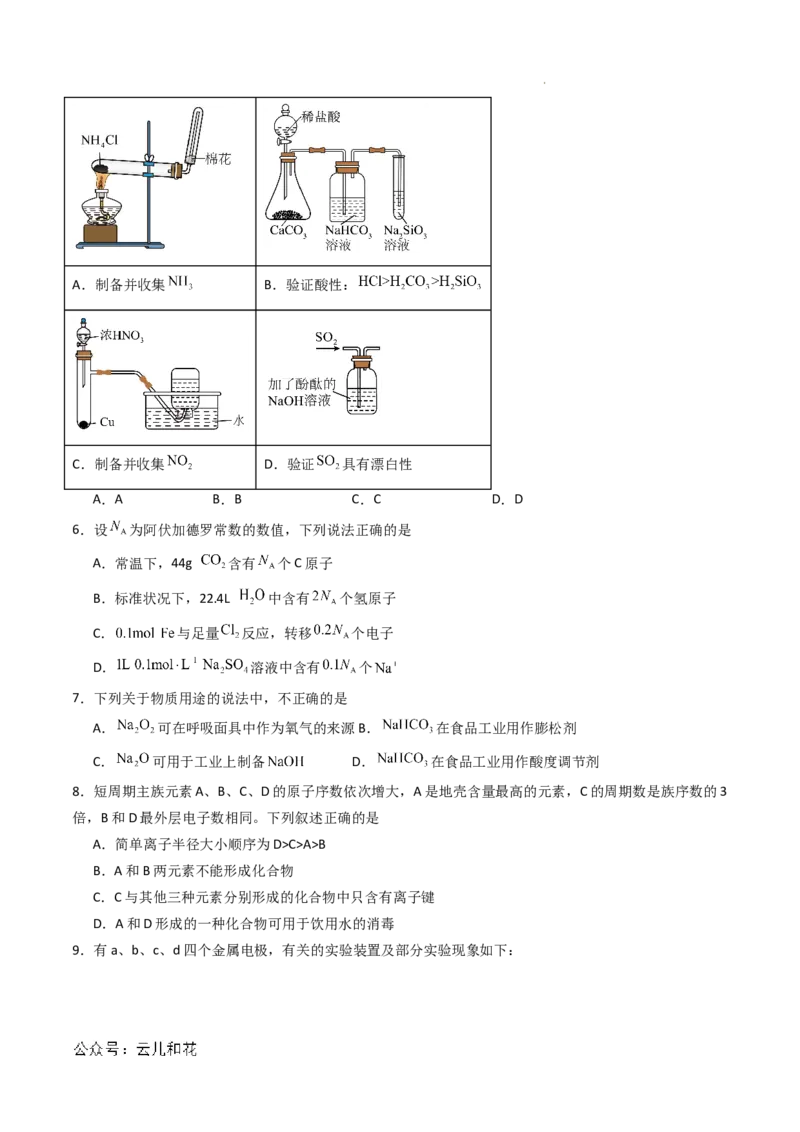
5.下列实验装置能达到实验目的的是
学科网(北京)股份有限公司A.制备并收集 B.验证酸性:
C.制备并收集 D.验证 具有漂白性
A.A B.B C.C D.D
6.设 为阿伏加德罗常数的数值,下列说法正确的是
A.常温下,44g 含有 个C原子
B.标准状况下,22.4L 中含有 个氢原子
C. 与足量 反应,转移 个电子
D. 溶液中含有 个
7.下列关于物质用途的说法中,不正确的是
A. 可在呼吸面具中作为氧气的来源B. 在食品工业用作膨松剂
C. 可用于工业上制备 D. 在食品工业用作酸度调节剂
8.短周期主族元素A、B、C、D的原子序数依次增大,A是地壳含量最高的元素,C的周期数是族序数的3
倍,B和D最外层电子数相同。下列叙述正确的是
A.简单离子半径大小顺序为D>C>A>B
B.A和B两元素不能形成化合物
C.C与其他三种元素分别形成的化合物中只含有离子键
D.A和D形成的一种化合物可用于饮用水的消毒
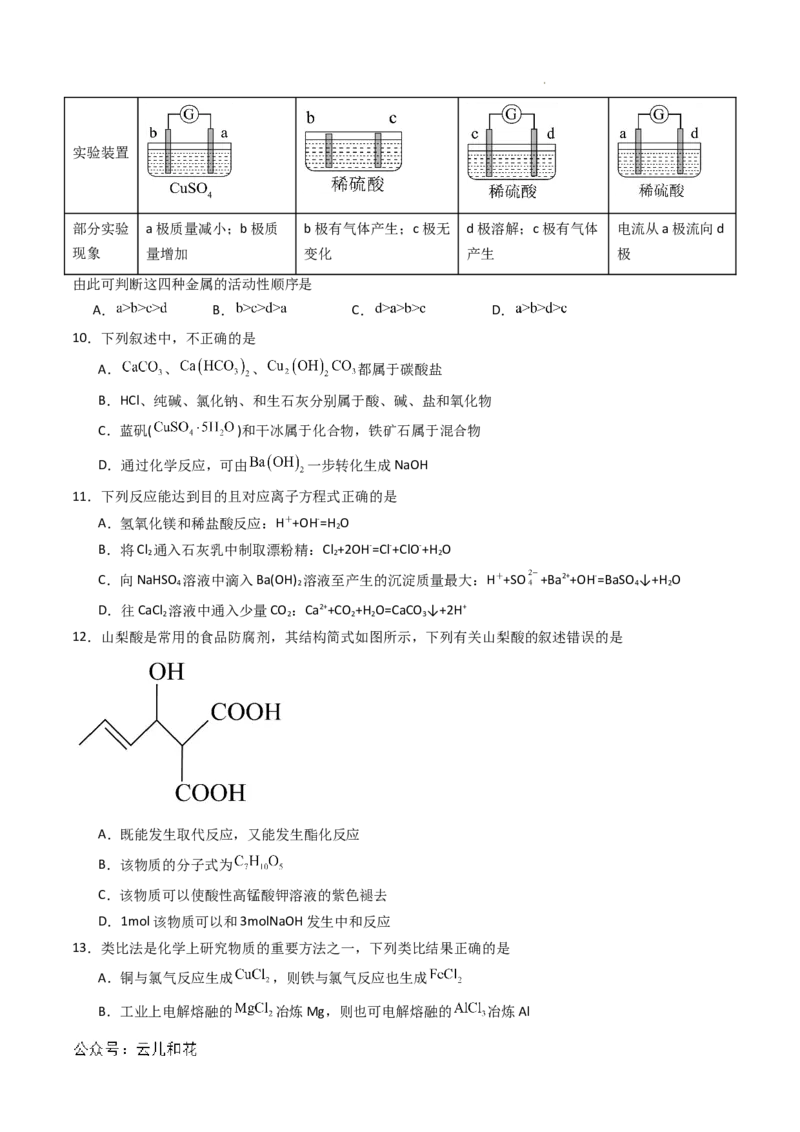
9.有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
学科网(北京)股份有限公司实验装置
部分实验 a极质量减小;b极质 b极有气体产生;c极无 d极溶解;c极有气体 电流从a极流向d
现象 量增加 变化 产生 极
由此可判断这四种金属的活动性顺序是
A. B. C. D.
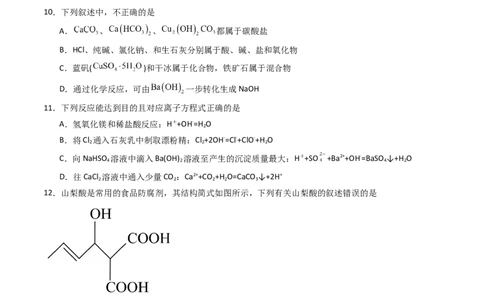
10.下列叙述中,不正确的是
A. 、 、 都属于碳酸盐
B.HCl、纯碱、氯化钠、和生石灰分别属于酸、碱、盐和氧化物
C.蓝矾( )和干冰属于化合物,铁矿石属于混合物
D.通过化学反应,可由 一步转化生成NaOH
11.下列反应能达到目的且对应离子方程式正确的是
A.氢氧化镁和稀盐酸反应:H++OH-=H O
2
B.将Cl 通入石灰乳中制取漂粉精:Cl +2OH-=Cl-+ClO-+H O
2 2 2
C.向NaHSO 溶液中滴入Ba(OH) 溶液至产生的沉淀质量最大:H++SO +Ba2++OH-=BaSO ↓+H O
4 2 4 2
D.往CaCl 溶液中通入少量CO :Ca2++CO +H O=CaCO ↓+2H+
2 2 2 2 3
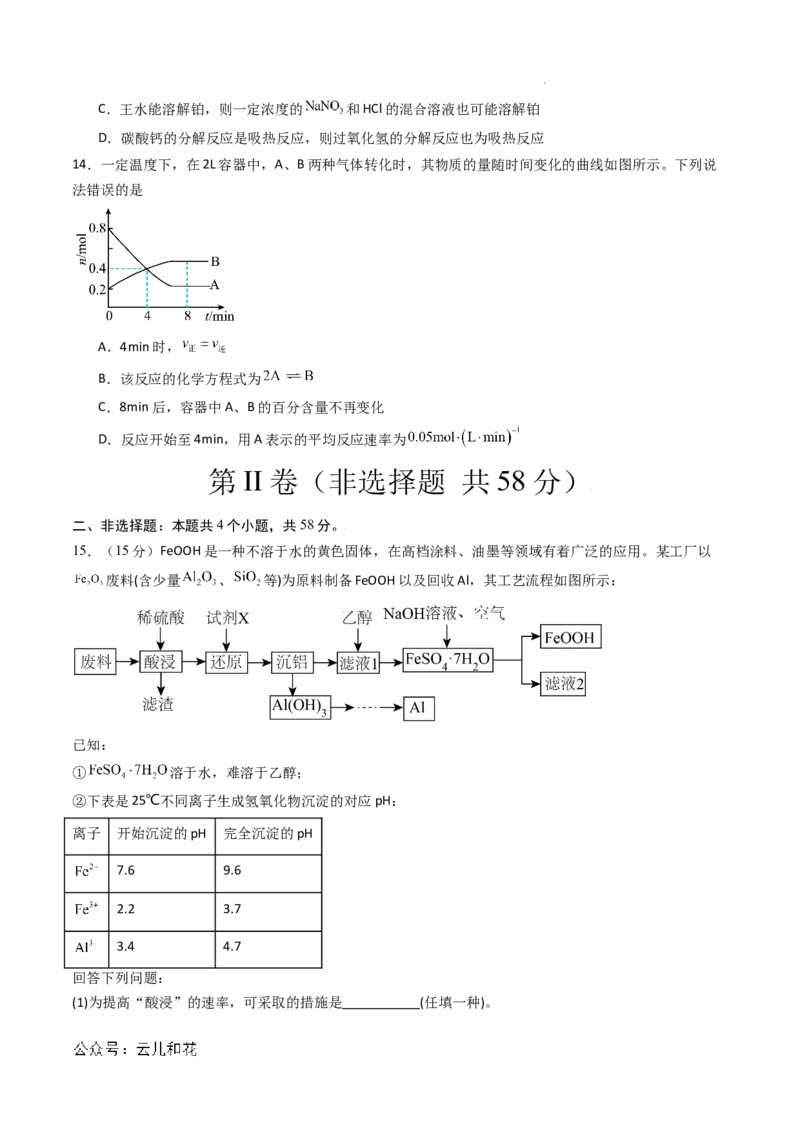
12.山梨酸是常用的食品防腐剂,其结构简式如图所示,下列有关山梨酸的叙述错误的是
A.既能发生取代反应,又能发生酯化反应
B.该物质的分子式为
C.该物质可以使酸性高锰酸钾溶液的紫色褪去
D.1mol该物质可以和3molNaOH发生中和反应
13.类比法是化学上研究物质的重要方法之一,下列类比结果正确的是
A.铜与氯气反应生成 ,则铁与氯气反应也生成
B.工业上电解熔融的 冶炼Mg,则也可电解熔融的 冶炼Al
学科网(北京)股份有限公司C.王水能溶解铂,则一定浓度的 和HCl的混合溶液也可能溶解铂
D.碳酸钙的分解反应是吸热反应,则过氧化氢的分解反应也为吸热反应
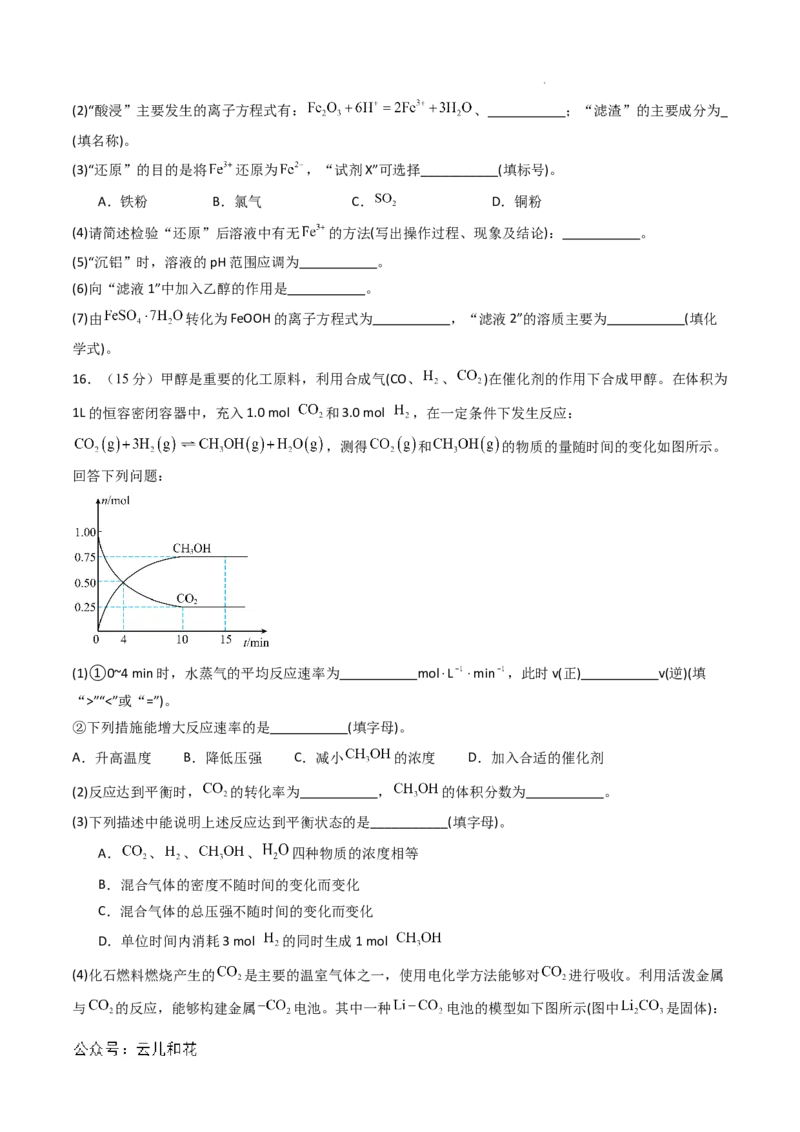
14.一定温度下,在2L容器中,A、B两种气体转化时,其物质的量随时间变化的曲线如图所示。下列说
法错误的是
A.4min时,
B.该反应的化学方程式为
C.8min后,容器中A、B的百分含量不再变化
D.反应开始至4min,用A表示的平均反应速率为
第 II 卷(非选择题 共 58 分)
二、非选择题:本题共4个小题,共58分。
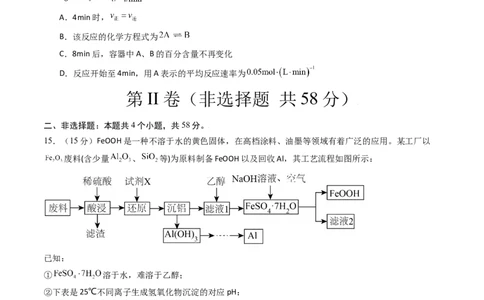
15.(15分)FeOOH是一种不溶于水的黄色固体,在高档涂料、油墨等领域有着广泛的应用。某工厂以
废料(含少量 、 等)为原料制备FeOOH以及回收Al,其工艺流程如图所示:
已知:
① 溶于水,难溶于乙醇;
②下表是25℃不同离子生成氢氧化物沉淀的对应pH:
离子 开始沉淀的pH 完全沉淀的pH
7.6 9.6
2.2 3.7
3.4 4.7
回答下列问题:
(1)为提高“酸浸”的速率,可采取的措施是 (任填一种)。
学科网(北京)股份有限公司(2)“酸浸”主要发生的离子方程式有: 、 ;“滤渣”的主要成分为
(填名称)。
(3)“还原”的目的是将 还原为 ,“试剂X”可选择___________(填标号)。
A.铁粉 B.氯气 C. D.铜粉
(4)请简述检验“还原”后溶液中有无 的方法(写出操作过程、现象及结论): 。
(5)“沉铝”时,溶液的pH范围应调为 。
(6)向“滤液1”中加入乙醇的作用是 。
(7)由 转化为FeOOH的离子方程式为 ,“滤液2”的溶质主要为 (填化
学式)。
16.(15分)甲醇是重要的化工原料,利用合成气(CO、 、 )在催化剂的作用下合成甲醇。在体积为
1L的恒容密闭容器中,充入1.0 mol 和3.0 mol ,在一定条件下发生反应:
,测得 和 的物质的量随时间的变化如图所示。
回答下列问题:
(1)①0~4 min时,水蒸气的平均反应速率为 mol⋅L ⋅min ,此时v(正) v(逆)(填
“>”“<”或“=”)。
②下列措施能增大反应速率的是 (填字母)。
A.升高温度 B.降低压强 C.减小 的浓度 D.加入合适的催化剂
(2)反应达到平衡时, 的转化率为 , 的体积分数为 。
(3)下列描述中能说明上述反应达到平衡状态的是___________(填字母)。
A. 、 、 、 四种物质的浓度相等
B.混合气体的密度不随时间的变化而变化
C.混合气体的总压强不随时间的变化而变化
D.单位时间内消耗3 mol 的同时生成1 mol
(4)化石燃料燃烧产生的 是主要的温室气体之一,使用电化学方法能够对 进行吸收。利用活泼金属
与 的反应,能够构建金属 电池。其中一种 电池的模型如下图所示(图中 是固体):
学科网(北京)股份有限公司①a电极为该电池的 (填“正”或“负”)极,正极电极反应式为 。
②该电池中每转移2 mol电子,能够吸收 mol 。
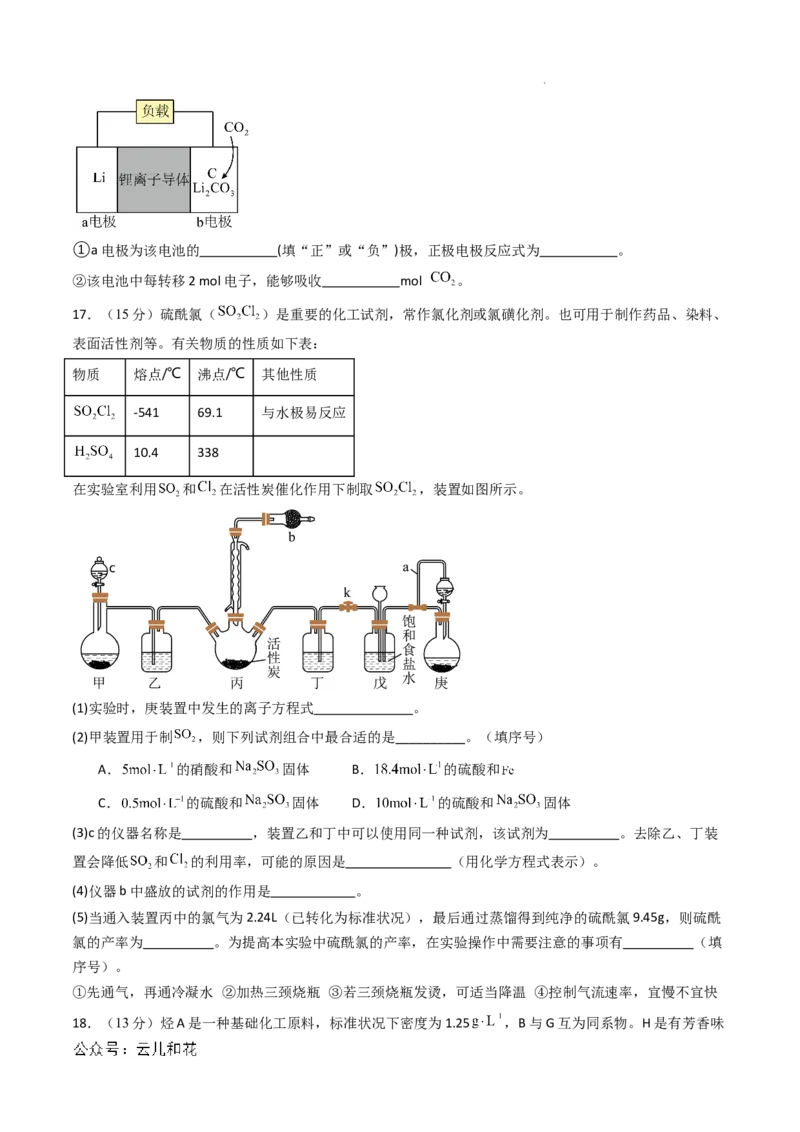
17.(15分)硫酰氯( )是重要的化工试剂,常作氯化剂或氯磺化剂。也可用于制作药品、染料、
表面活性剂等。有关物质的性质如下表:
物质 熔点/℃ 沸点/℃ 其他性质
-541 69.1 与水极易反应
10.4 338
在实验室利用 和 在活性炭催化作用下制取 ,装置如图所示。
(1)实验时,庚装置中发生的离子方程式 。
(2)甲装置用于制 ,则下列试剂组合中最合适的是__________。(填序号)
A. 的硝酸和 固体 B. 的硫酸和
C. 的硫酸和 固体 D. 的硫酸和 固体
(3)c的仪器名称是 ,装置乙和丁中可以使用同一种试剂,该试剂为 。去除乙、丁装
置会降低 和 的利用率,可能的原因是 (用化学方程式表示)。
(4)仪器b中盛放的试剂的作用是 。
(5)当通入装置丙中的氯气为2.24L(已转化为标准状况),最后通过蒸馏得到纯净的硫酰氯9.45g,则硫酰
氯的产率为 。为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有 (填
序号)。
①先通气,再通冷凝水 ②加热三颈烧瓶 ③若三颈烧瓶发烫,可适当降温 ④控制气流速率,宜慢不宜快
18.(13分)烃A是一种基础化工原料,标准状况下密度为1.25 ,B与G互为同系物。H是有芳香味
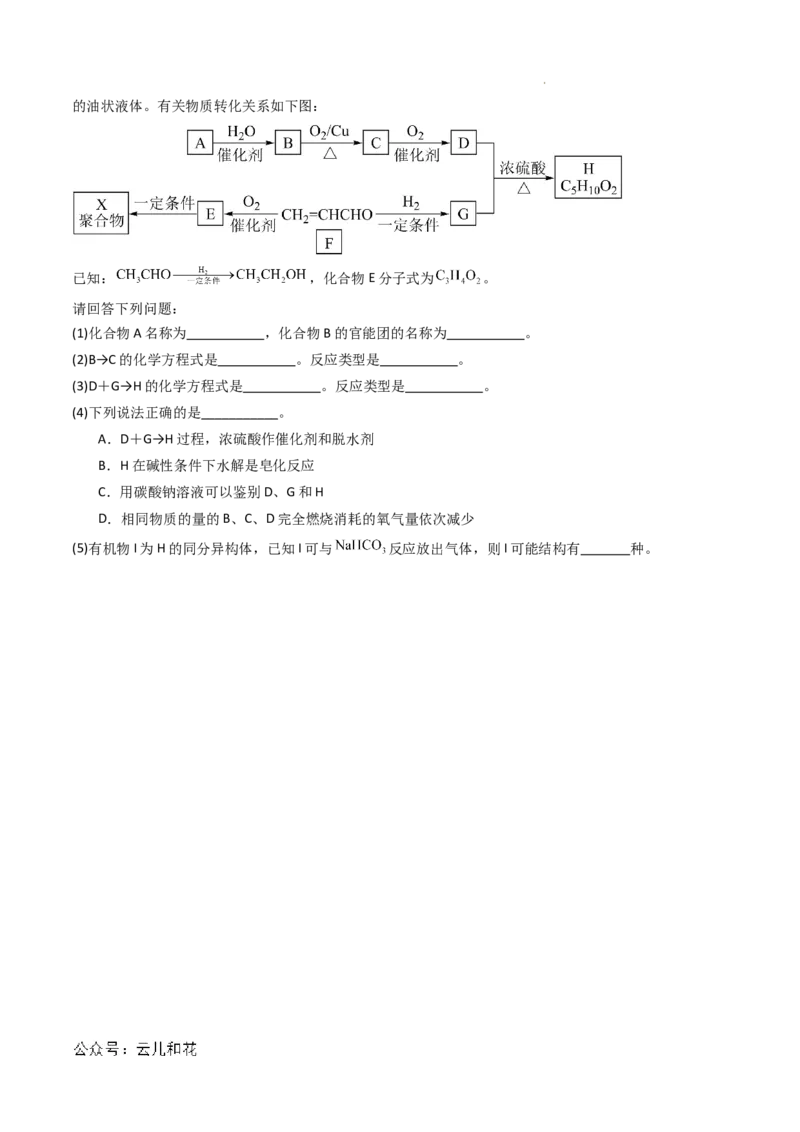
学科网(北京)股份有限公司的油状液体。有关物质转化关系如下图:
已知: ,化合物E分子式为 。
请回答下列问题:
(1)化合物A名称为 ,化合物B的官能团的名称为 。
(2)B→C的化学方程式是 。反应类型是 。
(3)D+G→H的化学方程式是 。反应类型是 。
(4)下列说法正确的是___________。
A.D+G→H过程,浓硫酸作催化剂和脱水剂
B.H在碱性条件下水解是皂化反应
C.用碳酸钠溶液可以鉴别D、G和H
D.相同物质的量的B、C、D完全燃烧消耗的氧气量依次减少
(5)有机物I为H的同分异构体,已知I可与 反应放出气体,则I可能结构有 种。
学科网(北京)股份有限公司