文档内容
让更多的孩子得到更好的教育
中考冲刺:化学图表题(提高)
撰稿:熊亚军 审稿:李伟
【巩固练习】
一、 选择题 (每小题只有一个选项符合题意)
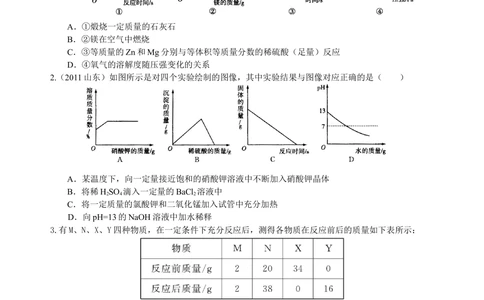
1.(2011兰州)下列图像不能正确反映所对应叙述关系的是( )
A.①煅烧一定质量的石灰石
B.②镁在空气中燃烧
C.③等质量的Zn和Mg分别与等体积等质量分数的稀硫酸(足量)反应
D.④氧气的溶解度随压强变化的关系
2.(2011山东)如图所示是对四个实验绘制的图像,其中实验结果与图像对应正确的是( )
A.某温度下,向一定量接近饱和的硝酸钾溶液中不断加入硝酸钾晶体
B.将稀HSO 滴入一定量的BaCl 溶液中
2 4 2
C.将一定质量的氯酸钾和二氧化锰加入试管中充分加热
D.向pH=13的NaOH溶液中加水稀释
3.有M、N、X、Y四种物质,在一定条件下充分反应后,测得各物质在反应前后的质量如下表所示:
对该反应的下列说法中错误的是( )
A.该反应生成的N、Y的质量比为9∶8
B.该反应属于化合反应
C.该反应属于分解反应
D.M在反应中可能作催化剂
二、填空题
4.化学课上老师表演了一个小魔术——“无中生有”:相同条件下,向A、B两个体积相同的集气瓶中分
别充满无色的硫化氢(HS)气体和二氧化硫气体。如图所示,抽走毛玻璃片,瓶口对紧,颠倒几次,使两种
2
气体充分混合。一会儿,观察到两瓶内壁附着淡黄色固体颗粒。
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第1页 共7页让更多的孩子得到更好的教育
请回答下列问题:
(1)若用“ ”表示氢原子,用“○”表示氧原子,用“ ”表示硫原子,上述反应过程可用图表
示:
该反应的化学方程式为________________;硫化氢、二氧化硫中硫元素的化合价分别为__________。
(2)如果这两个瓶子是质地较软的塑料瓶,我们将会观察到塑料瓶变瘪了,原因是_____________
。
(3)已知相同条件下,相等体积的气体所含的分子数目相等。反应完毕,瓶中剩余的气体为_______,
处理该气体的方法是 。
5.实验室用98%的浓硫酸配制成稀硫酸,并与锌粒反应制取氢气。
(1)查阅资料。
20℃时不同质量分数硫酸的密度(g/mL)
质量分 0%(纯 1% 4% 10% 16% 24% 32% 36% 44% 49% 60% 98%
数 水)
密度 1.00 1.01 1.02 1.07 1.11 1.17 1.24 1.27 1.34 1.39 1.50 1.84
分析以上数据,可得出结论(写2条):
①________________________;②________________________。
(2)计算。
配制200 g 24.5%的稀硫酸,需________g 98%的浓硫酸和________g水。实际操作时,取98%的浓
硫酸________mL(精确到1 mL)。
(3)配制稀硫酸。
分别用量筒量取所需水和浓硫酸,先将________倒入烧杯中,然后
。
(4)制取氢气。
①下图中可用于制取、收集氢气的装置是________(填字母);
②检验氢气纯度的方法如图所示,表明氢气不纯的现象是________________。
6.某课外活动小组用化学卡片玩起了趣味“接龙”游戏。下图是其中一位同学自创的“回龙”谜宫,
“——”表示相连的两种物质可以发生反应,“→”表示生成的物质。
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第2页 共7页让更多的孩子得到更好的教育
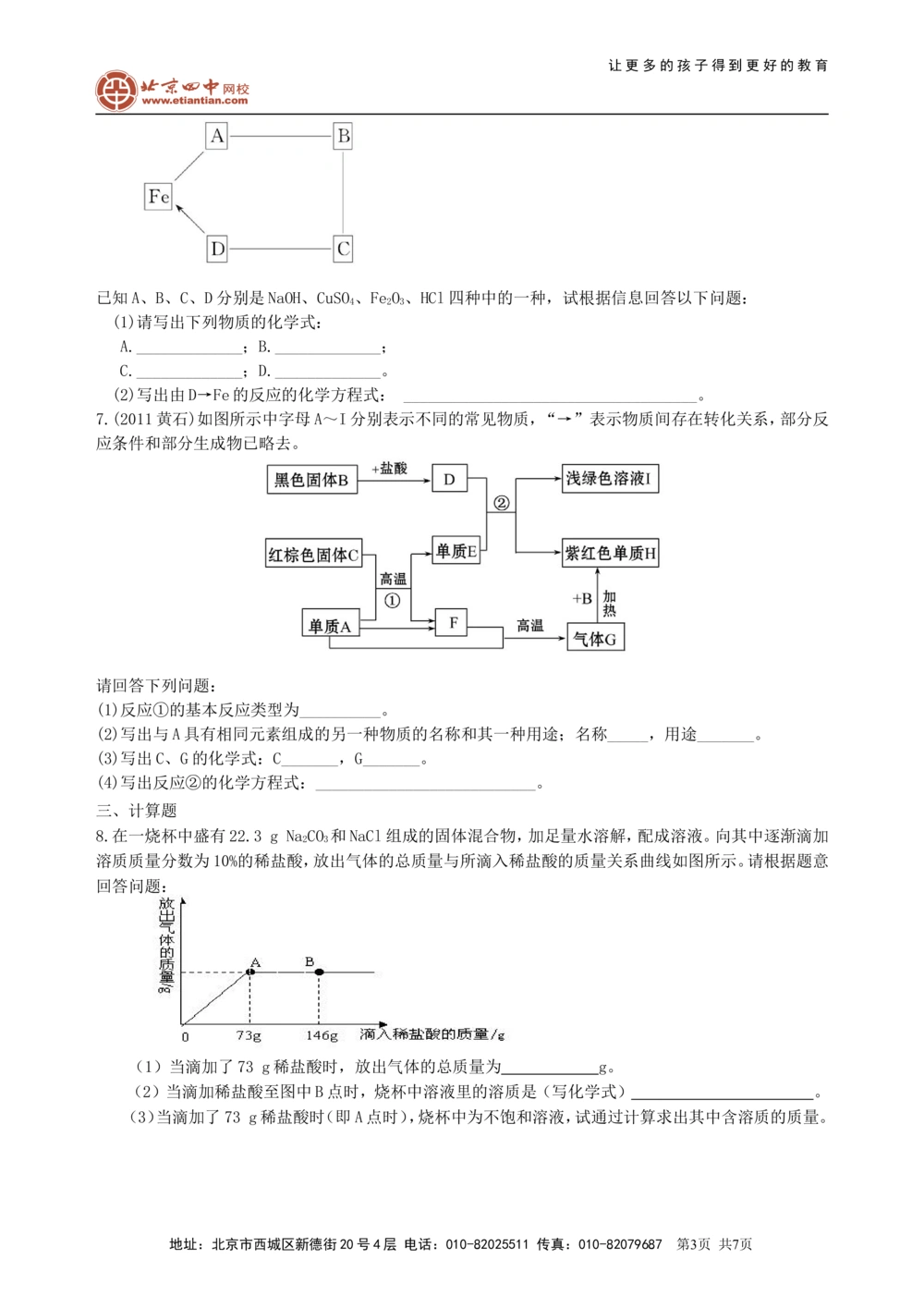
已知A、B、C、D分别是NaOH、CuSO、FeO、HCl四种中的一种,试根据信息回答以下问题:
4 2 3
(1)请写出下列物质的化学式:
A._____________;B._____________;
C._____________;D._____________。
(2)写出由D→Fe的反应的化学方程式: ____________________________________。
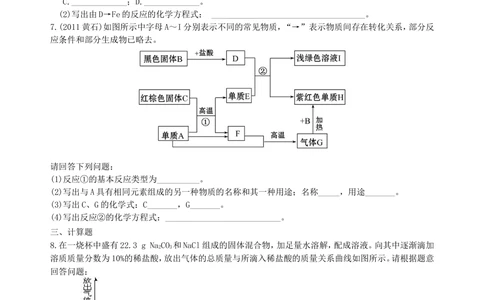
7.(2011黄石)如图所示中字母A~I分别表示不同的常见物质,“→”表示物质间存在转化关系,部分反
应条件和部分生成物已略去。
请回答下列问题:
(1)反应①的基本反应类型为__________。
(2)写出与A具有相同元素组成的另一种物质的名称和其一种用途;名称_____,用途_______。
(3)写出C、G的化学式:C_______,G_______。
(4)写出反应②的化学方程式:___________________________。
三、计算题
8.在一烧杯中盛有22.3 g NaCO 和NaCl组成的固体混合物,加足量水溶解,配成溶液。向其中逐渐滴加
2 3
溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示。请根据题意
回答问题:
(1)当滴加了73 g稀盐酸时,放出气体的总质量为 g。
(2)当滴加稀盐酸至图中B点时,烧杯中溶液里的溶质是(写化学式) 。
(3)当滴加了73 g稀盐酸时(即A点时),烧杯中为不饱和溶液,试通过计算求出其中含溶质的质量。
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第3页 共7页让更多的孩子得到更好的教育
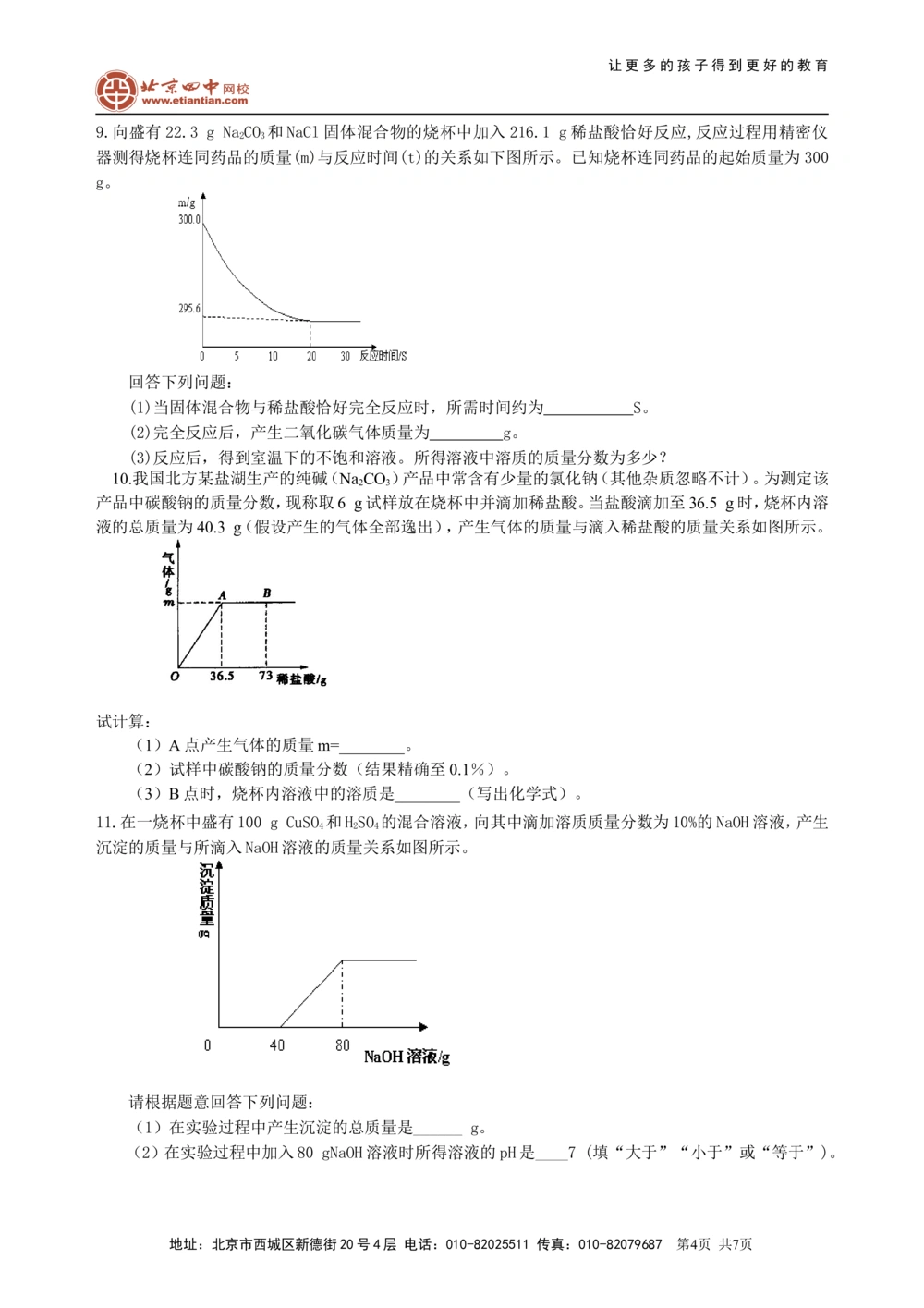
9.向盛有22.3 g NaCO 和NaCl固体混合物的烧杯中加入216.1 g稀盐酸恰好反应,反应过程用精密仪
2 3
器测得烧杯连同药品的质量(m)与反应时间(t)的关系如下图所示。已知烧杯连同药品的起始质量为300
g。
回答下列问题:
(1)当固体混合物与稀盐酸恰好完全反应时,所需时间约为 S。
(2)完全反应后,产生二氧化碳气体质量为 g。
(3)反应后,得到室温下的不饱和溶液。所得溶液中溶质的质量分数为多少?
10.我国北方某盐湖生产的纯碱(NaCO)产品中常含有少量的氯化钠(其他杂质忽略不计)。为测定该
2 3
产品中碳酸钠的质量分数,现称取6 g试样放在烧杯中并滴加稀盐酸。当盐酸滴加至36.5 g时,烧杯内溶
液的总质量为40.3 g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示。
试计算:
(1)A点产生气体的质量m=________。
(2)试样中碳酸钠的质量分数(结果精确至0.1%)。
(3)B点时,烧杯内溶液中的溶质是________(写出化学式)。
11.在一烧杯中盛有100 g CuSO 和HSO 的混合溶液,向其中滴加溶质质量分数为10%的NaOH溶液,产生
4 2 4
沉淀的质量与所滴入NaOH溶液的质量关系如图所示。
请根据题意回答下列问题:
(1)在实验过程中产生沉淀的总质量是______ g。
(2)在实验过程中加入80 gNaOH溶液时所得溶液的pH是____7 (填“大于”“小于”或“等于”)。
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第4页 共7页让更多的孩子得到更好的教育
(3)在实验过程中加入80 gNaOH溶液时,通过计算求此时所得不饱和溶液中溶质的质量分数。(计算
结果精确至0.1%)
【答案与解析】
1.【答案】A
【解析】煅烧石灰石生成固体氧化钙和气体二氧化碳,随着反应的进行,固体质量减少但不能减至为零。
2.【答案】A
【解析】因原硝酸钾溶液不饱和,刚开始加入的硝酸钾晶体会溶解,溶质质量分数增加,溶液一旦饱和,
溶质质量分数不再变化;BaCl 溶液中随着稀HSO 的滴入生成的沉淀逐渐增加,BaCl 一旦反应结束,生
2 2 4 2
成沉淀的质量就不再变化l因为KClO 中混有催化剂MnO ,受热分解除生成O 外还生成固体KCl,所以
3 2 2
固体质量减小,但不会为零;碱在稀释时,其pH接近于7,但永远达不到7,也不能小于7。
3.【答案】B
【解析】在化学反应中,质量减少的为反应物,质量增多的为生成物。分析表格得到N增多18 g,Y增多
16 g,X减少34 g。所以该反应为X N+Y,属于分解反应,生成的N、Y的质量比为9∶8 ,M质量没变,
可能作催化剂。
4.【答案】(1)2HS+SO=3S↓+2H O -2、+4
2 2 2
(2)HS与SO 反应后生成固态的硫和液态的水,使瓶内的压强小于瓶外的大气压,所以塑料瓶变瘪
2 2
了
(3)SO 向瓶内倒入NaOH溶液,振荡
2
【解析】由图示知2个HS分子与1个SO 分子生成了3个S原子和2个HO分子,故可写出化学方程
2 2 2
式;根据在化合物中元素正负化合价的代数和为零,可求出H2S中S显-2价,SO 中S显+4价。两个塑
2
料瓶变瘪的原因是HS和SO 反应的产物是固体和液体,使瓶内压强减小,所以塑料瓶变瘪了。根据2个
2 2
HS分子恰好与1个SO 分子反应.知反应后SO 有剩余,可利用NaOH溶液与SO 反应除去SO 。
2 2 2 2 2
5.【答案】(1)①硫酸质量分数越大溶液密度越大 ②随着质量分数增大,密度增大幅度变大
(2)50 150 27 (3)水 再将浓硫酸沿烧杯内壁慢慢注入水中,并用玻璃棒不断搅拌
(4)①AD ②听到尖锐爆鸣声
【解析】稀释溶液,溶质质量不变,计算液体体积可根据公式V=m/ρ求得。稀释浓硫酸一定将浓硫酸注
入水中,切不可将水倒人浓硫酸中。实验室制H 是“固体与液体常温”反应,故选A,由于氢气密度比空
2
气小,收集装置选D。检验氢气纯度时听到“噗噗声”表明氢气比较纯净;听到“尖锐爆鸣声”表明氢气
不纯。
6. 【答案】
(1)CuSO NaOH HCl FeO
4 2 3
(2)FeO+3CO 2Fe+3CO(或其他合理答案)
2 3 2
【解析】(1)由图示信息:D→Fe可知,D可生成Fe,所以D中含铁元素,即D为FeO,由图示信息可知
2 3
FeO 能与C发生反应,由题给物质可知C为HCl,由B与C可发生反应,推知B为NaOH,故A为CuSO。
2 3 4
(2)D→Fe即FeO→Fe,发生了还原反应,则另一反应物为还原剂,可为CO、H、C等。可写出相应反应
2 3 2
的化学方程式,注意反应条件及配平。
7.【答案】
(1)置换反应
(2)金刚石 制成钻石(或石墨 作润滑剂等合理即可)
(3)FeO CO (4)Fe+CuCl=Cu+FeCl
2 3 2 2
【解析】由H是紫红色单质可确定H为铜,由B能生成铜且是黑色固体可确定B为CuO,进一步可确定D
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第5页 共7页让更多的孩子得到更好的教育
为CuCl;由I是浅绿色溶液可知I为含有Fe2+的溶液,由单质E能与CuCl 反应生成Cu和Fe2+盐溶液知,E
2 2
为Fe,I为FeCl 溶液;由C是红棕色固体且能生成Fe知C为FeO,由单质A具有还原性且能反应生成另
2 2 3
一具有还原性的气体G知A为C、G为CO、F为CO。
2
8.【答案】
(1)4.4 (2)NaCl 、HCl
(3)解:73 g10%的稀盐酸中含HCl的质量是:73 g×10%=7.3 g
设参加反应的碳酸钠的质量为x,反应生成的氯化钠的质量为y。
NaCO + 2HCl = 2NaCl + CO↑ + HO
2 3 2 2
106 73 117
x 7.3 g y
106:73=x:7.3g 73:117=7.3g:y
x=10.6 g y=11.7 g
烧杯里不饱和溶液中溶质的质量为: 117. g + (22.3 g-10.6 g) = 23.4 g
答:A点对应的不饱和溶液中溶质的质量为23.4g。
【 解 析 】 由 题 意 知 : 在 NaCO 和 NaCl 组 成 的 混 合 溶 液 中 滴 加 稀 盐 酸 , 只 发 生 :
2 3
NaCO+2HCl=2NaCl+HO+CO↑,即:图像中OA段表示的反应过程;A点表示:盐酸与碳酸钠恰好完全反应,
2 3 2 2
产生CO 气体的质量达到最大值;溶液中溶质只有NaCl,且其质量为反应生成的NaCl和原混合物中含有
2
的NaCl质量之和。从A到B段,表示滴加的稀盐酸已经过量,无反应发生。故B点时,溶液中的溶质除了
NaCl以外还应该有过量的HCl。
9.【答案】
(1)20 (2)4.4 g
(3)解:设参加反应的碳酸钠的质量为x,反应生成的氯化钠的质量为y。
NaCO + 2HCl = 2NaCl + CO↑ + HO
2 3 2 2
106 117 44
x y 4.4 g
106:44=x:4.4g 117:44=y:4.4g
解得:x=10.6 g y=11.7 g
烧杯里不饱和溶液中溶质总质量为: 11.7 g + (22.3 g-10.6 g) = 23.4 g
烧杯里不饱和溶液的质量为: 22.3 g+216.1 g-4.4 g = 234 g
所得不饱和溶液的溶质质量分数:(23.4g÷234g)×100%=10%
答:所得溶液中溶质的质量分数为10%。
【解析】由图像变化趋势可知:从0~20秒,m逐渐减少,其原因是碳酸钠与盐酸反应产生的二氧化碳气
体跑出去了;从20秒开始,m不变了,即盐酸与碳酸钠反应结束了。故:二氧化碳的质量为300 g -295.6
g=4.4 g,然后据此代入化学方程式即可求出其它量。
10.【答案】(1)2.2 g
(2)解;设纯碱试样中碳酸钠的质量为x。
NaCO+2HCl=2NaCl+H O+CO ↑
2 3 2 2
106 44
x 2.2 g
x=5.3 g
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第6页 共7页让更多的孩子得到更好的教育
试样中碳酸钠的质量分数为
答:试样中NaCO 的质量分数为88.3%。
2 3
(3)NaCl、HCl
【解析】(1)产生气体CO 的质量:6 g+36.5 g-40.3 g=2.2 g;(2)根据2.2 g CO 可计算出6 g试样
2 2
中NaCO 的质量,从而求出NaCO 的质量分数;(3)A点表示NaCO 与盐酸恰好完全反应,当由A到B
2 3 2 3 2 3
时,表示加入盐酸过量,所以B点烧杯内溶液中溶质是NaCl和HCl。
11.【答案】
(1)4.9 g (2)等于
(3)解:设与硫酸反应生成的硫酸钠质量为x,与硫酸铜反应生成的硫酸钠质量为y。
2NaOH+HSO=NaSO+2HO
2 4 2 4 2
80 142
40 g×10% x
解得:x=7.1 g
2NaOH + CuSO = NaSO+ Cu(OH)↓
4 2 4 2
80 142
(80 g—40 g)×10% y
解得:y=7.1 g
不饱和溶液中NaSO 总质量为: 7.1 g+7.1 g = 14.2 g
2 4
不饱和溶液的质量为: 100 g+80 g-4.9 g = 175.1 g
所得不饱和溶液中NaSO 质量分数:(14.2g÷175.1g)×100%=8.1%
2 4
答:所得不饱和硫酸钠溶液中溶质的质量分数为8.1%。
【解析】由图像知,NaOH溶液的质量在 0~40 g之间并没有沉淀产生,故先发生的反应是:
2NaOH+HSO=NaSO+2HO。NaOH溶液的质量在40 g~80 g之间,沉淀质量随着加入NaOH溶液质量的增加
2 4 2 4 2
而逐渐达到最大值,故发生:2NaOH+CuSO=NaSO+Cu(OH)↓。在NaOH溶液加至80 g时,所得溶液中溶质
4 2 4 2
只有硫酸钠,且质量为上述两个反应产生的硫酸钠质量之和。需要注意的是,溶液质量的求法一般是:进
入反应容器的物质总质量减去沉淀质量、难溶性杂质质量和气体质量;求溶质质量时,要特别注意溶质包
括哪几部分质量,不要有遗漏。
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第7页 共7页