文档内容
曲靖一中 2025 届高考决胜全真模拟卷(二)参考答案
一、单选题(每题 3分)
题号 1 2 3 4 5 6 7 8 9 10
答案 A B A C A B A C B D
题号 11 12 13 14
答案 D C C D
二、单选题(除特殊标注外,每空 2分)
15.(1)5s25p3 (2)CuH O H SO CuSO 2H O (3) 1.7,2.0
2 2 2 4 4 2
(4)若加入Na S的量过少,则沉铜不完全;加入量过多,则会生成H S,污染大气
2 2
(5)H SO (6) 2 不一定
2 4
【分析】该工艺流程原料铅渣选铁尾矿(主要含有FeSbS、SiO 、Cu和CuO),产品为有色金属锑和铜,“氧化
2
酸浸”时SiO 不发生反应,滤渣主要成分除去,FeSbS、Cu和CuO溶解以Sb3、Fe3、Cu2+形式进入滤液1,
2
“沉锑”时,加入氨水调节pH值,使Sb3转化为SbOH 分离出来,而Fe3不沉淀,“沉铁”时,继续加入氨水
3
调节pH值,使Fe3完全沉淀分离出来,加入Na S“沉铜”使Cu2+转化为CuS。
2
【详解】(1)Sb位于第五周期第ⅤA族,价电子排布式为5s25p3;
(2)H O 作氧化剂在酸性环境下氧化Cu:CuH O H SO CuSO 2H O ;
2 2 2 2 2 4 4 2
(3)“沉锑”时,Sb3沉淀完全,根据K
sp
SbOH
3
c Sb3 c3 OH 1.251042,则
c3 OH 1.251037 molL13,c OH 51013molL1,pOH=12.3,pH=1.7;
Fe3开始沉淀时,根据K
sp
FeOH
3
c Fe3 c3 OH =2.81039,c Fe3 0.0028molL1,则
c3 OH 11036 molL1 3 ,c OH 11012molL1,pOH=12,pH=2;“沉锑”时,Sb3需沉淀完全而Fe3
不可开始沉淀,调节的pH范围为 1.7,2.0;
(4)若加入的Na S的量过少,c
S2
过小,沉铜不完全;加入Na S量过大,易产生H S的有毒有害气体;
2 2 2
(5)滤液2中有剩余的H SO ,可以回到“氧化酸浸”循环使用;(6)酒石酸分子中连有羟基官能团的2个碳
2 4
原子为手性碳原子;酒石酸分子含有2个对称的手性碳原子,故该分子不一定是手性分子;
16.【答案】(1) 球形冷凝管(1分) 吸收氨气 (2)产物 CoNH 3 6 Cl 2 的产率小 (3)A
1(4)2CoCl 2 +8NH 3 +H 2 O 2 +2NH 4 Cl=2 CoNH 3 5 Cl Cl 2 2H 2 O (5)乙醇 (6) ×100% (7)小于
0.8×238
【分析】步骤I中氯化铵、浓氨水、CoCl
2
6H
2
O反应,得到
CoNH
3
6
Cl
2
沉淀,25反0.5应式为
CoCl
2
+6NH
3
=
CoNH
3
6
Cl
2
;步骤II中加入30%过氧化氢,发生反应
2
CoNH
3
6
Cl
2
+H
2
O
2
+2NH
4
Cl=2
CoNH
3
5
H
2
O
Cl
3
4NH
3
,得到
CoNH
3
5
H
2
O
Cl
3
溶液;步骤III中加
入浓盐酸,存在平衡
CoNH
3
5
H
2
O
3 3Cl
CoNH
3
5
Cl
Cl
2
H
2
O,增加溶液中氯离子浓度,有助于
反应正向进行,有利于CoNH ClCl 沉淀的形成。据此解答:
3 5 2
【详解】(1)加入过氧化氢后的反应中有氨气产生,因此仪器d中需要加入氯化钙吸收氨气;
(2)浓氨水中存在电离平衡NH H O NH OH,加入氯化铵,NH浓度大抑制氨水的电离平衡,如果
3 2 4 4
不加氯化铵,氨水发生电离导致NH 浓度小,产物CoNH Cl 的产率小。
3 3 6 2
(5)紫红色沉淀先用冷水洗去表面杂质,再用冷的盐酸洗涤,使得
CoNH
3
5
H
2
O
3 Cl
CoNH
3
5
Cl
2 H
2
O平衡正向移动,减少产物损失,再用乙醇,洗去冷的盐酸。
(7)Co3+与NH 反应的K更大,反应进行的更彻底,CoNH 3 更稳定,故答案为:小于。
3 3 6
17.(1)413.3(2)AC(3) 50 24(4) 2CH OH催化剂CH OCH H O Sr-SAPO对反应Ⅰ的活化
3 3 3 2
能降低程度大于SAPO
(5)温度升高,反应Ⅰ正向移动,反应Ⅱ逆向移动,400~500℃内,Ⅰ、Ⅱ的移动程度相当,几乎不变
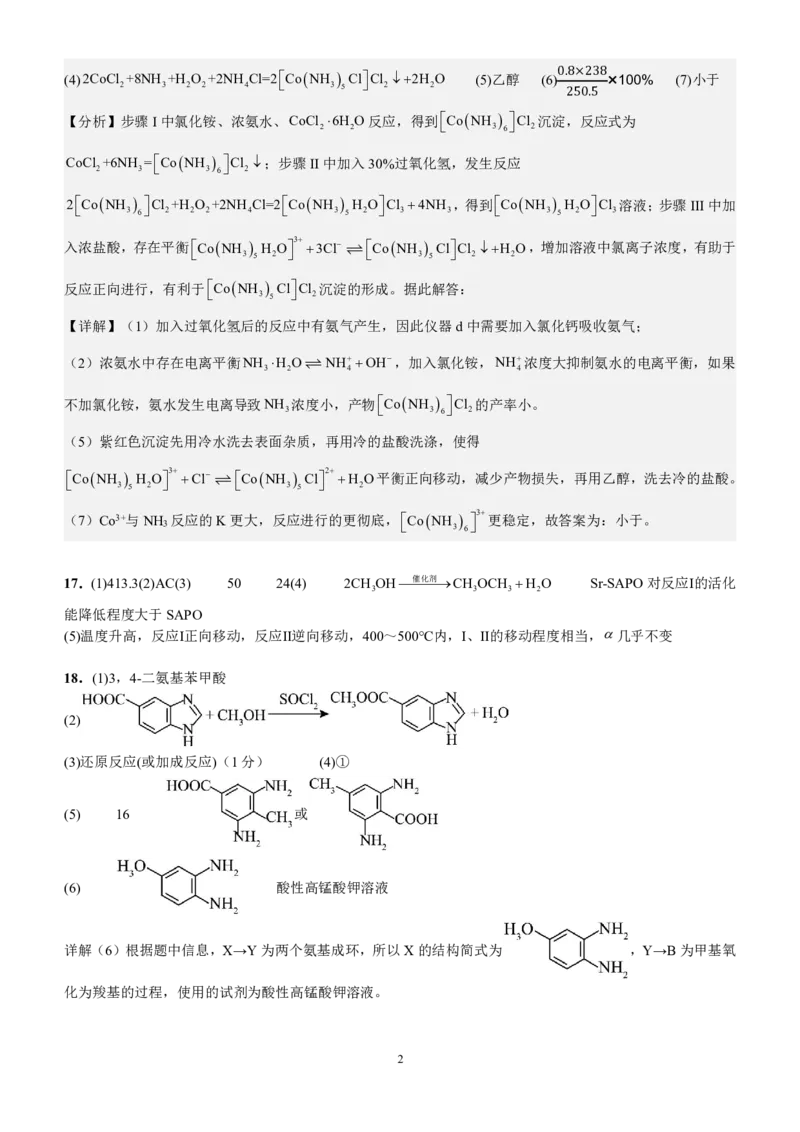
18.(1)3,4-二氨基苯甲酸
(2)
(3)还原反应(或加成反应)(1分) (4)①
(5) 16 或
(6) 酸性高锰酸钾溶液
详解(6)根据题中信息,X→Y为两个氨基成环,所以X的结构简式为 ,Y→B为甲基氧
化为羧基的过程,使用的试剂为酸性高锰酸钾溶液。
2