文档内容
2023-2024 学年高考第一次联合调研抽测
高三化学试题
(分数:100分,时间:75分钟)
一、选择题
1.在 反应中,表示该反应速率最快的是
A. B.
C. D.
2.在C H N中,N原子以三个单键与其他原子相连接,其同分异构体的数目为
4 11
A.9 B.8 C.7 D.6
3.下列有关生活中的化学知识叙述不正确的是
A.硫酸铜可用于游泳池消毒,也可用于配制农业杀菌剂
B.铁表面自然形成的铁锈比较疏松,不能阻止内层金属被空气氧化;钢制品往往要通过一定的发蓝
(或发黑)处理,使其表面产生致密且极薄的氧化物膜起到保护作用
C.乙二醇是一种无色、黏稠、有甜味的液体,主要用来生产聚酯纤维。乙二醇的水溶液凝固点很高,
可作汽车发动机的抗冻剂
D.热压氮化硅的强度很高,是世界上最坚硬的物质之一,具有高强度、低密度、耐高温等优点,
Si N 陶瓷能替代合金钢,用于制造汽车发动机的新型耐高温结构材料
3 4
4.下列说法正确的是
A. 和 互为同分异构体
B.乙酸与软脂酸互为同系物
C.单晶硅和石英互为同素异形体
D. 和 是两种不同的元素
5.用下图所示装置检验气体时,必需除杂的是
选
气体的制备 试剂X 试剂Y
项
A 二氧化锰和浓盐酸共热制备 饱和食盐水 碘化钾淀粉溶液
B 向 固体中滴加70%硫酸制备 浓硫酸 品红溶液
化学试卷 第 1 页 共 6 页
学科网(北京)股份有限公司C 向电石中滴加饱和食盐水制备 溶液 酸性溶液
D 与NaOH乙醇溶液共热制备 的 溶液
A.A B.B C.C D.D
6.在一定温度下,可逆反应A(g)+3B(g)⇌2C(g)达到平衡状态的标志是
A.C的生成速率与C的分解速率相等
B.单位时间生成nmolA,同时生成3nmolB
C.A、B、C的浓度相等
D.A、B、C的分子数比为1∶3∶2
7.《本草纲目》中有“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”记载。有关说法错误的是
A.薪柴之灰可做钾肥 B.取碱浇衣存在水解反应
C.碱浣衣与肥皂浣衣原理不同 D.上述过程涉及溶解、过滤、蒸馏操作
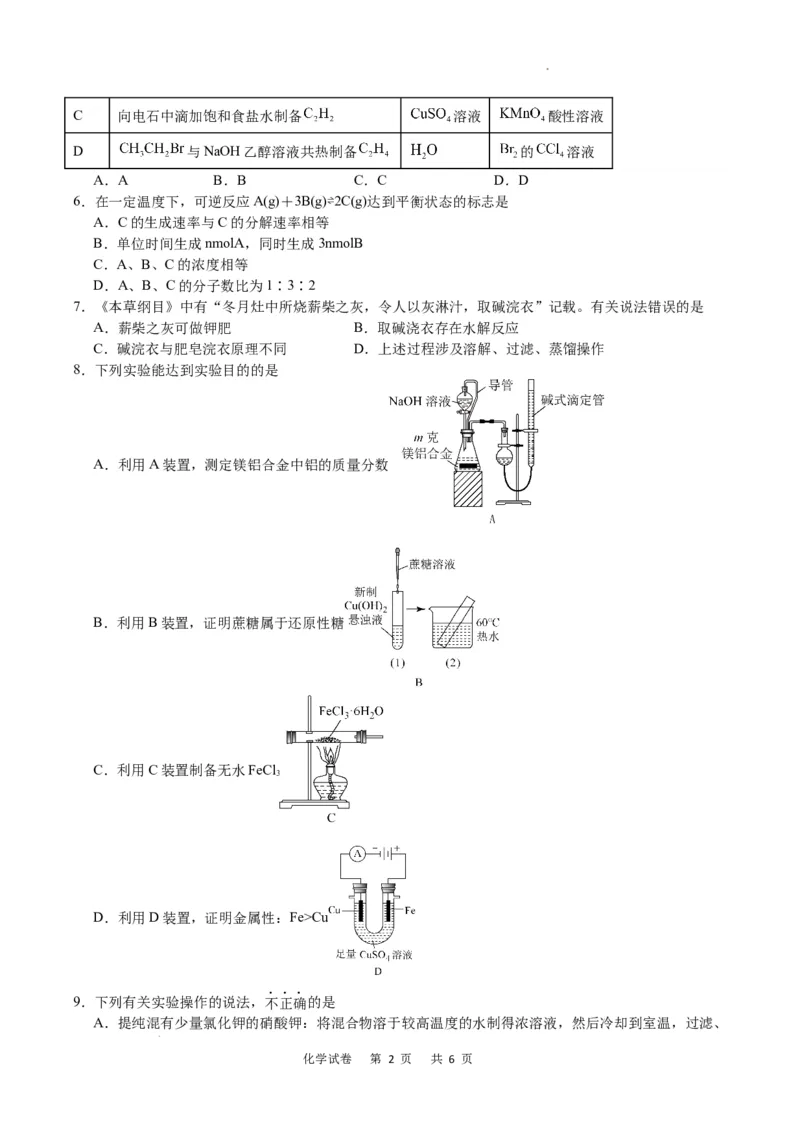
8.下列实验能达到实验目的的是
A.利用A装置,测定镁铝合金中铝的质量分数
B.利用B装置,证明蔗糖属于还原性糖
C.利用C装置制备无水FeCl
3
D.利用D装置,证明金属性:Fe>Cu
9.下列有关实验操作的说法,不正确的是
A.提纯混有少量氯化钾的硝酸钾:将混合物溶于较高温度的水制得浓溶液,然后冷却到室温,过滤、
化学试卷 第 2 页 共 6 页
学科网(北京)股份有限公司洗涤、干燥,得到较高纯度的硝酸钾晶体
B.检验溶液中的Na+:取一根洁净的铂丝,放在酒精灯火焰上灼烧至无色,然后蘸取少量试液,置于
火焰。上灼烧,若火焰呈黄色,则含有Na+
C.分离分液漏斗中互不相溶的两种液体:打开上口活塞,转动旋塞将下层液体放出,然后关闭旋塞,
将上层液体从上口倒出
D.配制100mL0.1mol·L-1氯化钠溶液:称取0.585g氯化钠固体,放入100mL量筒中,加水定容至
100mL刻度线
10.下列说法正确的是
A.无论是酸式或碱式滴定管装标准液前,都必须先用蒸馏水润洗
B.要制得无水三氯化铁可将三氯化铁溶液蒸干
C.分离乙醇和乙酸乙酯的混合物需要用分液漏斗
D.容量瓶用蒸馏水洗净后必须经酒精灯加热干燥后方可使用
11.关于药物的使用说法错误的是
A.青霉素药物不良反应是过敏反应,因此用此药前要进行皮肤敏感试验
B.减少药物剂量往往达不到治疗效果,甚至会产生耐药性
C.止咳糖浆不能用饮料服药,应该用温开水冲服
D.非处方药安全系数大,可以自行购买和使用
12.在硫酸工业生产中,为了有利于SO 的转化,且能充分利用热能,采用了中间
2
有热交换器的接触室(见图)。下列说法错误的是
A.a、b两处的混合气体成分含量相同,温度不同
B.c、d两处的混合气体成分含量不同,温度相同
C.热交换器的作用是预热待反应的气体,冷却反应后的气体
D.c处气体经热交换后再次催化氧化的目的是提高SO 的转化率
2
13.硫化锌是一种优良的宽带隙半导体锂离子电池负极材料,具有在充电的同时合
金化反应的特点。在充电过程中负极材料晶胞的组成变化如图所示。
下列说法正确的是
A.当1 mol 完全转化为 时,转移电子数为2 mol
B.在 体对角线的一维空间上会出现“ ”的排布规律
C.当 完全转化为 时,每转移6 mol电子,生成3 mol LiZn(合金相)
D.若 的晶胞参数为a nm,则EF间的距离为 nm
14.如图中的两条线分别代表的是:1g C H 和1g M气体在相同容积的容器中,测得容器中的压强和温度
3 6
化学试卷 第 3 页 共 6 页
学科网(北京)股份有限公司的关系,试根据图形判断M气体可能是
A.C H B.C H C.HS D.
2 4 3 8 2
NO
2 4
二、非选择题
15.氯化铁是常见的水处理剂。某氯化铁(FeCl ·6H O)样品含有少量FeCl 杂质。现要测定其中
3 2 2
FeCl ·6H O的质量分数,实验按以下步骤进行:
3 2
已知有关离子方程式为:2Fe3+ +2I- 2Fe2++ I , I+2S O2-2I- +S O2-
2 2 2 3 4 6
(1)取少量氯化铁样品滴入50mL沸水中,加热片刻,液体呈现红褐色,反应的离子方程式为:
。
(2)操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒外,还必须有 、 (填仪器名称)。
(3)操作Ⅱ必须用到的仪器是 (选填编号);
a.50mL烧杯 b.10mL量筒 c.20mL量筒 d.25mL滴定管
指示剂是淀粉溶液,则达到滴定终点的现象是 。
(4)滴定时,消耗浓度为0.1000mol/L的标准NaSO 溶液18.17mL。该样品中FeCl ·6H O的质量分数为
2 2 3 3 2
。
(5)要把样品氯化铁中的少量FeCl 杂质除去,可用的试剂是 (选填编号)。
2
a.铁粉 b.氯水 c.溴水 d.双氧水
(6)如果采用以下步骤测定氯化铁样品中铁元素的含量,完成下列填空。
①称量样品 ②加水溶解 ③加足量氨水,沉淀 ④过滤 ⑤灼烧 ⑥称量并进行恒重操作。
还缺少的一步操作是 ;在过滤前,需要检验是否沉淀完全,其操作是 ;判断是否
恒重的标准是 。
16.二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。
(1)科学家提出由CO 制取C的太阳能工艺如图所示。
2
①若“重整系统”发生的反应中 =6,则Fe O 的化学式
x y
为 。
②“热分解系统”中每分解l mol Fe O,转移电子的物质的量为
x y
。
(2)工业上用CO 和H 反应合成二甲醚。已知:
2 2
则 。
①一定条件下,上述合成二甲醚的反应达到平衡状态后,若改变反应的某一个条件,下列变化能说明平衡
一定向正反应方向移动的是 (填代号)。
化学试卷 第 4 页 共 6 页
学科网(北京)股份有限公司a.逆反应速率先增大后减小
b.H 的转化率增大
2
c.反应物的体积百分含量减小
d.容器中的 值变小
②在某压强下,合成二甲醚的反应在不同温度、不同投料比时,CO
2
的转化率如图所示。
T 温度下,将6 mol CO 和12 mol H 充入2 L的密闭容器中,5 min
1 2 2
后反应达到平衡状态,则0~5 min内的平均反应速率 =
;K 、K 、K 三者之间的大小关系为 。
A B C
(3)常温下,用氨水吸收CO 可得到NH HCO 溶液,在NH HCO
2 4 3 4 3
溶液中,c(NH +) c(HCO -)(填“>”、“<”或“=”);反应NH +
4 3 4
+HCO
3
-+H
2
O⇌NH
3
·H
2
O+H
2
CO
3
的平衡常数K= 。(已知常温下
NH ·H O的电离平衡常数K=2×10-5mol·L-1,HCO 的电离平衡常数K=4×10-7mol·L-1,K=4×10-11mol·L-1)
3 2 b 2 3 1 2
17.MnSO ·H O是一种浅粉色晶体,易溶于水,不溶于乙醇,是饲料中常用的添加剂,也是电解制备锰
4 2
及其他锰盐的原料,工业用途广泛。某同学设计如图甲所示实验装置制备硫酸锰。
回答下列问题:
(1)仪器a的名称是 。连接好实验仪器,装药品之前需进行的操作是 。
(2)装置Ⅱ中发生反应的化学方程式为 ;装置Ⅱ中水浴温度控制在80℃左右,温度过高时反应速率可
能减慢的原因是 。
(3)结合图乙,分析反应后从溶液中获得MnSO ·H O晶体的操作为 、酒精洗涤、低温干燥。
4 2
(4)测定饲料中硫酸锰的含量常将饲料溶于水,以磷酸作络合剂,用硝酸铵作氧化剂,将试样中的二价锰
定量氧化成三价锰,过量的硝酸铵立即与产生的亚硝酸盐反应而消除其影响。然后加入指示剂,用硫酸亚
铁铵[Fe(NH )(SO )]标准溶液滴定生成的三价锰,溶液由红色变为亮黄色为滴定终点。有关反应的离子方
4 2 4 2
程式如下:
化学试卷 第 5 页 共 6 页
学科网(北京)股份有限公司①2Mn2++NO +4PO +2H+=2[Mn(PO )]3-+NO +H O;
4 2 2
②NH +NO =N ↓+2H O;
2 2
③[Mn(PO )]3-+Fe2+=Mn2++[Fe(PO)]3-。
4 2 4 2
取ag饲料,消耗浓度为cmol•L-1的硫酸亚铁铵标准溶液VmL,则饲料中MnSO ·H O的质量分数为 %
4 2
(用含a、c、V的式子表示)。若实验时未用标准溶液润洗滴定管,会导致测定结果 (填“偏大”“偏
小”或“无影响”)。
(5)用惰性电极电解MnSO 酸性溶液可制得MnO ,请写出电解法制备MnO 时的阳极反应式: 。
4 2 2
18.芳香族化合物A含有碳、氢、氧三种元素,相对分子质量为136,能与NaHCO 反应产生CO,核磁
3 2
共振氢谱显示A分子内含四种氢(原子个数比为1:2:2:3;A用KMnO 加热氧化成B,B的相对分子质量为
4
166;当A与碱石灰共热时得化合物C,C的相对分子质量为92,通常用作有机溶剂;C被KMnO 氧化后
4
生成D,D在浓硫酸催化下加热与乙醇反应生成E,E通常情况下为液体,可用于配制依兰型香精和皂用
香精,其相对分子质量为150。
已知:(1)KMnO 可将甲苯氧化为苯甲酸(2)冰醋酸与碱石灰共热后脱羧得到甲烷。
4
请回答下列问题:
(1)A中含有的官能团名称是 ,D转化为E的反应类型是 。
(2)B与足量NaHCO 反应的化学方程式是 。
3
(3)C与Cl 在光照条件下1:1反应的有机产物的结构简式是 。
2
(4)E在一定条件下可转化为D,反应的化学方程式是 。
(5)A的同分异构体有多种,其中一种F能发生银镜反应,能与金属钠反应放出氢气,但不能与Fe3+发生显色
反应,其核磁共振氢谱显示有5种不同环境的氢原子(原子个数比为1:2:2:2:1),则F的结构简式为
,F与氢气1:1加成的芳香产物G中有3种氢,G与B发生聚合反应的化学方程式是
。
化学试卷 第 6 页 共 6 页
学科网(北京)股份有限公司