文档内容
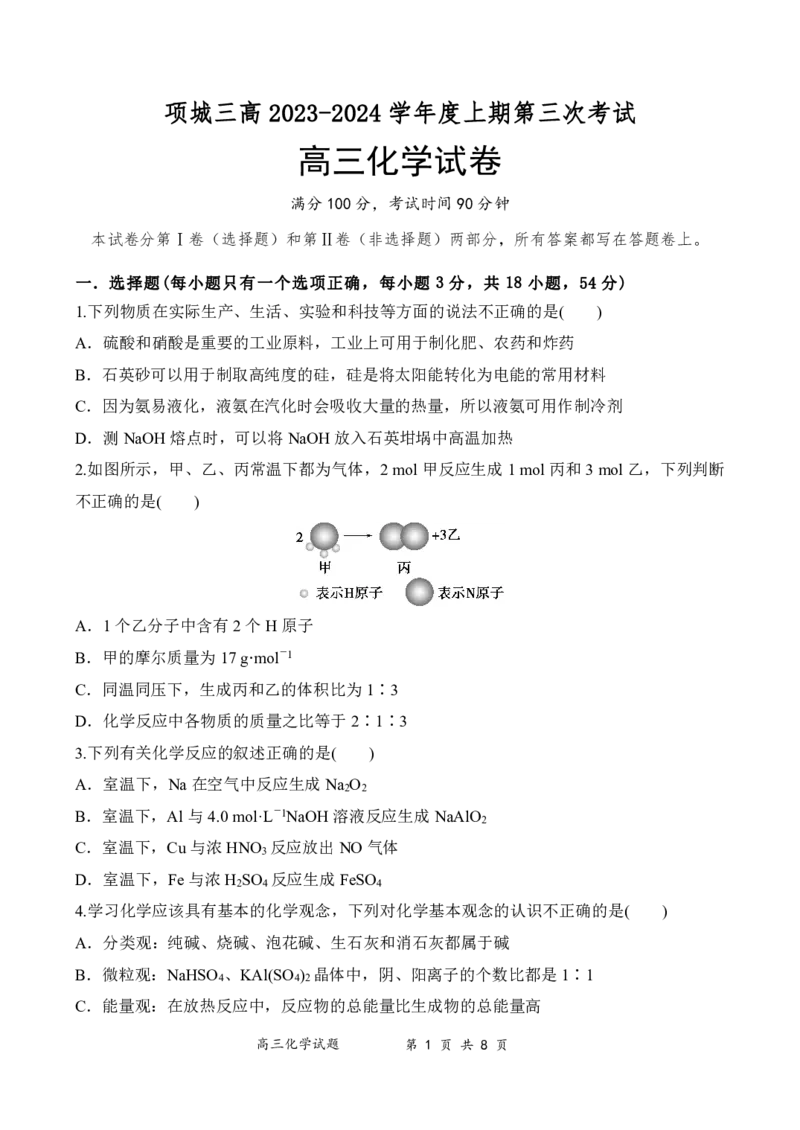
项城三高 2023-2024 学年度上期第三次考试
高三化学试卷
满分100分,考试时间90分钟
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,所有答案都写在答题卷上。
一.选择题(每小题只有一个选项正确,每小题 3 分,共 18 小题,54 分)
1.下列物质在实际生产、生活、实验和科技等方面的说法不正确的是( )
A.硫酸和硝酸是重要的工业原料,工业上可用于制化肥、农药和炸药
B.石英砂可以用于制取高纯度的硅,硅是将太阳能转化为电能的常用材料
C.因为氨易液化,液氨在汽化时会吸收大量的热量,所以液氨可用作制冷剂
D.测NaOH熔点时,可以将NaOH放入石英坩埚中高温加热
2.如图所示,甲、乙、丙常温下都为气体,2mol甲反应生成1mol丙和3mol乙,下列判断
不正确的是( )
A.1个乙分子中含有2个H原子
B.甲的摩尔质量为17g·mol-1
C.同温同压下,生成丙和乙的体积比为1∶3
D.化学反应中各物质的质量之比等于2∶1∶3
3.下列有关化学反应的叙述正确的是( )
A.室温下,Na在空气中反应生成Na O
2 2
B.室温下,Al与4.0mol·L-1NaOH溶液反应生成NaAlO
2
C.室温下,Cu与浓HNO 反应放出NO气体
3
D.室温下,Fe与浓H SO 反应生成FeSO
2 4 4
4.学习化学应该具有基本的化学观念,下列对化学基本观念的认识不正确的是( )
A.分类观:纯碱、烧碱、泡花碱、生石灰和消石灰都属于碱
B.微粒观:NaHSO 、KAl(SO ) 晶体中,阴、阳离子的个数比都是1∶1
4 4 2
C.能量观:在放热反应中,反应物的总能量比生成物的总能量高
高三化学试题 第 1 页 共 8 页
{#{QQABDYIUoggIABBAARgCQQHqCAKQkAGCAIoGABAMMAABgANABAA=}#}D.守恒观:氧化汞分解前后,元素种类和原子数目均不变
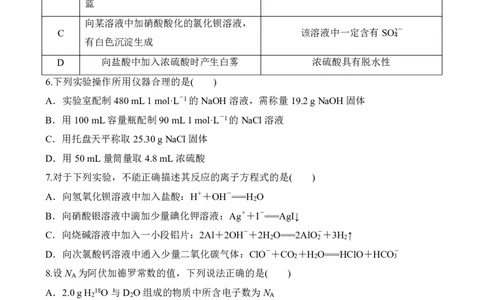
5.通过对实验现象的观察、分析推理得出正确的结论,这是化学学习的方法之一。下列对实
验现象的解释正确的是( )
选项 实验现象 解释
浓硝酸不稳定,见光易分解,生成的有
A 浓硝酸在光照条件下变黄
色产物能溶于浓硝酸
向淀粉KI溶液中通入适量Cl ,溶液变
2
B Cl 2 能与淀粉发生显色反应
蓝
向某溶液中加硝酸酸化的氯化钡溶液,
C 该溶液中一定含有SO2 4 -
有白色沉淀生成
D 向盐酸中加入浓硫酸时产生白雾 浓硫酸具有脱水性
6.下列实验操作所用仪器合理的是( )
A.实验室配制480mL1mol·L-1的NaOH溶液,需称量19.2gNaOH固体
B.用100mL容量瓶配制90mL1mol·L-1的NaCl溶液
C.用托盘天平称取25.30gNaCl固体
D.用50mL量筒量取4.8mL浓硫酸
7.对于下列实验,不能正确描述其反应的离子方程式的是( )
A.向氢氧化钡溶液中加入盐酸:H++OH-===H O
2
B.向硝酸银溶液中滴加少量碘化钾溶液:Ag++I-===AgI↓
C.向烧碱溶液中加入一小段铝片:2Al+2OH-+2H O===2AlO-+3H ↑
2 2 2
D.向次氯酸钙溶液中通入少量二氧化碳气体:ClO-+CO +H O===HClO+HCO-
2 2 3
8.设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.2.0gH 18O与D O组成的物质中所含电子数为N
2 2 A
B.64g铜与足量浓硫酸共热,转移的电子数小于2N
A
C.28g乙烯与环丙烷(C H )的混合气体中所含C—H键的数目为2N
3 6 A
D.标准状况下,22.4L甲烷完全燃烧生成的气体分子数为3N
A
9.下列实验对应的解释或结论正确的是( )
选项 实验 解释或结论
A 室温下,向含少量FeCl 3 的CuCl 2 溶液中 杂质FeCl 3 被除去,得到纯净的CuCl 2 溶
高三化学试题 第 2 页 共 8 页
{#{QQABDYIUoggIABBAARgCQQHqCAKQkAGCAIoGABAMMAABgANABAA=}#}加入铜屑,充分搅拌,过滤,得蓝色溶 液
液
Fe(NO ) 晶体溶于稀硫酸,滴加KSCN
3 2
B Fe(NO 3 ) 2 晶体已变质
溶液,溶液变红
向铅丹(Pb O )中滴加浓盐酸,生成黄绿
3 4
C 氧化性:Pb 3 O 4 >Cl 2
色气体
将铁的氧化物溶于过量稀盐酸中,再滴
D 铁的氧化物含有Fe2+
加几滴酸性KMnO 溶液,紫红色褪去
4
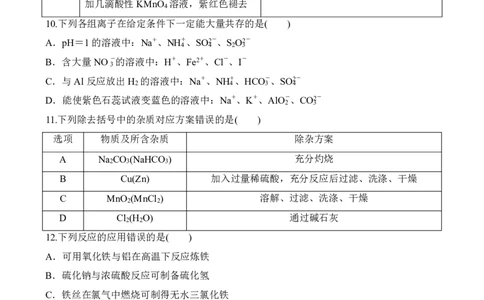
10.下列各组离子在给定条件下一定能大量共存的是( )
A.pH=1的溶液中:Na+、NH+、SO2-、S O2-
4 4 2 3
B.含大量NO-的溶液中:H+、Fe2+、Cl-、I-
3
C.与Al反应放出H 的溶液中:Na+、NH+、HCO-、SO2-
2 4 3 4
D.能使紫色石蕊试液变蓝色的溶液中:Na+、K+、AlO-、CO2-
2 3
11.下列除去括号中的杂质对应方案错误的是( )
选项 物质及所含杂质 除杂方案
A Na CO (NaHCO ) 充分灼烧
2 3 3
B Cu(Zn) 加入过量稀硫酸,充分反应后过滤、洗涤、干燥
C MnO (MnCl ) 溶解、过滤、洗涤、干燥
2 2
D Cl (H O) 通过碱石灰
2 2
12.下列反应的应用错误的是( )
A.可用氧化铁与铝在高温下反应炼铁
B.硫化钠与浓硫酸反应可制备硫化氢
C.铁丝在氯气中燃烧可制得无水三氯化铁
D.氧化钙与水反应可用于自热米饭加热
13.下列说法正确的是( )
A.22.4LCl (标准状况)与水充分反应转移1mol电子
2
B.H SO 和CuCl 均可通过化合反应得到
2 4 2
C.将蘸有浓氨水和浓硫酸的玻璃棒相互靠近,有白烟产生
D.SO 与KClO溶液反应:SO +2ClO-+H O===2HClO+SO2-
2 2 2 3
高三化学试题 第 3 页 共 8 页
{#{QQABDYIUoggIABBAARgCQQHqCAKQkAGCAIoGABAMMAABgANABAA=}#}14.下列与碳、氮、氧、硫、硅等非金属元素及其化合物有关的说法不正确的是( )
A.工业上,用焦炭在电炉中还原二氧化硅可得到含杂质的粗硅
B.氮的氧化物是形成光化学烟雾的主要物质,硫的氧化物是形成酸雨的主要物质
C.NO 、CO 和SO 溶于水均可导电,它们都是电解质
2 2 2
D.将SO 通入酸化的Ba(NO ) 溶液中会出现白色沉淀
2 3 2
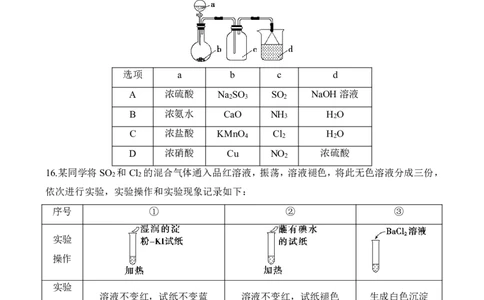
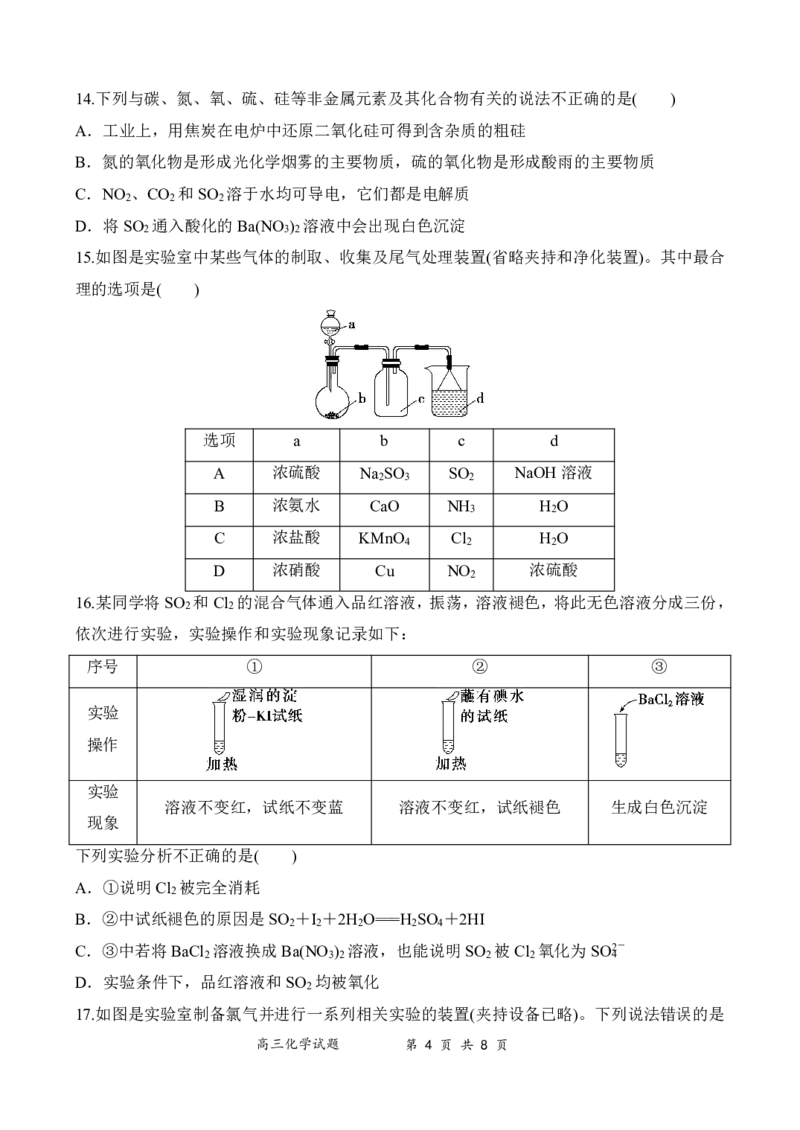
15.如图是实验室中某些气体的制取、收集及尾气处理装置(省略夹持和净化装置)。其中最合
理的选项是( )
选项 a b c d
A 浓硫酸 Na SO SO NaOH溶液
2 3 2
B 浓氨水 CaO NH H O
3 2
C 浓盐酸 KMnO Cl H O
4 2 2
D 浓硝酸 Cu NO 浓硫酸
2
16.某同学将SO 和Cl 的混合气体通入品红溶液,振荡,溶液褪色,将此无色溶液分成三份,
2 2
依次进行实验,实验操作和实验现象记录如下:
序号 ① ② ③
实验
操作
实验
溶液不变红,试纸不变蓝 溶液不变红,试纸褪色 生成白色沉淀
现象
下列实验分析不正确的是( )
A.①说明Cl 被完全消耗
2
B.②中试纸褪色的原因是SO +I +2H O===H SO +2HI
2 2 2 2 4
C.③中若将BaCl 溶液换成Ba(NO ) 溶液,也能说明SO 被Cl 氧化为SO2-
2 3 2 2 2 4
D.实验条件下,品红溶液和SO 均被氧化
2
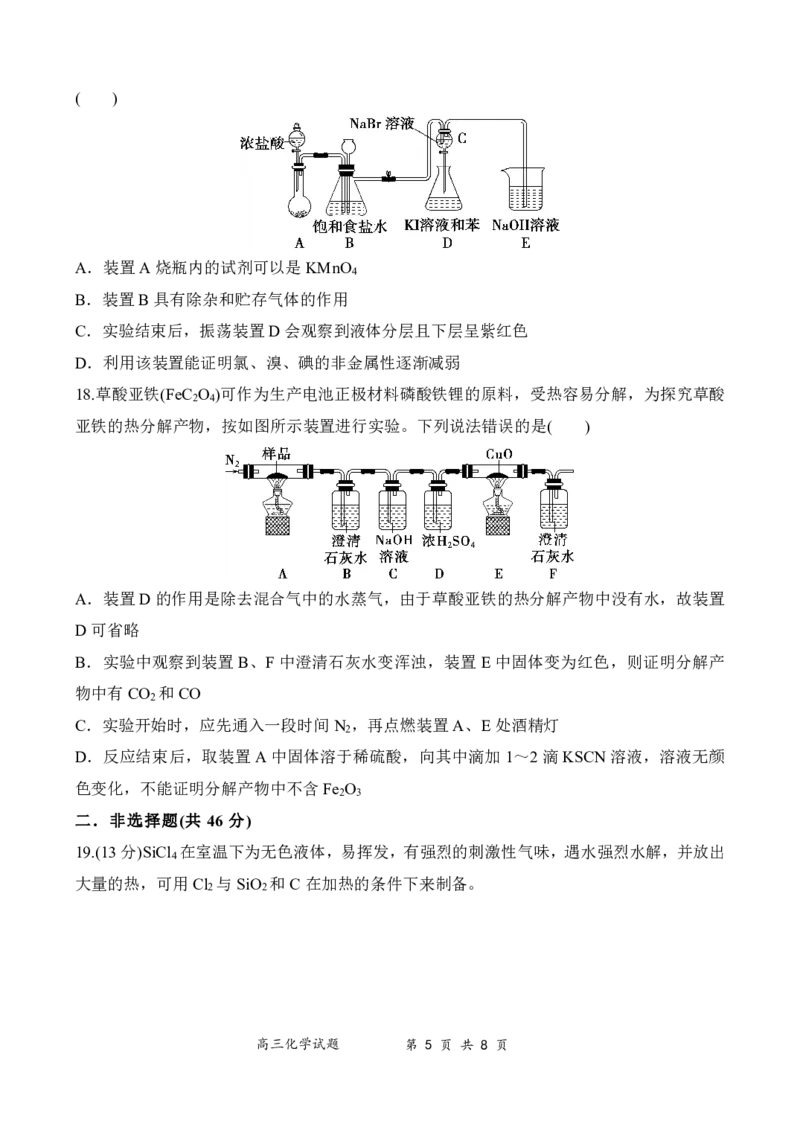
17.如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。下列说法错误的是
高三化学试题 第 4 页 共 8 页
{#{QQABDYIUoggIABBAARgCQQHqCAKQkAGCAIoGABAMMAABgANABAA=}#}( )
A.装置A烧瓶内的试剂可以是KMnO
4
B.装置B具有除杂和贮存气体的作用
C.实验结束后,振荡装置D会观察到液体分层且下层呈紫红色
D.利用该装置能证明氯、溴、碘的非金属性逐渐减弱
18.草酸亚铁(FeC O )可作为生产电池正极材料磷酸铁锂的原料,受热容易分解,为探究草酸
2 4
亚铁的热分解产物,按如图所示装置进行实验。下列说法错误的是( )
A.装置D的作用是除去混合气中的水蒸气,由于草酸亚铁的热分解产物中没有水,故装置
D可省略
B.实验中观察到装置B、F中澄清石灰水变浑浊,装置E中固体变为红色,则证明分解产
物中有CO 和CO
2
C.实验开始时,应先通入一段时间N ,再点燃装置A、E处酒精灯
2
D.反应结束后,取装置A中固体溶于稀硫酸,向其中滴加1~2滴KSCN溶液,溶液无颜
色变化,不能证明分解产物中不含Fe O
2 3
二.非选择题(共 46 分)
19.(13分)SiCl 在室温下为无色液体,易挥发,有强烈的刺激性气味,遇水强烈水解,并放出
4
大量的热,可用Cl 与SiO 和C在加热的条件下来制备。
2 2
高三化学试题 第 5 页 共 8 页
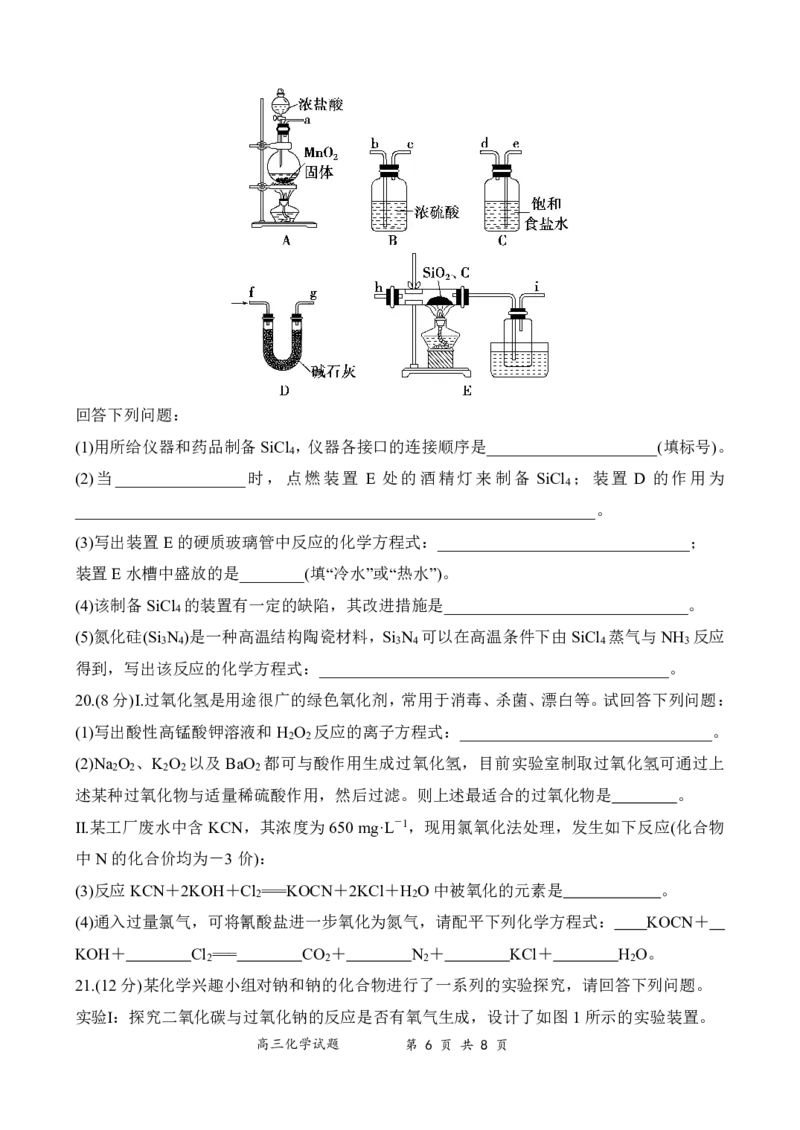
{#{QQABDYIUoggIABBAARgCQQHqCAKQkAGCAIoGABAMMAABgANABAA=}#}回答下列问题:
(1)用所给仪器和药品制备SiCl ,仪器各接口的连接顺序是_____________________(填标号)。
4
(2)当________________时,点燃装置 E 处的酒精灯来制备 SiCl ;装置 D 的作用为
4
________________________________________________________________。
(3)写出装置E的硬质玻璃管中反应的化学方程式:_______________________________;
装置E水槽中盛放的是________(填“冷水”或“热水”)。
(4)该制备SiCl 的装置有一定的缺陷,其改进措施是______________________________。
4
(5)氮化硅(Si N )是一种高温结构陶瓷材料,Si N 可以在高温条件下由SiCl 蒸气与NH 反应
3 4 3 4 4 3
得到,写出该反应的化学方程式:___________________________________________。
20.(8分)Ⅰ.过氧化氢是用途很广的绿色氧化剂,常用于消毒、杀菌、漂白等。试回答下列问题:
(1)写出酸性高锰酸钾溶液和H O 反应的离子方程式:_______________________________。
2 2
(2)Na O 、K O 以及BaO 都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上
2 2 2 2 2
述某种过氧化物与适量稀硫酸作用,然后过滤。则上述最适合的过氧化物是 。
Ⅱ.某工厂废水中含KCN,其浓度为650mg·L-1,现用氯氧化法处理,发生如下反应(化合物
中N的化合价均为-3价):
(3)反应KCN+2KOH+Cl ===KOCN+2KCl+H O中被氧化的元素是 。
2 2
(4)通入过量氯气,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式: KOCN+
KOH+ Cl === CO + N + KCl+ H O。
2 2 2 2
21.(12分)某化学兴趣小组对钠和钠的化合物进行了一系列的实验探究,请回答下列问题。
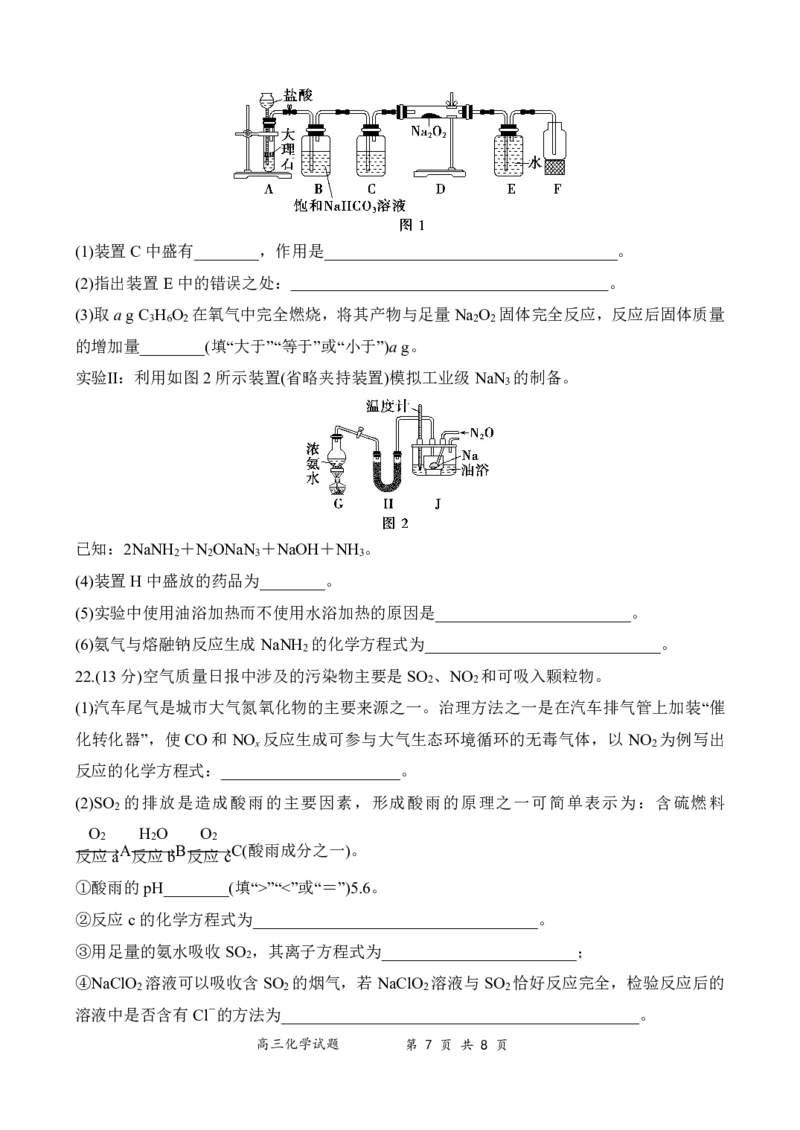
实验Ⅰ:探究二氧化碳与过氧化钠的反应是否有氧气生成,设计了如图1所示的实验装置。
高三化学试题 第 6 页 共 8 页
{#{QQABDYIUoggIABBAARgCQQHqCAKQkAGCAIoGABAMMAABgANABAA=}#}(1)装置C中盛有________,作用是____________________________________。
(2)指出装置E中的错误之处: 。
(3)取agC H O 在氧气中完全燃烧,将其产物与足量Na O 固体完全反应,反应后固体质量
3 6 2 2 2
的增加量________(填“大于”“等于”或“小于”)ag。
实验Ⅱ:利用如图2所示装置(省略夹持装置)模拟工业级NaN 的制备。
3
已知:2NaNH +N ONaN +NaOH+NH 。
2 2 3 3
(4)装置H中盛放的药品为________。
(5)实验中使用油浴加热而不使用水浴加热的原因是________________________。
(6)氨气与熔融钠反应生成NaNH 的化学方程式为_____________________________。
2
22.(13分)空气质量日报中涉及的污染物主要是SO 、NO 和可吸入颗粒物。
2 2
(1)汽车尾气是城市大气氮氧化物的主要来源之一。治理方法之一是在汽车排气管上加装“催
化转化器”,使CO和NO 反应生成可参与大气生态环境循环的无毒气体,以NO 为例写出
x 2
反应的化学方程式:______________________。
(2)SO 的排放是造成酸雨的主要因素,形成酸雨的原理之一可简单表示为:含硫燃料
2
O H O O
2 2 2
―反―应→
a
A―反―应→
b
B―反―应→
c
C(酸雨成分之一)。
①酸雨的pH________(填“>”“<”或“=”)5.6。
②反应c的化学方程式为___________________________________。
③用足量的氨水吸收SO ,其离子方程式为________________________;
2
④NaClO 溶液可以吸收含SO 的烟气,若NaClO 溶液与SO 恰好反应完全,检验反应后的
2 2 2 2
溶液中是否含有Cl-的方法为____________________________________________。
高三化学试题 第 7 页 共 8 页
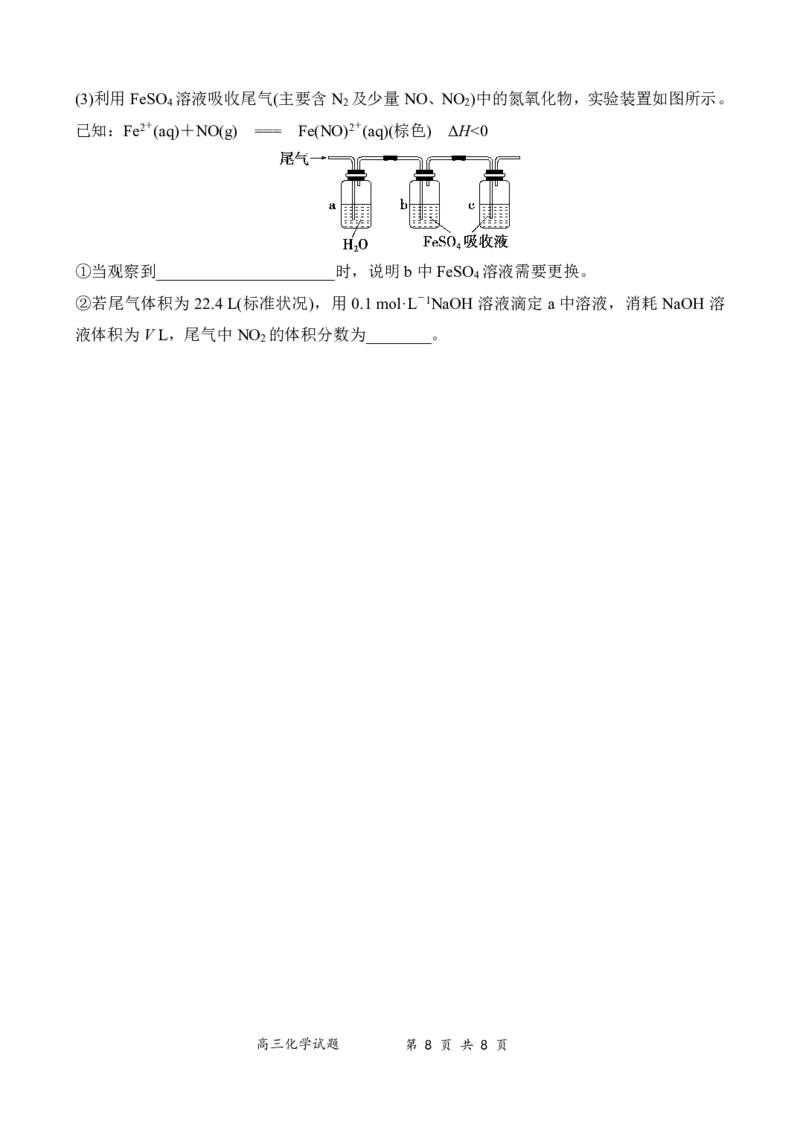
{#{QQABDYIUoggIABBAARgCQQHqCAKQkAGCAIoGABAMMAABgANABAA=}#}(3)利用FeSO 溶液吸收尾气(主要含N 及少量NO、NO )中的氮氧化物,实验装置如图所示。
4 2 2
已知:Fe2+(aq)+NO(g) === Fe(NO)2+(aq)(棕色) ΔH<0
①当观察到______________________时,说明b中FeSO 溶液需要更换。
4
②若尾气体积为22.4L(标准状况),用0.1mol·L-1NaOH溶液滴定a中溶液,消耗NaOH溶
液体积为VL,尾气中NO 的体积分数为________。
2
高三化学试题 第 8 页 共 8 页
{#{QQABDYIUoggIABBAARgCQQHqCAKQkAGCAIoGABAMMAABgANABAA=}#}