文档内容
2024 北京大兴高三(上)期末
化 学
2024.1
考 1.本试卷共8页,共19道小题,满分100分。考试时间90分钟。
生 2.在试卷和答题卡上准确填写学校名称、班级、姓名和准考证号。
须 3.试题答案一律填涂或书写在答题卡上,在试卷上作答无效。
知 4.在答题卡上,选择题用2B铅笔作答,其他题用黑色字迹签字笔作答。
可能用到的相对原子质量:H 1 O 16 Na 23 S 32 Ti 48 Ba 137
第一部分 选择题(共 42分)
本部分每小题只有一个选项符合题意,每小题3分
......
1. 2022 年 2 月,北京冬奥会秉承了创新、协调、绿色、开放、共享发展的理念。下列冬奥会使用的物品
中,主要材料不属于有机高分子材料的是
...
A B C D
冰墩墩中的聚酯纤维 速滑馆中的铝制幕墙 雪花花瓣中的聚碳酸酯 头盔表面的聚氨酯涂料
2.下列溶液中,酸碱性与其他三种不一致的是
...
A.H S溶液 B.NaHCO 溶液 C.K S溶液 D.氨水
2 3 2
3.下列有关化学用语或图示表达正确的是
A.二氧化硫的VSEPR模型:
B.CO 的电子式:
2
C.中子数为8的碳原子: 14C
8
D.基态氧原子的轨道表示式:
4. 用N 表示阿伏加德罗常数的值。下列说法正确的是
A
A.常温下,0.1 mol NH 的体积为2.24L
3
B.1 mol HC CH分子中含有σ键的数目为 2N
A
C.1 L 0.1 mol·L-1 Na CO 溶液中CO 2- 数目小于0.1N
2 3 3 A
D.25℃时, pH=5的NH Cl溶液中由水电离出的H+的浓度为10-9 mol·L-1
4
5.短周期元素G、M、W、X、Y、Z、Q的原子半径及其最高正化合价随原子序数递增的变化如图所示:
第1页/共11页下列说法正确的是
A.熔点:YM <Y
B.第一电离能:X > W > G
C.热稳定性: HQ > H Z >HW
2
D.酸性:HQO > H ZO > H YO
4 2 4 2 3
6.常温下,NH Cl溶于水得到无色溶液,为使溶液中的c(NH +):c(Cl-) = 1:1,下列采取的措施正确的是
4 4
A.加入适量的NaCl固体
B.加入适量的盐酸,抑制NH +水解
4
C.加入适量的氨水,使溶液的pH等于7
D.加入适量的NaOH固体,使溶液的pH等于7
7.下列实验事实所对应的离子方程式不正确的是
...
A.CO 溶于水产生HCO -: CO + H O H CO HCO - + H+
2 3 2 2 2 3 3
B.FeCl 溶液呈酸性: Fe3+ + 3H O === Fe(OH) ↓ +3H+
3 2 3
C.NO 溶于H O红棕色消失: 3NO + H O === H+ + 2NO - + NO
2 2 2 2 3
D.向海带灰浸出液(含I-)中滴加几滴酸化的过氧化氢溶液:2I- + H O + 2H+ ==I + 2H O
2 2 2 2
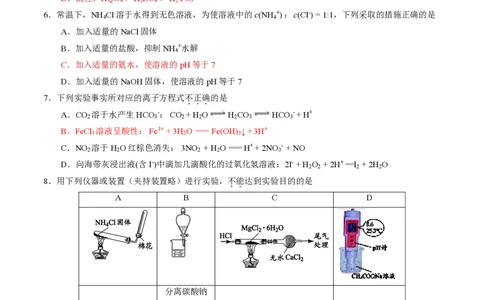
8.用下列仪器或装置(夹持装置略)进行实验,不能达到实验目的的是
..
A B C D
分离碳酸钠
实验室制取氨气 溶液和乙酸 制备无水氯化镁 证明醋酸为弱酸
乙酯
9. 离子液体具有较好的化学稳定性、较低的熔点及对无机物、有机化合物等不同物质良好溶解性等优点。
一种离子液体的结构简式如下图。
第2页/共11页下列说法不正确的是
...
A.该离子液体能与H O形成氢键
2
B.阳离子中C原子有sp2、sp3两种杂化方式
C.阴离子呈平面正方形,存在共价键和配位键
D.该离子液体熔点较低的可能原因是离子体积增大、距离增大、作用力减弱
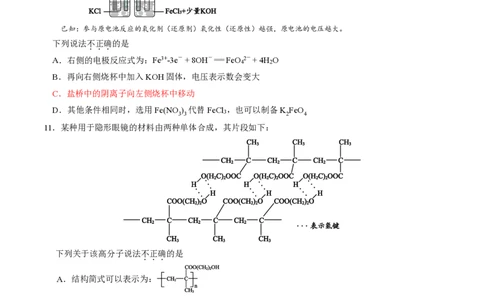
10.某小组同学在实验室利用下图装置制备水处理剂高铁酸钾(K FeO ),反应的化学方程式为:2FeCl +
2 4 3
3Cl + 16KOH 2K FeO + 12KCl + 8H O。
2 2 4 2
已知:参与原电池反应的氧化剂(还原剂)氧化性(还原性)越强,原电池的电压越大。
下列说法不正确的是
...
A.右侧的电极反应式为:Fe3+-3e- + 8OH- === FeO 4 2- + 4H 2 O
B.再向右侧烧杯中加入KOH固体,电压表示数会变大
C.盐桥中的阴离子向左侧烧杯中移动
D.其他条件相同时,选用Fe(NO ) 代替FeCl ,也可以制备K FeO
3 3 3 2 4
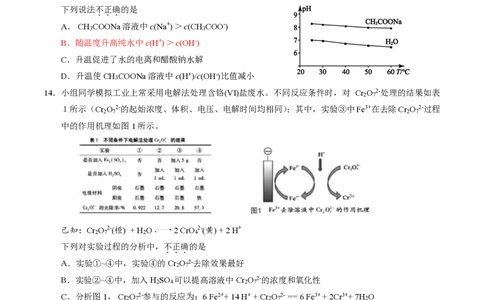
11.某种用于隐形眼镜的材料由两种单体合成,其片段如下:
下列关于该高分子说法不正确的是
...
A.结构简式可以表示为:
B.氢键对该高分子的性能会产生影响
C.合成该高分子的一种单体是CH = C(CH )COOH
2 3
D.两种单体都能与金属Na和NaHCO 反应
3
12.某同学在培养皿上做如下实验(如图所示),a、b、c、d是浸有相关溶液的滤纸。向KMnO 晶体上滴
4
加一滴浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO +16HCl = 2KCl+5Cl ↑+2MnCl +8H O
4 2 2 2
第3页/共11页下列对“实验现象”的“解释或结论”描述,不正确的是
...
选项 实验现象 解释或结论
A a处试纸变蓝 氧化性:Cl >I
2 2
B b处试纸变红 Cl +2Fe2+ == 2Cl- +2Fe3+
2
C c处试纸褪色 Cl 与H O反应生成了具有漂白性的物质
2 2
D d处红色褪去 Cl 和NaOH反应使溶液呈中性
2
13.实验测得0.5 mol·L-1 CH COONa溶液及纯水的pH随温度变化的曲线如图所示。
3
下列说法不正确的是
...
A. CH COONa溶液中c(Na+)>c(CH COO-)
3 3
B.随温度升高纯水中c(H+)>c(OH-)
C.升温促进了水的电离和醋酸钠水解
D.升温使CH COONa溶液中c(H+)/c(OH-)比值减小
3
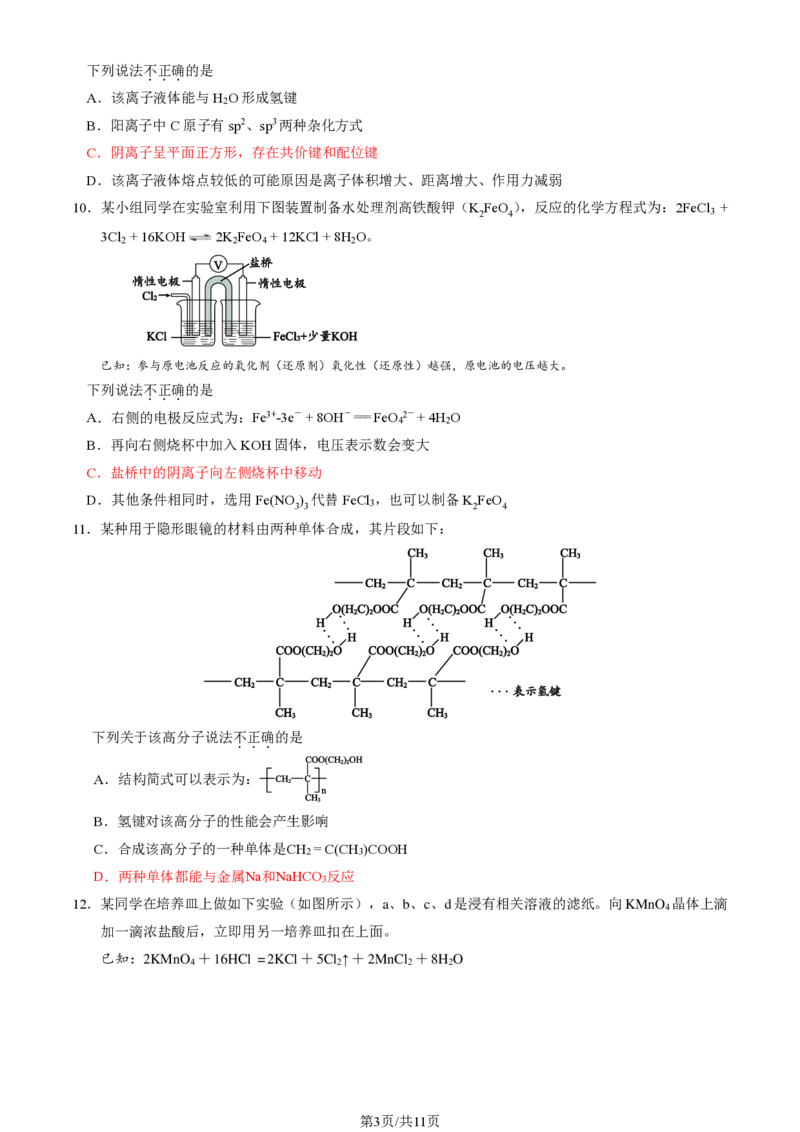
14.小组同学模拟工业上常采用电解法处理含铬(VI)盐废水。不同反应条件时,对 Cr O 2-处理的结果如表
2 7
1所示(Cr O 2-的起始浓度、体积、电压、电解时间均相同);其中,实验③中Fe3+在去除Cr O 2-过程
2 7 2 7
中的作用机理如图1所示。
已知:Cr O 2-(橙) + H O 2 CrO 2-(黄) + 2 H+
2 7 2 4
下列对实验过程的分析中,不正确的是
...
A.实验①~④中,实验④的Cr O 2-去除效果最好
2 7
B.实验②~④中,加入H SO 可以提高溶液中Cr O 2-的浓度和氧化性
2 4 2 7
C.分析图1, Cr O 2-参与的反应为:6 Fe2++ 14 H+ + Cr O 2- == 6 Fe3+ + 2Cr3++ 7H O
2 7 2 7 2
D.实验④中,阳极上Fe发生的反应为:Fe – 3e- == Fe3+
非选择题(共 58分)
15.(10分)过渡金属钛(Ti)性能优越,是继铁、铝之后应用广泛的“第三金属”。
回答下列问题。
(1)钛元素位于周期表的 区; 基态Ti原子核外电子占据的轨道数为 。
(2)下列状态的Ti原子中,失去最外层一个电子所需能量最大的是___ (填字母标号)。
a.[Ar]3d²4s¹4p¹ b.[Ar]3d²4s²
第4页/共11页c.[Ar]3d14s²4p¹ d.[Ar]3d¹4s¹4p²
(3)TiCl 是氧化法制取钛的中间产物,TiCl 分子结构与CCl 相同,二者常温下都是无色液体。TiCl 分
4 4 4 4
子的空间结构为 ,TiCl 极易水解且水解程度很大,生成TiO ·xH O沉淀,写出TiCl 水解的化学方
4 2 2 4
程式: 。
(4)钛的某配合物可用于催化环烯烃聚合,其结构如下图所示。
下列说法正确的是________(填字母)。
a.含有手性碳原子
b. 2号氧提供孤电子对与钛离子形成配位键
c. 1-4号原子不在同一平面上
d. ∠α大于∠B
(5)嫦娥三号卫星上的PIC元件(热敏电阻)的主要成分——钡钛
矿的晶胞结构如图所示。已知该晶体的密度为ρg·cm-3,阿伏加
德罗常数的值为N ,则该晶胞的边长为 cm (用含ρ、
A
第5页/共11页
N
A
的
式子表示)。(注:相对原子质量 Ba-137 Ti-48 O-16)
16.(11分) C O
2
的资源化利用是实现“碳中和、碳达峰”的途径。 C O
2
合成甲醇的过程中涉及如下反
应:
反应i. CO (g)+3H (g) CH OH(g) + H O(g) △H
2 2 3 2 1
反应ii. CO (g)+H (g) CO(g) + H O(g) △H == + 41.2 kJ·mol-1
2 2 2 2
回答下列问题。
(1)根据右图,△H = kJ·mol-1。
1
(2)T℃时,向1 L恒容、密闭容器中充入1 mol CO 和4 mol H 发生上述反
2 2
应。10 min末已达到平衡时测得容器中CO 的转化率为90%,CO的物质
2
的量为0.3 mol。
① 0~10 min内,平均反应速率v (CH OH) == mol·L-1·min-1。
3
② T℃时,反应ii的化学平衡常数K == 。
(3)将原料气n(CO ):n(H )=1:3充入某一恒容、密闭容器中,若只发生反应i,在不同催化剂作用下,
2 2
反应t min时CO 的转化率随温度的变化如下图所示。
2
① 图中达到化学平衡状态的是_________(填“a”“b”“c” “d”)。② 其他条件相同,若将原料气按n (CO ):n(H )=1:2.8充入同一恒容、密闭容器中,在催化剂I的作用
2 2
下发生反应。该条件下,a点时CO 的转化率_________(填
2
“增大”或“不变”或“减小”)。
(4)近日,我国学者研究发现,在单原子Cu/ZrO 催化时,反应i
2
的历程以及中间体
HCOO与
第6页/共11页
C H
3
O 物质的量之比随时间变化图如下:
第一步 CO +H →HCOO+H
2 2
第二步 H C O O + 2 H
2
→ C H
3
O + H
2
O
第三步 CH O+H →CH OH
3 3
下列说法正确的是_______。
A.其他条件相同时,升高温度时,三步反应速率均加快
B.用不同催化剂催化反应可以改变反应历程,提高平衡转化率
C.反应历程中,第二步反应的活化能最高,是反应的决速步骤
(5)光催化CO 制甲醇技术也是研究热点。铜基纳米光催化材料
2
还原CO 的机理如图所示。写出CO 转化为CH OH的电极反应式
2 2 3
为 。
17.(11分)化合物 G是用于治疗慢性便秘药品普卡必利的中间体,其合成路线如下:
已知:
回答下列问题。
(1)有机物A中的官能团为羟基、羧基和________。
(2)反应A→B的化学方程式为_______。(3)M + C→D为可逆反应,推测K CO 的作用:_______。
2 3
(4)E的结构简式为_______。
(5)写出符合下列条件的B的一种同分异构体的结构简式___________。
① 属于α-氨基酸(氨基连接在与羧基相连的碳原子上)
② 遇FeCl 溶液显紫色
3
(6)请根据流程中的信息,设计以苯酚和 CH = CH-CH Br为原料合成
2 2
的合成路线。
18.(13分)五水合硫代硫酸钠(Na S O • 5H O)俗称“海波”,常用作棉织物漂白后的脱氧剂、定量分
2 2 3 2
析中的还原剂。
资料:① Na S O • 5H O无色、易溶于水,难溶于乙醇;
2 2 3 2
② Na S O 在酸性溶液中反应有S和SO 产生
2 2 3 2
(一)制备
工业上可用SO 、Na S和 Na CO 制备Na S O • 5H O,其工艺流程示意图如下:
2 2 2 3 2 2 3 2
(1)实验室可用浓硫酸与Cu反应制备SO 气体,该反应的化学方程式是_______。
2
(2) ① 配平I中反应的化学方程式:
Na S + SO + Na CO == Na S O + CO
2 2 2 3 2 2 3 2
② 当I中溶液的pH约为7时应停止通入SO ,否则Na S O 的产率下降,结合离子方程式说明其原
2 2 2 3
因_______。
II.粗产品提纯
(3)已知粗产品中可能会含有少量Na SO 和Na SO ,Na S O 在水中的溶解度随温度的升高而显著增
.. 2 3 2 4 2 2 3
大。
① 检验粗产品中含有Na SO 的方法是:取少量固体溶解, 先加足量的______溶液,静置、过滤,
2 4
_______,有白色沉淀生成。
② 粗产品的提纯过程III中,操作a的步骤为:加热溶解、趁热过滤、_______、过滤、_______(填洗
涤试剂名称)洗涤、干燥。
III.纯度测定
(4)准确称取a g产品于锥形瓶中,加入一定量蒸馏水完全溶解后,加入适量甲醛溶液预处理(防止
Na SO 与I 反应),以淀粉作指示剂,用c mol/L I 的标准溶液滴定,发生如下反应:I + 2S O2- == 2I
2 3 2 2 2 2 3
-+S O2-,三次平行实验,平均消耗v mL I 溶液。
4 6 2
(已知:Na S O • 5H O的摩尔质量为248 g/mol )
2 2 3 2
① 产品中Na S O •5H O的纯度为______ (写出质量分数的表达式即可)。
2 2 3 2
第7页/共11页② 下列操作可能造成实验结果偏高的是_______。
A.滴定管未用I 标准溶液润洗
2
B.滴定终点时仰视读数
C.滴定过程中锥形瓶内有少量液体溅出瓶外
19.(13分)某小组同学将过量的AgNO 溶液滴加到饱和氯水中,发现氯水的漂白性出现异常,于是对
3
相关的反应进行了探究。
I.发现问题
(1)①氯气与水反应的化学方程式为 。小组同学猜测加入AgNO 溶液后,生成 沉淀,使c
3
(Cl-)降低,c(HClO)增大,氯水漂白性增强,于是进行如下实验。
②与过量AgNO 溶液反应后,氯水漂白性减弱的实验证据是 。
3
Ⅱ.查阅资料:AgClO为白色晶体,常温下难溶于水
提出猜想:反应中除生成AgCl外,还有AgClO生成
III.实验探究
已知:AgI + I- AgI -
2
编号 实验操作 实验现象
i 向a 试管中加入2 mL浓盐酸,并用湿润的 产生刺激气味的气体,试纸变蓝
1
淀粉KI试纸靠近试管口
ii 向a 试管中加入2 mL饱和KI溶液,振荡, 加入饱和KI溶液,白色沉淀变为黄色,振荡后沉淀溶
2
再滴入2滴淀粉溶液 解,滴加淀粉溶液,溶液变蓝。
iii 向另一支试管a 中只加入2 mL饱和KI溶
3
液,振荡,再滴入2滴淀粉溶液,与实验ii 滴入淀粉溶液,无明显变化
放置相同时间
(2)操作 a的名称是 。
(3)实验i中产生刺激气味的气体,可能的反应方程式是 。
第8页/共11页(4)实验ii表明,固体b中含有AgClO,且AgClO的溶解度大于AgI,请结合实验现象进行解释 。
(5)实验iii的作用是 。
(6)综上,过量的AgNO 溶液滴加到饱和氯水后,氯水漂白性减弱的可能原因是 。
3
第9页/共11页参考答案
第一部分 选择题(共 42分)
本部分共14小题,每小题3分,共42分。
题号 1 2 3 4 5 6 7
答案 B A A C D C B
题号 8 9 10 11 12 13 14
答案 A C C D D B D
第二部分 非选择题(58分)
说明:(1)分值为2分的化学方程式或离子方程式,配平1分,各物质化学式1分;
除特殊要求外,反应条件、气体符号↑、沉淀符号↓不占分。
(2)答案合理酌情给分。
15.(10分)
(1)d,12 (各1分,共2分)
(2)b (1分)
(3)正四面体,TiCl + (x+2) H O == TiO · xH O + 4HCl (1分,2分,共3分)
4 2 2 2
(4)b d (2分)
233
(5)3 (2分)
N
A
16.(11分)
(1)-49.4 (1分)
(2)①0.06 (2分)
②27/19或1.4 (2分)
(3)①a、c (1分)
②减小 (1分)
(4)A C (2分)
(5)CO + 6e- + 6H+ = CH OH+ H O (2分)
2 3 2
17.(11分)
(1)氨基 (1分)
(2) (2分)
第10页/共11页(3)K CO 与该反应生成的HBr发生反应,降低了HBr浓度,促进平衡正向移动。
2 3
(2分)
(4) (1分)
(5) (2分)
(6)
(3分)
18.(13分)
(1) Cu + 2H SO (浓) ==== CuSO + 2H O + SO ↑ (2分)
2 4 4 2 2
(2)① 2 Na S + 4 SO +Na CO = 3 Na S O +CO ↑ (2分)
2 2 2 3 2 2 3 2
② 若SO 过量,溶液显酸性,产物会发生反应:S O2- + 2H+ == S↓ + SO ↑ + H O,
2 2 3 2 2
导致产率下降 (2分)
(3)① 加入足量稀盐酸,向滤液中加入少量 BaCl 溶液 (2分)
2
② 冷却结晶 ,乙醇 (2分)
(4)①
第11页/共11页
2 c v 1 0 -3 m o
a
l
g
2 4 8 g / m o l
1 0 0 %
Δ
(可以不带单位也可以化简) (1分)
②AB (2分)
19.(13分)
(1)① Cl + H O HClO + HCl。 AgCl沉淀 (2分,1分共3分)
2 2
② 加入过量AgNO 溶液后红色褪去变慢。(或实验组中,10min 后溶液红色褪去,对照组中,8s后溶
3
液红色褪去)。 (1分)
(2)过滤 (1分)
(3)AgClO + 2HCl === AgCl + H O +Cl ↑ (2分)
2 2
(4)加入饱和KI溶液后,白色沉淀变为黄色,证明AgCl、AgClO的溶解度大于AgI,生成AgI后,溶液
中c(ClO-)增大,将过量的I-氧化为I ,加入淀粉溶液变蓝。 (2分)
2
(5)对照实验,排除空气对I-的氧化对实验现象产生影响。 (2 分)
(6)过量的AgNO 溶液与氯水反应,生成了 AgCl和AgClO,使溶液中c(ClO-) [或c(HClO)]降低,氯水
3
漂白性减弱。 (2分)