文档内容
2 0 2 5 年 上 教 师 资 格 · 化 学 学 科 笔 试
主讲老师 王双奕
粉笔教师教育 粉笔教师目
录
content
1 化学反应与能量
2 化学反应速率和化学平衡
3 水溶液中的离子平衡
4 电化学基础电化学基础P162
一、原电池
(一)原电池的工作原理
1.定义
把化学能直接转化为电能的装置。
2.工作原理
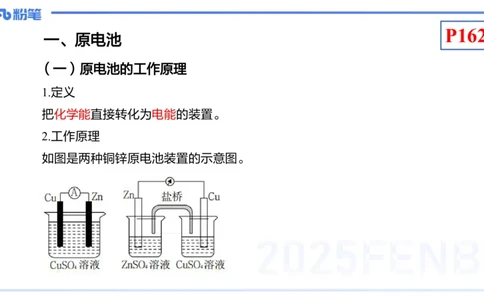
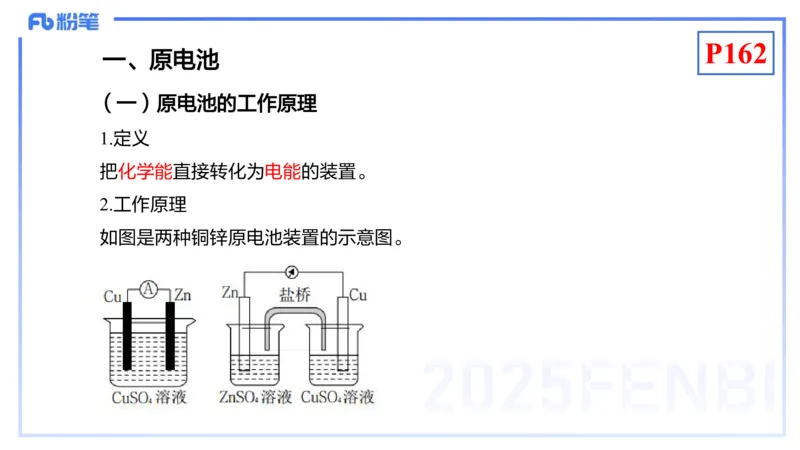
如图是两种铜锌原电池装置的示意图。P162
在两个装置中锌片作负极、铜片作正极,Zn失去电子发生氧化反应而溶
解,电子经 Zn 片流入 Cu 片,Cu2+ 得电子发生还原反应变成 Cu 沉淀在铜片
上因此有电流产生,化学能转化为电能。电极反应和总反应如下:
锌片作负极:Zn-2e-= Zn2+(氧化反应)
铜片作正极:Cu2++2e-= Cu(还原反应)
总反应:Zn+Cu2+= Cu+Zn2+P162
(1)两极判断
负极:一般较活泼金属的电极为负极;
电子流出的电极为负极;
阴离子移向的电极为负极;
发生氧化反应的电极为负极。
正极:一般较不活泼金属的电极为正极;
电子流入的电极为正极;
阳离子移向的电极为正极;
发生还原反应的电极为正极。P163
【粉笔提示】
原电池中必须有自发的氧化还原反应发生,据此可以判断正负极。
1.Mg—Al—NaOH 溶液形成的原电池中,Al 作负极,Mg 作正极;
2.Fe—Cu—浓 HNO 形成的原电池中,Cu 作负极,Fe 作正极;
3
3.Fe—Cu (通入空气)—NaCl 溶液形成的原电池中,Fe 作负极,Cu 作正极。
(吸氧腐蚀)P163
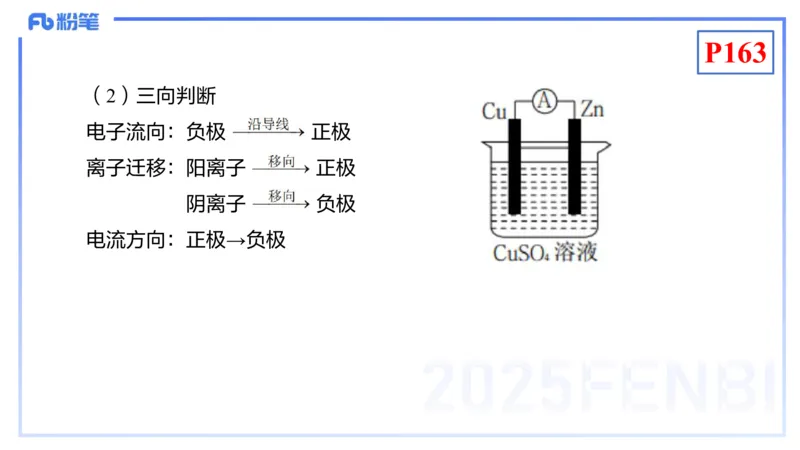
(2)三向判断
电子流向:负极 正极
离子迁移:阳离子 正极
阴离子 负极
电流方向:正极→负极P163
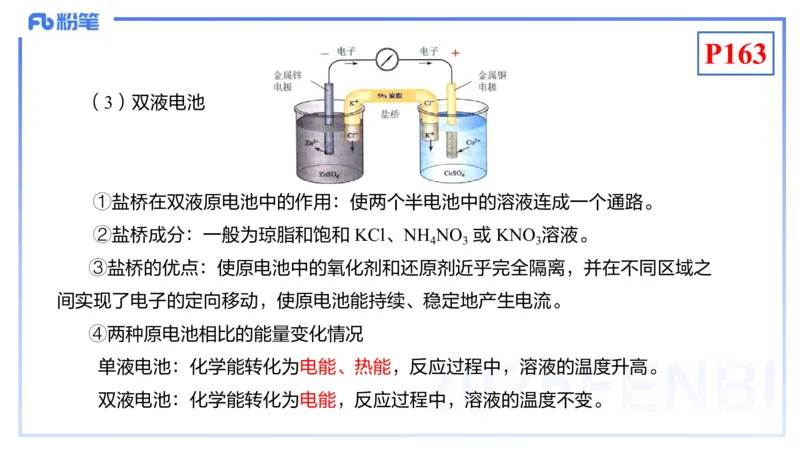
(3)双液电池
①盐桥在双液原电池中的作用:使两个半电池中的溶液连成一个通路。
②盐桥成分:一般为琼脂和饱和 KCl、NH NO 或 KNO 溶液。
4 3 3
③盐桥的优点:使原电池中的氧化剂和还原剂近乎完全隔离,并在不同区域之
间实现了电子的定向移动,使原电池能持续、稳定地产生电流。
④两种原电池相比的能量变化情况
单液电池:化学能转化为电能、热能,反应过程中,溶液的温度升高。
双液电池:化学能转化为电能,反应过程中,溶液的温度不变。P163
3.工作条件
(1)两个活泼性不同的电极
(2)电解质溶液 缺一不可
(3)形成闭合回路P163
(二)化学电源
化学电源是根据原电池的反应原理设计的将化学能转化为电能的装
置,又称为电池。
化学电源是能够实际应用的原电池。化学电源包括一次电池、二次
电池(或可充电电池)、燃料电池等。P164
1.一次电池—碱性锌锰干电池
干电池的电压通常约为1.5V,不能充电。负极是Zn,正极是MnO 。
2
负极反应:Zn+2OH--2e- Zn(OH) (负极质量增大)
2
正极反应:2MnO +2H O+2e- 2MnOOH+2OH-
2 2
总反应:Zn+2MnO +2H O Zn(OH) +2MnOOH
2 2 2P164
2.二次电池(或可充电电池)
铅蓄电池是最常见的二次电池,可以放电和充电,负极材料是 Pb,正极材
料是 PbO ,电解质溶液是 H SO 溶液。
2 2 4
(1)放电时的反应
负极:Pb+SO 2--2e- PbSO (负极质量增大)
4 4
正极:PbO +4H++SO 2-+2e- PbSO +2H O
2 4 4 2
电池总反应:Pb+PbO +2H SO 2PbSO +2H O
2 2 4 4 2P164
(2)充电时的反应
阴极:PbSO +2e- Pb+SO 2-
4 4
阳极:PbSO +2H O-2e- PbO +4H++SO 2-
4 2 2 4
电池总反应:2PbSO +2H O Pb+PbO +2H SO
4 2 2 2 4P164
3.燃料电池
原理:利用原电池的工作原理,连续地将燃料和氧化剂(如 O )的化学
2
能直接转化为电能。
燃料电池是一种高效、环境友好的发电装置,它的电极材料一般具有很
强的催化活性,如铂电极、活性炭电极等。P164
燃料电池由 3个 主要部分组成:
负极(燃料电极);
正极(氧气或空气电极);
电解质溶液。
两电极材料均为惰性电极,电极本身不发生反应,而是由引入到两电极上
的燃料和氧化剂发生反应。P164
常见的燃料电池:
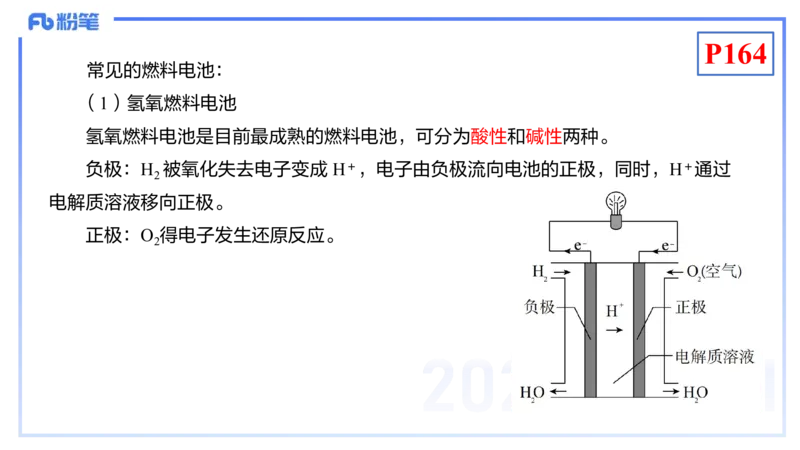
(1)氢氧燃料电池
氢氧燃料电池是目前最成熟的燃料电池,可分为酸性和碱性两种。
负极:H 被氧化失去电子变成 H+,电子由负极流向电池的正极,同时,H+通过
2
电解质溶液移向正极。
正极:O 得电子发生还原反应。
2P165
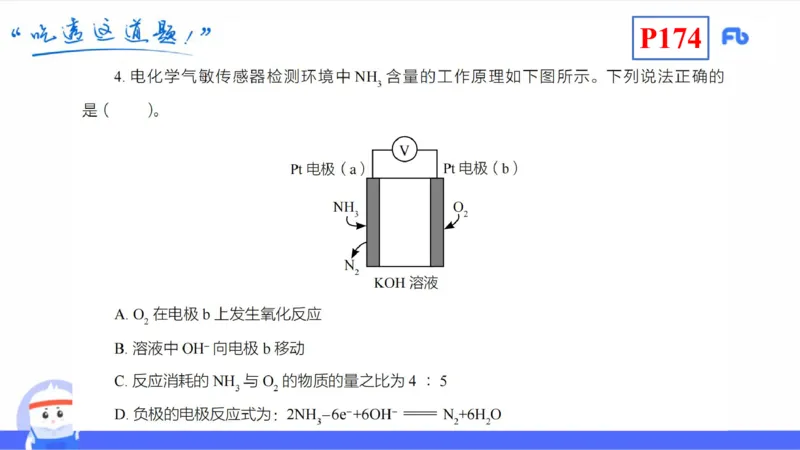
(2)CH 燃料电池
4
该电池用金属铂片插入 KOH 溶液中作电极,在两极上分别通入甲烷和氧气。
负极反应:CH +10OH--8e- CO 2-+7H O
4 3 2
正极反应:2O +4H O+8e- 8OH-
2 2
总反应:CH +2O +2KOH K CO +3H O
4 2 2 3 2P165
【粉笔提示】
1.燃料电池中方程式的书写方法:两剂定产物,守恒依次行。即先根据氧化剂、
还原剂的性质确定反应的产物,再依次利用得失电子守恒、电荷守恒、原子守恒配平
和补齐物质。
2.电化学方程式的书写要尤其注意离子共存问题,如,碱性电池中不能出现H+,
酸性电池中不能出现 OH- 。
3.电解质溶液参与反应,所以要写入总反应方程式。
4.复杂题目中可根据元素化合价升降法判断正负极,写出方程式。P174P165
(三)原电池原理的主要应用
1.加快氧化还原反应的速率
例如:在锌与稀H SO 反应时加入少量CuSO 溶液能使产生H 的速率加快。
2 4 4 2P166
2.比较金属活动性强弱
例如:有两种金属 a 和 b,用导线连接后插入稀 H SO 中,观察到 a 极逐
2 4
渐溶解,b 极上有气泡产生。根据现象判断出 a 是负极,b 是正极,由原电
池原理可知,金属活动性: a > b 。P166
3.用于金属的防护
使被保护的金属制品作原电池的正极而受到保护。
例如,要保护一个铁质的输水管道或钢铁桥梁等,可用导线将其与一锌块
相连,使锌作原电池的负极。P166
4.设计制作原电池
设计原电池时要紧扣原电池的构成条件。具体方法如下:
①电极材料的选择
a.选择还原性较强的物质作为负极。
b.选择氧化性较强的物质作为正极。
c.原电池的电极必须导电。P166
②电解质溶液的选择
a.电解质溶液或其中溶解的物质(O )必须能够与负极反应。
2
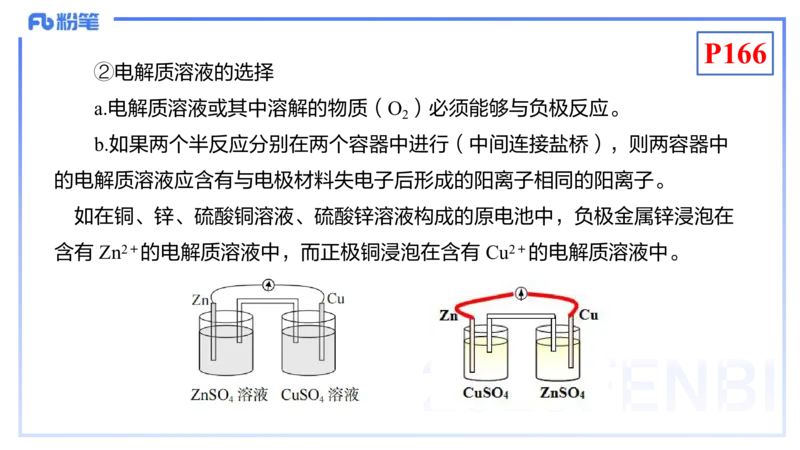
b.如果两个半反应分别在两个容器中进行(中间连接盐桥),则两容器中
的电解质溶液应含有与电极材料失电子后形成的阳离子相同的阳离子。
如在铜、锌、硫酸铜溶液、硫酸锌溶液构成的原电池中,负极金属锌浸泡在
含有 Zn2+的电解质溶液中,而正极铜浸泡在含有 Cu2+的电解质溶液中。P167
二、电解池
(一)电解池的工作原理
1.定义
电解:使电流通过电解质溶液(或熔融的电解质)而在阴、阳两极引
起氧化还原反应的过程。
电解池:把电能直接转化为化学能的装置。(由外界电能驱动,不需
要自发的氧化还原反应)P167
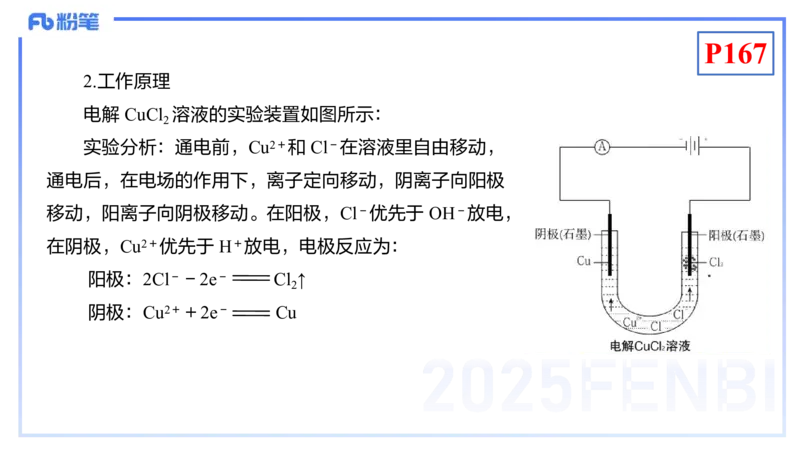
2.工作原理
电解 CuCl 溶液的实验装置如图所示:
2
实验分析:通电前,Cu2+和 Cl-在溶液里自由移动,
通电后,在电场的作用下,离子定向移动,阴离子向阳极
移动,阳离子向阴极移动。在阳极,Cl-优先于 OH-放电,
在阴极,Cu2+优先于 H+放电,电极反应为:
阳极:2Cl--2e- Cl ↑
2
阴极:Cu2++2e- CuP167
实验现象:阴极上有红色固体析出,阳极产生气泡,有刺激性气味,能
使湿润的淀粉碘化钾试纸变蓝。
实验结论:CuCl 发生了电解反应:CuCl Cu+Cl ↑
2 2 2P167
再比如,电解熔融的氯化钠,通电后,Na+和 Cl-分别向阴极和阳极定向
移动,并在两极上放电,电极反应为:
阴极:2Na++2e-= 2Na
阳极:2Cl--2e-= Cl ↑
2
在电流的作用下,反应 2NaCl(熔融) 2Na+Cl ↑ 得以发生。
2P168
(1)两极判断
阴极:与外接电源负极相连的一极。
阳极:与外接电源正极相连的一极。
(2)三向判断
沿导线 沿导线
电子流向:阳极 电源正极 ,电源负极 阴极
电子不下水,
离子不上岸
移向 移向
离子迁移:阳离子 阴极 ,阴离子 阳极
电流方向:电源正极→电源负极 电流可以跨越“海洋”,在整个电路循环P168
【粉笔提示】
电解池放电顺序:
(1)阴极:阳离子放电,得电子能力强的先放电 。
Ag+> Hg2+> Fe3+> Cu2+> H+(酸)> Pb2+>Sn2+>Fe2+>Zn2+> H+(H O)>
2
Al3+>Mg2+>Na+>Ca2+>K+P168
(2)阳极:阴离子放电或电极放电,失电子能力强的先放电。
a.活泼金属(金属活动性顺序中 Ag 以前)作电极时,溶液中的阴离子一律
不放电,而是电极材料先失电子。
b.惰性材料(Pt、Au、石墨)作电极时,放电顺序:S2->I->Fe2+>Br->
Cl->OH->含氧酸根离子。P168
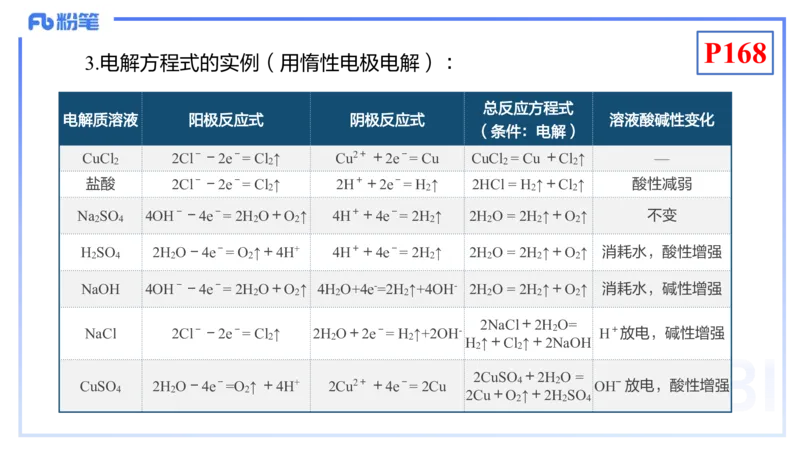
3.电解方程式的实例(用惰性电极电解) :
总反应方程式
电解质溶液 阳极反应式 阴极反应式 溶液酸碱性变化
(条件:电解)
CuCl 2Cl --2e - = Cl ↑ Cu2+ +2e - = Cu CuCl = Cu +Cl ↑ —
2 2 2 2
盐酸 2Cl --2e - = Cl ↑ 2H ++2e - = H ↑ 2HCl = H ↑+Cl ↑ 酸性减弱
2 2 2 2
Na SO 4OH --4e - = 2H O+O ↑ 4H ++4e - = 2H ↑ 2H O = 2H ↑+O ↑ 不变
2 4 2 2 2 2 2 2
H SO 2H O-4e - = O ↑+4H+ 4H ++4e - = 2H ↑ 2H O = 2H ↑+O ↑ 消耗水,酸性增强
2 4 2 2 2 2 2 2
NaOH 4OH --4e - = 2H O+O ↑ 4H O+4e-=2H ↑+4OH- 2H O = 2H ↑+O ↑ 消耗水,碱性增强
2 2 2 2 2 2 2
2NaCl+2H O=
NaCl 2Cl --2e - = Cl ↑ 2H O+2e - = H ↑+2OH- 2 H +放电,碱性增强
2 2 2
H ↑+Cl ↑+2NaOH
2 2
2CuSO +2H O =
CuSO 2H O-4e - =O ↑ +4H+ 2Cu2+ +4e - = 2Cu 4 2 OHˉ 放电,酸性增强
4 2 2
2Cu+O ↑+2H SO
2 2 4P169
(二)电解原理的应用
1.电解法冶炼活泼金属(冶金工业)
电解熔融的 NaCl、MgCl 、Al O -Na AlF 可分别冶炼金属 Na、Mg、Al 。
2 2 3 3 6
2.铜的电解精炼
粗铜作阳极:Cu-2e-= Cu2+,M-ne-= Mn+(M 是比 Cu 活泼的金属杂
质,如 Zn、Ni、Fe 等);
纯铜作阴极:Cu2++2e-= Cu;
CuSO 溶液(含H SO )作电解液。
4 2 4P169
3.电镀
电镀是一种特殊的电解,是应用电解原理在某些金属表面镀上一薄层其他
金属或合金的方法。
条件:①要求镀件必须作阴极;
②镀层金属作阳极;
③含有镀层金属离子的溶液作电镀液。
电镀时,理论上电解质溶液的浓度保持不变。如以铁制品为阴极,铜片为
阳极,CuSO 溶液为电镀液,可在铁制品表面镀上铜。
4P169
电镀铜与精炼铜比较:
项目 电镀铜 精炼铜
镀层金属做阳极,镀件做阴极, 粗铜作阳极,精铜作阴极,
形成条件
电镀液必须含有镀层金属的离子 CuSO 溶液作电解液
4
阳极:Zn-2e-= Zn2+
阳极:Cu-2e-=Cu2+
电极反应 Cu-2e-= Cu2+ 等
阴极:Cu2++2e-=Cu
阴极:Cu2+ + 2e-= Cu
溶液变化 电镀液的浓度基本不变 溶液中 Cu2+ 浓度减小P170
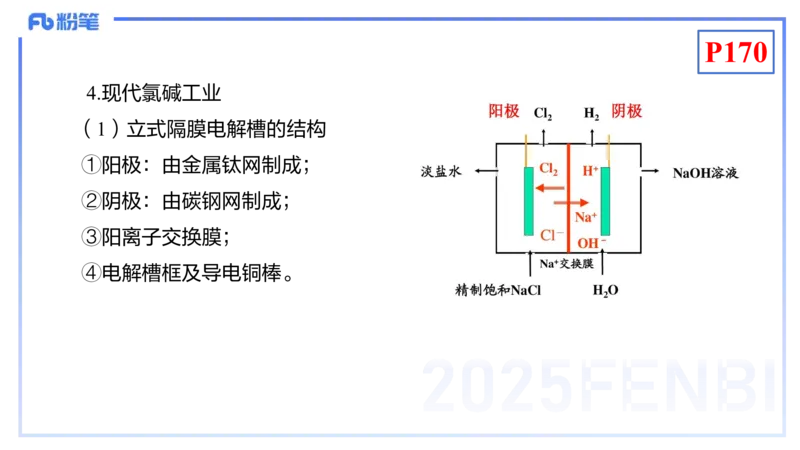
4.现代氯碱工业
(1)立式隔膜电解槽的结构
①阳极:由金属钛网制成;
②阴极:由碳钢网制成;
③阳离子交换膜;
④电解槽框及导电铜棒。P170
(2)食盐水的精制
电解前应通过 NaOH、BaCl 、Na CO 溶液和盐酸等试剂及离子交换树脂
2 2 3
除去食盐溶液中的 Ca2+、Mg2+、SO 2-等杂质离子,得到精制的饱和食盐水。
4
【粉笔提示】
Na CO 溶液必须在 BaCl 溶液的后面加入,以除去过量的 Ba2+ 。
2 3 2P170
(3)反应原理
阳极反应:2Cl--2e-= Cl ↑(放电能力:Cl-> OH-)
2
阴极反应:2H++2e-= H ↑(放电能力:H+> Na+)
2
电解反应:2NaCl+2H O 2NaOH+H ↑+Cl ↑
2 2 2
(4)产品
阳极:Cl
2
阴极:NaOH、H
2(三)原电池、电解池的总结
P170
1.原电池和电解池的比较
项目 原电池 电解池
装置
氧化还原反应中电子定向移动从而 使电流通过电解质溶液而在阴、阳两极引
原理 形成电流。这种把化学能转变为电 起氧化还原反应的过程叫作电解。这种把
能的装置叫作原电池 电能转变为化学能的装置叫作电解池
①能自发进行的氧化还原反应; ①电源;
形成 ②两个金属活动性不同的电极; ②电极(惰性或非惰性);
条件 ③电解质溶液; ③电解质(水溶液或熔融态);
④形成闭合回路 ④形成闭合回路P171
反应类型 自发的氧化还原反应 非自发的氧化还原反应
由电极本身性质决定: 由外接电源决定:
电极
正极:材料性质较不活泼的电极; 阳极:连接外接电源的正极;
名称
负极:材料性质较活泼的电极 阴极:连接外接电源的负极
负极:Zn-2e-= Zn2+ (氧化反应)阴极:Cu2+ +2e-= Cu (还原反应)
电极反应
正极:2H++2e-= H ↑(还原反应)阳极:2Cl--2e-= Cl ↑ (氧化反应)
2 2
电子流向 负极→正极 电源负极→阴极,阳极→电源正极
电流方向 正极→负极 电源正极→阳极→阴极→电源负极
能量转化 化学能→电能 电能→化学能
①电解食盐水(氯碱工业);
①金属的电化学防护; ②电镀(镀铜);
应用
②实用电池 ③电冶(冶炼Na、Mg、Al);
④精炼(精炼铜)P171
2.电解、电离和电镀的区别
项目 电解 电离 电镀
条件 受直流电作用 受热或水分子作用 受直流电作用
阴阳离子定向移动, 阴阳离子自由移动, 用电解的方法在金属表
实质
在两极发生氧化还原反应 无明显的化学变化 面镀上一层金属或合金
阳极:Cu-2e-= Cu2+
实例 CuCl Cu+Cl ↑ CuCl = Cu2++2Clˉ
2 2 2
阴极:Cu2++2e-= Cu
关系 先电离后电解,电镀是电解的应用P173P173P172
三、金属的腐蚀与防护
1.金属的腐蚀
金属腐蚀是指金属或合金与周围的气体或液体发生氧化还原反应而引
起损耗的现象。
2.金属腐蚀的实质
金属原子(M)失去电子而被氧化的过程,即M-ne-= Mn+。P172
3.金属腐蚀的类型
金属腐蚀分为电化学腐蚀和化学腐蚀两种,化学腐蚀和电化学腐蚀的
区别:
化学腐蚀 电化学腐蚀
一般条件 金属直接和强氧化剂接触 不纯金属,表面潮湿
反应过程 氧化还原反应,不形成原电池 因原电池反应而腐蚀
有无电流 无电流产生 有微弱电流产生
反应速率 电化学腐蚀 > 化学腐蚀
结果 金属被腐蚀 较活泼的金属被腐蚀P172
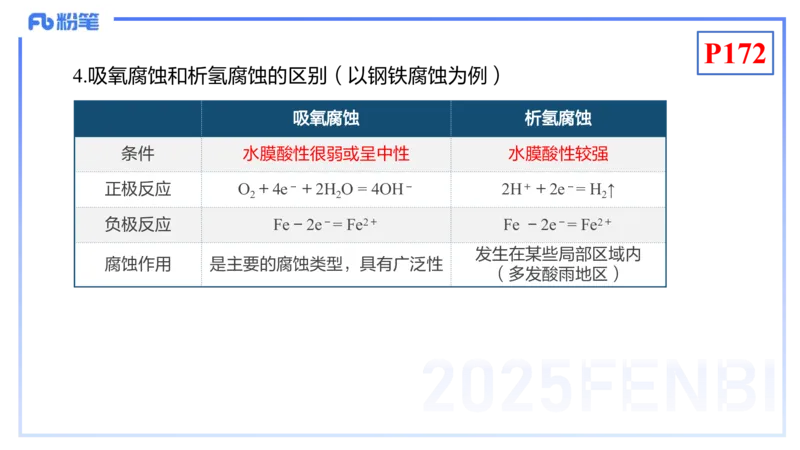
4.吸氧腐蚀和析氢腐蚀的区别(以钢铁腐蚀为例)
吸氧腐蚀 析氢腐蚀
条件 水膜酸性很弱或呈中性 水膜酸性较强
正极反应 O +4e-+2H O = 4OH- 2H++2e-= H ↑
2 2 2
负极反应 Fe-2e-= Fe2+ Fe -2e-= Fe2+
发生在某些局部区域内
腐蚀作用 是主要的腐蚀类型,具有广泛性
(多发酸雨地区)P172
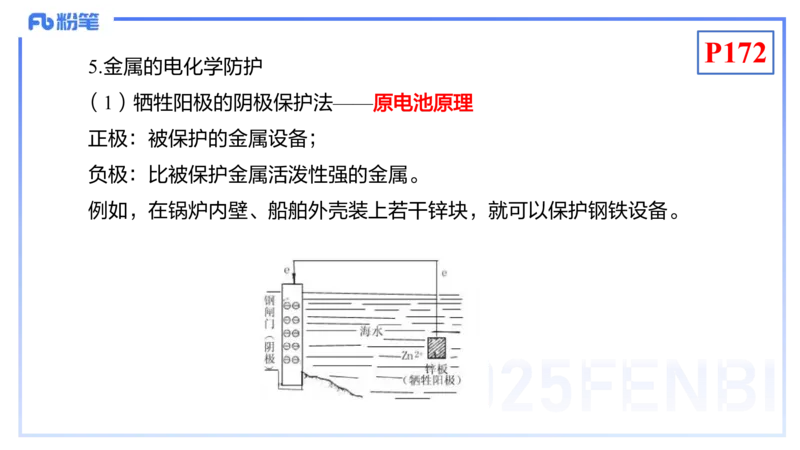
5.金属的电化学防护
(1)牺牲阳极的阴极保护法——原电池原理
正极:被保护的金属设备;
负极:比被保护金属活泼性强的金属。
例如,在锅炉内壁、船舶外壳装上若干锌块,就可以保护钢铁设备。P172
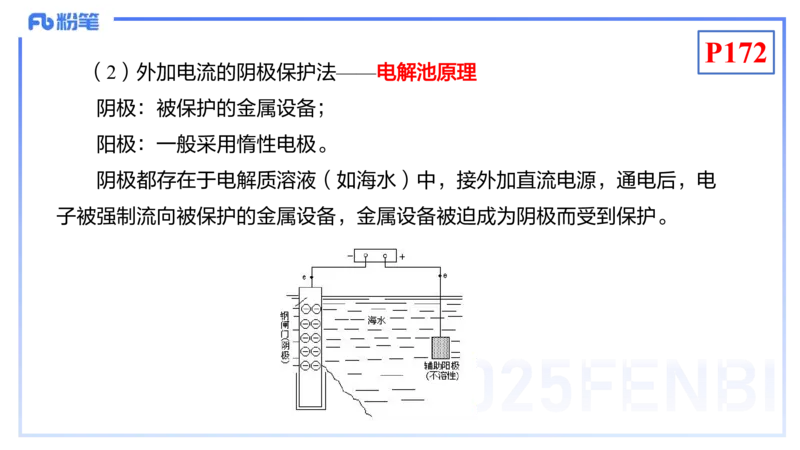
(2)外加电流的阴极保护法——电解池原理
阴极:被保护的金属设备;
阳极:一般采用惰性电极。
阴极都存在于电解质溶液(如海水)中,接外加直流电源,通电后,电
子被强制流向被保护的金属设备,金属设备被迫成为阴极而受到保护。P174