文档内容
天津市部分区 2023~2024 学年度第一学期期末练习
高三化学
注意:本学期期末练习使用答题卡机读。所有题目按要求填涂或填写在规定位置上,不要超出
答题范围!
以下数据可供解题时参考。
相对原子质量:
第Ⅰ卷
注意事项:
1.每题选出答案后,用铅笔将答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,
再选涂其他答案标号。
2.本卷共12题,每题3分,共36分。在每题给出的四个选项中,只有一项是最符合题目要求
的。
1.下列食品添加剂属于无机物的是( )。
A.味精 B.食盐 C.维生素C D.葡萄糖酸 内酯
2.下列说法错误的是( )。
A.液氨汽化时吸收大量的热,工业上可用作制冷剂
B.铁强化酱油中的 可预防缺铁性贫血
C.工业上用焦炭和石英砂制备粗硅
D.工业上用 和水反应制备
3.下列化合物中同时含有离子键、共价键、配位键的是( )。
A. B. C. D.
4.下列离子方程式正确的是( )。
A. 制备84消毒液:
B.食醋去除水垢中的 :
C.将稀硫酸滴入 溶液中:
D.电解 水溶液:
5.设 为阿伏加德罗常数的值,下列说法正确的是( )。
学科网(北京)股份有限公司A. 中所含离子总数为
B.标准状况下, 中的原子总数为
C. 所含电子的数目为
D. 溶液中所含 的数目为
6.下列化学用语的表达正确的是( )。
A. 的共价键的电子云图形:
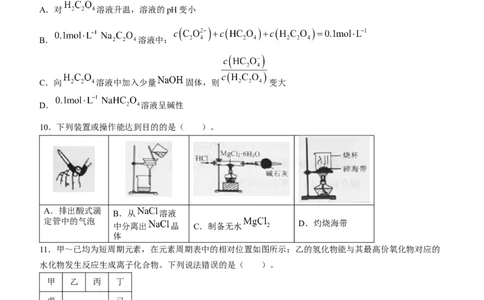
B.基团“ ”的电子式为:
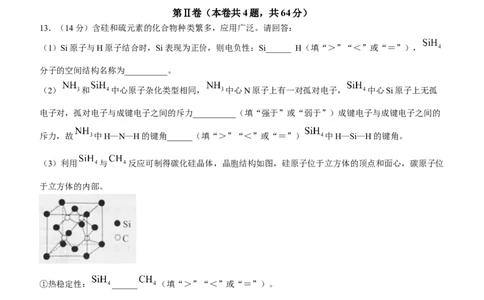
C. 的VSEPR模型:
D.邻羟基苯甲醛分子内氢键示意图:
7.浓度均为 的 、 、 三种溶液,仅用一种试剂就可以鉴别出来的是(
).
A.滴加 盐酸溶液 B.滴加酚酞试剂
C.滴加 溶液 D.滴加饱和 溶液
8. 的波恩哈(Bom-Haber)循环如图所示。已知:元素的一个气态原子获得电子成为气态阴离子时所
放出的能量称为电子亲和能。下列有关说法正确的是( )。
学科网(北京)股份有限公司A.Cl的第一电子亲和能为
B.Na的第一电离能为
C.Cl—Cl键的键能为
D.
9.常温下 的电离常数 , 。下列说法错误的是( )。
A.对 溶液升温,溶液的pH变小
B. 溶液中:
C.向 溶液中加入少量 固体,则 变大
D. 溶液呈碱性
10.下列装置或操作能达到目的的是( )。
A.排出酸式滴
B.从 溶液
定管中的气泡 D.灼烧海带
中分离出 晶 C.制备无水
体
11.甲~已均为短周期元素,在元素周期表中的相对位置如图所示:乙的氢化物能与其最高价氧化物对应的
水化物发生反应生成离子化合物。下列说法错误的是( )。
甲 乙 丙 丁
戊 已
A.最高价氧化物对应水化物的酸性:丁>已
B.原子半径:戊>丙>丁
C.第一电离能: (乙)> (丙)> (甲)
D.最简单氢化物的沸点:丙>甲
12.一定条件下,向容积均为 的两个恒温密闭容器中通入一定量的一氧化碳和水蒸气,发生反应:
,达平衡后获得数据如下表。下列说法错误的
学科网(北京)股份有限公司是( )。
起始时各物质的物质的量/mol
达到平衡的 达到平衡时体系能
容器编号
时间/min 量的变化
CO
① 1 4 0 0 放出 热量
② 2 8 0 0 放出 热量
A.①中反应达平衡时,CO的转化率为80% B.平衡时 :①=②
C.达到平衡的时间:①>② D.反应②中,
第Ⅱ卷(本卷共4题,共64分)
13.(14分)含硅和硫元素的化合物种类繁多,应用广泛。请回答:
(1)Si原子与H原子结合时,Si表现为正价,则电负性:Si______ H(填“>”“<”或“=”),
分子的空间结构名称为__________。
(2) 和 中心原子杂化类型相同, 中心N原子上有一对孤对电子, 中心Si原子上无孤
电子对,孤对电子与成键电子之间的斥力__________(填“强于”或“弱于”)成键电子与成键电子之间的
斥力,故 中H—N—H的键角______(填“>”“<”或“=”) 中H—Si—H的键角。
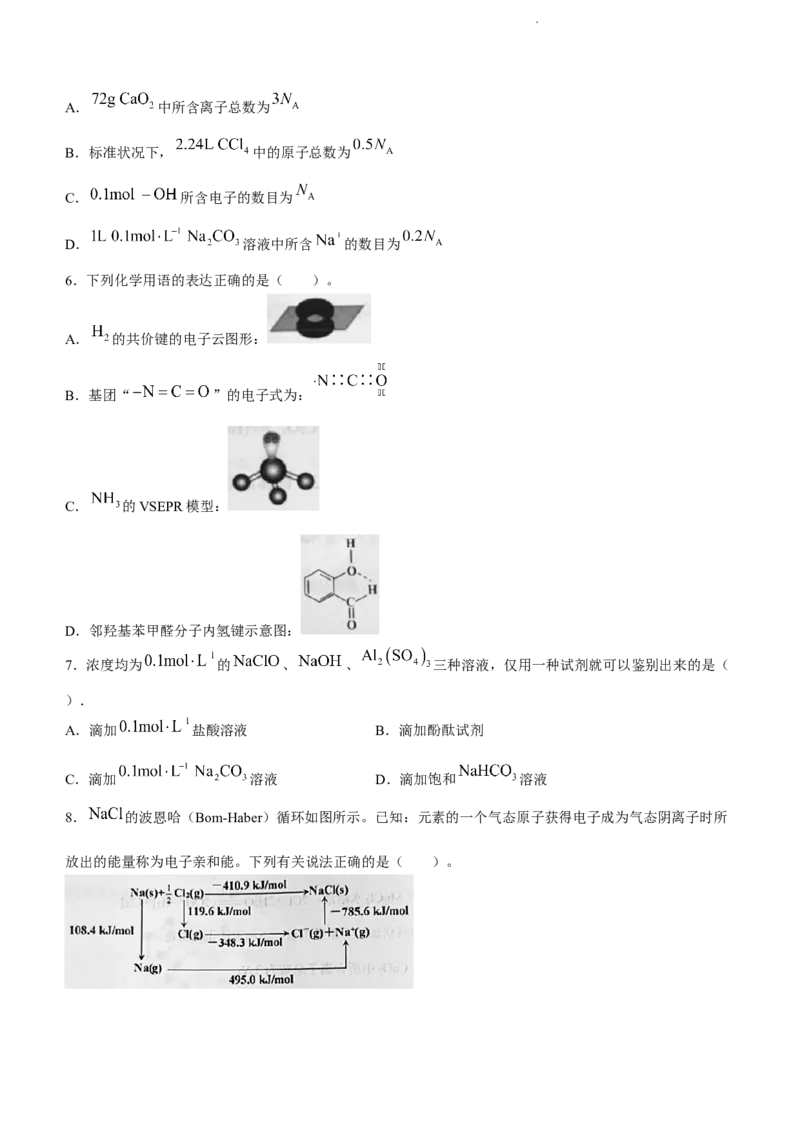
(3)利用 与 反应可制得碳化硅晶体,晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位
于立方体的内部。
①热稳定性: ______ (填“>”“<”或“=”)。
② 的晶体类型是__________。
③测定晶体结构最常用的方法是__________(填序号)。
a.质谱法 b.X射线行射 c.核磁共振氢谱 d.红外光谱
(4)已知硫代硫酸根 可看作是 中的一个O原子被S原子取代的产物。 作为配体可提供
孤电子对与 形成 。
学科网(北京)股份有限公司① 中硫原子的杂化类型是__________。
② 中的S原子,能做配位原子的是__________(填序号)。
a.中心S原子 b.端基S原子
c.两个S原子均可 d.无法确定
14.(18分)某小组同学探究 的相关性质。
实验Ⅰ:探究 对 平衡体系的影响。
将已用稀盐酸酸化的 溶液和 溶液等体积混合,静置至体系平衡,
得红色溶液X。
已知:ⅰ. 与 能发生络合反应: (黄色);
ⅱ.忽略 对颜色的影响。
(1)本实验配制溶液时用到的玻璃仪器除烧杯、量简、玻璃棒、容量瓶外,还需要的仪器是__________,用
稀盐酸酸化 溶液的目的是__________。
(2) 用途十分广泛,请写出其中的一种用途__________。
(3)分别取 溶液X放入试管中,进行如下实验。
①若试管注入蒸馏水后溶液颜色变浅,可能原因是稀释的过程中, 平衡向
______(填“正”或“逆”)反应方向移动,还可能是__________导致颜色变浅。
②若向试管中注入5滴 溶液后,溶液颜色变浅,其原因是__________。
③若向试管中分别注入 溶液或 溶液后,颜色变浅程度不同,
可能是__________不同导致的(答出种影响因素即可)。
实验Ⅱ:探究 与Cu的反应,进行如图实验:
学科网(北京)股份有限公司(1)写出 与Cu粉反应的离子方程式__________。
(2)为了探究实验中生成白色沉淀的原因,继续如下实验。
已知:① 是难溶于水的白色固体
② 的化学性质与 相似
③
步骤1:取 溶液,向其中滴加3滴 溶液,无明显现象。
步骤2:取 __________ 溶液,向其中滴加3滴 溶液,产生白色沉淀。
写出 与 反应的离子方程式__________。
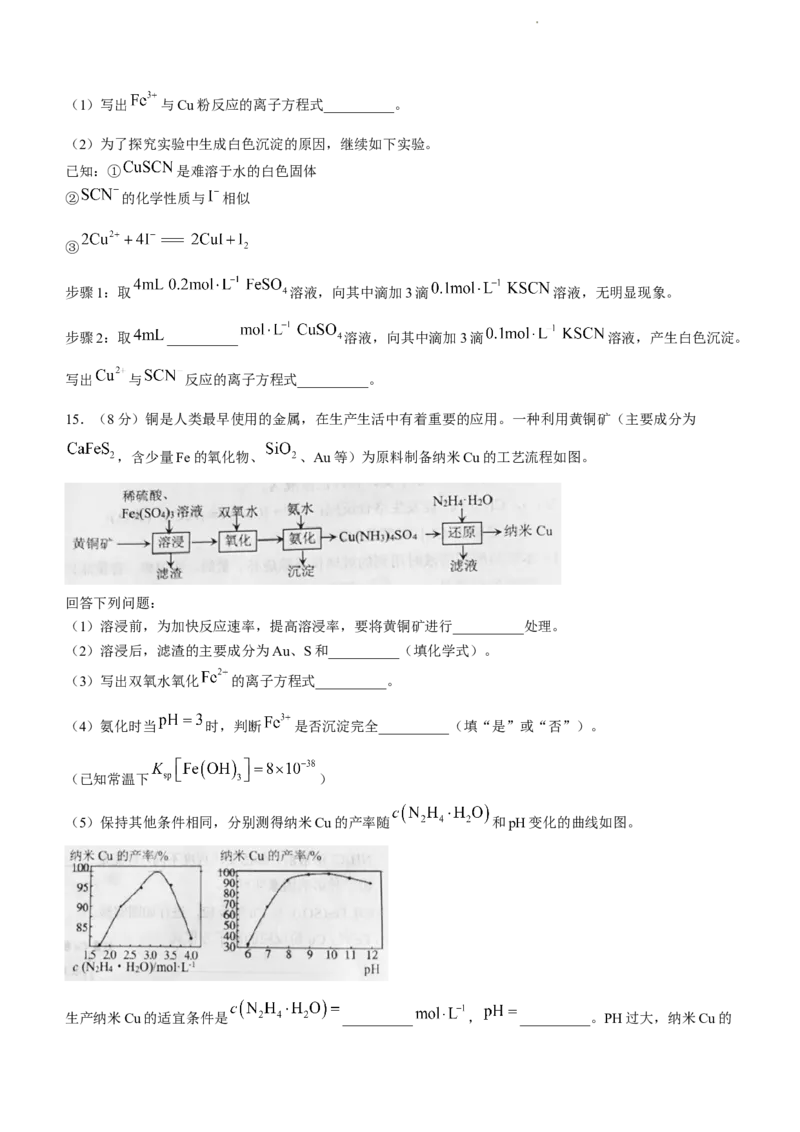
15.(8分)铜是人类最早使用的金属,在生产生活中有着重要的应用。一种利用黄铜矿(主要成分为
,含少量Fe的氧化物、 、Au等)为原料制备纳米Cu的工艺流程如图。
回答下列问题:
(1)溶浸前,为加快反应速率,提高溶浸率,要将黄铜矿进行__________处理。
(2)溶浸后,滤渣的主要成分为Au、S和__________(填化学式)。
(3)写出双氧水氧化 的离子方程式__________。
(4)氨化时当 时,判断 是否沉淀完全__________(填“是”或“否”)。
(已知常温下 )
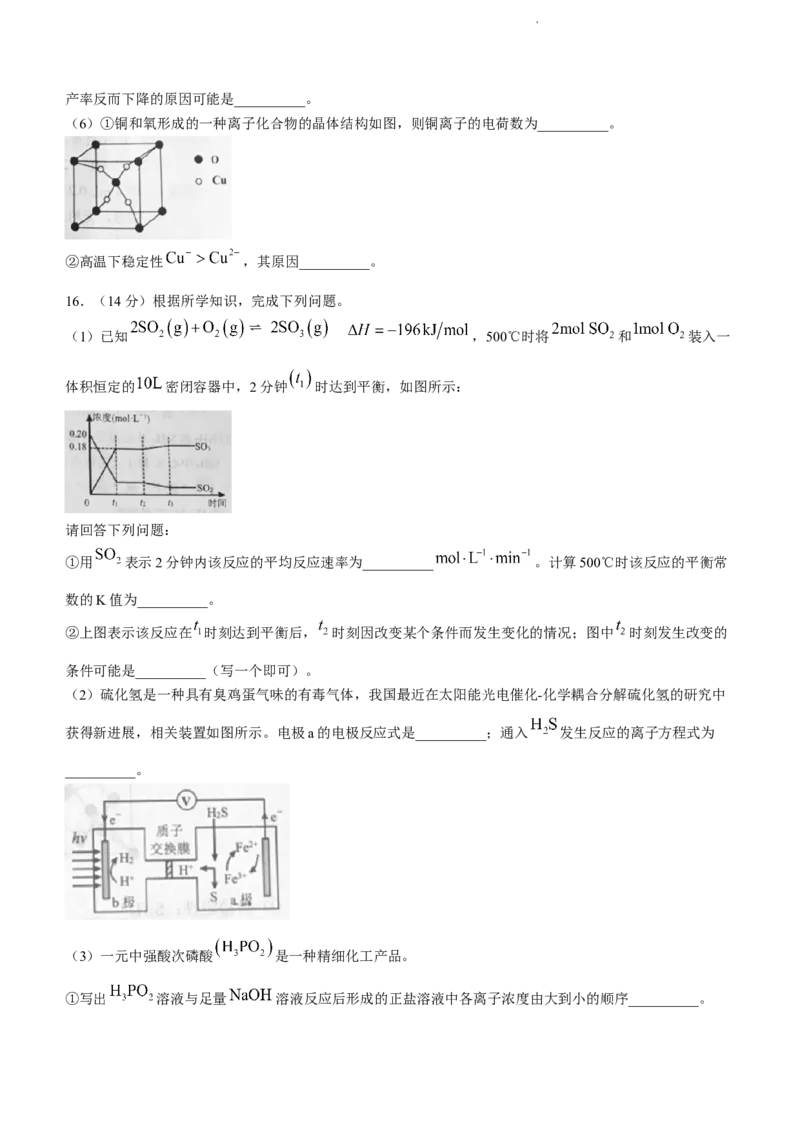
(5)保持其他条件相同,分别测得纳米Cu的产率随 和pH变化的曲线如图。
生产纳米Cu的适宜条件是 __________ , __________。PH过大,纳米Cu的
学科网(北京)股份有限公司产率反而下降的原因可能是__________。
(6)①铜和氧形成的一种离子化合物的晶体结构如图,则铜离子的电荷数为__________。
②高温下稳定性 ,其原因__________。
16.(14分)根据所学知识,完成下列问题。
(1)已知 ,500℃时将 和 装入一
体积恒定的 密闭容器中,2分钟 时达到平衡,如图所示:
请回答下列问题:
①用 表示2分钟内该反应的平均反应速率为__________ 。计算500℃时该反应的平衡常
数的K值为__________。
②上图表示该反应在 时刻达到平衡后, 时刻因改变某个条件而发生变化的情况;图中 时刻发生改变的
条件可能是__________(写一个即可)。
(2)硫化氢是一种具有臭鸡蛋气味的有毒气体,我国最近在太阳能光电催化-化学耦合分解硫化氢的研究中
获得新进展,相关装置如图所示。电极a的电极反应式是__________;通入 发生反应的离子方程式为
__________。
(3)一元中强酸次磷酸 是一种精细化工产品。
①写出 溶液与足量 溶液反应后形成的正盐溶液中各离子浓度由大到小的顺序__________。
学科网(北京)股份有限公司② 溶液与 溶液等体积混合后所得溶液中:
__________ 。(溶液体积变化忽略不计)
学科网(北京)股份有限公司