文档内容
2023~2024 学年佛山市普通高中教学质量检测(一)
高三化学
2024.1
本试卷共8页,20题,全卷满分100分,考试用时75分钟.
注意事项:
1.答卷前,考生务必用黑色字迹的钢笔或签字笔将自己的学校、班级、姓名、试室、座位号和
准考证号填写在答题卡上.将条形码横贴在答题卡右上角“条形码粘贴处”.
2.作答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目选项的答案信息点涂黑;
如需改动,用橡皮擦干净后,再选涂其他答案,答案不能答在试卷上.
3.非选择题必须用黑色字迹钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内相应位
置上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液.不按以
上要求作答的答案无效.
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Mg 24 Cu 64 I 127
一、选择题:本题包括16小题,共44分.第1~10小题,每小题2分;第11~16小题,每小题
4分.在每小题给出的四个选项中,只有一项符合题目要求.
1.骑楼极具岭南特色,其建筑材料主要成分为硅酸盐的是( )
A.金漆 B.木雕 C.陶塑 D.蚝壳窗
2.杭州亚运会展示了我国科技力量.下列说法错误的是( )
A.会场使用的5G通信光纤的主要材料是Si
B.场馆能源来自风能和太阳能,二者都属于可再生能源
C.竞赛自行车车架采用碳纤维材料,它是一种无机非金属材料
D.体育场馆形状类似“莲花碗”,采用的异形钢材料韧性比生铁强
3.化学使环境更美好.下列说法错误的是( )
A.推广使用电动车,可减少光化学烟雾 B.燃煤时加生石灰,可减少温室气体产生
C.将 合成甲醇,有助于实现碳中和 D.使用可降解塑料,有利于减少白色污染
4.“劳动最光荣,勤奋出智慧”.下列劳动项目与所述化学知识没有关联的是( )
选项 劳动项目 化学知识
A 试剂运输:常用铁罐车运输浓硫酸 常温下,铁遇浓硫酸钝化
B 医学手术:医生用聚乳酸作手术缝合线 聚乳酸在人体内可水解、吸收
C 泳池消毒:用漂粉精作游泳池的消毒剂 漂粉精有漂白性
D 消防宣传:消防员使用泡沫灭火器灭火 碳酸氢钠与硫酸铝发生双水解
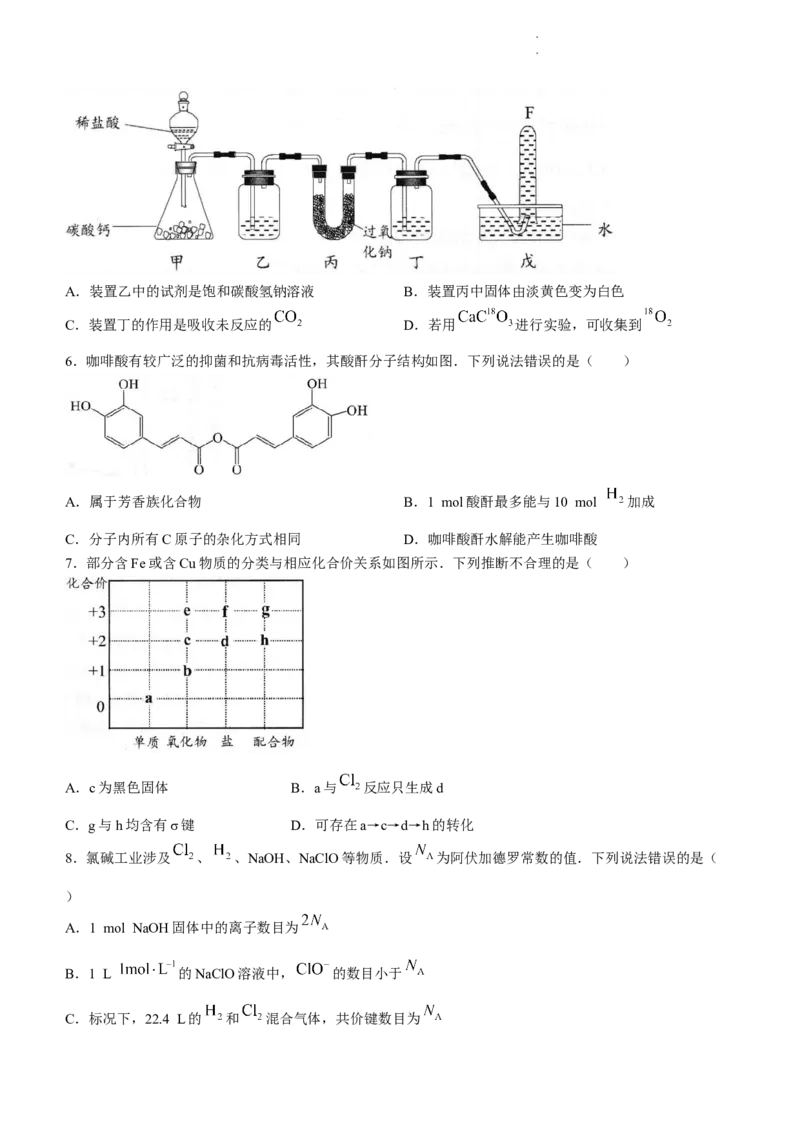
5.利用如下装置验证 可做供氧剂,下列说法错误的是( )
学学科科网网((北北京京))股股份份有有限限公公司司A.装置乙中的试剂是饱和碳酸氢钠溶液 B.装置丙中固体由淡黄色变为白色
C.装置丁的作用是吸收未反应的 D.若用 进行实验,可收集到
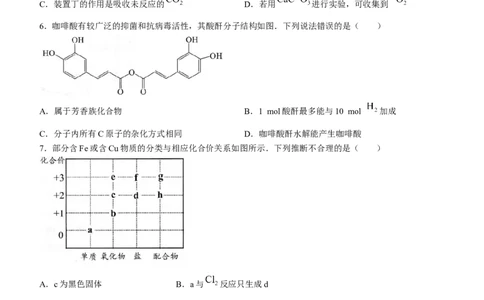
6.咖啡酸有较广泛的抑菌和抗病毒活性,其酸酐分子结构如图.下列说法错误的是( )
A.属于芳香族化合物 B.1 mol酸酐最多能与10 mol 加成
C.分子内所有C原子的杂化方式相同 D.咖啡酸酐水解能产生咖啡酸
7.部分含Fe或含Cu物质的分类与相应化合价关系如图所示.下列推断不合理的是( )
A.c为黑色固体 B.a与 反应只生成d
C.g与h均含有σ键 D.可存在a→c→d→h的转化
8.氯碱工业涉及 、 、NaOH、NaClO等物质.设 为阿伏加德罗常数的值.下列说法错误的是(
)
A.1 mol NaOH固体中的离子数目为
B.1 L 的NaClO溶液中, 的数目小于
C.标况下,22.4 L的 和 混合气体,共价键数目为
学学科科网网((北北京京))股股份份有有限限公公司司D.1 mol 与足量NaOH溶液反应生成NaClO转移电子数为
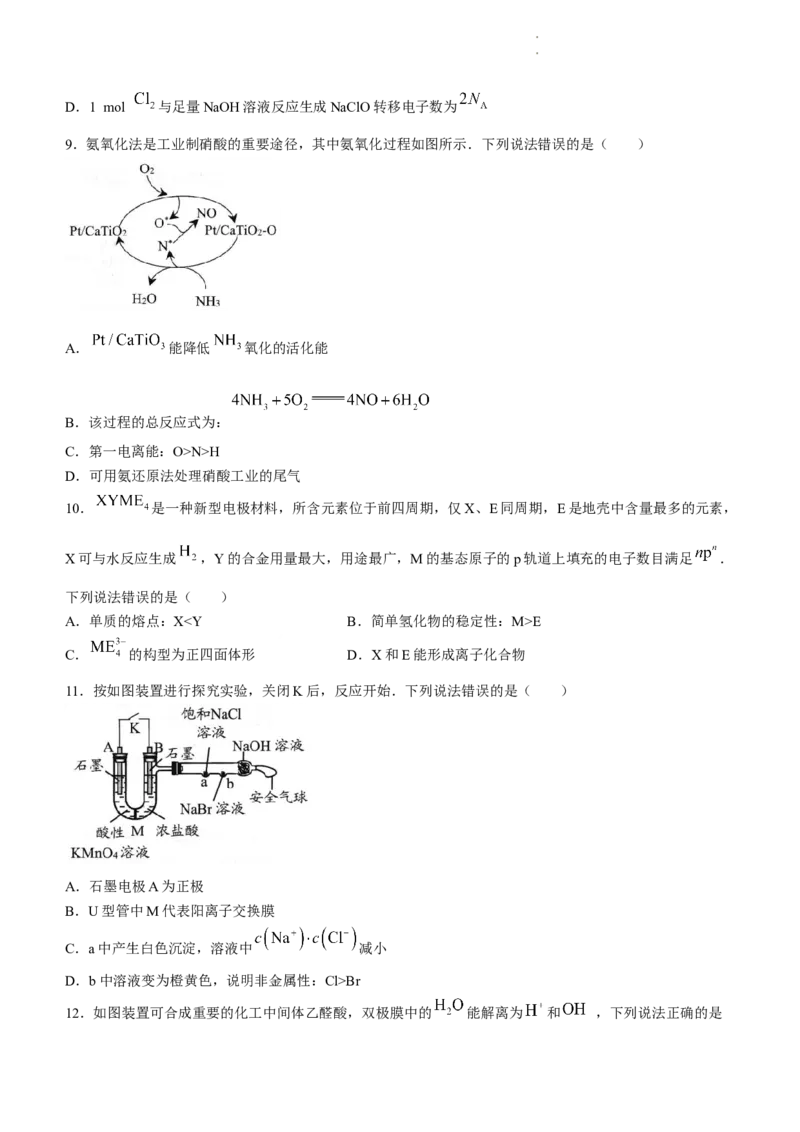
9.氨氧化法是工业制硝酸的重要途径,其中氨氧化过程如图所示.下列说法错误的是( )
A. 能降低 氧化的活化能
B.该过程的总反应式为:
C.第一电离能:O>N>H
D.可用氨还原法处理硝酸工业的尾气
10. 是一种新型电极材料,所含元素位于前四周期,仅X、E同周期,E是地壳中含量最多的元素,
X可与水反应生成 ,Y的合金用量最大,用途最广,M的基态原子的p轨道上填充的电子数目满足 .
下列说法错误的是( )
A.单质的熔点:XE
C. 的构型为正四面体形 D.X和E能形成离子化合物
11.按如图装置进行探究实验,关闭K后,反应开始.下列说法错误的是( )
A.石墨电极A为正极
B.U型管中M代表阳离子交换膜
C.a中产生白色沉淀,溶液中 减小
D.b中溶液变为橙黄色,说明非金属性:Cl>Br
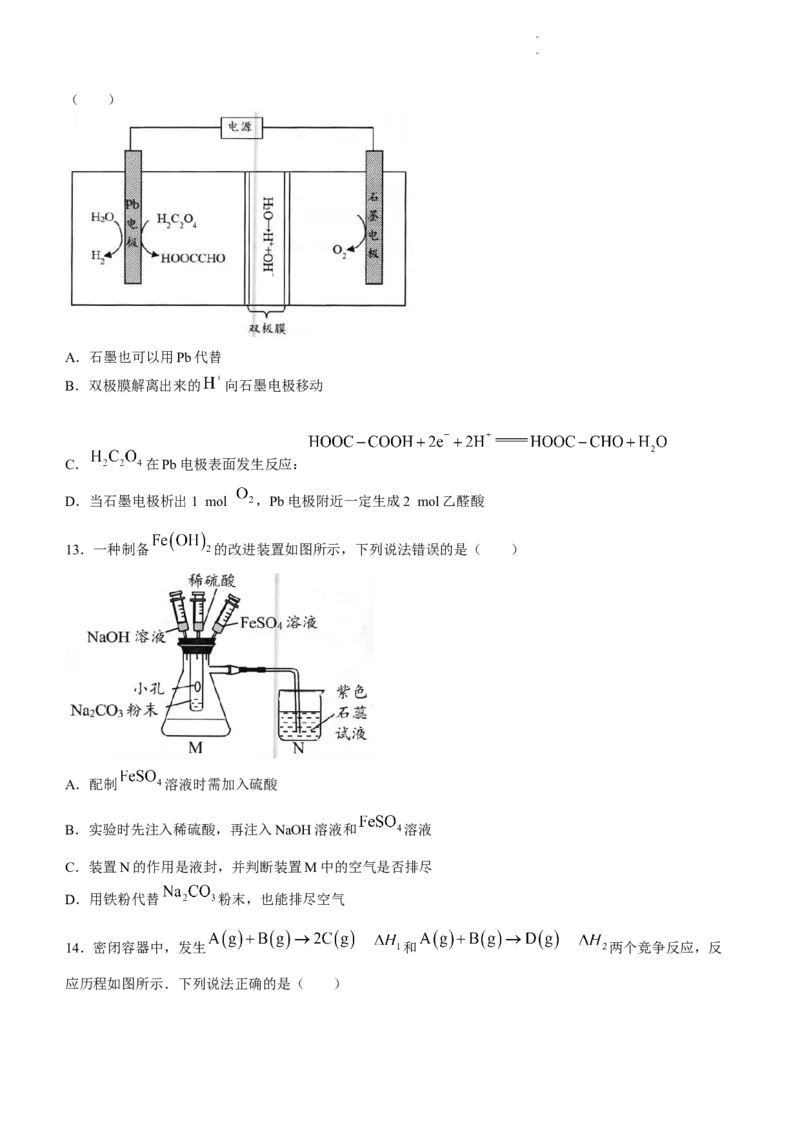
12.如图装置可合成重要的化工中间体乙醛酸,双极膜中的 能解离为 和 ,下列说法正确的是
学学科科网网((北北京京))股股份份有有限限公公司司( )
A.石墨也可以用Pb代替
B.双极膜解离出来的 向石墨电极移动
C. 在Pb电极表面发生反应:
D.当石墨电极析出1 mol ,Pb电极附近一定生成2 mol乙醛酸
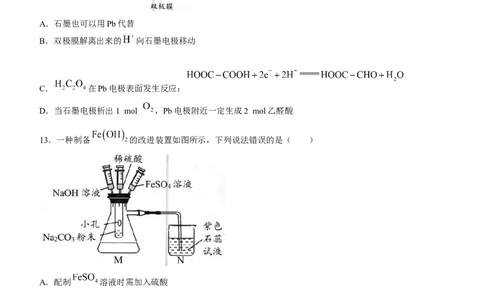
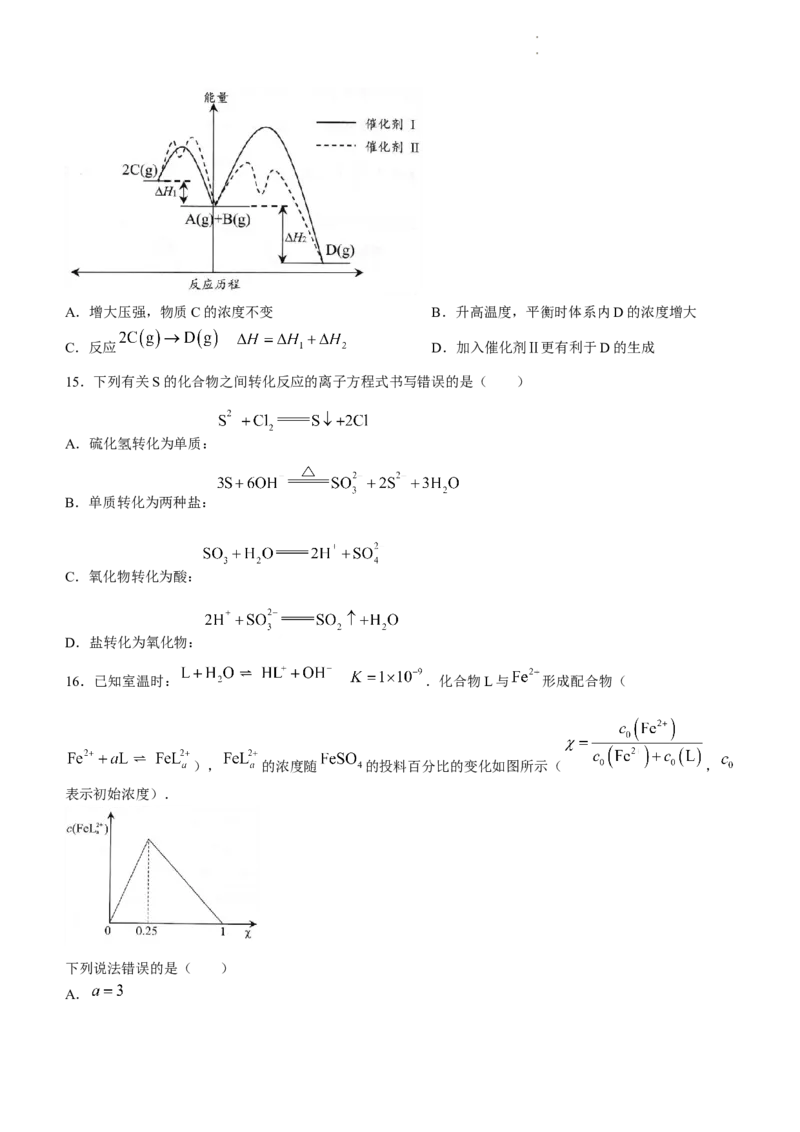
13.一种制备 的改进装置如图所示,下列说法错误的是( )
A.配制 溶液时需加入硫酸
B.实验时先注入稀硫酸,再注入NaOH溶液和 溶液
C.装置N的作用是液封,并判断装置M中的空气是否排尽
D.用铁粉代替 粉末,也能排尽空气
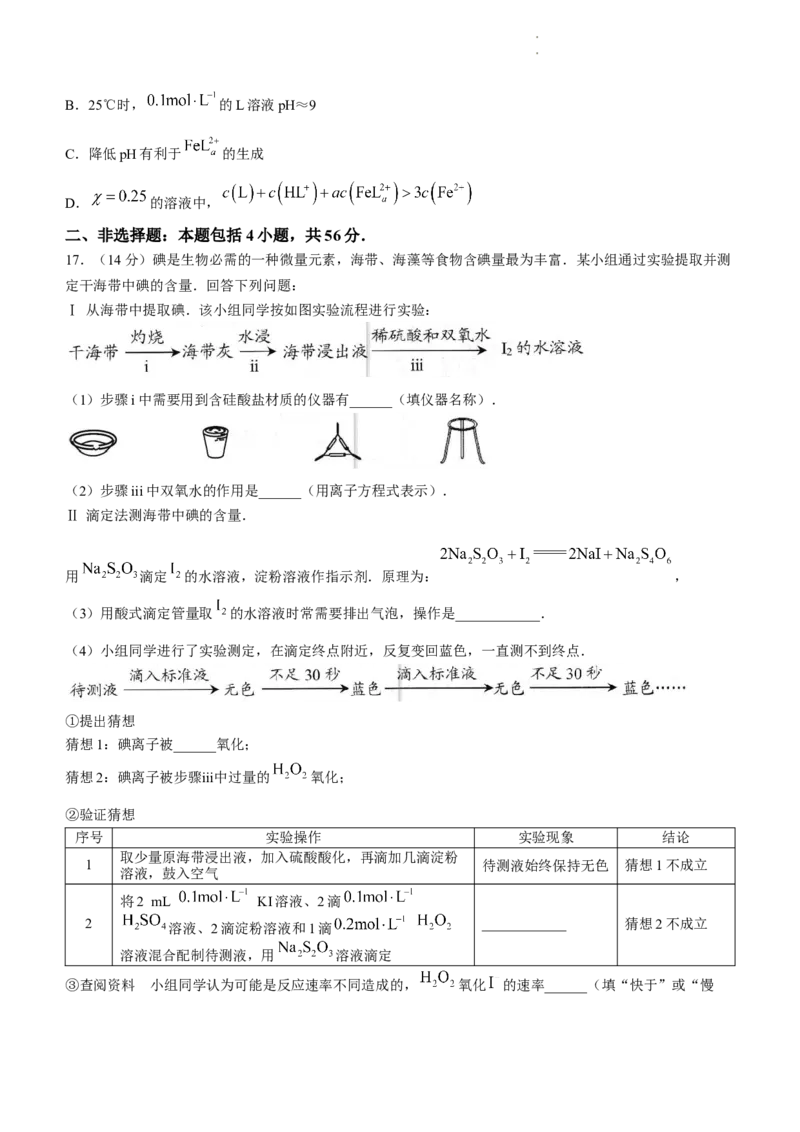
14.密闭容器中,发生 和 两个竞争反应,反
应历程如图所示.下列说法正确的是( )
学学科科网网((北北京京))股股份份有有限限公公司司A.增大压强,物质C的浓度不变 B.升高温度,平衡时体系内D的浓度增大
C.反应 D.加入催化剂Ⅱ更有利于D的生成
15.下列有关S的化合物之间转化反应的离子方程式书写错误的是( )
A.硫化氢转化为单质:
B.单质转化为两种盐:
C.氧化物转化为酸:
D.盐转化为氧化物:
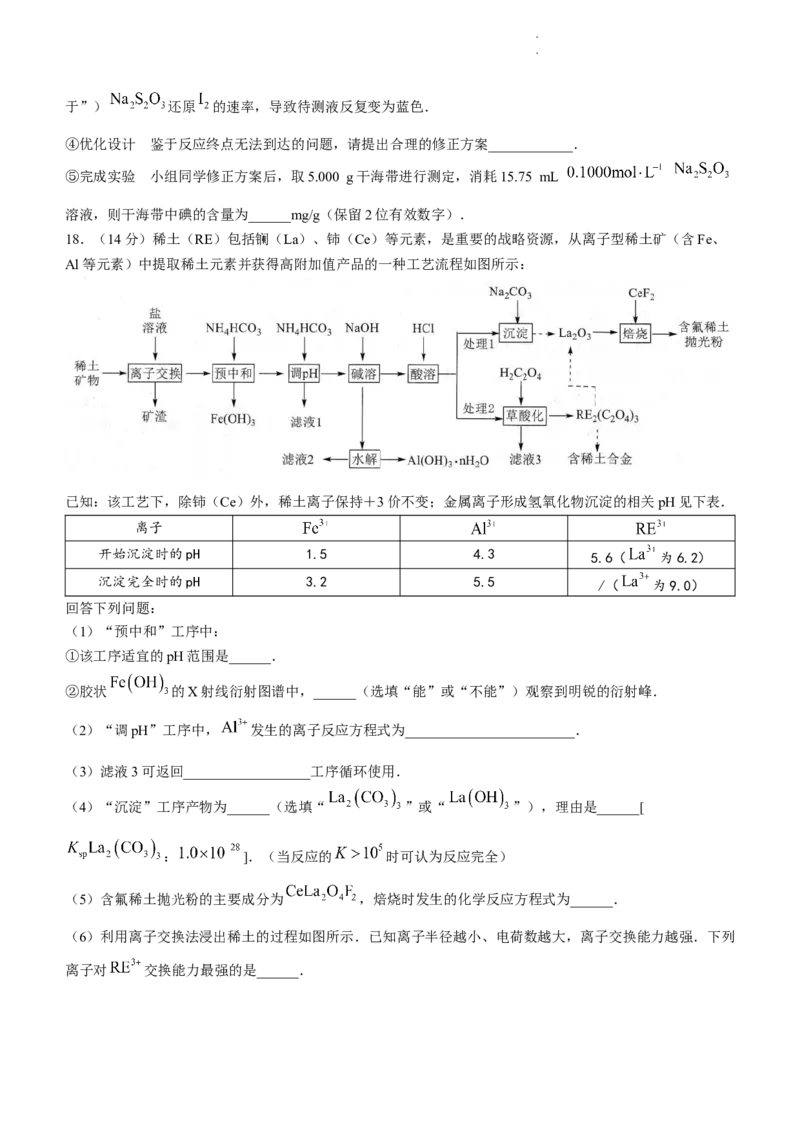
16.已知室温时: .化合物L与 形成配合物(
), 的浓度随 的投料百分比的变化如图所示( ,
表示初始浓度).
下列说法错误的是( )
A.
学学科科网网((北北京京))股股份份有有限限公公司司B.25℃时, 的L溶液pH≈9
C.降低pH有利于 的生成
D. 的溶液中,
二、非选择题:本题包括4小题,共56分.
17.(14分)碘是生物必需的一种微量元素,海带、海藻等食物含碘量最为丰富.某小组通过实验提取并测
定干海带中碘的含量.回答下列问题:
Ⅰ 从海带中提取碘.该小组同学按如图实验流程进行实验:
(1)步骤i中需要用到含硅酸盐材质的仪器有______(填仪器名称).
(2)步骤iii中双氧水的作用是______(用离子方程式表示).
Ⅱ 滴定法测海带中碘的含量.
用 滴定 的水溶液,淀粉溶液作指示剂.原理为: ,
(3)用酸式滴定管量取 的水溶液时常需要排出气泡,操作是____________.
(4)小组同学进行了实验测定,在滴定终点附近,反复变回蓝色,一直测不到终点.
①提出猜想
猜想1:碘离子被______氧化;
猜想2:碘离子被步骤iii中过量的 氧化;
②验证猜想
序号 实验操作 实验现象 结论
取少量原海带浸出液,加入硫酸酸化,再滴加几滴淀粉
1 待测液始终保持无色 猜想1不成立
溶液,鼓入空气
将2 mL KI溶液、2滴
2 溶液、2滴淀粉溶液和1滴 ____________ 猜想2不成立
溶液混合配制待测液,用 溶液滴定
③查阅资料 小组同学认为可能是反应速率不同造成的, 氧化 的速率______(填“快于”或“慢
学学科科网网((北北京京))股股份份有有限限公公司司于”) 还原 的速率,导致待测液反复变为蓝色.
④优化设计 鉴于反应终点无法到达的问题,请提出合理的修正方案____________.
⑤完成实验 小组同学修正方案后,取5.000 g干海带进行测定,消耗15.75 mL
溶液,则干海带中碘的含量为______mg/g(保留2位有效数字).
18.(14分)稀土(RE)包括镧(La)、铈(Ce)等元素,是重要的战略资源,从离子型稀土矿(含Fe、
Al等元素)中提取稀土元素并获得高附加值产品的一种工艺流程如图所示:
已知:该工艺下,除铈(Ce)外,稀土离子保持+3价不变;金属离子形成氢氧化物沉淀的相关pH见下表.
离子
开始沉淀时的pH 1.5 4.3 5.6( 为6.2)
沉淀完全时的pH 3.2 5.5 /( 为9.0)
回答下列问题:
(1)“预中和”工序中:
①该工序适宜的pH范围是______.
②胶状 的X射线衍射图谱中,______(选填“能”或“不能”)观察到明锐的衍射峰.
(2)“调pH”工序中, 发生的离子反应方程式为________________________.
(3)滤液3可返回__________________工序循环使用.
(4)“沉淀”工序产物为______(选填“ ”或“ ”),理由是______[
: ].(当反应的 时可认为反应完全)
(5)含氟稀土抛光粉的主要成分为 ,焙烧时发生的化学反应方程式为______.
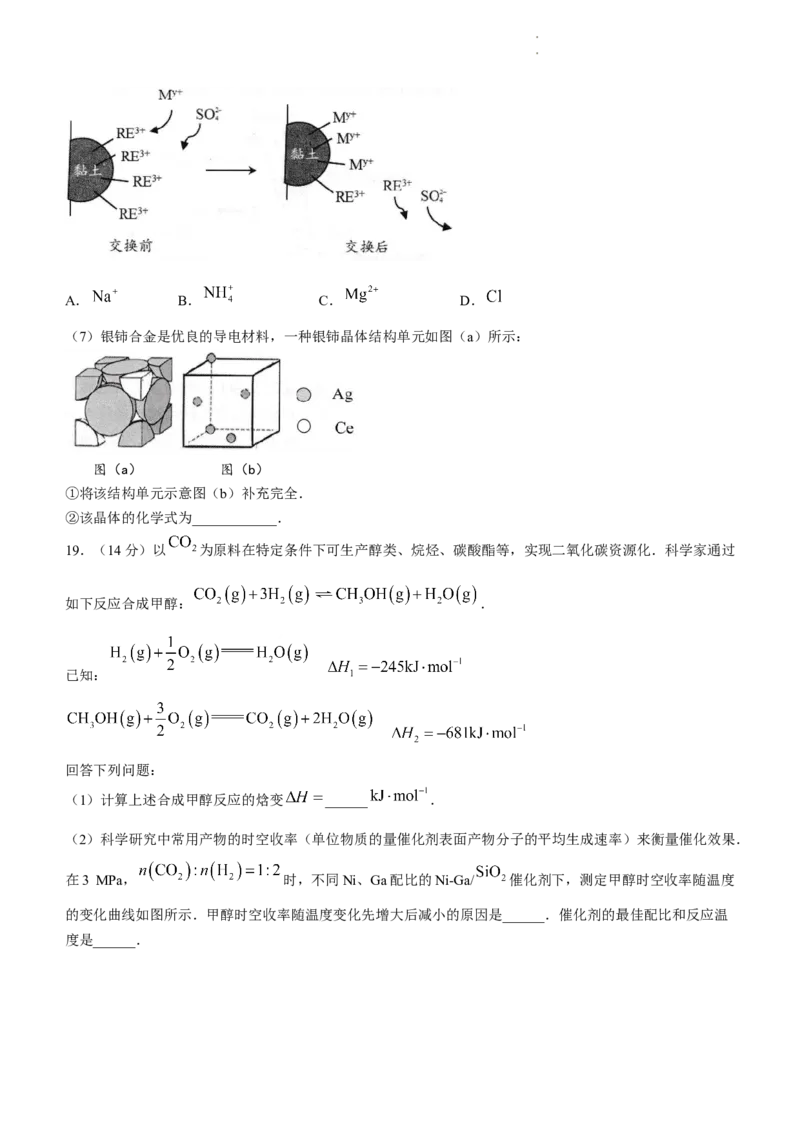
(6)利用离子交换法浸出稀土的过程如图所示.已知离子半径越小、电荷数越大,离子交换能力越强.下列
离子对 交换能力最强的是______.
学学科科网网((北北京京))股股份份有有限限公公司司A. B. C. D.
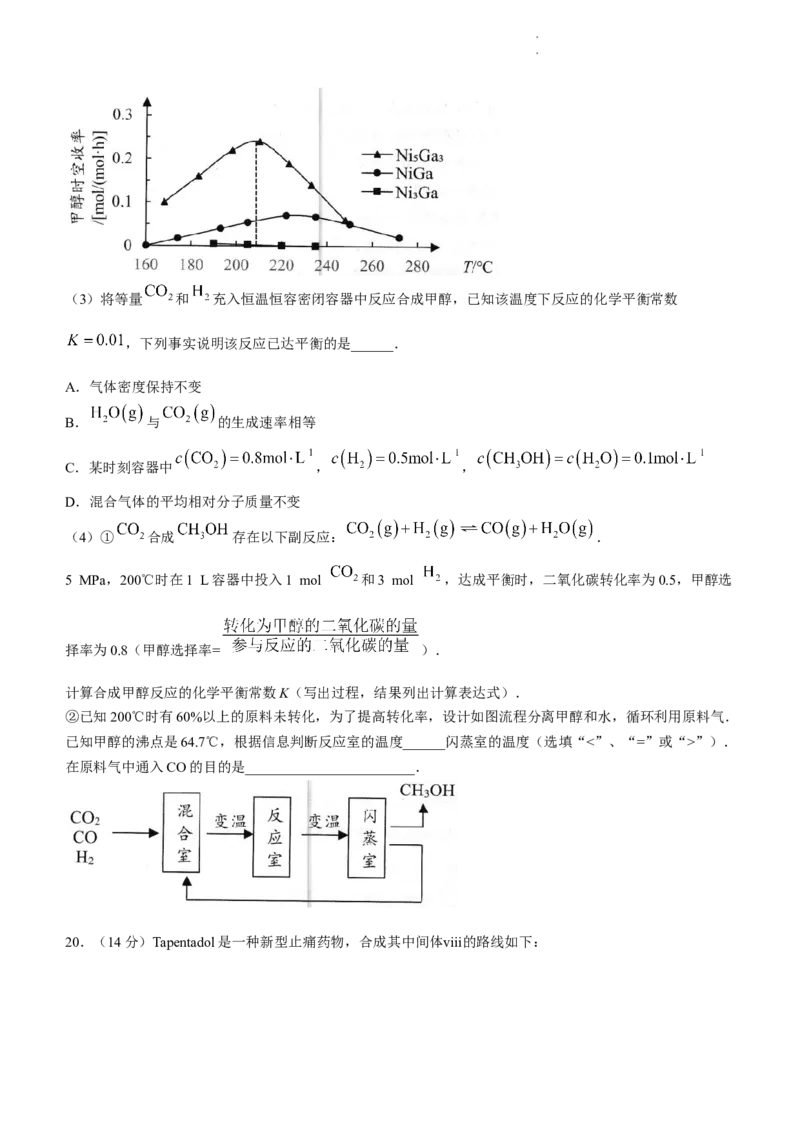
(7)银铈合金是优良的导电材料,一种银铈晶体结构单元如图(a)所示:
图(a) 图(b)
①将该结构单元示意图(b)补充完全.
②该晶体的化学式为____________.
19.(14分)以 为原料在特定条件下可生产醇类、烷烃、碳酸酯等,实现二氧化碳资源化.科学家通过
如下反应合成甲醇: .
已知:
回答下列问题:
(1)计算上述合成甲醇反应的焓变 ______ .
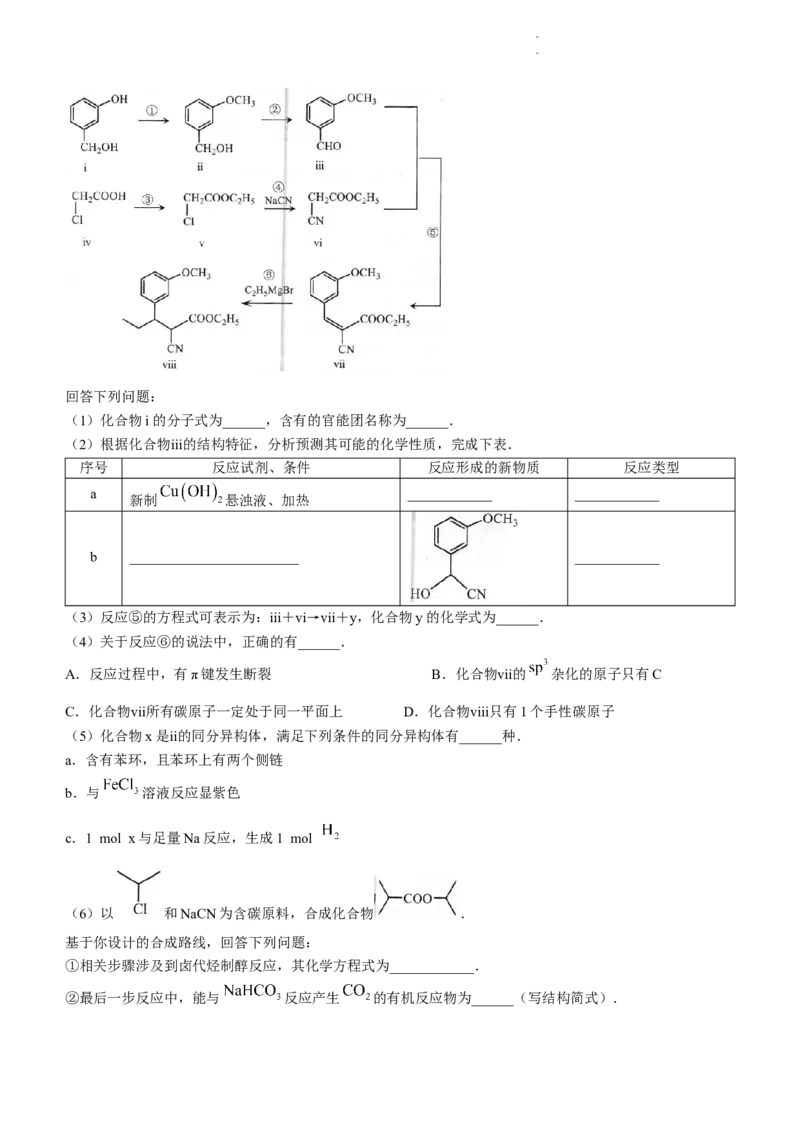
(2)科学研究中常用产物的时空收率(单位物质的量催化剂表面产物分子的平均生成速率)来衡量催化效果.
在3 MPa, 时,不同Ni、Ga配比的Ni-Ga/ 催化剂下,测定甲醇时空收率随温度
的变化曲线如图所示.甲醇时空收率随温度变化先增大后减小的原因是______.催化剂的最佳配比和反应温
度是______.
学学科科网网((北北京京))股股份份有有限限公公司司(3)将等量 和 充入恒温恒容密闭容器中反应合成甲醇,已知该温度下反应的化学平衡常数
,下列事实说明该反应已达平衡的是______.
A.气体密度保持不变
B. 与 的生成速率相等
C.某时刻容器中 , ,
D.混合气体的平均相对分子质量不变
(4)① 合成 存在以下副反应: .
5 MPa,200℃时在1 L容器中投入1 mol 和3 mol ,达成平衡时,二氧化碳转化率为0.5,甲醇选
择率为0.8(甲醇选择率= ).
计算合成甲醇反应的化学平衡常数K(写出过程,结果列出计算表达式).
②已知200℃时有60%以上的原料未转化,为了提高转化率,设计如图流程分离甲醇和水,循环利用原料气.
已知甲醇的沸点是64.7℃,根据信息判断反应室的温度______闪蒸室的温度(选填“<”、“=”或“>”).
在原料气中通入CO的目的是________________________.
20.(14分)Tapentadol是一种新型止痛药物,合成其中间体viii的路线如下:
学学科科网网((北北京京))股股份份有有限限公公司司回答下列问题:
(1)化合物i的分子式为______,含有的官能团名称为______.
(2)根据化合物iii的结构特征,分析预测其可能的化学性质,完成下表.
序号 反应试剂、条件 反应形成的新物质 反应类型
a ____________ ____________
新制 悬浊液、加热
b ________________________ ____________
(3)反应⑤的方程式可表示为:iii+vi→vii+y,化合物y的化学式为______.
(4)关于反应⑥的说法中,正确的有______.
A.反应过程中,有π键发生断裂 B.化合物vii的 杂化的原子只有C
C.化合物vii所有碳原子一定处于同一平面上 D.化合物viii只有1个手性碳原子
(5)化合物x是ii的同分异构体,满足下列条件的同分异构体有______种.
a.含有苯环,且苯环上有两个侧链
b.与 溶液反应显紫色
c.1 mol x与足量Na反应,生成1 mol
(6)以 和NaCN为含碳原料,合成化合物 .
基于你设计的合成路线,回答下列问题:
①相关步骤涉及到卤代烃制醇反应,其化学方程式为____________.
②最后一步反应中,能与 反应产生 的有机反应物为______(写结构简式).
学学科科网网((北北京京))股股份份有有限限公公司司学学科科网网((北北京京))股股份份有有限限公公司司