文档内容
重庆市 2022 年初中学业水平暨高中招生考试
化学试题(A 卷)
(全卷共四个大题,满分70分,与物理共用120分钟)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Al-27 S-32 Fe-56 Zn-65
一、选择题(本大题包括16个小题,每小题2分,共32分)每小题只有一个选项符合题意。
1. 垃圾是放错地方的资源。易拉罐属于
A. B. C. D.
2. 神州十三号返回舱在返回过程中,一定涉及化学变化的是
A. 脱离空间站 B. 自由下落 C. 外壳烧蚀 D. 打开降落伞
3. 物质分类是一种化学观念。厨房里的下列物质属于纯净物的是
A. 酸奶 B. 冰块 C. 白酒 D. 食醋
4. 化肥能提高农作物的产量。下列化肥属于复合肥的是
A. Ca (PO ) B. NH Cl C. KNO D. CO(NH )(尿素)
3 4 2 4 3 2 2
5. 液氮能长时间保存活体组织和生物样品,主要利用氮气的性质是
A. 密度小 B. 沸点低 C. 难溶于水 D. 无色无味
6. 工业炼钨原理为WO+3H W+3H O,发生还原反应的物质是
3 2 2
A. H B. WO C. W D. HO
2 3 2
7. “含氟牙膏”中的氟元素在周期表中的信息及氟原子的结构示意图如下,下列说法不正确的是
A. 氟属于非金属元素 B. 氟的原子序数是9
C. 氟的相对原子质量是19.00 D. 氟原子失去1个电子变成氟离子
8. 重庆是热门旅游城市。下列对游客和商户的提醒中正确的是A. 燃着的烟头扔进垃圾箱 B. 甲醛浸泡毛肚防变质
C. 在封闭室内进行炭火烧烤 D. 常吃蔬菜水果补充维生素
9. 千金藤素(C H NO)对新冠病毒有良好抑制作用。下列有关千金藤素说法正确的是
37 38 2 6
A. 含有3个氧气分子 B. 含有83个原子
C. 所含氢元素质量分数最大 D. 由四种元素组成
的
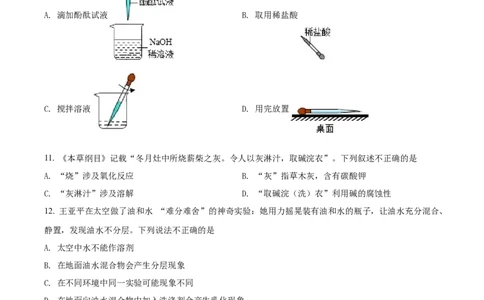
10. “中和反应”实验中使用胶头滴管 下列操作,正确的是
A. 滴加酚酞试液 B. 取用稀盐酸
C. 搅拌溶液 D. 用完放置
11. 《本草纲目》记载“冬月灶中所烧薪柴之灰。令人以灰淋汁,取碱浣衣”。下列叙述不正确的是
A. “烧”涉及氧化反应 B. “灰”指草木灰,含有碳酸钾
C. “灰淋汁”涉及溶解 D. “取碱浣(洗)衣”利用碱的腐蚀性
12. 王亚平在太空做了油和水 “难分难舍”的神奇实验:她用力摇晃装有油和水的瓶子,让油水充分混合、
静置,发现油水不分层。下列说法不正确的是
A. 太空中水不能作溶剂
B. 在地面油水混合物会产生分层现象
C. 在不同环境中同一实验可能现象不同
D. 在地面向油水混合物中加入洗涤剂会产生乳化现象
13. 科学家利用太阳光在新型催化剂表面高效分解水,微观过程如下图。下列说法不正确的是
A. 该反应为分解反应
B. 反应前后分子数目不变
C. 反应前后元素种类不变D. 该过程可看出化学反应经历了原子重新组合
14. 实验室制取CO、O 和H 是初中化学必备知识。下列说法不正确的是
2 2 2
A. CO 和O 的发生装置可以相同 B. CO 和O 的发生装置可以不同
2 2 2 2
C. CO 和H 的收集装置完全相同 D. O 和H 的发生和收集装置可以相同
2 2 2 2
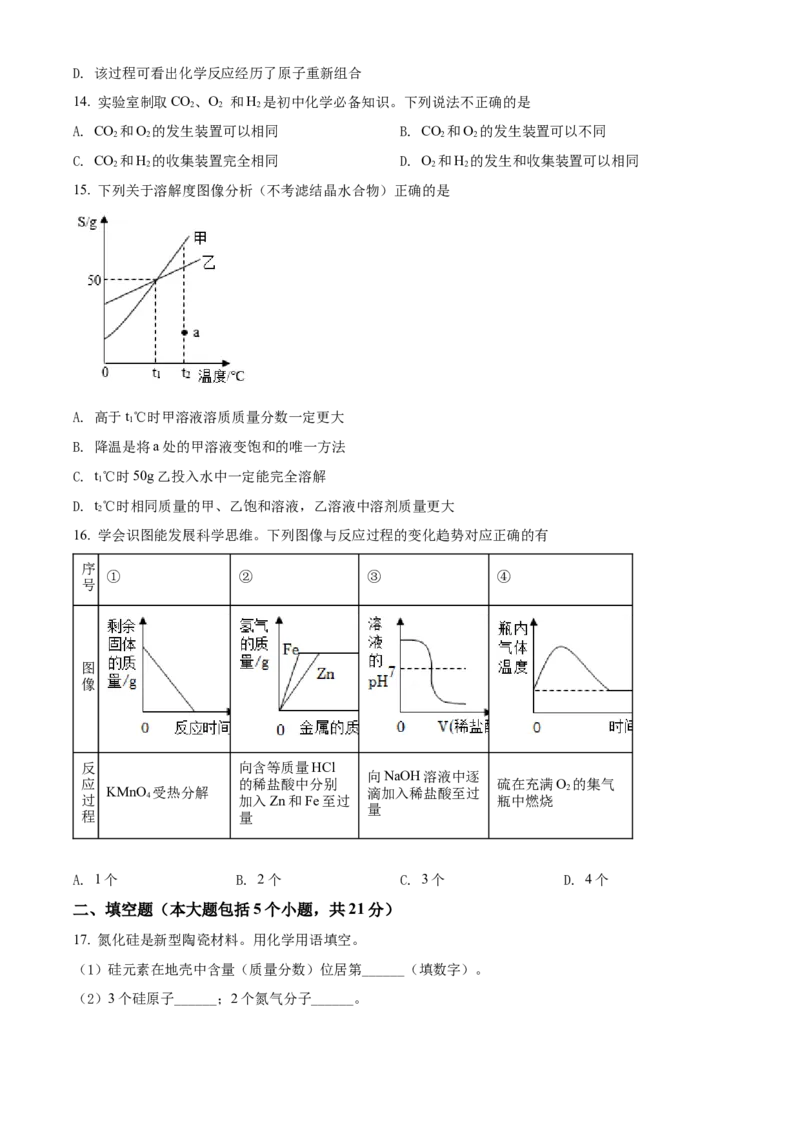
15. 下列关于溶解度图像分析(不考滤结晶水合物)正确的是
A. 高于t℃时甲溶液溶质质量分数一定更大
1
B. 降温是将a处的甲溶液变饱和的唯一方法
C. t℃时50g乙投入水中一定能完全溶解
1
D. t℃时相同质量的甲、乙饱和溶液,乙溶液中溶剂质量更大
2
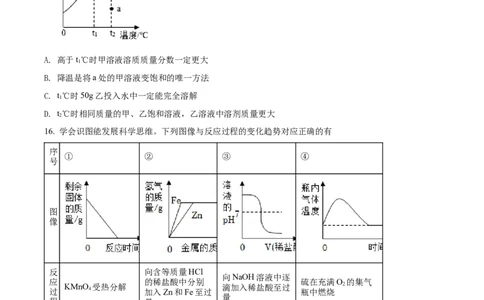
16. 学会识图能发展科学思维。下列图像与反应过程的变化趋势对应正确的有
序
① ② ③ ④
号
图
像
反 向含等质量HCl
向NaOH溶液中逐
应 的稀盐酸中分别 硫在充满O 的集气
KMnO 受热分解 滴加入稀盐酸至过 2
过 4 加入Zn和Fe至过 瓶中燃烧
量
程 量
A. 1个 B. 2个 C. 3个 D. 4个
二、填空题(本大题包括5个小题,共21分)
17. 氮化硅是新型陶瓷材料。用化学用语填空。
(1)硅元素在地壳中含量(质量分数)位居第______(填数字)。
(2)3个硅原子______;2个氮气分子______。(3)氮化硅中硅、氮元素化合价分别为+4和-3,其化学式为______。
18. 2025年长安汽车厂将停止销售传统燃油车,新能源汽车发展成为主要趋势。
(1)下列不属于新能源的是______(填序号)。
A. 氢能 B. 汽油 C. 生物质能
(2)乙醇是一种生物燃料,它是______(填 “可再生”或“不可再生”)能源。乙醇在空气中完全燃烧
生成水和______(写化学式),并放出大量热。
(3)肼-空气燃料电池有织应用于汽车工业,其原理是肼(NH)与氧气反应生成一种单质和水,反应化
2 4
学方程式为______。
19. 钛合金、铝合金广泛应用于航空工业。
(1)下列矿石主要成分含相同金属元素的是______(填序号)。
A. 磁铁矿 B. 铝土矿 C. 菱铁矿
(2)钛与盐馥反应:2Ti+6HCl=2X+3H ↑,则X化学式为______。若把钛放入硝酸银溶液中______(填
2
“有”或“没有“)单质银析出。
(3)工业制铝原理为电解熔融的Al O,生成铝和一种可供呼吸的气体。该反应的化学方程式为______。
2 3
20. 北京冬奥会,融入中国元素,彰显科技力量,向世界贡献中国方案。
(1)冰墩墩外壳材料是环保PVC塑料,它属于______(填“天然有机高分子”或“有机合成")材料。
(2)颁奖礼仪服内胆添加了由碳原子直接构成的石墨烯发热材料。下列物质也是由原子直接构成的是
______(填序号)。
A. 氯化钠 B. 金刚石 C. 二氧化碳
(3)“冰丝带”速滑馆采用了CO 直冷制冰技术,利用高压获得的液态CO 蒸发吸热,降低水温,快速
2 2
制冰。下列说法正确的是______(填序号)。
A. 加压后CO 分子体积变小
2
B. 水变为冰后分子停止运动
C. 蒸发后CO 分子间隔变大
2
(4)《千里江山图》为运动员服装设计提供灵感,其真迹颜料含有石绿。石绿[主要成分Cu (OH)CO]
2 2 3
受热分解生成三种氧化物(无化合价变化),反应的化学方程式为______。
21. 我国承诺:2030年“碳达峰”,2060年“碳中和”,体现大国担当。丁仲礼院士认为“碳中和”是让
人为排放的CO,被人为努力和自然过程所吸收。
2
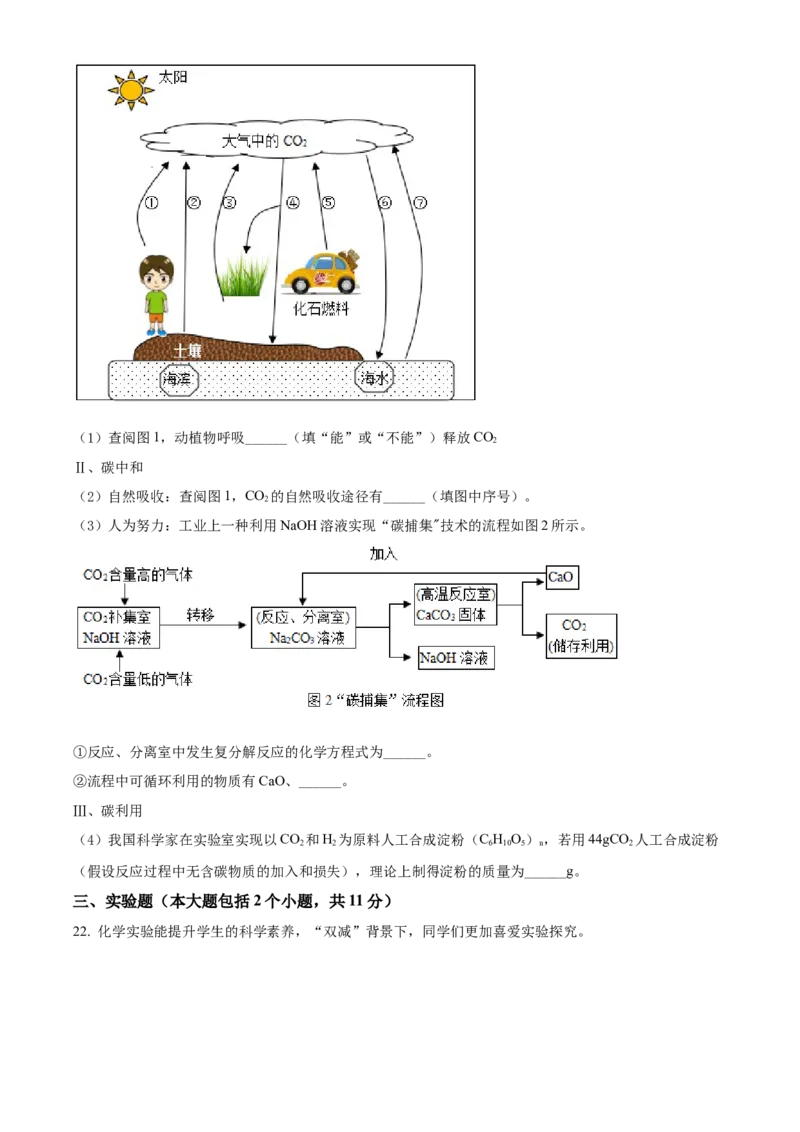
Ⅰ、碳排放(1)查阅图1,动植物呼吸______(填“能”或“不能”)释放CO 。
2
Ⅱ、碳中和
(2)自然吸收:查阅图1,CO 的自然吸收途径有______(填图中序号)。
2
(3)人为努力:工业上一种利用NaOH溶液实现“碳捕集"技术的流程如图2所示。
①反应、分离室中发生复分解反应的化学方程式为______。
②流程中可循环利用的物质有CaO、______。
Ⅲ、碳利用
(4)我国科学家在实验室实现以CO 和H 为原料人工合成淀粉(C H O),若用44gCO 人工合成淀粉
2 2 6 10 5 n 2
(假设反应过程中无含碳物质的加入和损失),理论上制得淀粉的质量为______g。
三、实验题(本大题包括2个小题,共11分)
22. 化学实验能提升学生的科学素养,“双减”背景下,同学们更加喜爱实验探究。(1)实验一:去除粗盐中的泥沙。过滤器的制作过程如图1所示,正确操作的顺序为______(填序号)。
蒸发过程中,提供热源的玻璃仪器名称为______。
(2)实验二:探究可燃物燃烧的条件(白磷化学式为P,着火点为40℃)。
4
向图2装置中通入O 后,______(填“甲”或“乙”)烧怀中的白磷燃烧,反应化学方程式为______。比
2
较乙烧杯中通入O 前、后的现象,得出燃烧需要的条件是______(填序号)。
2
A.可燃物 B.温度达到着火点 C.需要氧气参与
23. 化学产品制备正向着绿色、低碳、可持续的方向发展。
(1)工业制备硫酸铜的两种方案原理如下:
Ⅰ:Cu+2H SO (浓)=CuSO+SO ↑+ 2H O
2 4 4 2 2
Ⅱ:2Cu+O 2CuO CuO+H SO =______(完成化学方程式)
2 2 4
(2)某兴趣小组三名同学探究制备硫酸铜的新方案,原理如下:
Ⅲ:Cu+H O+ H SO =CuSO+2H O
2 2 2 4 4 2
将反应物混合,观察到:开始有少量气泡,而后反应剧烈产生大量气泡,溶液呈蓝色,试管发热。逸出气
体能使带火星木条复燃,该气体为______。他们对反应产生大量气泡非常好奇,推测是某些因素导致了
HO 分解。
2 2
甲同学认为是反应生成的CuSO 所导致,乙同学认为是反应放热使温度升高所导致。于是设计了下表实验
4
进行探究。
编号 试剂 温度 现象
① 10mL30%H O、1mL10%CuSO 30℃ 产生少量气泡
2 2 4
② 10mL30%H O、______ 30℃ 无明显现象
2 2
③ 10mL30%H O、1mL10%CuSO 80℃ 快速放出气泡
2 2 4甲同学对比实验①②认为自己的推测正确,请将表中实验②补充完整。
乙同学对比实验______(填编号)认为自己的推测正确。
丙同学认为,甲、乙同学的结论都不严谨,其理由是______。
(3)综合评价制备CuSO 的方案Ⅲ,下列说法正确的是______(填序号)。
4
A. Ⅲ比Ⅰ更环保、比Ⅱ更节能
.
B 消耗等质量铜,Ⅲ生成CuSO 最多
4
.
C Ⅲ中有原料发生分解,造成试剂浪费
四、计算题(本大题包括1个小题,共6分)
24. 化学泡沫灭火器是常用灭火器之一,其反应原理为:Al (SO )+6NaHCO=3Na SO +2Al(OH)
2 4 3 3 2 4
的
↓+6CO ↑。现将34.2 kg质量分数为10% Al2(SO4)3溶液与270 kg NaHCO3溶液混合,恰好完全反应
3 2
(假设生成的气体全部逸出)。
已知相对分子质量:Al (SO ) 342;NaSO 142;Al(OH) 78
2 4 3 2 4 3
试计算:
(1)Al (SO ) 中O元素与S元素的质量比为______。
2 4 3
(2)最后所得溶液中NaSO 的质量分数。
2 4
(3)将34.2 kg Al (SO ) 溶液的溶质质量分数由10%变为20%可以用不同方法。请选择一种方法进行计
2 4 3
算(只写出计算过程,不答具体操作)。