文档内容
2025年邵阳市高三第一次联考试题参考答案与评分标准
化 学
一、选择题:本题共 小题,每小题 分,共 分。
14 3 42
题 号
1 2 3 4 5 6 7
答 案
D C B C D D A
题 号
8 9 10 11 12 13 14
答 案
B A D B A C B
解析: 项 点溶液为 溶液和 溶液的混合溶液
14. A :a 0.1mol/LHA 0.1mol/LMCl ,
由K -5 得K + -14 K -9 根据 水解反应
b(MOH)=1×10 h(M )=10 ÷ b=10 , MCl
c + c c + 2
M
+
+H2OMOH+H
+
,
K
h=
(H
c
)
(
·
M +
(M
)
OH)
≈ 0.1
( H
mol
)
/L =10
-9
,
得c
(H
+
)=
-5
因此相对 点溶液中c
+ -2.7
水解可忽略不计 点溶
10 mol/L, a (H )=10 mol/L,MCl ,a
液中 + 主要由 电离产生 则 - + K -2.7 2 -4.4 所
H HA , HAA +H a≈(10 )÷0.1=10 ,
以 的电离平衡常数的数量级为
-5
HA 10 ;
项 等浓度的 和 的混合溶液对应图中的 点溶液 由电荷守恒
B : NaA MCl b , :
c + c + c + c — c — c —
(Na )+ (M )+ (H )= (A )+ (Cl )+ (OH ),
点 知 + c — 则c + c + c — c —
b pH=6.51, (H )> (OH ), (Na )+ (M )< (A )+ (Cl );
项 点溶液为 的混合溶液 且c c 电离
C :c NaA、MCl、MOH , (MOH)> (MCl),MOH
程度 水解程度 则 —主要来源于 的电离
≫NaA , OH MOH ;
项 由物料守恒n — n -3
D : :(A )+ (HA)=0.1mol/L×10mL=10 mol
点溶液体积V c — c -3
d ≈ (10+20)mL=30mL,(A )+ (HA)=10 mol÷30mL≈
0.033mol/L。
二、非选择题:本题共 小题,共 分。除特殊标记外,其余每空 分。(反应条件未写,未
4 58 2
配平, 、 未写计 分;化学式写错计 分。)
↑ ↓ 1 0
分 去除铁屑表面的油污 分
15.(15 )(1) (1 )
2+ +
(2)H2S+Cu CuS↓+2H
减少绿矾的损耗 便于后续干燥
(3) ,
(4)①b ②<
在 装置中加入适量的水 关闭 打开 在 处稍加热 中有气泡产生 停止
(5) D , K1、 K2, A ,D ,
加热后 中的导管内形成一段水柱 且一段时间后 水柱不下降 则气密性良好(答
,D , , ,
案合理即可)
高温
( 不打“ ”符号不扣分)
(6)2FeSO4·7H2OFe2O3+SO2↑+SO3↑+14H2O↑ H2O ↑
(7)29.5
年邵阳市高三第一次联考试题参考答案与评分标准(化学) 第 页(共 页)
2025 1 3
{#{QQABKYaEogCAAhBAABgCEQUACEGQkBGAAagOhEAYIAIAiQFABAA=}#}分 将矿渣粉碎或空气从焙烧炉底部通入 矿渣从顶部加入(答案合理即可)
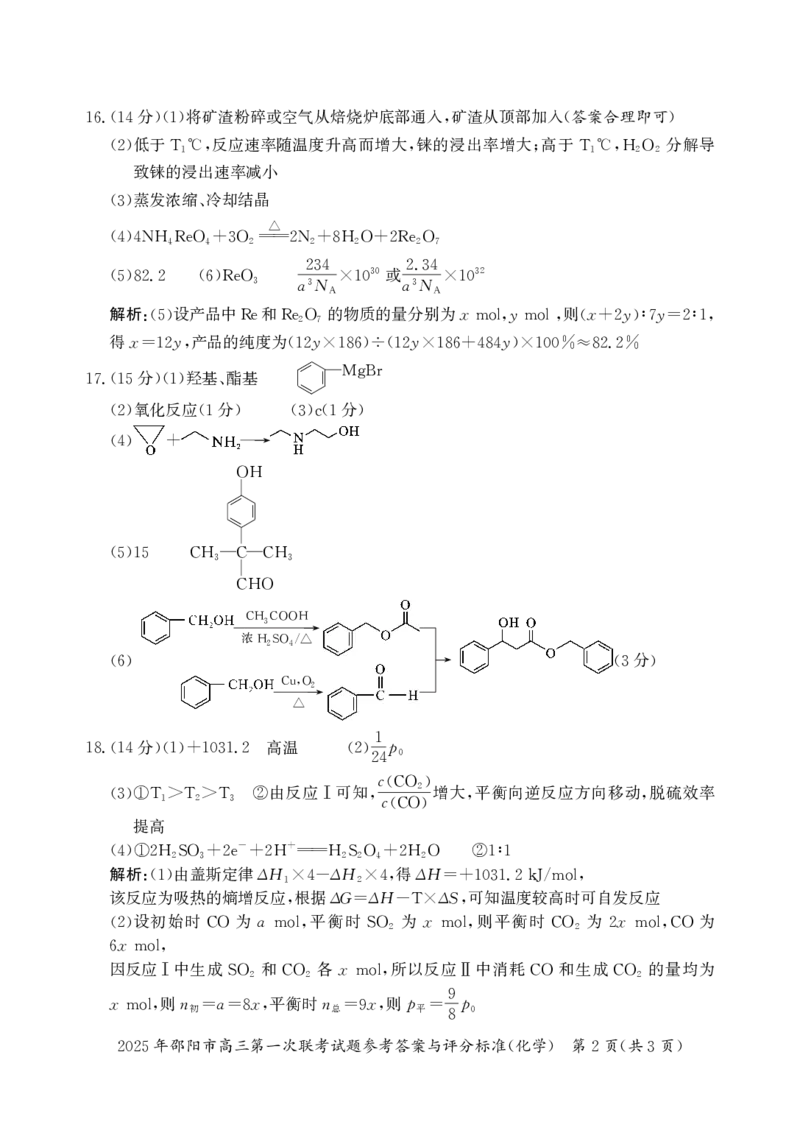
16.(14 )(1) ,
低于 反应速率随温度升高而增大 铼的浸出率增大 高于 分解导
(2) T1℃, , ; T1℃,H2O2
致铼的浸出速率减小
蒸发浓缩 冷却结晶
(3) 、
△
(4)4NH4ReO4+3O22N2+8H2O+2Re2O7
234 30 或2.34 32
(5)82.2 (6)ReO3 a3N ×10 a3N ×10
A A
解析: 设产品中 和 的物质的量分别为x y 则x y y
(5) Re Re2O7 mol, mol, (+2 )∶7 =2∶1,
得x y 产品的纯度为 y y y
=12 , (12 ×186)÷(12 ×186+484 )×100%≈82.2%
分 羟基 酯基
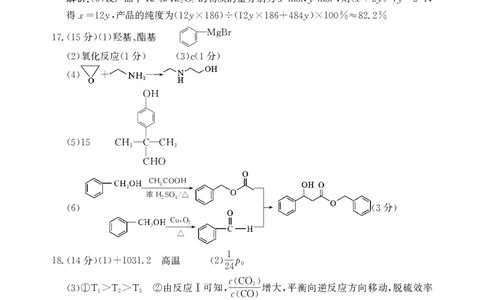
17.(15 )(1) 、
年邵阳市高三第一次联考试题参考答案与评分标准(化学) 第 页(共 页)
2025 2 3
MgBr
氧化反应 分 分
(2) (1 ) (3)c(1 )
(4) + →
(5)15 CH3 C CH3
CHO
OH
CH3COOH
浓 →
H2SO4/△
分
(6) → (3 )
Cu,O2
→
△
分 高温 1p
18.(14 )(1)+1031.2 (2) 0
24
c
由反应 可知 (CO2)增大 平衡向逆反应方向移动 脱硫效率
(3)①T1>T2>T3 ② Ⅰ ,c , ,
(CO)
提高
- +
(4)①2H2SO3+2e +2H H2S2O4+2H2O ②1∶1
解析: 由盖斯定律ΔH ΔH 得ΔH
(1) 1×4- 2×4, =+1031.2kJ/mol,
该反应为吸热的熵增反应 根据ΔG ΔH ΔS 可知温度较高时可自发反应
, = -T× ,
设初始时 为a 平衡时 为x 则平衡时 为 x 为
(2) CO mol, SO2 mol, CO2 2 mol,CO
x
6 mol,
因反应 中生成 和 各x 所以反应 中消耗 和生成 的量均为
Ⅰ SO2 CO2 mol, Ⅱ CO CO2
x
mol,
则n初
=
a
=8
x
,
平衡时n总
=9
x
,
则p平
=
9p
0
8
{#{QQABKYaEogCAAhBAABgCEQUACEGQkBGAAagOhEAYIAIAiQFABAA=}#}CaSO4 s +CO g CaO s +SO2 g +CO2 g
初始时物质的量 a
: 0 0
变化时物质的量 x x x
:
平衡时物质的量 a x x x x
: -2 =6 2
平衡时各组分压强
:
6p平 1p平 2p平
9 9 9
1 1
CaSO4(s)+CO(g) CaS s +CO2(g)
4 4
变化的物质的量 x x
:
1p平· 2p平
∴
K
p=
9 9
=
1p平
=
1p
0
6p平 27 24
9
略
(3)
由 根据得失电子守恒可知 为 反应
(4) SO2→H2SO4,NO→N2 SO2∽NO 1∶1 。
年邵阳市高三第一次联考试题参考答案与评分标准(化学) 第 页(共 页)
2025 3 3
{#{QQABKYaEogCAAhBAABgCEQUACEGQkBGAAagOhEAYIAIAiQFABAA=}#}