文档内容
九月调研考试化学测试题参考答案及解析
1~15选择题,每小题3分,共45分。
题号 1 2 3 4 5 6 7 8
答案 C B A D B B A C
题号 9 10 11 12 13 14 15
答案 D B A A D D C
16.(14分)
(1)5s2(1分) (2)C(2分)
(3)将矿石粉碎或适当提高盐酸的浓度或适当升温(1分,答出一点即可,其它合理答案也给分)
(4)Ca2+、Mg2+(2分,错写0分,漏写1分)
(5)SrSO (s)+Ba2+(aq) BaSO (s)+Sr2+(aq) (2分) 5×10−10(2分)
4 4
(6)A(2分)
(7)窝穴体a的空腔与Sr2+更匹配,可形成结构更稳定的超分子(2分,合理即可)
17.(13分)
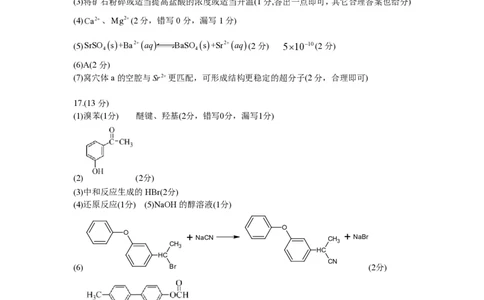
(1)溴苯(1分) 醚键、羟基(2分,错写0分,漏写1分)
(2) (2分)
(3)中和反应生成的HBr(2分)
(4)还原反应(1分) (5)NaOH的醇溶液(1分)
O
O
+ NaCN CH + NaBr
CH 3
3
HC
HC
CN
(6) Br (2分)
(7) (2分)
18.(14分)
(1)4(2分) N、O(2分,漏写1分,错写0分)
(2)三颈烧瓶(三口烧瓶也给分)(2分)
作为溶剂,使水杨醛和乙二胺充分接触反应(2分,合理即可)
(3)ABD(2分,错选0分,漏选一项扣1分,扣完为止)
(4)CH COOH(2分)
3
(5)ABC(2分,错选0分,漏选一项扣1分,扣完为止)
1
{#{QQABDQQkxgqwkAbACJ5qQ00MCUoQsIIiLUoMAVAQuA4CyJNABKA=}#}19.(14分)
(1)①B(2分) ② CH 3 O(CO)O − +CH 3 I→CO(OCH 3 ) 2 +I−(2分)
(2)①ds(2分)
②吸附的 H*浓度越高,催化剂上形成的氧空位越多,反应速率越快(2分)(答出“催化剂
上形成的氧空位越多”,给2分)
③该温度下,甲醇炭化,碳覆盖在催化剂表面(1分),使催化剂活性下降(1分)(共2分)
400(a−b)
(3)① %(2分) ② (2分)
a
2
{#{QQABDQQkxgqwkAbACJ5qQ00MCUoQsIIiLUoMAVAQuA4CyJNABKA=}#}九月调研考试化学测试题详细解析
1. C A 项,用秸秆制取燃料乙醇的过程碳元素变价;D 项,在野外用氢化钠制氢气时,
氢元素变价。
2. B B项,该模型是空间填充模型,不是球棍模型;SiO 为共价晶体,其球棍模型应为
2
立体网状结构。
3. A A项,浓盐酸和浓硝酸的混合物(体积比为3:1)叫做王水。
4. D A项,肥皂中的高级脂肪酸盐含亲水基(羧酸根)和疏水基(长链烷基),可乳化油污;B
项,生石灰能与酸性氧化物反应,故煤炭中加入生石灰生成硫酸钙,可减少煤燃烧时产生的
SO ; C项,施加电场时,液晶的长轴取向发生不同程度的改变从而显示出数字、文字或图
2
像。故液晶可用于电脑、手机和电视的显示器。D项,用焦炭与SiO 反应制粗硅的反应方
2
高温
程式为 2C+SiO = Si+2CO↑,在这个反应中,碳是还原剂,SiO 2 氧化剂,该反应能发
2
生是因为生成了气态的CO,使平衡正向移动;
5.B A项,1个甲基中含有9个电子,则1 mol甲基(-CH )所含的电子数为9N ; B项,
3 A
1mol冰中含有2mol氢键,含有的氢键数目为2N ;C项,12gNaHSO 固体中含阳离子数目
A 4
12g
为 ×1×N /mol=0.1N ;D项,Na HPO 为正盐,可知1molH PO 为二元酸,故
120g/mol A A 2 3 3 3
1molH PO 在水中最多电离的H+为2N
3 3 A。
6.B a的核外电子总数与其周期数相同,说明a是H元素;b的价电子层中的末成对电
子有3个,则b是N元素;c的最外层电子数为其内层电子数的3倍,则c是O元素;d与
c同族,则d是S元素;e的最外层只有1个电子,但次外层有18个电子,则e是Cu元素。
bc -、bc -分子的中心原子的价层电子对数均为3。
2 3
7. A A项,Na与水反应生成氢气。
8. C C→E的反应是可逆反应, C不能全部转变成E。
9.D A项,铋离子位于顶点,与其最近且距离相等的O2−位于棱心,有6个,分别位于上
下、前后、左右;B项,K+替换Ba2+后,Bi的价态升高;C项,K第一电离能小于O;D
3.45×1023
项,晶体的密度是 g⋅cm−3,而晶胞体积是( a×10−7)3 cm3,故晶胞的质量是
a3⋅N
A
345
1
g。晶胞中Ba或K位于体心,个数为总和1,O2−位于棱心,有12× =3,所以x=0.5。
N 4
A
10.B 根据化合价升降法和电荷守恒,实验Ⅱ反应离子方程式为2MnO -+3SO 2-+H O
4 3 2
=2MnO ↓+3SO 2-+2OH-。
2 4
11. A A项,甲中N的杂化类型是sp3杂化,所以不可能所有原子共平面。
12. A A项,金属晶体的熔点与金属性无关,与金属键的强弱有关;B项,H O沸点高于
2
H S的主要原因是H O分子间存在氢键,H S分子间不存在氢键;C项.金刚石硬度大于碳
2 2 2
化硅是因为C原子半径小于Si,C-C键键能更大,共价结构更稳定;D项.HClO和HBrO
结构相似,均为H-O-X(X代表卤原子)。因为Cl的电负性大于Br,导致O-H键极性更强,
更易解离H+,故HClO酸性强于HBrO。
3
{#{QQABDQQkxgqwkAbACJ5qQ00MCUoQsIIiLUoMAVAQuA4CyJNABKA=}#}13.D 向深蓝色
Cu(NH
3
)
4
(OH)
2
溶液中加入稀硫酸可得到蓝色
Cu(H
2
O)
4
SO
4
溶液,
因为与Cu2+与氨形成配位键的能力小于H+与氨形成配位键的能力。
14.D A项,K (H AsO )=10-9.2,数量级为10-10。B项,pH=12时,
a1 3 3
c(H AsO -)>c(HAsO 2-)>c(AsO 3-)。C项,血液pH在7.35﹣7.45之间时,As元素主要存在
2 3 3 3
c
( H+)
⋅c
( AsO3−)
形式为H AsO 。D项,该条件下,HAsO2−的电离平衡常数K = 3 ,当
3 3 3 a3 c ( HAsO2−)
3
c(HAsO2−)=c(AsO3−)时,pH介于12~14之间,设为10-a,此时K =c(H+)=1×10-a;AsO3−的
3 3 a3 3
K
水解平衡常数K = W =10-(14-a)>1×10-a,所以K <K 。
h1 a3 h1
K
a3
CaO CaO
15.C C 项根据图可知,生成 2的活化能更低,反应更快;且 2比CaO能量低,
稳定,故主要生成 CaO 2。O 2参与的主要反应的电极反应式: O 2 +2e−+Ca2+ =CaO 2。
16.(14分)
(1)5s2(1分) (2)C(2分)
(3) 将矿石粉碎或适当提高盐酸的浓度或适当升温(1分,答出一点即可,其它合理答案也给
分)
(4)Ca2+、Mg2+(2分,错写0分,漏写1分)
(5)SrSO (s)+Ba2+(aq) BaSO (s)+Sr2+(aq) (2分) 5×10−10(2分)
4 4
(6)A(2分)
(7)窝穴体a的空腔与Sr2+更匹配,可形成结构更稳定的超分子(2分,合理即可)
【试题解析】
(2)蟹壳中含有碳酸钙,由于锶元素与钙元素属于同一主族,较易取代钙元素的位置,因此
蟹壳中锶元素的含量往往较高,便于分析、测量,因此蟹壳是锶溯源技术的最佳样品。
(4)由分析可知,碳酸盐均能溶于盐酸,“浸出液”中主要的金属离子有Sr2+、Ca2+、Mg2+。
(5)由分析可知,“盐浸”中发生沉淀的转化,离子方程式:
;该反应的平衡常数
103.5,平衡常数很大,近似认为SrSO 完全转化,溶液中
4
K (BaSO )
剩余n(Ba2+)=2x10-3mol,则c ( SO
4
2−) = s
c
p
( Ba2+)
4 =15×10−9.0mol⋅L−1,理论上溶液中
c ( Sr2+) ⋅c ( SO2-) =10−1mol⋅L−1×5×10−9.0mol⋅L−1 =5×10−10 ( mol⋅L-1)2。
4
17.(13分)
(1)溴苯(1分) 醚键、羟基(2分,错写0分,漏写1分)
4
{#{QQABDQQkxgqwkAbACJ5qQ00MCUoQsIIiLUoMAVAQuA4CyJNABKA=}#}(2) (2分) (3)中和反应生成的HBr(2分)
(4)还原反应(1分) (5)NaOH的醇溶液(1分)
O
O
+ NaCN CH + NaBr
CH 3
3
HC
HC
CN
(6) Br (2分)
(7) (2分)
【试题解析】
Br
(2)由 变成 ,发生取代反应,加入反应的物质的化学式为
C H O ,则X的结构简式为
8 8 2
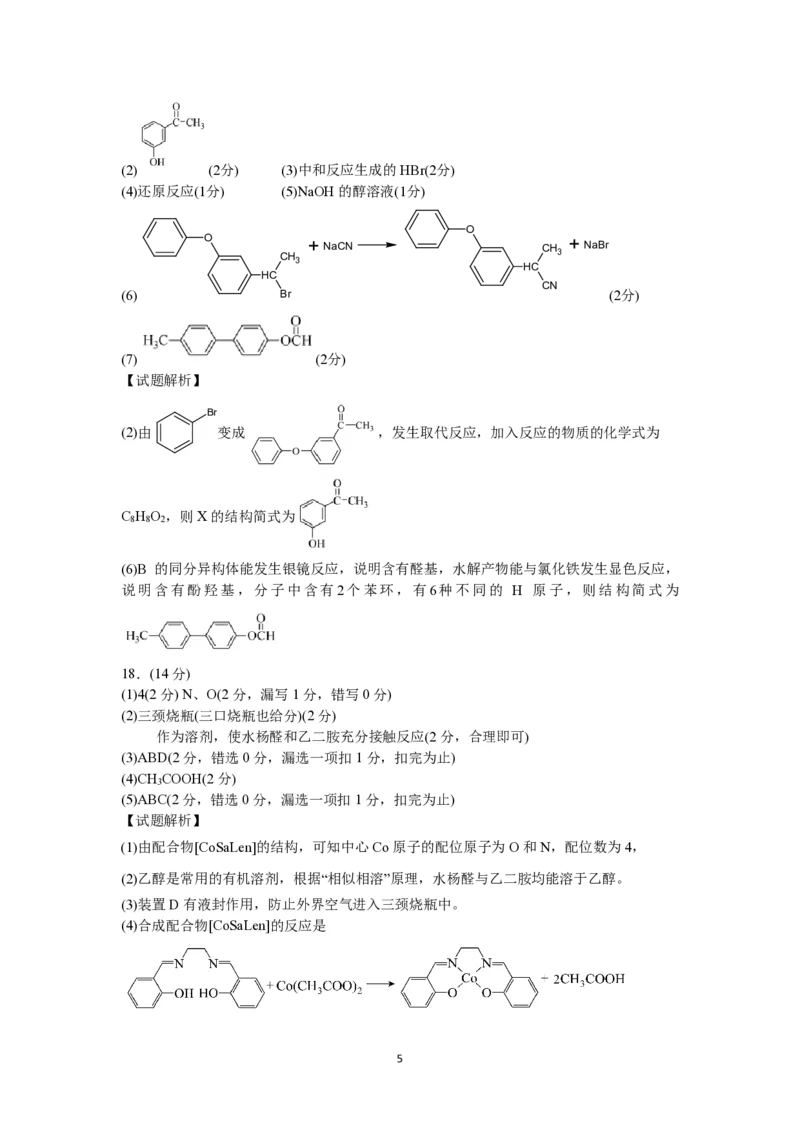
(6)B 的同分异构体能发生银镜反应,说明含有醛基,水解产物能与氯化铁发生显色反应,
说明含有酚羟基,分子中含有2个苯环,有6种不同的 H 原子,则结构简式为
18.(14分)
(1)4(2分) N、O(2分,漏写1分,错写0分)
(2)三颈烧瓶(三口烧瓶也给分)(2分)
作为溶剂,使水杨醛和乙二胺充分接触反应(2分,合理即可)
(3)ABD(2分,错选0分,漏选一项扣1分,扣完为止)
(4)CH COOH(2分)
3
(5)ABC(2分,错选0分,漏选一项扣1分,扣完为止)
【试题解析】
(1)由配合物[CoSaLen]的结构,可知中心Co原子的配位原子为O和N,配位数为4,
(2)乙醇是常用的有机溶剂,根据“相似相溶”原理,水杨醛与乙二胺均能溶于乙醇。
(3)装置D有液封作用,防止外界空气进入三颈烧瓶中。
(4)合成配合物[CoSaLen]的反应是
5
{#{QQABDQQkxgqwkAbACJ5qQ00MCUoQsIIiLUoMAVAQuA4CyJNABKA=}#}(5)进行化学实验需要佩戴护目镜保护眼睛;化学实验结束后,离开实验室前需用肥皂等
清洗双手;该实验涉及加热操作,需要防止热烫,要选择合适的工具进行操作,避免直
接触碰;该实验中未涉及锐器的操作,故D不符合题意,
19.(14分)
(1)①B(2分) ② CH 3 O(CO)O − +CH 3 I→CO(OCH 3 ) 2 +I−(2分)
(2)①ds(2分)
②吸附的 H*浓度越高,催化剂上形成的氧空位越多,反应速率越快(2分)(答出“催化
剂上形成的氧空位越多”,给2分)
③该温度下,甲醇炭化,碳覆盖在催化剂表面(1分),使催化剂活性下降(1分)(共2分)
400(a−b)
(3)① %(2分) ② (2分)
a
【试题解析】
(3)n(CO ):n(H )=1:1,假设CO 和H 的物质的量各为1mol,主反应转化的CO 为x,
2 2 2 2 2
副反应转化的CO 为y,根据三段式有
2
CO (g) + H (g) CO(g) + H O(g)
2 2 2
起始mol 1 1 0 0 ,则平衡时CO 的物质的量为
2
变化mol y y y y
(1−x−y),H 的物质的量为(1−x−y),HCOOH的物质的量为x,CO的物质的量等于H
O
2 2
的物质的量等于y,CO与HCOOH的浓度相等,物质的量也相等,即x=y,则平衡时气体
a 2 2a−2b
的物质的量为1−x−y+1−x−y+x+y+y=2−x,则 = ,x= ,CO 的转
2
b 2−x a
4a−4b
化率为 a 400(a−b)
×100%= %
1 a
4a−4b 2a−2b
1−
p(CO )= p(H )= a ×p= 4b−3a kPa,p(HCOOH)= a ×p= 2a−2b kPa,
2 2 2b 2 2b 2
a a
2a−2b
反应Ⅰ的平衡常数计算式K = 2 =
4a−4b
kPa−1;
p 4b−3a 4b−3a (4b−3a)2
×
2 2
6
{#{QQABDQQkxgqwkAbACJ5qQ00MCUoQsIIiLUoMAVAQuA4CyJNABKA=}#}