文档内容
2024 学年第二学期高三第二次模拟考试
化学
考生注意:
1.本试卷满分100分,考试时间60分钟。
2.本考试设试卷和答题纸两部分,试卷包括试题与答题要求,所有答案必须涂(选择题)或写
(非选择题)在答题纸上,做在试卷上一律不得分。
3.答题前,考生务必在答题纸上用水笔清楚填写姓名、准考证号。
4.本试题的选择题,没有特别注明,为单选题,只有一个正确选项;若注明双选,有两个正
确选项;若注明不定项,有1~2个正确选项,多选、错选不得分,漏选得一半分。
相对原子质量:H-1 C-12 O-16 Li-7 Fe-56 Se-79
一、人体内不可缺少的微量元素——硒(本题共20分)
1. 硒(Se)是人体内不可缺少 的微量元素,硒及其化合物在医药、催化、材料等领域有广泛应用,回答下列
问题。
(1)Se在周期表中的位置___________。
(2)O、S、Se气态氢化物的键角由大到小的顺序为___________(填化学式)。
(3)已知SeO 与SO 的部分性质如下表:
2 2
物 状态(常
熔 点
质 温)
SeO 固体 340-350℃
2
SO 气体 -755℃
2
根据X射线衍射分析,SeO 晶体具有如图所示的长链状结构,请解释SeO 与SO 熔点差异较大的可能原
2 2 2
因___________。
(4)“依布硒”是一种有机硒化物,具有良好的抗炎活性,其结构简式如图所示。“依布硒”中Se原子
的杂化类型为___________,元素Se、O、N的第一电离能由大到小的顺序为___________。
第1页/共19页
学科网(北京)股份有限公司【答案】(1)第4周期ⅥA族
(2)HO>HS>HSe
2 2 2
(3)SeO 与SO 都属于分子晶体,SeO 的链状结构分子量远大于SO ,范德华力大得多
2 2 2 2
(4) ①. sp3杂化 ②. N>O>Se
【解析】
【小问1详解】
Se的原子序数为34,在元素周期表中的位置是第四周期ⅥA族;
【小问2详解】
O、S、Se气态氢化物分别为HO、HS、HSe,分子中O、S、Se都发生sp3杂化,中心原子最外层都存在
2 2 2
2对孤对电子,电负性O>S>Se,电负性越大,成键电子对越靠近中心原子,斥力越大、键角越大,所以
HO、HS、HSe键角由大到小的顺序为 ;
2 2 2
【小问3详解】
SeO 与SO 均为分子晶体,相对分子质量链状SeO 比SO 大的多,分子间作用力SeO 更大,所以SeO 与
2 2 2 2 2 2
SO 熔点差异较大;
2
【小问4详解】
Se的原子序数为34,在元素周期表中的位置是第四周期ⅥA族,“依布硒”中Se原子形成2个σ键,孤电
子对数为2,价层电子对数为4,其杂化类型为sp3;O、N元素同周期,N为VA族元素,第一电离能大于
同周期相邻的两种元素,即第一电离能N>O,Se、O 元素同主族,同一主族从上至下第一电离能逐渐减
小,所以Se、O、N的第一电离能由大到小的顺序为N>O>Se。
2. 常温下,亚硒酸和碳酸的电离常数如表。
二元酸
HSeO
2 3
HCO
2 3
(1)常温下,比较等物质的量浓度的NaSeO 和NaCO 溶液的pH___________。
2 3 2 3
A. 前者大 B. 后者大 C. 无法比较 D. 一样大
第2页/共19页
学科网(北京)股份有限公司(2)常温下,等物质的量浓度的NaHSeO 和NaHCO 溶液中水的电离程度___________。
3 3
A. 前者大 B. 后者大 C. 无法比较 D. 一样大
(3)亚硒酸氢钠(NaHSeO )可用于制药工业、用作防腐剂、抗氧化剂等。NaHSeO 溶液中有关微粒浓度关
3 3
系正确的是___________。(不定项)
A.
B.
C.
D.
【答案】(1)B (2)B (3)BC
【解析】
【小问1详解】
由表中数据可知酸性: ,NaSeO 和NaCO 溶液中均会发生水解,根据越弱越水解,则
> 2 3 2 3
水解程度更大,则等物质的量浓度的NaSeO 和NaCO 溶液的pH后者大,故选B。
2 3 2 3
【小问2详解】
NaHSeO 中同时存在 的电离和水解, < ,电离
3
大于水解,以电离为主,则水的电离受到抑制;NaHCO 中同时存在 的电离和水解,
3
> ,电离小于水解,以水解为主,则水的电离受到促
进;故水的电离程度后者大,故选B。
【小问3详解】
A.NaHSeO 中的电荷守恒为: ,A错误;
3
B.NaHSeO 中同时存在 的电离和水解, < ,
3
第3页/共19页
学科网(北京)股份有限公司电离大于水解,故 ,B正确;
C.NaHSeO 中的Na和Se元素为1:1,物料守恒为 ,C正确;
3
D.由电荷守恒 和元素守恒式子
得: ,D错误;
故选BC。
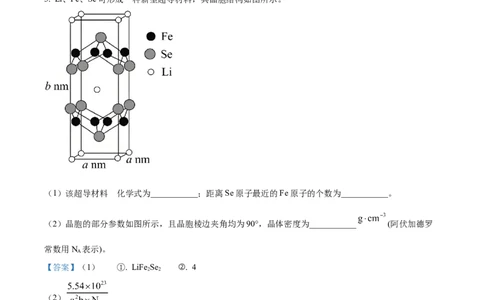
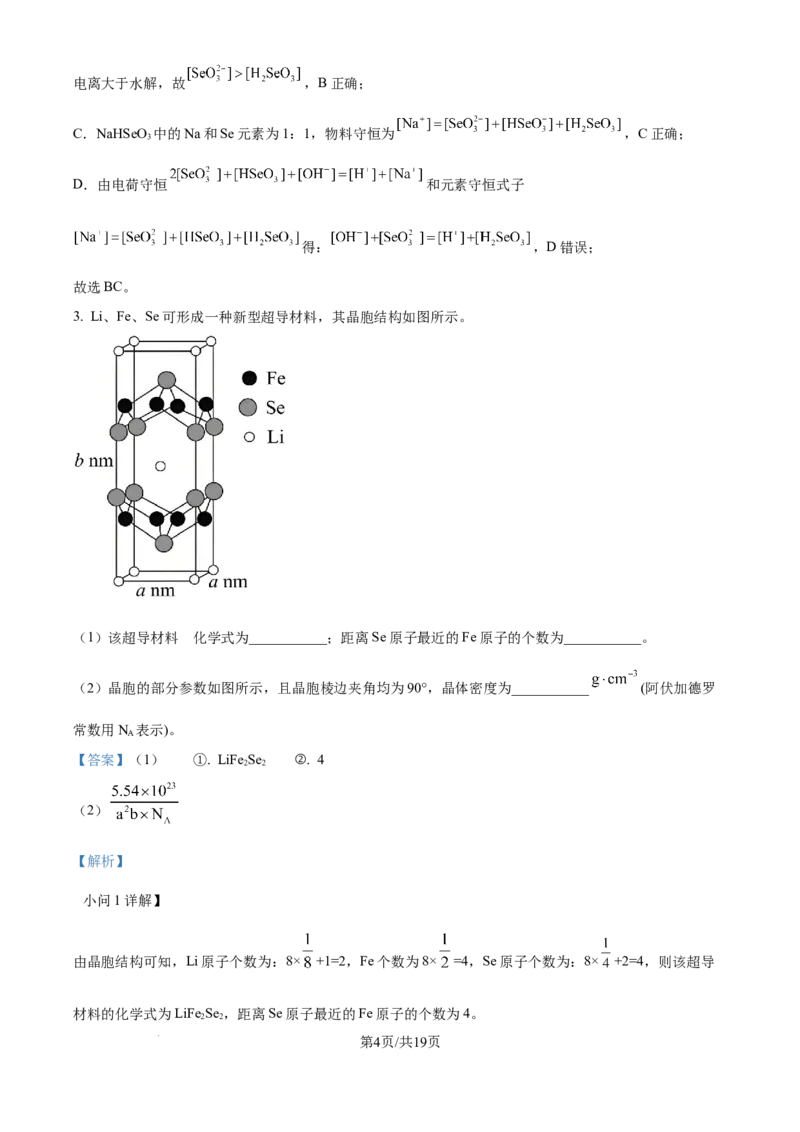
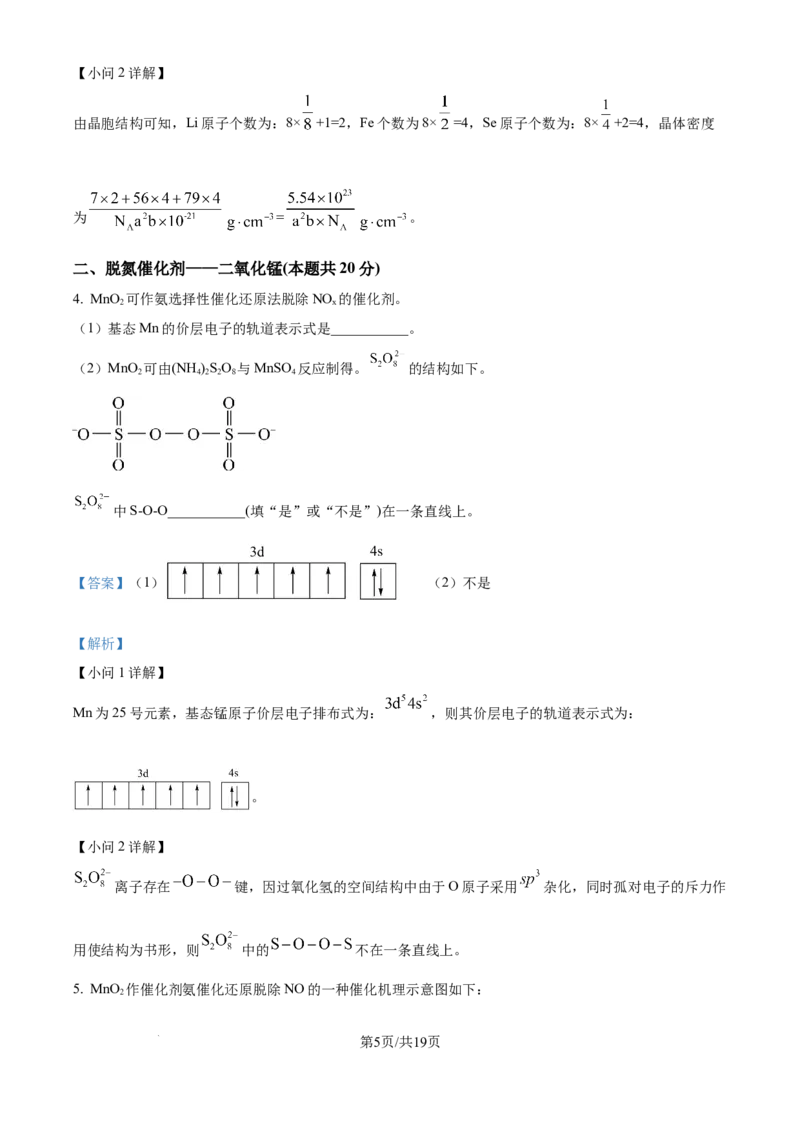
3. Li、Fe、Se可形成一种新型超导材料,其晶胞结构如图所示。
的
(1)该超导材料 化学式为___________;距离Se原子最近的Fe原子的个数为___________。
(2)晶胞的部分参数如图所示,且晶胞棱边夹角均为90°,晶体密度为___________ (阿伏加德罗
常数用N 表示)。
A
【答案】(1) ①. LiFe Se ②. 4
2 2
(2)
【解析】
【
小问1详解】
由晶胞结构可知,Li原子个数为:8× +1=2,Fe个数为8× =4,Se原子个数为:8× +2=4,则该超导
材料的化学式为LiFe Se ,距离Se原子最近的Fe原子的个数为4。
2 2
第4页/共19页
学科网(北京)股份有限公司【小问2详解】
由晶胞结构可知,Li原子个数为:8× +1=2,Fe个数为8× =4,Se原子个数为:8× +2=4,晶体密度
为 = 。
二、脱氮催化剂——二氧化锰(本题共20分)
4. MnO 可作氨选择性催化还原法脱除NO 的催化剂。
2 x
(1)基态Mn的价层电子的轨道表示式是___________。
(2)MnO 可由(NH )SO 与MnSO 反应制得。 的结构如下。
2 4 2 2 8 4
中S-O-O___________(填“是”或“不是”)在一条直线上。
【答案】(1) (2)不是
【解析】
【小问1详解】
Mn为25号元素,基态锰原子价层电子排布式为: ,则其价层电子的轨道表示式为:
。
【小问2详解】
离子存在 键,因过氧化氢的空间结构中由于O原子采用 杂化,同时孤对电子的斥力作
用使结构为书形,则 中的 不在一条直线上。
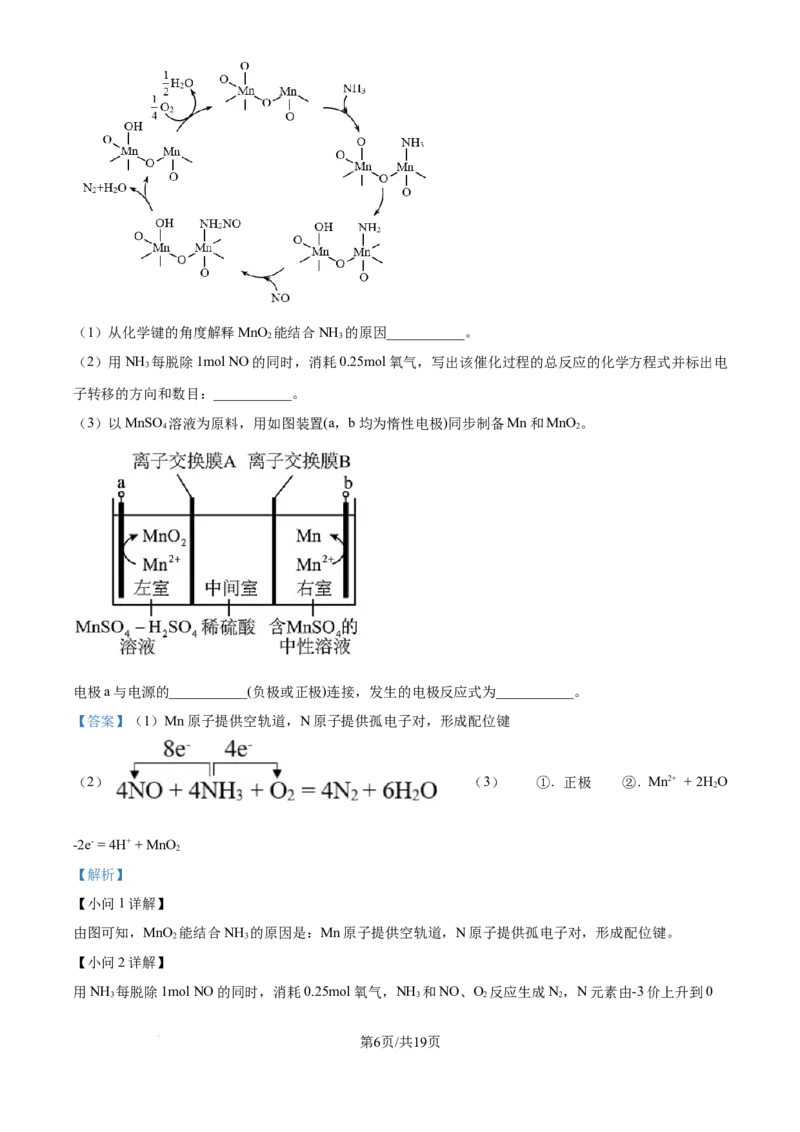
5. MnO 作催化剂氨催化还原脱除NO的一种催化机理示意图如下:
2
第5页/共19页
学科网(北京)股份有限公司(1)从化学键的角度解释MnO 能结合NH 的原因___________。
2 3
(2)用NH 每脱除1mol NO的同时,消耗0.25mol氧气,写出该催化过程的总反应的化学方程式并标出电
3
子转移的方向和数目:___________。
(3)以MnSO 溶液为原料,用如图装置(a,b均为惰性电极)同步制备Mn和MnO 。
4 2
电极a与电源的___________(负极或正极)连接,发生的电极反应式为___________。
【答案】(1)Mn原子提供空轨道,N原子提供孤电子对,形成配位键
(2) (3) ①. 正极 ②. Mn2+ + 2H O
2
-2e- = 4H++ MnO
2
【解析】
【小问1详解】
由图可知,MnO 能结合NH 的原因是:Mn原子提供空轨道,N原子提供孤电子对,形成配位键。
2 3
【小问2详解】
用NH 每脱除1mol NO的同时,消耗0.25mol氧气,NH 和NO、O 反应生成N,N元素由-3价上升到0
3 3 2 2
第6页/共19页
学科网(北京)股份有限公司价,N元素由+2价下降到0价,O元素由0价下降到-2价,根据得失电子守恒和原子守恒配平化学方程式
并标出电子转移的方向和数目: 。
【小问3详解】
由图可知,Mn2+在b电极得到电子生成Mn,b电极为阴极,Mn2+在a电极失去电子生成MnO ,a电极为阳
2
极,电极a与电源的正极连接,发生的电极反应式为Mn2+ + 2H O -2e- = 4H++ MnO 。
2 2
6. 电解锰渣的主要成分是MnS。一种由电解锰渣制取高纯MnSO 的流程如下。
4
(1)MnS不溶于水,它与硫酸溶液发生复分解反应的离子方程式为___________。
(2)浸出过程中加入MnO 可减少有毒气体的生成,同时产生更多MnSO 。利用了MnO 的化学性质是
2 4 2
___________。结合离子方程式解释从浸出液中除去Fe3+的原理:___________。
【答案】(1)MnS + 2H+ = Mn2+ + H S↑
2
(2) ①. 氧化性 ②. Fe3+ + 3H O 3H++ Fe(OH) ,增大pH、升高温度,使平衡向右移动,Fe3+
2 3
转化为Fe(OH) 沉淀
3
【解析】
【分析】由电解锰渣(主要成分是 )为原料制取高纯 的工艺流程,首先用MnO 和硫酸浸取
2
电解锰渣,获得浸出液,浸出液中含杂质Fe3+和Ca2+,后调节溶液的pH为4,使得铁离子转化为Fe(OH)
3
沉淀,再将浓缩液进行萃取除去Ca2+,最后获得纯净的MnSO ,据此分析;
4
【小问1详解】
与 发生复分解反应的离子方程式为 ;
【小问2详解】
浸出过程中,会产生有毒气体HS,加入 可减少有毒气体的生成,同时产生更多 ,锰元素
2
由+4价转变为+2价,被还原,则 为氧化剂,利用了其氧化性;Fe3+ + 3H O 3H+ + Fe(OH) ,增
2 3
第7页/共19页
学科网(北京)股份有限公司大pH、升高温度,使平衡向右移动,Fe3+ 转化为Fe(OH) 沉淀。
3
三、二氧化碳的综合利用(本题共20分)
7. 为了缓解温室效应与能源供应之间的冲突,CO 的资源化利用已成为研究的热点。
2
Ⅰ.【资源化一:利用CO 制水煤气】
2
在容积为 L 的恒容密闭容器中进行反应,方程式为
。当投料比 时,CO 的平衡转化率 与温度 、初始压强 的关系
2
如图所示。
(1)在恒温恒容条件下,关于以上反应下列表述能说明反应已经达到化学平衡状态的是___________。(不
定项)
A. B. 气体的平均相对分子质量不再变化
C. 气体的密度不再变化 D. CH 和CO 的物质的量之比不再改变
4 2
(2)初始压强 ___________ (填“>”“<”或“=”,下同);当温度为 ℃、初始压强为 时,a点
时的 ___________ 。
的
(3)起始时向容器中加入 mol CH 和 mol CO,在温度为 ℃时反应,此时初始压强为 ,该反应
4 2
平衡常数 ___________,温度和体积不变的情况下,继续加入 mol CH 和 mol CO,再次达到平衡后,
4 2
CO 的转化率___________。(填“增大”“减小”或“不变”)
2
Ⅱ.【资源化二:利用CO 制天然气】
2
二氧化碳加氢制甲烷过程中主要发生反应:
第8页/共19页
学科网(北京)股份有限公司反应I:
反应II:
在密闭容器中,压强恒为 Pa、 时,CO 平衡转化率、在催化剂作用下
2
反应相同时间所测得的CO 实际转化率随温度的变化如图所示。
2
(4)结合【资源化一】中信息,反应I的 ___________ ,该反应在___________条件下能
自发进行。
A.高温 B.低温 C.任意温度
(5)CO 平衡转化率后升高的主要原因是___________。
2
(6)CO 制备甲烷过程中,CO 活化的可能途径有两种,如图所示。请从反应速率和反应方向两个角度分
2 2
析说明CO*是CO 活化的优势中间体的原因是___________。
2
【答案】(1)B (2) ①. < ②. >
(3) ①. 4 ②. 减小
(4) ①. -164.7 ②. B
(5)600℃左右以后升高温度,反应I平衡向左移动的程度小于反应II平衡向右移动的程度
(6)得到CO*中间体的反应活化能较低,反应速率较快,而且ΔH较小,反应容易自发进行
【解析】
第9页/共19页
学科网(北京)股份有限公司【小问1详解】
A.对于反应 ,根据化学反应速率之比等于化学计量数之比,平
衡时应满足 ,而该选项中 ,正逆反应速率不相等,反应未达
到平衡状态,A错误;
B.反应前后气体的总质量不变,但气体的物质的量在反应过程中发生变化(反应前气体计量数之和为
1+1=2,反应后气体计量数之和为2+2=4 )。根据 (M为平均相对分子质量,m为总质量,n为总
物质的量 ),当气体的平均相对分子质量不再变化时,说明气体的总物质的量不再改变,反应达到平衡
状态,B正确;
C.在恒容密闭容器中,气体的总质量不变,容器体积不变,根据 (ρ为密度,m为质量,V为体积
),气体密度始终不变,所以密度不再变化不能说明反应达到平衡状态,C错误;
D.起始时投料比 ,反应过程中CH 和CO 按照1:1的比例反应,其物质的量之比始终为
4 2
1:1 ,不能据此判断反应达到平衡状态,D错误;
故选B。
【小问2详解】
① 是体积增大的反应,T℃时,从下到上,二氧化碳平衡转化
3
率升高,平衡正向移动,即减小压强向体积增大的方向移动,因此压强 < ;②当温度为T℃、初始
3
压强为 时,从a点到平衡点,二氧化碳平衡转化率减小,说明平衡逆向移动,因此a点时的 > 。
【
小问3详解】
①起始时向容器中加入 mol CH 和 mol CO,在温度为 ℃、初始压强为 时反应,二氧化碳平衡转化
4 2
第10页/共19页
学科网(北京)股份有限公司率为50%,列出三段式得: ,该反应
的平衡常数 ;②温度和体积不变,继续加入1mol CH 和1mol CO ,相当于在原平衡
4 2
的基础上增大压强,压强增大使得反应向气体分子数减少的方向移动,导致平衡逆向移动,所以再次达到
平衡后,CO 的转化率减小。
2
【小问4详解】
①根据盖斯定律可知,反应I=反应II×2-资源化一中的反应,则反应I的
;②对于反应 Ⅰ,ΔH<0 ,反应后气体分子
1
数减少,ΔS<0 (混乱度减小 )。根据吉布斯自由能公式ΔG=ΔH−TΔS(T为温度 ),当ΔG<0时反应自
发进行。要使ΔG=ΔH−TΔS<0 ,因为ΔH<0 ,ΔS<0 ,则需低温(T较小 )时才能保证ΔG<0 ,所以反应
在低温条件下能自发进行,答案选 B。
【小问5详解】
因为反应I: 是放热反应,当温度
升高,平衡逆向移动,二氧化碳转化率降低;反应 II:
是吸热反应,当温度升高,平衡正向移动,导致二氧化碳转化率增大,当温度升
高到一定程度以后,此时反应以反应II为主,导致随着温度的升高,反应II的二氧化碳转化率增大幅度大
于反应I的减小幅度。答案为:600℃左右以后升高温度,反应I平衡向左移动的程度小于反应II平衡向右
移动的程度。
【小问6详解】
从图中可以看出,生成CO*中间体反应的活化能小,反应速率快;CO*中间体能量低,较稳定,利于生成
(或反应放热,利于中间体的生成),故CO*是CO 活化的优势中间体;故答案为:得到CO*中间体的反应
2
活化能较低,反应速率较快,而且ΔH较小,反应容易自发进行。
第11页/共19页
学科网(北京)股份有限公司四、新型有机物与液晶发展(本题共20分)
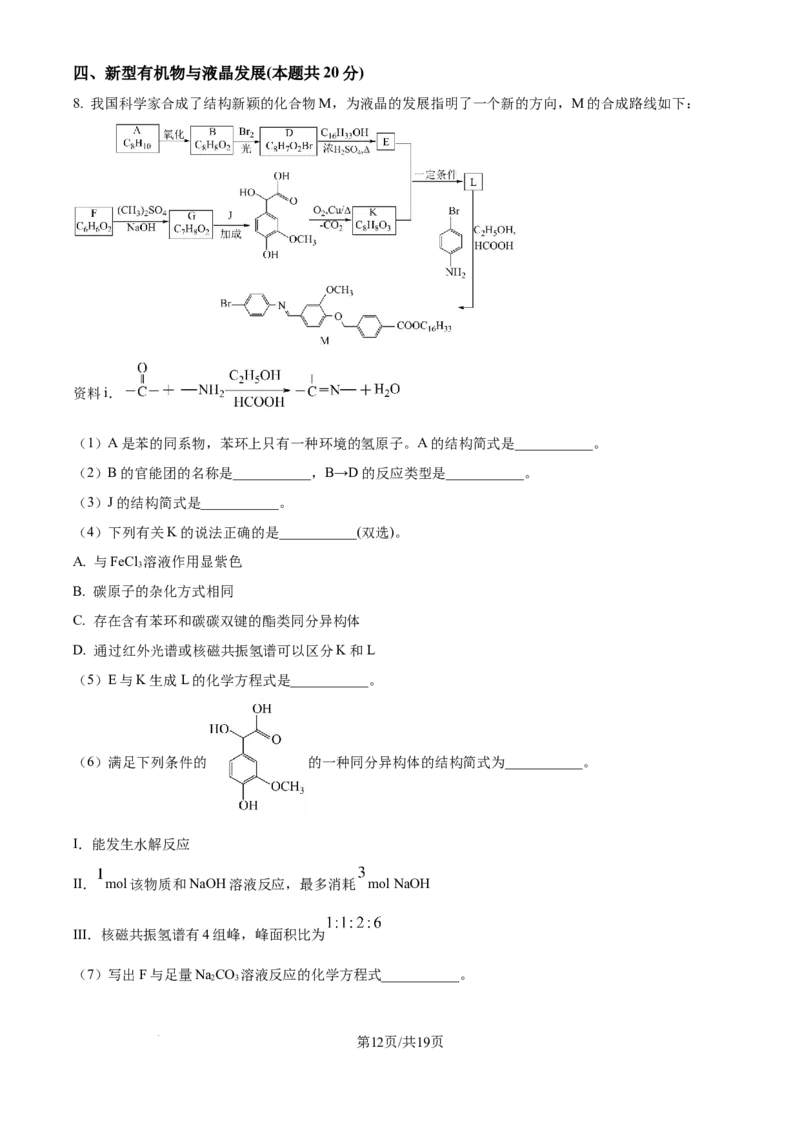
8. 我国科学家合成了结构新颖的化合物M,为液晶的发展指明了一个新的方向,M的合成路线如下:
资料i.
(1)A是苯的同系物,苯环上只有一种环境的氢原子。A的结构简式是___________。
(2)B的官能团的名称是___________,B→D的反应类型是___________。
(3)J的结构简式是___________。
(4)下列有关K的说法正确的是___________(双选)。
A. 与FeCl 溶液作用显紫色
3
B. 碳原子的杂化方式相同
C. 存在含有苯环和碳碳双键的酯类同分异构体
D. 通过红外光谱或核磁共振氢谱可以区分K和L
(5)E与K生成L的化学方程式是___________。
(6)满足下列条件的 的一种同分异构体的结构简式为___________。
I.能发生水解反应
II. mol该物质和NaOH溶液反应,最多消耗 mol NaOH
III.核磁共振氢谱有4组峰,峰面积比为
(7)写出F与足量NaCO 溶液反应的化学方程式___________。
2 3
第12页/共19页
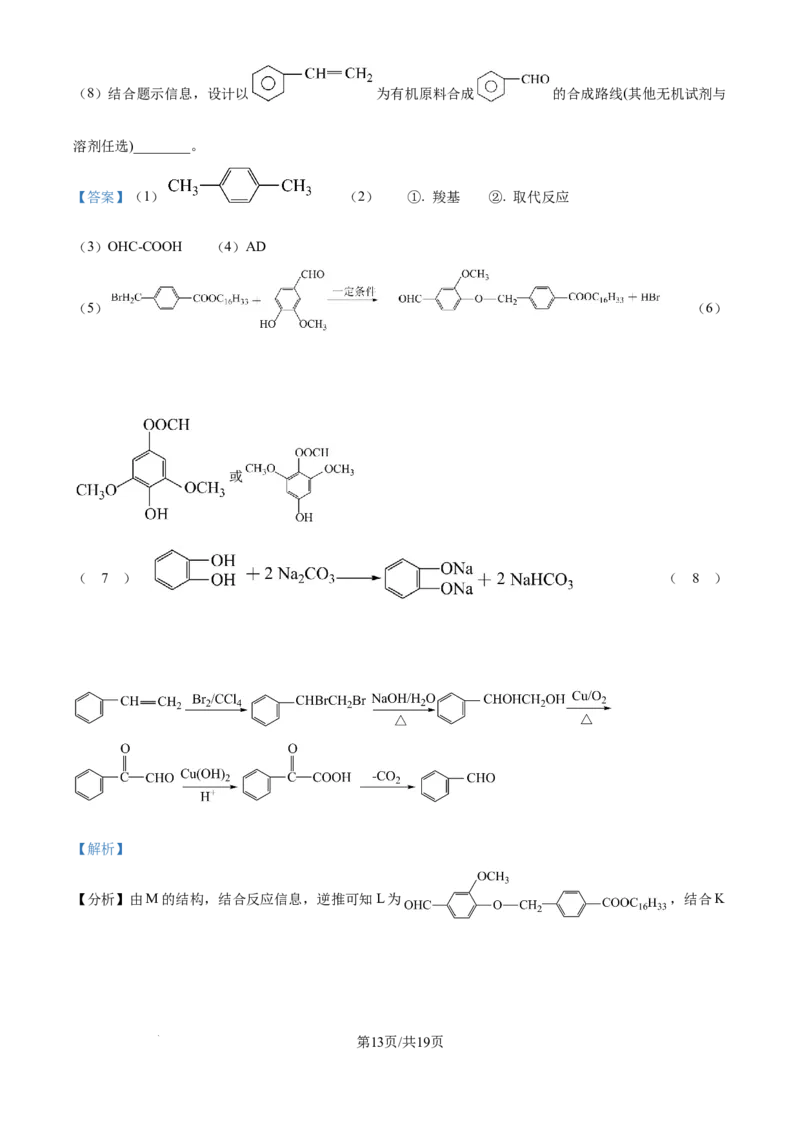
学科网(北京)股份有限公司(8)结合题示信息,设计以 为有机原料合成 的合成路线(其他无机试剂与
溶剂任选)________。
【答案】(1) (2) ①. 羧基 ②. 取代反应
(3)OHC-COOH (4)AD
(5) (6)
或
( 7 ) ( 8 )
【解析】
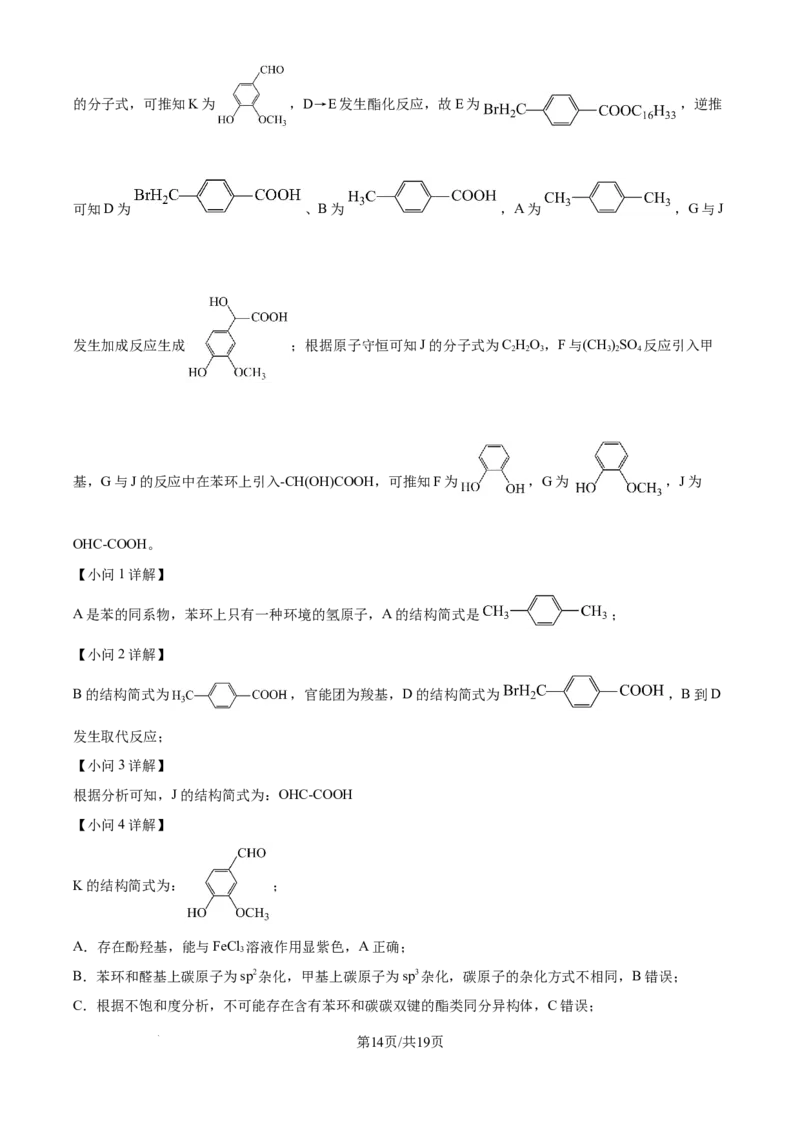
【分析】由M的结构,结合反应信息,逆推可知L为 ,结合K
第13页/共19页
学科网(北京)股份有限公司的分子式,可推知K为 ,D→E发生酯化反应,故E为 ,逆推
可知D为 、B为 ,A为 ,G与J
发生加成反应生成 ;根据原子守恒可知J的分子式为C HO,F与(CH)SO 反应引入甲
2 2 3 3 2 4
基,G与J的反应中在苯环上引入-CH(OH)COOH,可推知F为 ,G为 ,J为
OHC-COOH。
【小问1详解】
A是苯的同系物,苯环上只有一种环境的氢原子,A的结构简式是 ;
【小问2详解】
B的结构简式为 ,官能团为羧基,D的结构简式为 ,B到D
发生取代反应;
【小问3详解】
根据分析可知,J的结构简式为:OHC-COOH
【小问4详解】
K的结构简式为: ;
A.存在酚羟基,能与FeCl 溶液作用显紫色,A正确;
3
B.苯环和醛基上碳原子为sp2杂化,甲基上碳原子为sp3杂化,碳原子的杂化方式不相同,B错误;
C.根据不饱和度分析,不可能存在含有苯环和碳碳双键的酯类同分异构体,C错误;
第14页/共19页
学科网(北京)股份有限公司D.L的结构简式为: ,二者的官能团和化学键不同,可以通过红
外光谱或核磁共振氢谱可以区分K和L,D正确;
答案选AD;
【小问5详解】
E的结构简式为: ,K的结构简式为: ,L的结构简式为
,E与K发生取代反应得到L和HBr,反应的化学方程式为:
;
【小问6详解】
I.能发生水解反应,含有酯基;
II.1 mol该物质和NaOH溶液反应,最多消耗3mol NaOH;
III.核磁共振氢谱有4组峰,峰面积比为 ,有2个等效的甲基;
符合条件的结构简式有 、 ;
【小问7详解】
F的结构简式为 ,与足量NaCO 反应得到 和NaHCO ,方程式为:
2 3 3
;
第15页/共19页
学科网(北京)股份有限公司【小问8详解】
根据题目中信息,由 脱去CO 得到生成物K存在醛基,
2
与Br 发生加成反应得到 , 水解得到 ,
2
氧化得到 , 再氧化得到 ,
脱去CO 得到 ;合成路线为:
2
。
五、废旧锂离子电池制备碳酸锂(本题共20分)
9. 废旧锂离子电池的正极材料含钴酸锂(LiCoO ),锰酸锂(Li MnO ),镍酸锂(LiNiO )以及铝片、石墨粉等,
2 2 4 2
某小组设计方案回收金属元素,流程如下:
已知:过硫酸根离子的结构为:
(1)锂离子电池工作时,能量的主要转化方式为___________。
第16页/共19页
学科网(北京)股份有限公司(2)在废旧电池的初步处理及碱浸环节,为加快速率,除了对原料粉碎处理,还可以采用的措施有
___________(写出其中一种即可),步骤①发生反应的离子方程式为___________。
(3)滤液A中的Co、Ni、Mn均为+2价,则HO 作为反应物的半反应式为___________。
2 2
(4)写出过程③中 发生反应的离子方程式___________;步骤②中不能用盐酸酸化溶液的原因是
___________。
(5)常温下滤液C中 ___________mol/L。(常温: )
(6)所得碳酸锂样品含有少量NaSO 杂质,拟通过图示装置测定样品中LiCO 的含量,b中液体为硫酸
2 4 2 3
溶液,量气管中可以加入的试剂可以是___________。(不定项)
A. 饱和NaCO 溶液 B. 饱和NaHCO 溶液
2 3 3
C. 饱和食盐水 D. 覆盖油层的水
(7)下列情况会导致测定结果偏低的是___________。
A. 反应产生的气体一部分滞留在“Y”型试管中
B. 没有恢复到室温就进行读数
C. 水准管液面高于量气管
D. 固体样品称量后,在反应之前吸收空气中的水蒸气
【答案】(1)化学能转化为电能
(2) ①. 搅拌或者适当升高温度 (合理均可) ②. 2Al + 2OH-+ 6H O = 2[Al(OH) ]-+ 3H ↑
2 4 2
(3)HO-2e-= 2H+ + O
2 2 2
(4) ①. Mn2+ + S O + 2H O = 4H+ + MnO + 2SO ②. MnO 会在酸性条件下氧化Cl-生成Cl
2 2 2 2
(5)1.09×10-6 (6)BD (7)C
【解析】
【分析】正极材料含钴酸锂(LiCoO ),锰酸锂(Li MnO ),镍酸锂(LiNiO )以及铝片、石墨粉等,初步处理
2 2 4 2
后进行碱浸,Al反应生成四羟基合铝酸钠溶液,滤渣经过氧化氢酸性溶液溶解,HO 将LiCoO 、
2 2 2
LiMnO 、LiNiO 等物质中的Co、Mn、Ni还原为+2价,过滤分离出石墨,滤液在过程 中Mn2+被SO
2 4 2 2
③
第17页/共19页
学科网(北京)股份有限公司氧化为MnO ,过程 中加入NaOH调pH使Ni2+和Co2+变为氢氧化物沉淀,过滤后在滤液C中加入浓碳酸
2
钠生成碳酸锂。 ④
【小问1详解】
锂离子电池属于原电池,原电池工作时,是将化学能转化为电能,所以锂离子电池工作时,能量的主要转
化方式为化学能转化为电能;
【小问2详解】
在废旧电池的初步处理及碱浸环节,为加快速率,根据化学反应速率的影响因素,除了对原料粉碎处理增
大接触面积外,还可以采用搅拌、升高温度、适当增大碱的浓度等措施,步骤 是铝片与碱液反应,铝与
氢氧化钠溶液反应生成四羟基合铝酸钠和氢气,离子方程式为:2Al + 2OH-+ 6①H O = 2[Al(OH) ]-+ 3H ↑;
2 4 2
【小问3详解】
滤液A中的Co、Ni、Mn均为+2价,说明HO 将LiCoO 、LiMnO 、LiNiO 等物质中的Co、Mn、Ni还
2 2 2 2 4 2
原为+2价,所以HO 的主要作用是还原剂,HO 半反应式为HO-2e-= 2H+ + O ;
2 2 2 2 2 2 2
【小问4详解】
SO 中有过氧键,具有氧化性,过程 中Mn2+被SO 氧化为MnO ,离子方程式为Mn2+ + S O +
2 2 2 2
③
2HO = 4H+ + MnO + 2SO ,步骤 中不能用盐酸酸化溶液,因为溶液中的MnO 具有强氧化性,能与
2 2
②
盐酸中的Cl-发生氧化还原反应,Cl-被氧化为Cl,MnO 被还原,会导致后续反应受影响,所以原因是酸
2
性条件下MnO 会氧化Cl-生成Cl;
2
【小问5详解】
滤液C中形成Co(OH) 沉淀,K [Co(OH) ]=c(Co2+)×c2(OH-)=1.09×10-15,一般情况下溶液为碱性,假设
2 sp 2
c(OH-)=1.0×10-2mol/L(具体OH-浓度应根据题目中其他条件确定,此处假设为常见碱性环境浓度),则
c(Co2+)= = ==1.09×10-6mol/L;
【小问6详解】
测定样品中LiCO 的含量,利用硫酸与样品反应,测定CO 的体积,通过CO 的量计算LiCO 的含量;
2 3 2 2 2 3
A.CO 与饱和NaCO 溶液要反应,故不符合;
2 2 3
B.CO 在饱和NaHCO 溶液中溶解度很小,故符合;
2 3
C.CO 可以溶于饱和食盐水,故不符合;
2
第18页/共19页
学科网(北京)股份有限公司D.覆盖油层的水不会溶解CO,故符合;
2
答案选BD;
【小问7详解】
A.反应产生的气体一部分滞留在“Y”型试管中,但是会有等量的空气进入量气管,CO 的体积不会偏小,
2
结果不会偏低,故A不选;
B.没有恢复到室温就进行读数导致测得的CO 的体积偏大,结果偏高,故B不选;
2
C.水准管高于量气管,则CO 的压强大于大于大气压,使测得的体积偏低,结果偏低,故C选;
2
D.固体样品称量后,在反应之前吸收空气中的水蒸气,不影响生成的CO,结果无影响,故D不选;
2
答案选C。
第19页/共19页
学科网(北京)股份有限公司