文档内容
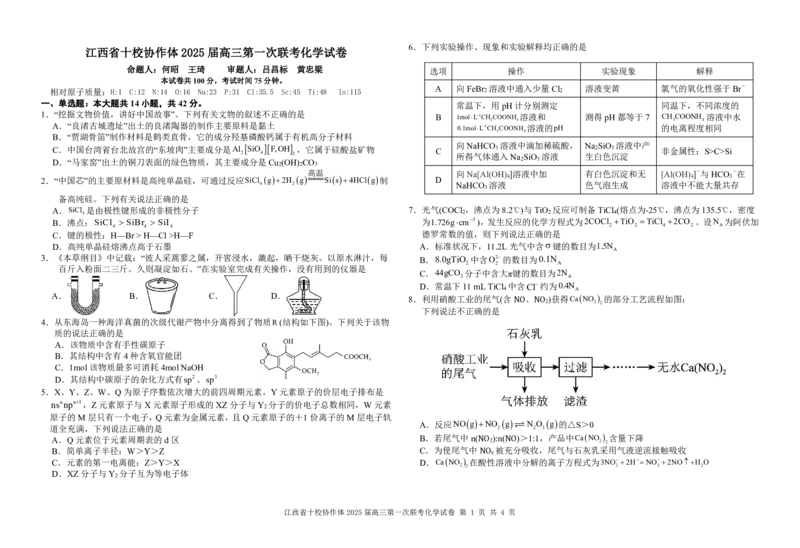
6.下列实验操作、现象和实验解释均正确的是
江西省十校协作体 2025 届高三第一次联考化学试卷
命题人:何昭 王琦 审题人:吕昌标 黄忠梁 选项 操作 实验现象 解释
本试卷共100分,考试时间75分钟。
相对原子质量:H:1 C:12 N:14 O:16 Na:23 P:31 Cl:35.5 Sc:45 Ti:48 In:115 A 向 FeBr 2 溶液中通入少量 Cl 2 溶液变黄 氯气的氧化性强于 Br-
一、单选题:本大题共 14小题,共 42分。
常温下,用pH计分别测定 同温下,不同浓度的
1.“挖掘文物价值,讲好中国故事”。下列有关文物的叙述不正确的是
B 1molL1CH COONH 溶液和 测得 pH都等于 7 CH COONH 溶液中水
3 4 3 4
A.“良渚古城遗址”出土的良渚陶器的制作主要原料是黏土
0.1molL1CH COONH 溶液的pH 的电离程度相同
3 4
B.“贾湖骨笛”制作材料是鹤类直骨,它的成分羟基磷酸钙属于有机高分子材料
C.中国台湾省台北故宫的“东坡肉”主要成分是Al 2 SiO 4 F,OH 2 ,它属于硅酸盐矿物 C 向 所得 Na 气 H 体 CO 通 3 入 溶液 Na 中 S 滴 iO 加 溶 稀 液 硫酸, 生 Na 白 2 S 色 iO 沉 3 溶 淀 液中产 非金属性:S>C>Si
D.“马家窑”出土的铜刀表面的绿色物质,其主要成分是Cu (OH) CO 2 3
2 2 3
高温 向Na[Al(OH) ]溶液中加 有白色沉淀和无 [Al(OH) ] -与HCO -在
2.“中国芯”的主要原材料是高纯单晶硅,可通过反应SiCl g2H g Sis4HClg制 D 4 4 3
4 2 NaHCO 溶液 色气泡生成 溶液中不能大量共存
3
备高纯硅。下列有关说法正确的是
A.SiCl 是由极性键形成的非极性分子 7.光气(COCl ,沸点为 8.2℃)与 TiO 反应可制备TiCl (熔点为-25℃,沸点为135.5℃,密度
4 2 2 4
B.沸点:SiCl SiBr SiI 为1.726gcm3),发生反应的化学方程式为2COCl TiO TiCl 2CO 。设N 为阿伏加
4 4 4 2 2 4 2 A
C.键的极性:H—Br >H—Cl>H—F 德罗常数的值,则下列说法正确的是
D.高纯单晶硅熔沸点高于石墨 A.标准状况下,11.2L 光气中含σ键的数目为1.5N
A
3.《本草纲目》中记载:“彼人采蒿蓼之属,开窖浸水,漉起,晒干烧灰。以原水淋汁,每 B.8.0gTiO 中含O2的数目为0.1N
2 2 A
百斤入粉面二三斤。久则凝淀如石。”在实验室完成有关操作,没有用到的仪器是
C.44gCO 分子中含大π键的数目为2N
2 A
D.常温下11mL TiCl 中含Cl约为0.4N
4 A
A. B. C. D.
8.利用硝酸工业的尾气(含 、 )获得CaNO 的部分工艺流程如图:
2 2 2
下列说法不正确的是
NO NO
4.从东海岛一种海洋真菌的次级代谢产物中分离得到了物质R(结构如下图)。下列关于该物
质的说法正确的是
A.该物质中含有手性碳原子
B.其结构中含有4种含氧官能团
C.1mol该物质最多可消耗4mol NaOH
D.其结构中碳原子的杂化方式有sp2、sp3
5.X、Y、Z、W、Q 为原子序数依次增大的前四周期元素,Y元素原子的价层电子排布是
nsnnpn+1,Z元素原子与 X元素原子形成的XZ 分子与 Y 分子的价电子总数相同,W元素
2
原子的M 层只有一个电子,Q元素为金属元素,且 Q元素原子的+1价离子的 M 层电子轨
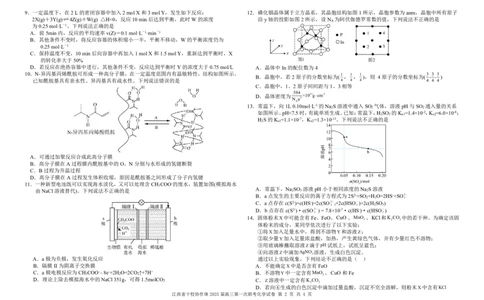
A.反应NO g NO g N O g 的△S>0
道全充满,下列说法正确的是 2 2 3
A.Q元素位于元素周期表的 d 区 B.若尾气中 n( 2 ):n( )>1:1,产品中CaNO 2 2 含量下降
B.简单离子半径:W>Y>Z C.为使尾气中
x
被充分吸收,尾气与石灰乳采用气液逆流接触吸收
NO NO
C.元素的第一电离能:Z>Y>X D.CaNO 在酸性溶液中分解的离子方程式为3NO2HNO2NOH O
2 2 NO 2 3 2
D.XZ分子与 Y 分子互为等电子体
2
江西省十校协作体2025届高三第一次联考化学试卷 第 1 页 共 4 页
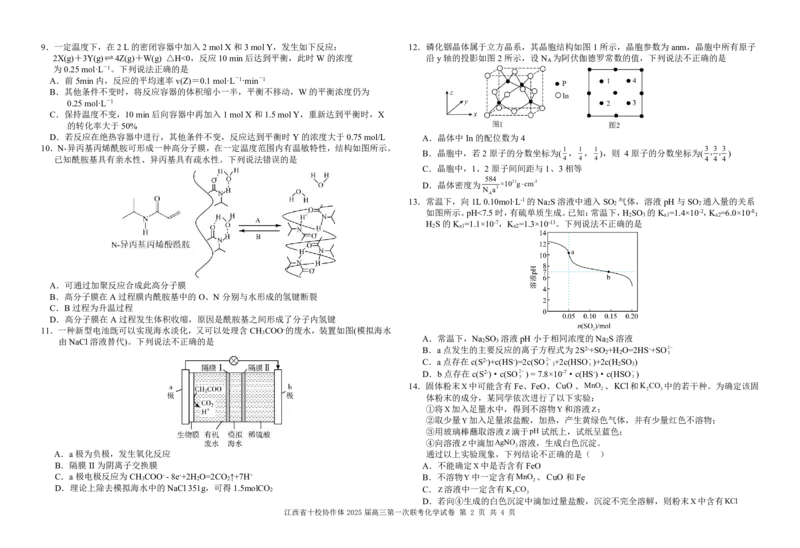
{#{QQABbYCAogigQBIAABgCEwHACAMQkhCACagGBAAIsAAAyQNABCA=}#}9.一定温度下,在2L的密闭容器中加入2mol X和3mol Y,发生如下反应: 12.磷化铟晶体属于立方晶系,其晶胞结构如图1所示,晶胞参数为anm,晶胞中所有原子
2X(g)+3Y(g)4Z(g)+W(g) △H<0,反应10min后达到平衡,此时W 的浓度 沿y轴的投影如图2所示,设N 为阿伏伽德罗常数的值,下列说法不正确的是
A
为0.25mol·L-1。下列说法正确的是
A.前5min内,反应的平均速率v(Z)=0.1mol·L-1·min-1
B.其他条件不变时,将反应容器的体积缩小一半,平衡不移动,W的平衡浓度仍为
0.25mol·L-1
C.保持温度不变,10min 后向容器中再加入1molX和1.5mol Y,重新达到平衡时,X
的转化率大于50%
D.若反应在绝热容器中进行,其他条件不变,反应达到平衡时Y的浓度大于0.75mol/L A.晶体中In 的配位数为4
10.N-异丙基丙烯酰胺可形成一种高分子膜,在一定温度范围内有温敏特性,结构如图所示。 1 1 1 3 3 3
B.晶胞中,若2原子的分数坐标为( , , ),则 4原子的分数坐标为( ,, )
已知酰胺基具有亲水性、异丙基具有疏水性。下列说法错误的是 4 4 4 4 4 4
C.晶胞中,1、2原子间间距与1、3相等
584
D.晶体密度为 ×1021gcm-3
N a3
A
13.常温下,向1L 0.10mol·L-1的Na S 溶液中通入SO 气体,溶液pH与SO 通入量的关系
2 2 2
如图所示。pH<7.5 时,有硫单质生成。已知:常温下,H SO 的K =1.4×10-2,K =6.0×10-8;
2 3 a1 a2
H S 的K =1.1×10-7,K =1.3×10-13。下列说法不正确的是
2 a1 a2
A.可通过加聚反应合成此高分子膜
B.高分子膜在 A过程膜内酰胺基中的O、N 分别与水形成的氢键断裂
C.B 过程为升温过程
D.高分子膜在A过程发生体积收缩,原因是酰胺基之间形成了分子内氢键
11.一种新型电池既可以实现海水淡化,又可以处理含CH COO-的废水,装置如图(模拟海水
3
由NaCl 溶液替代)。下列说法不正确的是 A.常温下,Na 2 SO 3 溶液pH小于相同浓度的Na 2 S溶液
B.a点发生的主要反应的离子方程式为2S2-+SO +H O=2HS-+SO2
2 2 3
C.a点存在c(S2-)+c(HS-)=2c(SO2 +2c(HSO)+2c(H SO )
3 ) 3 2 3
D.b点存在c(S2-)·c(SO2) =7.8×10-7·c(HS-)·c(HSO)
3 3
14.固体粉末X中可能含有Fe、FeO、CuO、MnO 、KCl和K CO 中的若干种。为确定该固
2 2 3
体粉末的成分,某同学依次进行了以下实验:
①将X加入足量水中,得到不溶物Y和溶液Z;
②取少量Y加入足量浓盐酸,加热,产生黄绿色气体,并有少量红色不溶物;
③用玻璃棒蘸取溶液Z滴于pH试纸上,试纸呈蓝色;
④向溶液Z中滴加AgNO 溶液,生成白色沉淀。
3
A.a极为负极,发生氧化反应 通过以上实验现象,下列结论不正确的是( )
B.隔膜II 为阴离子交换膜 A.不能确定X中是否含有FeO
C.a 极电极反应为CH
3
COO--8e-+2H
2
O=2CO
2
↑+7H+ B.不溶物Y中一定含有MnO
2
、CuO 和Fe
D.理论上除去模拟海水中的 NaCl 351g,可得1.5molCO 2 C.Z溶液中一定含有K CO
2 3
D.若向④生成的白色沉淀中滴加过量盐酸,沉淀不完全溶解,则粉末X中含有KCl
江西省十校协作体2025届高三第一次联考化学试卷 第 2 页 共 4 页
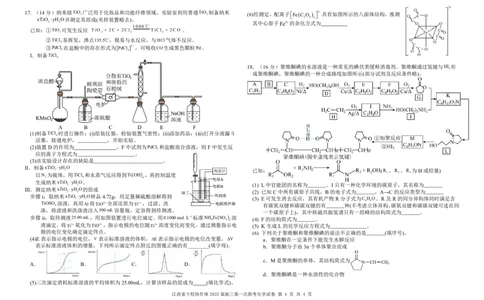
{#{QQABbYCAogigQBIAABgCEwHACAMQkhCACagGBAAIsAAAyQNABCA=}#}16.(14分)利用可见光催化还原CO ,将CO 转化为增值化学原料(HCOOH、HCHO、
二、简答题:本大题共 4 小题,共 58 分。 2 2
CH OH等), 被认为是一种可持续的CO 资源化有效途径。
3 2
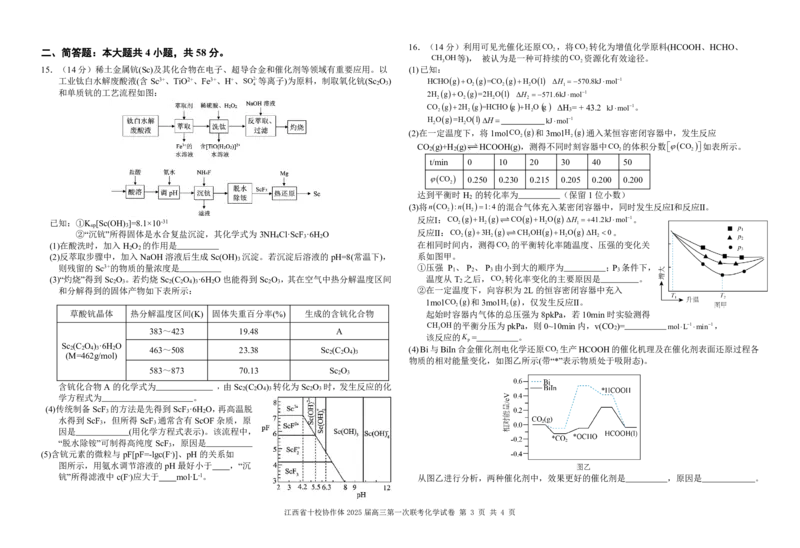
15.(14分)稀土金属钪(Sc)及其化合物在电子、超导合金和催化剂等领域有重要应用。以 (1)已知:
工业钛白水解废酸液(含Sc3+、TiO2+、Fe3+、H+、SO2-等离子)为原料,制取氧化钪(Sc O ) HCHOgO g=CO gH Ol ΔH 570.8kJmol1
4 2 3 2 2 2 1
和单质钪的工艺流程如图: 2H gO g=2H Ol ΔH 571.6kJmol1
2 2 2 2
CO
2
g2H
2
g=HCHO g H
2
O g ΔH
3
=+ 43.2 kJmol1。
H Og=H Ol H kJmol1
2 2
(2)在一定温度下,将1molCO g和3molH g通入某恒容密闭容器中,发生反应
2 2
CO 2 (g)+H 2 (g) HCOOH(g),测得不同时刻容器中CO 2 的体积分数 CO 2 如表所示。
t/min 0 10 20 30 40 50
CO
0.250 0.230 0.215 0.205 0.200 0.200
2
达到平衡时H 的转化率为 (保留1位小数)
2
(3)将nCO :nH 1:4的混合气体充入某密闭容器中,同时发生反应Ⅰ和反应Ⅱ。
2 2
已知:①K sp [Sc(OH) 3 ]=8.1×10-31 反应Ⅰ:CO 2 gH 2 g COgH 2 Og ΔH l 41.2kJmol1。
②“沉钪”所得固体是水合复盐沉淀,其化学式为3NH 4 Cl·ScF 3 ·6H 2 O 反应Ⅱ:CO 2 g3H 2 g CH 3 OHgH 2 Og H 2 0。
(1)在酸洗时,加入 H O 的作用是 在相同时间内,测得CO 的平衡转化率随温度、压强的变化关
2 2 2
(2)反萃取步骤中,加入 NaOH 溶液后生成Sc(OH) 沉淀。若沉淀后溶液的pH=8(常温下), 系如图甲。
3
则残留的Sc3+的物质的量浓度是 ①压强 P
1
、 P
2
、 P
3
由小到大的顺序为 ;P
3
条件下,
(3)“灼烧”得到Sc O 。若灼烧Sc (C O ) ·6H O也能得到Sc O ,其在空气中热分解温度区间 温度从T 之后,CO 转化率变化的主要原因是 。
2 3 2 2 4 3 2 2 3 2 2
和分解得到的固体产物如下表所示: ②在一定温度下,向容积为2L 的恒容密闭容器中充入
1molCO g和3molH g,仅发生反应Ⅱ。
2 2
草酸钪晶体 热分解温度区间(K) 固体失重百分率(%) 生成的含钪化合物 起始时容器内气体的总压强为8pkPa,若10min 时实验测得
383~423 19.48 A
CH
3
OH的平衡分压为pkPa,则0~10min内,v(CO
2
)= molL1min1,
该反应的K = 。
p
Sc 2 (C 2 O 4 ) 3 ·6H 2 O 463~508 23.38 Sc (C O ) (4)Bi与BiIn合金催化剂电化学还原CO 生产HCOOH的催化机理及在催化剂表面还原过程各
2 2 4 3 2
(M=462g/mol)
物质的相对能量变化,如图乙所示(带“*”表示物质处于吸附态)。
583~873 70.13 Sc O
2 3
含钪化合物A 的化学式为 ,由Sc (C O ) 转化为Sc O 时,发生反应的化
2 2 4 3 2 3
学方程式为 。
(4)传统制备ScF 的方法是先得到ScF ·6H O,再高温脱
3 3 2
水得到ScF ,但所得ScF 通常含有ScOF 杂质,原
3 3
因是 (用化学方程式表示)。该流程中,
“脱水除铵”可制得高纯度ScF ,原因是
3
(5)含钪元素的微粒与 pF[pF=-lgc(F-)]、pH 的关系如
图所示,用氨水调节溶液的 pH 最好小于 ,“沉
钪”所得滤液中c(F-)应大于 mol·L-1。 从图乙进行分析,两种催化剂中,效果更好的催化剂是 ,原因是 。
江西省十校协作体2025届高三第一次联考化学试卷 第 3 页 共 4 页
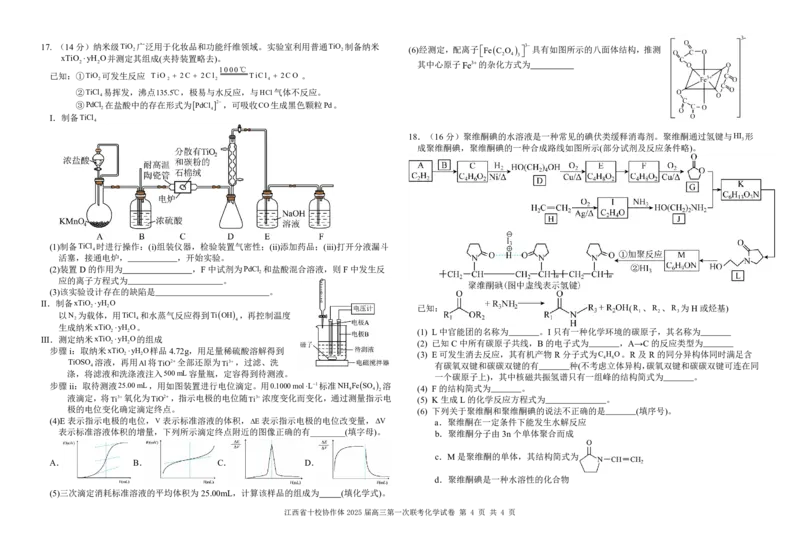
{#{QQABbYCAogigQBIAABgCEwHACAMQkhCACagGBAAIsAAAyQNABCA=}#}17. (14分)纳米级TiO 2 广泛用于化妆品和功能纤维领域。实验室利用普通TiO 2 制备纳米 (6)经测定,配离子Fe C O 3 具有如图所示的八面体结构,推测
xTiO yH O并测定其组成(夹持装置略去)。 2 4 3
2 2 其中心原子Fe3的杂化方式为
1000℃
已知:①TiO 可发生反应 TiO 2C 2Cl TiCl 2CO 。
2 2 2 4
②TiCl 易挥发,沸点135.5℃,极易与水反应,与HCl气体不反应。
4
③PdCl 在盐酸中的存在形式为PdCl 2,可吸收CO生成黑色颗粒Pd。
2 4
I.制备TiCl
4
18.(16分)聚维酮碘的水溶液是一种常见的碘伏类缓释消毒剂。聚维酮通过氢键与HI 形
3
成聚维酮碘,聚维酮碘的一种合成路线如图所示(部分试剂及反应条件略)。
(1)制备TiCl 时进行操作:(i)组装仪器,检验装置气密性;(ii)添加药品;(iii)打开分液漏斗
4
活塞,接通电炉, ,开始实验。
(2)装置D的作用为 ,F 中试剂为PdCl 和盐酸混合溶液,则F 中发生反
2
应的离子方程式为 。
(3)该实验设计存在的缺陷是 。
II.制备xTiO yH O
2 2 已知: (R 、R 、R 为 H 或烃基)
以N 为载体,用TiCl 和水蒸气反应得到TiOH ,再控制温度 1 2 3
2 4 4
生成纳米xTiO yH O。
2 2 (1) L中官能团的名称为 。I 只有一种化学环境的碳原子,其名称为
III.测定纳米xTiO yH O的组成
2 2 (2) 已知C 中所有碳原子共线,B 的电子式为 ,A→C 的反应类型为
步骤i:取纳米xTiO
2
yH
2
O样品4.72g,用足量稀硫酸溶解得到
(3) E可发生消去反应,其有机产物R 分子式为C H O。R 及 R 的同分异构体同时满足含
4 6
TiOSO
4
溶液,再用Al将 TiO2全部还原为 Ti3,过滤、洗
有碳氧双键和碳碳双键的有 种(不考虑立体异构,碳氧双键和碳碳双键可连在同
涤,将滤液和洗涤液注入500mL容量瓶,定容得到待测液。
一个碳原子上),其中核磁共振氢谱只有一组峰的结构简式为 。
步骤ii:取待测液25.00mL,用如图装置进行电位滴定。用0.1000molL1标准NH
4
FeSO
4
2
溶
(4) F 的结构简式为 。
液滴定,将 Ti3氧化为 TiO2,指示电极的电位随 Ti3浓度变化而变化,通过测量指示电 (5) K 生成 L的化学反应方程式为 。
极的电位变化确定滴定终点。 (6) 下列关于聚维酮和聚维酮碘的说法不正确的是 (填序号)。
(4)E 表示指示电极的电位,V表示标准溶液的体积,E表示指示电极的电位改变量,V a.聚维酮在一定条件下能发生水解反应
表示标准溶液体积的增量,下列所示滴定终点附近的图像正确的有________(填字母)。 b.聚维酮分子由3n个单体聚合而成
c.M 是聚维酮的单体,其结构简式为
A. B. C. D.
d.聚维酮碘是一种水溶性的化合物
(5)三次滴定消耗标准溶液的平均体积为 25.00mL,计算该样品的组成为 (填化学式)。
江西省十校协作体2025届高三第一次联考化学试卷 第 4 页 共 4 页
{#{QQABbYCAogigQBIAABgCEwHACAMQkhCACagGBAAIsAAAyQNABCA=}#}