文档内容
浙江强基联盟!"!#年$月高三联考
化学试题参考答案
!#$!%&’()
*
是含氧酸盐#$正确$+%,%-均不正确&
.#,!中子数为!/的氧原子#则质量数为!/012!1#则中子数为!/的氧原子为!1
1
)#+错误$ 的主链
上有3个碳原子#甲基和乙基分别位于.%*号碳原子上#名称为.4甲基4*4乙基戊烷#,正确$,% 中,原子价
*
*5*6!
层电子对个数为*0 2*#且不含孤电子对#则其价层电子对互斥!789:;"模型为 #$错误$铬
.
为第."号元素#价层电子排布式为*<3"=!#基态$>原子的价层电子轨道表示式为 " " " " " " #-
*< "=
错误&
*#-!因为铁粉能与)
.
反应#所以可用作食品保存的脱氧剂#+正确$四氧化三铁具有磁性#可作为*-打印的
磁性材料#,正确$%&$? 与$@反应生成%&$? 和$@$?#主要利用其氧化性#$正确$聚合硫酸铁能水解并形
* . .
成胶体#具有吸附性#可用于净水#-错误&
"#,!同周期元素#核电荷数越大#原子核对外层电子吸引力越大#原子半径越小#故原子半径’+?#AB#+不正
确$同主族元素#核电荷数越大#原子核对外层电子吸引力减小#故电负性’$$8(#,正确$同主族元素从上到
下#非金属性依次减弱#所以非金属性’)$8#$不正确$同主族元素#非金属性越强#氢化物越稳定#热稳定
性’C$?$C,>#-不正确&
3#$!观察时应该垂直于光线方向进行观察#可以看到明亮的光路#+错误$应左手控制旋塞#右手应持续旋转
摇动锥形瓶#,错误$热水浴中的烧瓶颜色深#冷水浴中烧瓶颜色浅#说明温度升高平衡向生成A) 的方向
.
移动#$正确$实验没有排除乙醇的干扰#-错误&
D#+!CA)
*
只体现酸性#+错误$同一个氧化还原反应中#氧化剂的氧化性大于氧化产物的氧化性#反应!中
氧化剂是8&)
.
#氧化产物是E
.
#所以氧化性’8&) .$E
.
#,正确$8)
.
与8&)
.
的中心原子的价层电子对数均为
*#则中心原子均为=F.杂化#$正确$反应!中每生成!GH?E
.
转移.GH?电子#则每有/I1GH?E
.
生成#转移
电子!IDGH?#即转移电子数目为!ID! #-正确&
+
J#-!($%
*
是吸电子基团#($C
*
是推电子基团#三氟乙酸中羟基的极性大于乙酸中羟基的极性#三氟乙酸
酸性大于乙酸#+正确$邻羟苯甲酸在分子内形成了氢键#对羟苯甲酸在分子间形成了氢键#故前者沸点低于
后者#,正确$%&熔点高于AB是因其金属键更强#$正确$A的电子排布是半充满的#比较稳定#电离能高#与
非金属性无关#-不正确&
1#-!过氧化钠与水反应#过氧化钠不能拆#离子方程式为.AB
.
)
.
0.C
.
)%%%"AB00")C50) ."#+正确$
尿素溶于热水#相当于酰胺基水解#得到碳酸铵#离子方程式为$)!AC
.
"
.
0.C
.
)%%%.AC
"
00$).
*
5#,正
确$用饱和碳酸钠溶液处理水垢中的硫酸钙#实现硫酸钙转化为易溶于酸的碳酸钙#离子方程式为$B8)!="
"
0$).
*
5!BK"&’$B$)
*
!="08).
"
5!BK"#$正确$$?
.
少量#则8
.
).
*
5 有剩余#与C0还会继续发生反应’8
.
).
*
5
0.C0%%%8(08) ."0C
.
)#-错误&
L#$!由题干图示有机物M%N的结构简式可知#M含有碳碳双键和醚键#N含有碳碳双键和酮羰基#M%N存在
不同的官能团#+正确$由题干图示有机物M的结构简式可知#M分子中存在两个碳碳双键所在的平面#单键
可以任意旋转#M中所有碳原子可能共平面#同理N中所有碳原子也可能共平面#,正确$M和N官能团不
同#并不是互为镜像#不互为对映异构体#$错误$类比上述反应# 的异构化产物为 #-
正确&
!/#,!M的核外电子数等于其周期数#则M为C$NM
*
分子呈三角锥形#则N为A$O的核外电子数等于M%N
化学卷参考答案!第!!!!!页!共"页"
{#{QQABTQa1wwiwkAZACR76B0HsC0mQkIGQLYoGBQCWKAQLSRFAFAA=}#}
书书书核外电子数之和#则O为)$P与M同主族#则P为AB$Q是同周期中非金属性最强的元素#则Q为$?&M
为C#O为)#则其形成的!/电子微粒有C)%)C5%C)0#+不符合题意$O为)#Q为$?#可形成$?) #
. * .
$?) 具有强氧化性#可用于饮用水的消毒#,符合题意$O为)#P为AB#Q为$?#则 PO为AB)#PQ为
. . .
AB$?#两者均为离子晶体#$不符合题意$M为C#N为A#O为)#这三种元素可以形成AC )C)#其溶液
* .
显碱性#-不符合题意&
!!#$!由图可知#$C
"
!R"0.C
.
8!R"&’$8
.
!R"0"C
.
!R"!!""$/分两步完成’!.C
.
8!R"&’.C
.
!R"0
8
.
!R"!"" !$/$#8
.
!R"0$C
"
!R"&’$8
.
!R"0.C
.
!R"!"" .$/#且活化能第二步大于第一步#第二步
较难发生&从图.可知#!///S之后第二步反应才会发生#且温度越高#第二步反应速率增加得更快#平衡
正向移动反应物转化率越高&该反应的反应$为.C
.
8!R"&’.C
.
!R"08
.
!R"#反应%为8
.
!R"0$C
"
!R"
&’$8
.
!R"0.C
.
!R"#+错误$!///S之后第二步反应才会发生#L1/S时提高#!$C
"
"*#!C
.
8"的投料比#
C8的转化率不会提高#,错误$其他条件不变时#适量通入氮气相当于减压#可以提高C 的产率#$正确$
. .
在L3/&!!3/S范围内#其他条件不变时升高温度#活化能大的反应速率受温度影响更大#所以反应#的速
率随温度升高#增大更快#8 的体积分数先升高后降低#-错误&
.
!.#-!由图可知#该装置为电解池#与直流电源正极相连的E>)
$
4’(电极为电解池的阳极#水在阳极失去电子
发生氧化反应生成氧气和氢离子#电极反应式为.C
.
)5"&5%%%) ."0"C0#铜电极为阴极#酸性条件下
二氧化碳在阴极得到电子发生还原反应生成乙烯%乙醇等#电极反应式为.$)
.
0!.C00!.&5%%%$
.
C
"
0
"C
.
)%.$)
.
0!.C00!.&5%%%$
.
C
3
)C0*C
.
)#电解池工作时#氢离子通过质子交换膜由阳极室进入阴
极室&该装置是先将太阳能转化为电能#再转化成化学能#+错误$离子交换膜为质子交换膜#只允许氢离
子通过#T0不能通过#,错误$由分析可知#铜电极为阴极#酸性条件下二氧化碳在阴极得到电子发生还原
反应生成乙烯%乙醇等#电极反应式有.$)
.
0!.C00!.&5%%%$
.
C
"
0"C
.
)#$正确$T$?的加入可以提高
导电性能#但不会增加氢离子浓度!抑制副反应析氢的进行"#-正确&
)) ))
!*#,!C
.
)
.
的电子式为C) ))) ))) )C#结构式为C()()(C#+正确$C
.
)
.
含有极性共价键和非极性共
)) ))
价键#两个C犹如在半展开的书的两面上#是极性分子#,不正确$C) 与C)比较#沸点受分子极性%相
. . .
对分子质量%氢键等影响!C
.
)
.
沸点比C
.
)高#沸点受分子极性和相对分子质量影响为主"#沸点’C
.
)$
C)#$正确$C) 的氧原子中有孤电子对#C) 分子间存在氢键#-正确&
. . . . .
!"#-!化合物’和(分子式相同#结构不同#互为同分异构体#+正确$化合物’选择性比(高#说明)的稳定
性弱于*#,正确$消去反应的结构条件是有+5C#化合物’有两个相应+5C#所以 是’),的副产
,>
物#$正确$主要产物是** ** #-错误&
!3#-!%!AC
*
"越多#FAC
*
越小#++R!AC
*
"
.
,0越多#因此!. 代表的是!-++R!AC
*
"
.
,0.#+正确$溶液中根
据电荷守恒有%!C0"0%!+R0"0%++R!AC
*
"
.
,00%!AC
"
0"2%!)C5"0%!A)
*
5"#,正确$向体系中滴入
稀硝酸#AC
*
与 C0反应生成 AC
"
0#%!AC
*
"减小#+R00.AC
*
&’++R!AC
*
"
.
,0的平衡逆向移动#
!-++R!AC
*
"
.
,0.减小#$正确$B点#!!+R0"2!-++R!AC
*
"
.
,0.#FAC
*
2*I3#%!AC
*
"2!/5*I3#则+R0
0.AC *&’++R!AC
*
"
.
,0的平衡常数&2 %
%
!
-
+
+
R
+R
0
!
"
A
)%
C
.
*
!
"
A
. ,
C
0
*
.
" 2
%!++
%
R
!
!
+
A
R
C
0
*
"
" . ,0"
)%.!AC
*
"2!6
!!/5*#3".2!#/6!/5J#对于反应+R$?0.AC *&’++R!AC
*
"
.
,00$?5#&2
%-++R!A
%
C
.
*
!
"
A
.
C
,0.
"
)%!$?5"
*
2
%-++R!AC
*
"
.
,0.)%!$?5"
6
%!+R0"
2
%-++R!AC
*
"
.
,0.
6
%!+R0")%!$?5"
2
&
=F
!+R$?"
2
%.!AC
*
" %!+R0" %!+R0")%.!AC
*
" ! &U
!#D6!/5!/
2!#D6!/5*#-错误&
!#/6!/5J
!D#,!步骤B中#由溶液得到 AB$?)
.
固体#进行的操作为过滤%洗涤和干燥#+正确$吸收器中发生反应’
.$?)
.
0.AB)C0C
.
) .%%%.AB$?)
.
0)
.
0.C
.
)#离子方程式为.$?)
.
0.)C50C
.
) .%%%.$?)
.
50)
.
0.C)#,错误$固体比气体更便于贮存和运输#工业上可将$?) 制成AB$?) 固体#$正确$反应结束后#
. . .
发生器中仍有少量$?) #用空气可以将其排出#确保其在吸收器中被充分吸收#-正确&
.
化学卷参考答案!第!!!!.页!共"页"
{#{QQABTQa1wwiwkAZACR76B0HsC0mQkIGQLYoGBQCWKAQLSRFAFAA=}#}!J#$#!!"+,$!.分"
!."$@
*
+@!!分"!!.!.分"
!*"$!!分"
!""#!!分"!电负性’)大于8#$)!AC
.
"
.
中A原子上电子云密度降低#结合质子能力下降!!分"
%#!!"8).
"
5!!分"
!."温度升高浸出速率提高#温度太高一水合氨分解#氨气挥发!各!分#共.分"
!*"OV0+$@!AC
*
"
"
,.0%%%$@0+OV!AC
*
"
"
,.0!!分"或OV0+$@!AC
*
"
"
,.0%%%$@0OV.00"AC *"及
其他合理答案均可
!"":W!)C"!.分"
.
真空热解
!3":W+))$!$C)C"
.
$)),%%%%%:W0"$)"0.C
.
)"!.分"
/解析0!!"同一周期元素从左到右#电负性递增#电负性’$#A#)#+错误$$)的成键情况与A
.
相似#
+$@!AC
*
"
*
$),0含有-键和.键#,正确$$@变成$@0失去最外层上的电子#即"=轨道上的电子#$正确$
$原子含"种不同空间运动状态的电子#-错误&
!."根据均摊法可以得出化学式为$@+@#配位数之比等于化学式的反比#所以+@周围有!.个等距离
*
的$@&
!*"A原子上孤电子对与$@0配位后#对成键电子对排斥力减小&
!""电负性’)$8#$)!AC
.
"
.
中A原子上电子云密度降低#结合质子能力下降&
%#!!"8
.
).
1
5 中的8没有发生化合价变化#变化的是过氧键#所以8
.
).
1
5 转变为8).
"
5
!."温度升高浸出速率提高#温度太高一水合氨分解#氨气挥发&
!*"由题干可知滤液B中含+$@!AC
*
"
"
,.0#可能发生OV0+$@!AC
*
"
"
,.0%%%$@0+OV!AC
*
"
"
,.0&
!""碱性过强#:W元素有可能转化为:W!)C"&
.
真空热解
!3"由元素守恒及氧化还原反应原理可得化学方程式’:W+))$!$C)C"
.
$)),%%%%%:W0"$)"0
.C
.
)"&
!1#!!"!!D.!!分"
!.",$!.分"
!*"!#!!分"!X!!分"!’ !#’
.
#且X点反应物浓度更大#故X点反应速率更快!.分"
#/I/.GH?)Y5!)G(V5!!.分"!1/Z!.分"
催化剂
!"".AC
*
0A)0A) .%%%%.A
.
0*C
.
)!!分"
/解析0!!"由图!知放出热量为3*".5"!1/2!!D.[\&
!."因为反应!在体积为.Y的恒容密闭容器中进行#参与反应的物质均为气体#混合气体的密度保持不
变#不能说明反应达到平衡状态#+不正确$单位时间内每断裂"GH?$(C#同时断裂"GH?)(C#正%逆反
应速率相等#说明反应达到了平衡状态#,正确$%!A)"和%!A "的浓度比保持不变#说明反应达到平衡状
.
态#$正确$因为反应!是化学计量数保持不变的反应#容器内气体的平均相对分子质量不变#不能说明反
应达到了平衡状态#-不正确&
!*"!由图.中知#’
.
曲线先拐到平行线#说明’ .$’
!
$由图.知#W点$C
"
浓度小于X点#X点反应物浓度
更大#故X点反应速率更快$
!/I*35/I.3"GH?)Y5!
#由图.中知#’
!
温度下#(!C
.
)"2.(!$C
"
"2.6
!/G(V
2/I/.GH?)Y5!)G(V5!$
!/I3/5/I!/"GH?
$C 的平衡转化率为 6!//Z21/Z&
" /I3/GH?
催化剂
!""AC
*
也可脱除废气中的 A)和 A)
.
#生成两种无毒物质的总反应为.AC
*
0A)0A) .%%%%.A
.
0*C)&
.
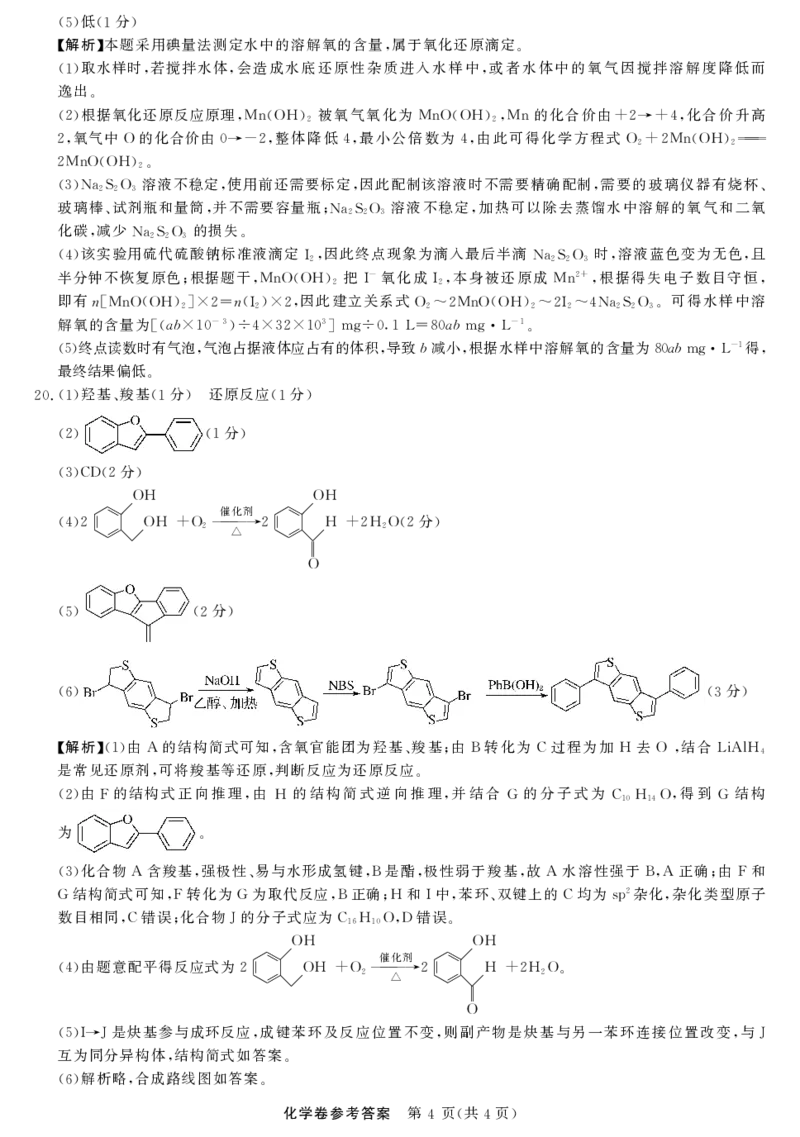
!L#!!"使溶解氧的测定值与水体中的实际值保持一致#避免产生误差!.分"
!.")
.
0.PV!)C" .%%%.PV)!)C"
.
!.分"
!*"量筒!!分"!氧气!.分"
!""滴入最后半滴AB
.
8
.
)
*
时#溶液蓝色变为无色#且半分钟不恢复原色!.分"!1/)*!.分"
化学卷参考答案!第!!!!*页!共"页"
{#{QQABTQa1wwiwkAZACR76B0HsC0mQkIGQLYoGBQCWKAQLSRFAFAA=}#}!3"低!!分"
/解析0本题采用碘量法测定水中的溶解氧的含量#属于氧化还原滴定&
!!"取水样时#若搅拌水体#会造成水底还原性杂质进入水样中#或者水体中的氧气因搅拌溶解度降低而
逸出&
!."根据氧化还原反应原理#PV!)C"
.
被氧气氧化为 PV)!)C"
.
#PV的化合价由0.)0"#化合价升高
.#氧气中)的化合价由/)5.#整体降低"#最小公倍数为"#由此可得化学方程式) . 0.PV!)C" .%%%
.PV)!)C"&
.
!*"AB8) 溶液不稳定#使用前还需要标定#因此配制该溶液时不需要精确配制#需要的玻璃仪器有烧杯%
. . *
玻璃棒%试剂瓶和量筒#并不需要容量瓶$AB8) 溶液不稳定#加热可以除去蒸馏水中溶解的氧气和二氧
. . *
化碳#减少AB8) 的损失&
. . *
!""该实验用硫代硫酸钠标准液滴定E#因此终点现象为滴入最后半滴AB8) 时#溶液蓝色变为无色#且
. . . *
半分钟不恢复原色$根据题干#PV)!)C"把E5氧化成E#本身被还原成 PV.0#根据得失电子数目守恒#
. .
即有#+PV)!)C"
.
,6.2#!E
.
"6.#因此建立关系式) .&.PV)!)C" .&.E .&"AB
.
8
.
)
*
&可得水样中溶
解氧的含量为+!)*6!/5*"]"6*.6!/*,GR]/I!Y21/)*GR)Y5!&
!3"终点读数时有气泡#气泡占据液体应占有的体积#导致*减小#根据水样中溶解氧的含量为1/)*GR)Y5!得#
最终结果偏低&
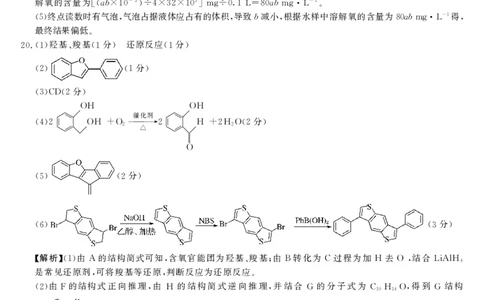
./#!!"羟基%羧基!!分"!还原反应!!分"
!." !!分"
!*"$-!.分"
)C )C
,, 催化剂 ,,
!"".++,,** )C 0) ....).++,,** C 0.C
.
)!.分"
-
//
)
!3" !.分"
!D" !*分"
/解析0!!"由+的结构简式可知#含氧官能团为羟基%羧基$由,转化为$过程为加C去)#结合Y(+?C
"
是常见还原剂#可将羧基等还原#判断反应为还原反应&
!."由%的结构式正向推理#由 C的结构简式逆向推理#并结合^的分子式为$ C )#得到^结构
!/ !"
为 &
!*"化合物+含羧基#强极性%易与水形成氢键#,是酯#极性弱于羧基#故+水溶性强于,#+正确$由%和
^结构简式可知#%转化为^为取代反应#,正确$C和E中#苯环%双键上的$均为=F.杂化#杂化类型原子
数目相同#$错误$化合物\的分子式应为$ C )#-错误&
!D !/
)C )C
,, 催化剂 ,,
!""由题意配平得反应式为.++,,** )C 0) ....).++,,** C 0.C
.
)&
-
//
)
!3"E)\是炔基参与成环反应#成键苯环及反应位置不变#则副产物是炔基与另一苯环连接位置改变#与\
互为同分异构体#结构简式如答案&
!D"解析略#合成路线图如答案&
化学卷参考答案!第!!!!"页!共"页"
{#{QQABTQa1wwiwkAZACR76B0HsC0mQkIGQLYoGBQCWKAQLSRFAFAA=}#}