文档内容
蚌埠市 2026届高三调研性监测
化 学
注意事项:
1答卷前,务必将自己的姓名和座位号填写在答题卡和试卷上。
2回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,务必擦净后再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试
卷上无效。
3考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H1 N14 O16 Na23 S32 Cu64
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合
题目要求。
1中华传统技艺,凸显人民智慧。下列选项所涉及材料的主要成分属于合金的是
A木斗拱 B泥活字 C不锈钢针 D纸哪吒
2七叶亭是一种植物抗菌素,适用于细菌性痢疾,其结构如图所示:
下列有关该物质分子说法正确的是
A存在4个C-Oσ键 B所有碳原子共平面
C存在2种官能团 D1mol该物质最多消耗3molNaOH
3下列实例与解释不相符的是
獉
选项 实例 解释
A 沸点:SbH >NH >PH NH 分子间形成氢键,但SbH 分子间作用力更强
3 3 3 3 3
B 用杯酚分离C 和C 杯酚与C 通过配位键形成超分子
60 70 60
C 熔点:SiO >CO Si-O键能大于CO 分子间作用力
2 2 2
D 酸性:邻羟基苯甲酸>苯甲酸 邻羟基苯甲酸易形成分子内氢键有利于羧基氢的电离
蚌埠市高三年级化学试卷第1页(共8页)
书书书依据下列材料,完成4~5小题:
从黑火药发明,到现代侯德榜的“联合制碱法”;从徐光宪提出稀土串级萃取理论,到闵
恩泽研制新型催化剂解决重油裂解难题;从钮经义团队首次人工全合成结晶牛胰岛素而提
名诺贝尔化学奖,到屠呦呦提取青蒿素而问鼎诺贝尔奖。中国化学家对世界科技的贡献从
未停止。
4下列有关说法不正确的是
獉
ASc属于稀土元素
B结晶牛胰岛素水解最终产物为氨基酸
C乙醚与青蒿素极性相似,可用乙醚萃取青蒿素
D利用烃的密度不同,通过分馏石油获得汽油、柴油
5下列有关描述及化学用语均正确的是
△
A黑火药爆炸:S+2KNO +3CKS+N↑+3CO↑
3 2 2 2
B向饱和食盐水中依次通入过量CO、NH:Na++NH +HO+CONaHCO↓+NH+
2 3 3 2 2 3 4
△
CNaHCO 固体热分解制纯碱:2HCO-CO2-+HO+CO↑
3 3 3 2 2
D十六烷裂解获得辛烷和辛烯:C H (十六烷)→CH (辛烷)+CH (辛烯)
16 34 8 18 8 16
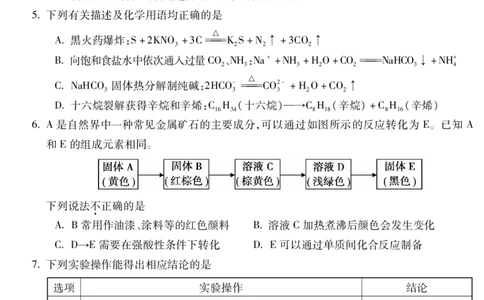
6A是自然界中一种常见金属矿石的主要成分,可以通过如图所示的反应转化为 E。已知 A
和E的组成元素相同。
下列说法不正确的是
獉
AB常用作油漆、涂料等的红色颜料 B溶液C加热煮沸后颜色会发生变化
CD→E需要在强酸性条件下转化 DE可以通过单质间化合反应制备
7下列实验操作能得出相应结论的是
选项 实验操作 结论
A 室温下,测定001mol·L-1某盐溶液的pH为7 该盐为强酸强碱盐
B 向ZnS的悬浊液中加入几滴稀CuSO溶液,产生黑色沉淀 K(CuS)<K(ZnS)
4 sp sp
C 在烧瓶中加入浓硝酸和红热的木炭,有红棕色气体产生 木炭能还原浓HNO
3
D 向某溶液中加入盐酸酸化的BaCl溶液,产生白色沉淀 该溶液一定含SO2-
2 4
8一种紫外双折射晶体材料,由五种原子序数依次增大的短周期元素 M、W、X、Y、Z组成。M
与X同周期,基态X原子p轨道半充满,基态Y和Z原子的原子核外均只有1个未成对电
子,且二者核电荷数之和为M的4倍。下列说法正确的是
AMY 为非极性分子 BZ和Y可形成分子晶体
3
C简单离子半径:X<Z DX 分子中X为sp杂化
2
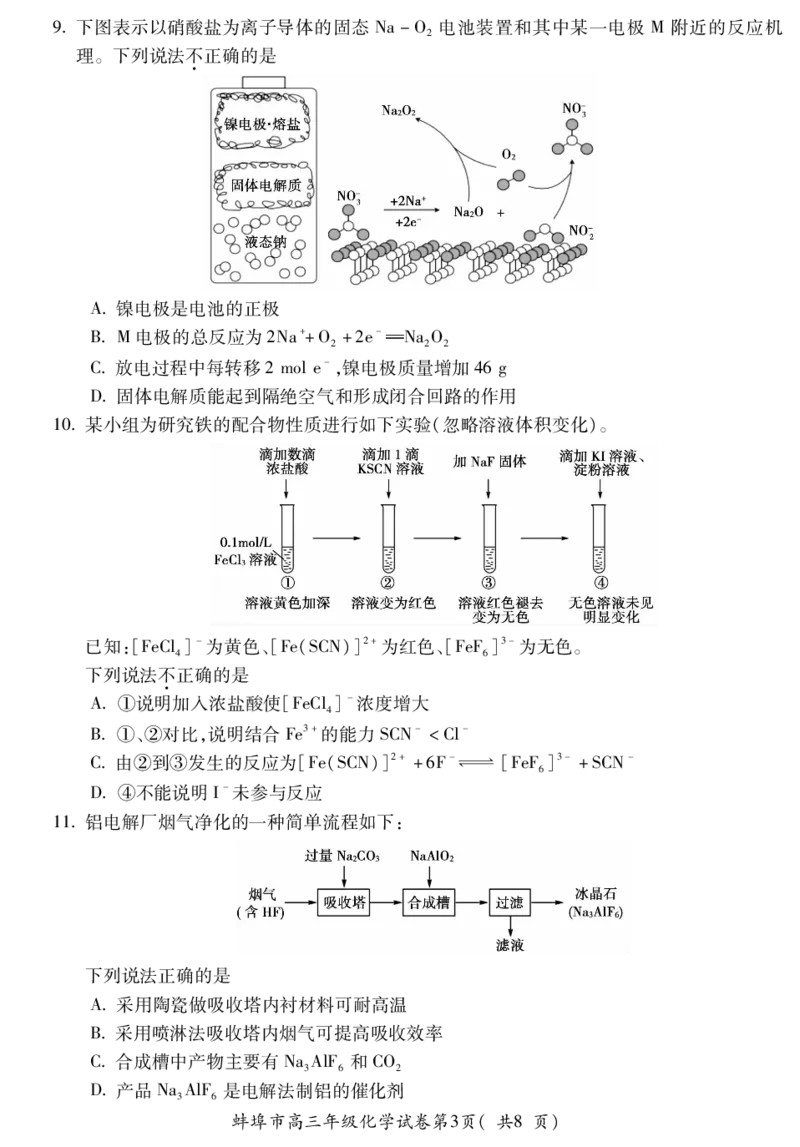
蚌埠市高三年级化学试卷第2页(共8页)9下图表示以硝酸盐为离子导体的固态 Na-O 电池装置和其中某一电极 M附近的反应机
2
理。下列说法不正确的是
獉
A镍电极是电池的正极
BM电极的总反应为2Na++O +2e-NaO
2 2 2
C放电过程中每转移2mole-,镍电极质量增加46g
D固体电解质能起到隔绝空气和形成闭合回路的作用
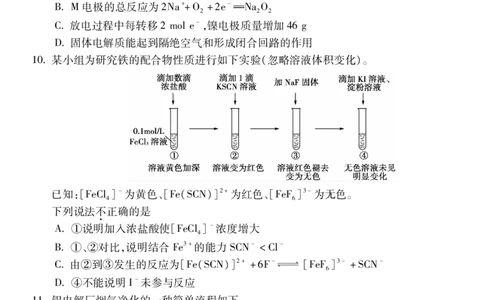
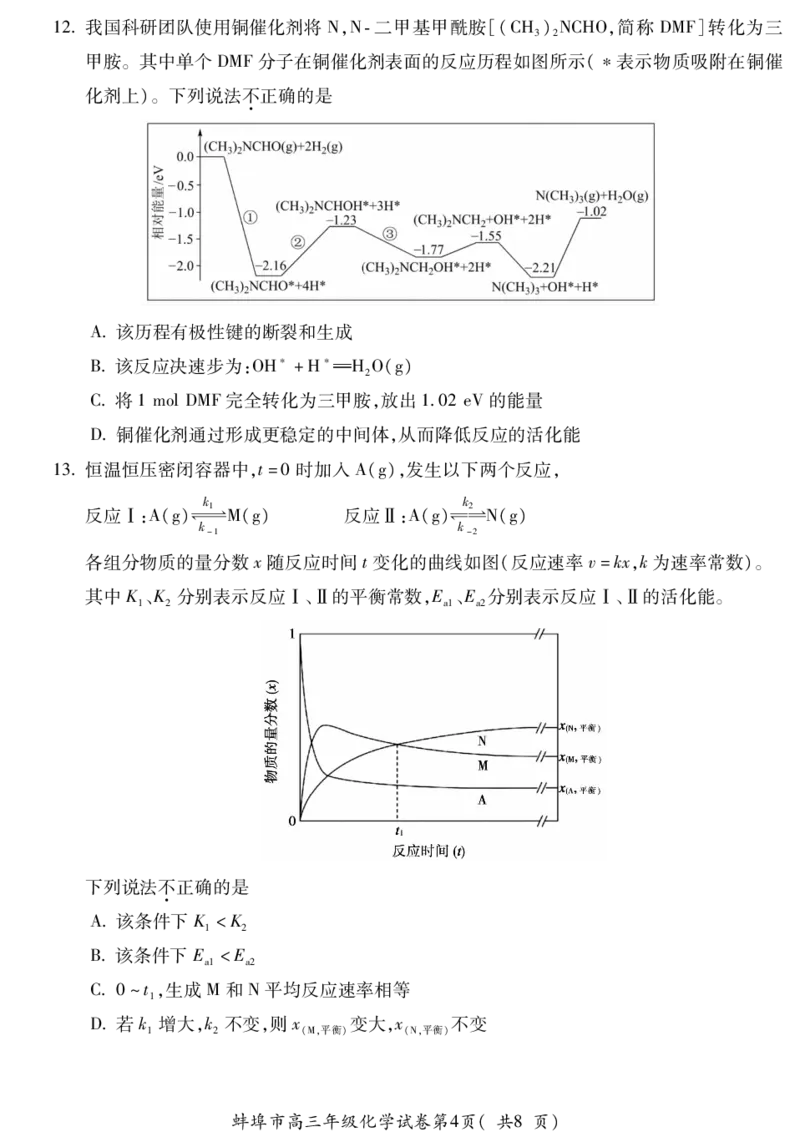
10某小组为研究铁的配合物性质进行如下实验(忽略溶液体积变化)。
已知:[FeCl]-为黄色、[Fe(SCN)]2+为红色、[FeF]3-为无色。
4 6
下列说法不正确的是
獉
A①说明加入浓盐酸使[FeCl]-浓度增大
4
B①、②对比,说明结合Fe3+的能力SCN-<Cl-
C由②到③发生的反应为[Fe(SCN)]2++6F-幑幐 [FeF]3-+SCN-
6
D④不能说明I-未参与反应
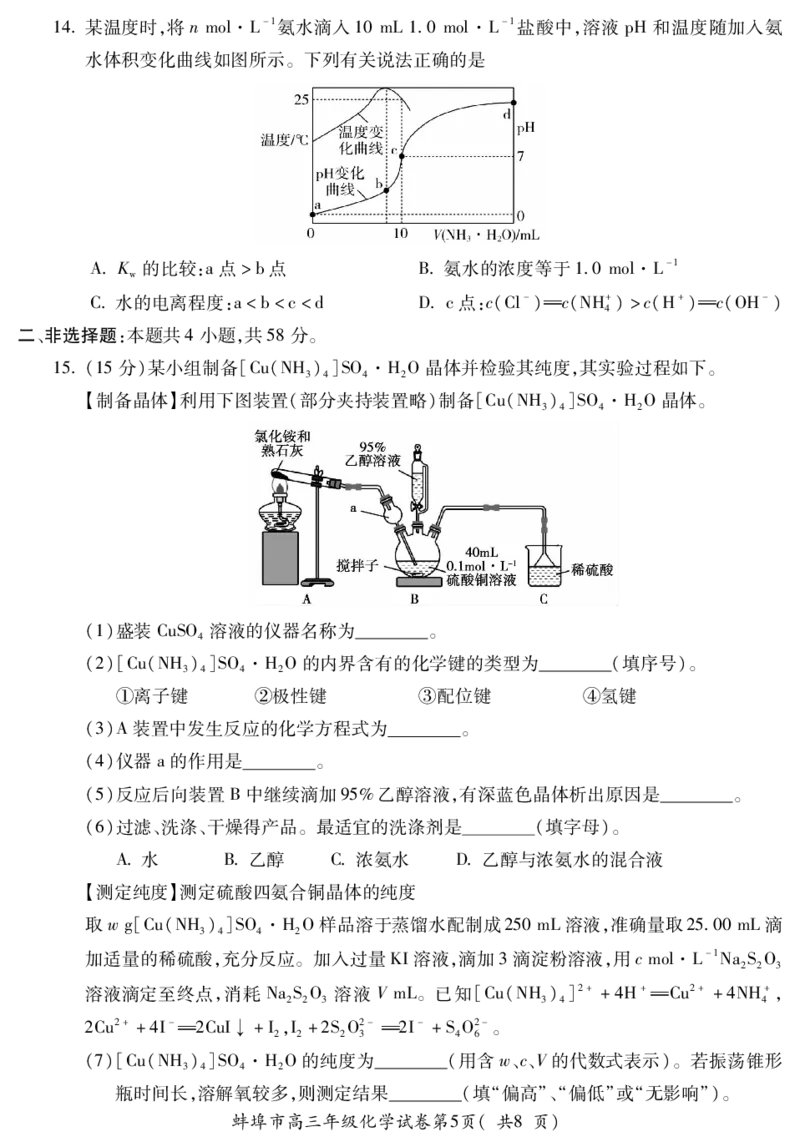
11铝电解厂烟气净化的一种简单流程如下:
下列说法正确的是
A采用陶瓷做吸收塔内衬材料可耐高温
B采用喷淋法吸收塔内烟气可提高吸收效率
C合成槽中产物主要有NaAlF和CO
3 6 2
D产品NaAlF是电解法制铝的催化剂
3 6
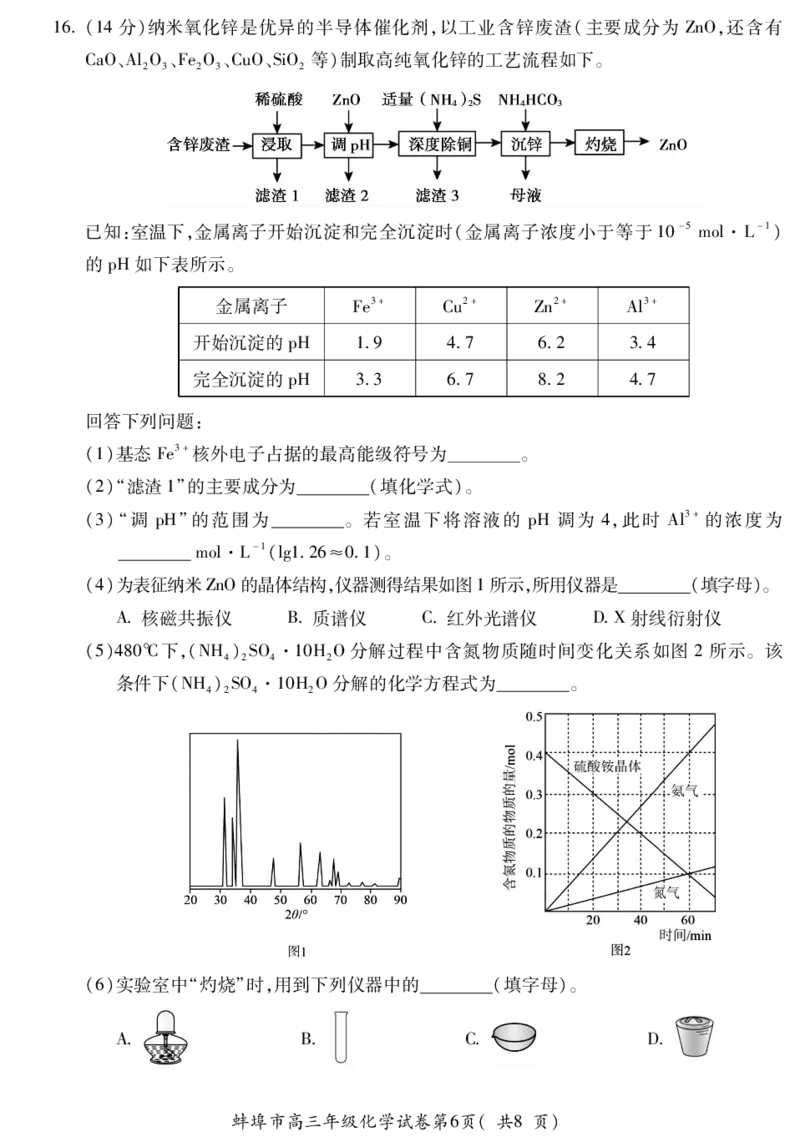
蚌埠市高三年级化学试卷第3页(共8页)12我国科研团队使用铜催化剂将 N,N﹣二甲基甲酰胺[(CH)NCHO,简称 DMF]转化为三
3 2
甲胺。其中单个DMF分子在铜催化剂表面的反应历程如图所示(表示物质吸附在铜催
化剂上)。下列说法不正确的是
獉
A该历程有极性键的断裂和生成
B该反应决速步为:OH +HHO(g)
2
C将1molDMF完全转化为三甲胺,放出102eV的能量
D铜催化剂通过形成更稳定的中间体,从而降低反应的活化能
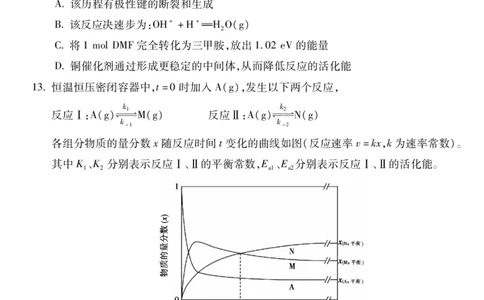
13恒温恒压密闭容器中,t=0时加入A(g),发生以下两个反应,
k k
1 2
反应Ⅰ:A(g)幑幐M(g) 反应Ⅱ:A(g)幑幐N(g)
k k
-1 -2
各组分物质的量分数x随反应时间t变化的曲线如图(反应速率v=kx,k为速率常数)。
其中K、K分别表示反应Ⅰ、Ⅱ的平衡常数,E 、E 分别表示反应Ⅰ、Ⅱ的活化能。
1 2 a1 a2
下列说法不正确的是
獉
A该条件下K<K
1 2
B该条件下E <E
a1 a2
C0~t,生成M和N平均反应速率相等
1
D若k增大,k不变,则x 变大,x 不变
1 2 (M,平衡) (N,平衡)
蚌埠市高三年级化学试卷第4页(共8页)14某温度时,将nmol·L-1氨水滴入10mL10mol·L-1盐酸中,溶液 pH和温度随加入氨
水体积变化曲线如图所示。下列有关说法正确的是
AK 的比较:a点>b点 B氨水的浓度等于10mol·L-1
w
C水的电离程度:a<b<c<d Dc点:c(Cl-)c(NH+)>c(H+)c(OH-)
4
二、非选择题:本题共4小题,共58分。
15(15分)某小组制备[Cu(NH)]SO·HO晶体并检验其纯度,其实验过程如下。
3 4 4 2
【制备晶体】利用下图装置(部分夹持装置略)制备[Cu(NH)]SO·HO晶体。
3 4 4 2
(1)盛装CuSO 溶液的仪器名称为 。
4
(2)[Cu(NH)]SO·HO的内界含有的化学键的类型为 (填序号)。
3 4 4 2
①离子键 ②极性键 ③配位键 ④氢键
(3)A装置中发生反应的化学方程式为 。
(4)仪器a的作用是 。
(5)反应后向装置B中继续滴加95%乙醇溶液,有深蓝色晶体析出原因是 。
(6)过滤、洗涤、干燥得产品。最适宜的洗涤剂是 (填字母)。
A水 B乙醇 C浓氨水 D乙醇与浓氨水的混合液
【测定纯度】测定硫酸四氨合铜晶体的纯度
取wg[Cu(NH)]SO·HO样品溶于蒸馏水配制成250mL溶液,准确量取2500mL滴
3 4 4 2
加适量的稀硫酸,充分反应。加入过量KI溶液,滴加3滴淀粉溶液,用cmol·L-1NaSO
2 2 3
溶液滴定至终点,消耗 NaSO 溶液 VmL。已知[Cu(NH)]2++4H+Cu2++4NH+,
2 2 3 3 4 4
2Cu2++4I-2CuI↓+I,I+2SO2-2I-+SO2-。
2 2 2 3 4 6
(7)[Cu(NH)]SO·HO的纯度为 (用含w、c、V的代数式表示)。若振荡锥形
3 4 4 2
瓶时间长,溶解氧较多,则测定结果 (填“偏高”、“偏低”或“无影响”)。
蚌埠市高三年级化学试卷第5页(共8页)16(14分)纳米氧化锌是优异的半导体催化剂,以工业含锌废渣(主要成分为 ZnO,还含有
CaO、AlO、FeO、CuO、SiO 等)制取高纯氧化锌的工艺流程如下。
2 3 2 3 2
已知:室温下,金属离子开始沉淀和完全沉淀时(金属离子浓度小于等于10-5mol·L-1)
的pH如下表所示。
金属离子 Fe3+ Cu2+ Zn2+ Al3+
开始沉淀的pH 19 47 62 34
完全沉淀的pH 33 67 82 47
回答下列问题:
(1)基态Fe3+核外电子占据的最高能级符号为 。
(2)“滤渣1”的主要成分为 (填化学式)。
(3)“调 pH”的范围为 。若室温下将溶液的 pH调为 4,此时 Al3+的浓度为
mol·L-1(lg126≈01)。
(4)为表征纳米ZnO的晶体结构,仪器测得结果如图1所示,所用仪器是 (填字母)。
A核磁共振仪 B质谱仪 C红外光谱仪 DX射线衍射仪
(5)480℃下,(NH)SO·10HO分解过程中含氮物质随时间变化关系如图2所示。该
4 2 4 2
条件下(NH)SO·10HO分解的化学方程式为 。
4 2 4 2
(6)实验室中“灼烧”时,用到下列仪器中的 (填字母)。
A B C D
蚌埠市高三年级化学试卷第6页(共8页)17(14分)通过捕捉空气中的 CO 和电解水产生的 H 可以合成“零碳甲醇”,实现碳中和。
2 2
回答下列问题:
(1)已知H 燃烧热为akJ·mol-1,甲醇的燃烧热为bkJ·mol-1。反应CO(g)+3H(g)
2 2 2
幑幐CHOH(l)+HO(l),ΔH= kJ·mol-1(用含a、b的代数式表示)。
3 2
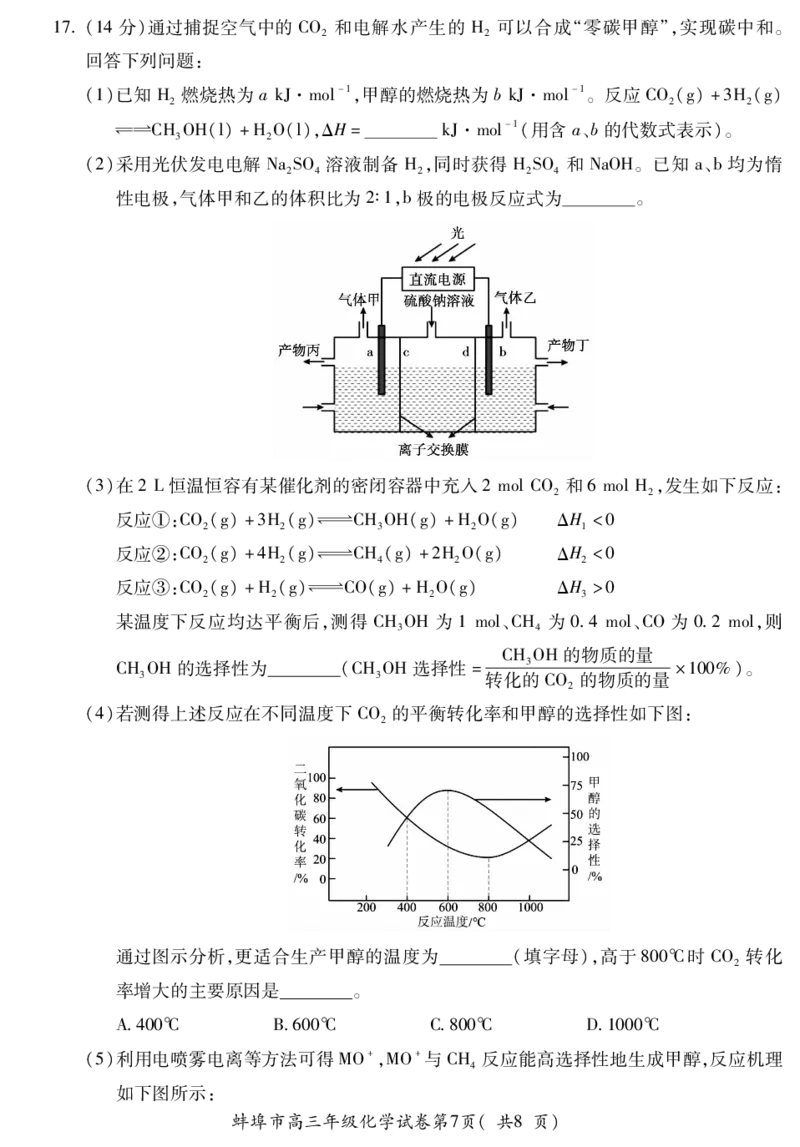
(2)采用光伏发电电解NaSO 溶液制备 H,同时获得 HSO 和 NaOH。已知 a、b均为惰
2 4 2 2 4
性电极,气体甲和乙的体积比为2∶1,b极的电极反应式为 。
(3)在2L恒温恒容有某催化剂的密闭容器中充入2molCO 和6molH,发生如下反应:
2 2
反应①:CO(g)+3H(g)幑幐CHOH(g)+HO(g) ΔH <0
2 2 3 2 1
反应②:CO(g)+4H(g)幑幐CH(g)+2HO(g) ΔH <0
2 2 4 2 2
反应③:CO(g)+H(g)幑幐CO(g)+HO(g) ΔH >0
2 2 2 3
某温度下反应均达平衡后,测得 CHOH为1mol、CH 为04mol、CO为02mol,则
3 4
CHOH的物质的量
CHOH的选择性为 (CHOH选择性= 3 ×100%)。
3 3 转化的CO 的物质的量
2
(4)若测得上述反应在不同温度下CO 的平衡转化率和甲醇的选择性如下图:
2
通过图示分析,更适合生产甲醇的温度为 (填字母),高于800℃时 CO 转化
2
率增大的主要原因是 。
A400℃ B600℃ C800℃ D1000℃
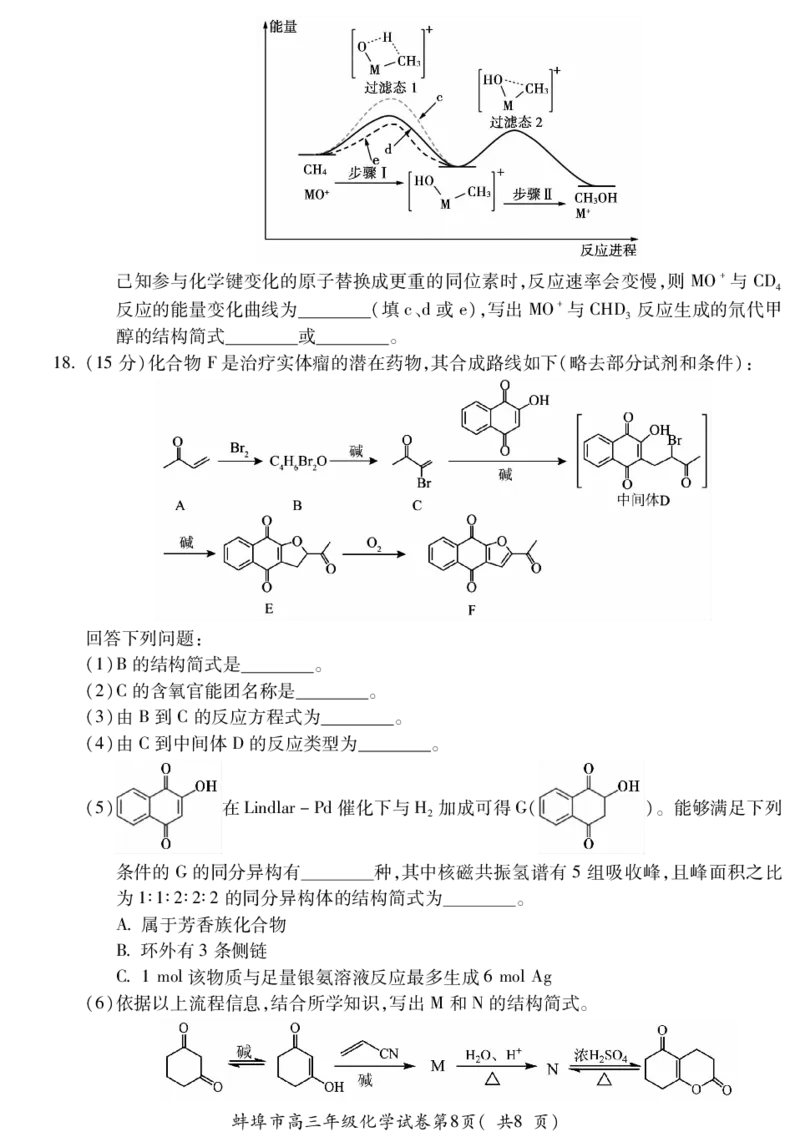
(5)利用电喷雾电离等方法可得MO+,MO+与CH 反应能高选择性地生成甲醇,反应机理
4
如下图所示:
蚌埠市高三年级化学试卷第7页(共8页)己知参与化学键变化的原子替换成更重的同位素时,反应速率会变慢,则 MO+与 CD
4
反应的能量变化曲线为 (填c、d或e),写出MO+与CHD 反应生成的氘代甲
3
醇的结构简式 或 。
18(15分)化合物F是治疗实体瘤的潜在药物,其合成路线如下(略去部分试剂和条件):
回答下列问题:
(1)B的结构简式是 。
(2)C的含氧官能团名称是 。
(3)由B到C的反应方程式为 。
(4)由C到中间体D的反应类型为 。
(5) 在Lindlar-Pd催化下与H 加成可得G( )。能够满足下列
2
条件的G的同分异构有 种,其中核磁共振氢谱有5组吸收峰,且峰面积之比
为1∶1∶2∶2∶2的同分异构体的结构简式为 。
A属于芳香族化合物
B环外有3条侧链
C1mol该物质与足量银氨溶液反应最多生成6molAg
(6)依据以上流程信息,结合所学知识,写出M和N的结构简式。
蚌埠市高三年级化学试卷第8页(共8页)