文档内容
2023级高三学年上学期九月份月考
D.制作面点时加入食用纯碱,利用 中和发酵过程产生的酸
化 学 试 题
考试时间:75分钟 分值:100分
可能用到的相对原子质量: H-1 C-12 O-16 Na-23 Fe-56 5.下列过程对应的离子方程式正确的是
一、选择题(每题只有一个正确选项,每题3分,共45分) A. 溶于氢碘酸:
1.化学在科技和生活中扮演着重要的角色,下列说法正确的是
B.将 通入到含 的溶液中:
A.“雪龙2”号破冰船极地科考:破冰过程中水发生了化学变化
C.将少量SO 气体通入NaClO溶液中:SO +ClO-+H O = +Cl-+2H+
2 2 2
B.过量服用阿司匹林引起酸中毒后,可用静脉注射NaHCO 溶液的方法解毒
3
D. 的烧碱溶液与 的 溶液等体积混合:
C.奥运主火炬采用 灯照射喷发的水雾产生“火焰”,产生该“火焰”的原理与焰色试验原
理相同
D.“嫦娥五号”使用的铝基复合材料,属于合金材料 6.常温,下列各组离子在指定溶液中一定能大量共存的是
2.下列关于金属冶炼或富集方法的叙述不正确的是
A.澄清透明的溶液中:Fe3+、K+、SO、Cl-
选项 金属 冶炼或富集方法
B.pH=3的溶液中:K+、Ba2+、I-、NO
A 钠 用电解饱和NaCl溶液的方法冶炼
C.加入Al能放出H 的溶液中:K+、NH 、SO、S2-
2
B 银 用加热Ag O的方法冶炼
2
D.紫色石蕊试液呈红色的溶液中:Ca2+、K+、F-、NO
C 铁 用CO在高温下还原铁矿石中铁的氧化物的方法冶炼
7.下列说法正确的是
D 金 金子比沙子密度大,利用水洗法直接分离的方法富集
①将久置空气中的铝片加入NaOH溶液中,开始无气体生成,之后铝片表面有气泡产生,说明开
3.设N 为阿伏加德罗常数的值,下列说法正确的是
A 始没有化学反应发生
A.标准状况下,11.2L HCl气体中含有的 数目为0.5 ②AlCl 熔点低,可用于工业电解铝的原料
3
③将Na[Al(OH) ]溶液与NaHCO 溶液混合,观察现象,验证结合质子能力:[Al(OH) ]->CO2-
B. 与足量 在催化剂作用下合成氨,生成的 分子数为 4 3 4 3
④向Al(OH) 沉淀中分别滴加盐酸和氨水,观察沉淀变化,探究Al(OH) 为两性氢氧化物
3 3
C. 与足量 充分反应,转移的电子数为
A.①② B.①③ C.③ D.③④
D.标准状况下,33.6L HF含有的分子数为
8.某实验需配置1 溶液90 用于制备NaSO ,反应原理为
2 4
4.下列叙述正确的是
NaOH+NaHSO=Na SO +H O,下列说法正确的是
4 2 4 2
A. 与水反应,红热的 与水蒸气反应均有气体单质生成
A.托盘天平和滤纸称取3.6g氢氧化钠固体
B.向饱和食盐水中先通 后,再通 ,可获得大量纯碱
B.若该NaOH溶液的密度为1.2g·cm-3,则该溶液溶质的质量分数约为3.3%
C. 的金属活性比 强,工业上用 与 的水溶液反应制
C.若称量的固体NaOH中混有少量Na O,会使所配溶液浓度偏低
2D.0.1 的 NaHSO 溶液中含有的离子数为0.3
4
9.下列实验操作、现象和解释或结论都正确的是
选项 实验操作 现象 解释或结论
A.工业上电解熔融MgCl 可制备金属Mg
2
A 将 气体通入紫色石蕊试液 溶液褪色 有漂白性 B.用金属镁还原TiCl 过程中需通入N 或Ar作保护气
4 2
①中玻璃管内的pH试纸 宜用pH计测定新制 C.“高温还原”时,发生反应的化学方程式为2Mg+TiCl 4 ====Ti+2MgCl 2
①将干燥的氯气通过一装有干燥的pH
无明显变化②中蘸有新 氯水的pH,而不宜
B 试纸的玻璃管②用一根玻璃棒蘸取新制 D.“真空蒸馏”的目的是使Mg、MgCl 气化,实现与Ti的分离
制氯水的pH试纸先变红 用pH试纸测定新制 2
的氯水滴在pH试纸上
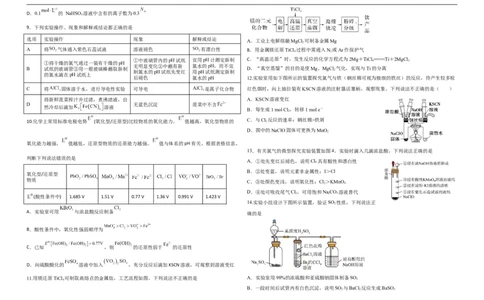
后褪色 氯水的pH 12.实验室用如下图所示的装置探究氯气与铁(钢丝棉可视为极细的铁丝)的反应,待产生较多棕
C 将 固体溶于水,进行导电性实验 可导电 是离子化合物 红色烟时,向上抽拉装有KSCN溶液的注射器活塞柄,观察现象。下列说法不正确的是( )
将新鲜菠菜榨汁并过滤,煮沸滤液,自 A.KSCN溶液变红
D 无蓝色沉淀 菠菜中不含
然冷却后滴加 溶液
B.每生成1 mol Cl ,转移1 mol e-
2
10.化学上常用标准电极电势 (氧化型/还原型)比较物质的氧化能力。 值越高,氧化型物质的
C.与Cl
2
反应的速率:钢丝棉>铁屑
D.图中的NaClO固体可更换为MnO
2
氧化能力越强, 值越低,还原型物质的还原能力越强。 值与体系的pH有关。根据表格信息,
13.有关氯气的微型探究实验装置如图4。实验时滴入几滴浓盐酸,下列说法正确的是
判断下列说法错误的是
A.①处先变红后褪色,说明Cl₂具有酸性和漂白性
B.②处变蓝,说明元素非金属性:I>Cl
氧化型/还原型
物质
C.③处颜色变浅,说明氧化性:Cl>KMnO
2 4
D.④处可吸收尾气Cl,可用饱和NaCO 溶液替代
2 2 3
(酸性条件中) 1.685 V 1.51 V 0.77 V 1.36 V 0.991 V 1.423 V
14.实验小组设计下图所示装置,验证SO 性质,下列说法正
2
A.实验室可用 与浓盐酸反应制备
确的是
B.酸性条件中,氧化性强弱顺序为
C.已知 ,则 的还原性弱于 的还原性
D.向硫酸酸化的 溶液中加入 ,充分反应后滴加KSCN溶液,可观察到溶液变红
11.用镁还原TiCl
4
可制取高熔点的金属钛,工艺流程如图。下列说法不正确的是 A.实验室用98%的浓硫酸和亚硫酸钠固体制备SO
2
B.一段时间后试管内有白色沉淀,说明SO 与BaCl 反应生成BaSO
2 2 3C.试管中的红色花瓣褪色,滴有酚酞的NaOH溶液红色变浅,均说明SO 具有漂白性 (3)氢化钠( )可在野外用作生氢剂。写出 用作生氢剂时的化学方程式 ,每生成2mol
2
D.试管内Br 的CCl 溶液褪色,说明SO 具有还原性 氢气分子,反应转移电子数目为 。
2 4 2
Ⅱ.铁是人体必需的微量元素,严重缺铁时需要服用补铁剂。实验小组为研究某补铁剂中铁元素的
价态及其含量,设计并进行了如下实验:
15.某工厂利用铜屑脱除锌浸出液中的 并制备 ,流程如下“脱氯”步骤仅 元素化合价发
【查阅资料】
生改变。下列说法正确的是
锌浸出液中相关成分(其他成分无干扰)
该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸),KSCN的硫元素为-2价。
离子 实验一.检验该补铁剂中铁元素的价态。
浓度 145 0.03 1
(4)将补铁剂碾碎的目的是 。
(5)能证明溶液①中含有Fe2+的实验现象是 。
A.“浸铜”时应加入足量 ,确保铜屑溶解完全 (6)甲同学猜测深红色溶液③迅速变为无色溶液④的原因可能是 。
实验二. 测定该补铁剂中铁元素的含量。
B.“浸铜”反应:
C.“脱氯”反应:
D.脱氯液的溶质主要成分为ZnCl
2
二、填空题(共55分) (7)计算每片该补铁剂含铁元素的质量为 g。
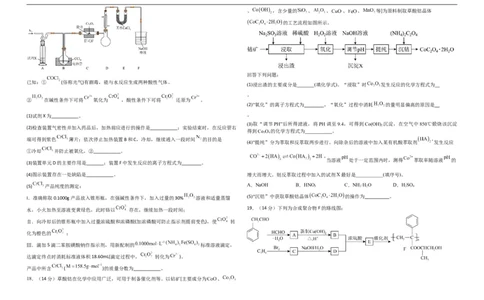
16.(14分)I. 是一种重要的化工原料,可以由其制备许多化工产品。 为阿伏加德罗常 17.(13分)三氯化铬( )是工业上常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧
数的值,常见的相关转化关系如下图所示:
(1) 溶液在通电条件下发生反应的化学方程式为
气氧化。实验室利用反应 制备无水 的装置(夹持装置略)
。
(2)下列关于 导电的相关说法,正确的是
如下图所示。回答下列问题:
__________。
A. 固体在电流作用下产生自由移动的 和
B. 溶液能导电,所以 溶液属于电解质
C. 在熔融状态下电离产生了自由移动的钠离子和氯离子
D. 固体不能导电,但是其属于电解质、 ,含少量的 、 、 、 、 等]为原料制取草酸钴晶体
的工艺流程如图所示。
回答下列问题:
已知:① (俗称光气)有剧毒,能与水反应生成两种酸性气体。
(1)浸出渣的主要成分是 (填化学式)。“浸取”时 发生反应的化学方程式为
。
② 在碱性条件下可将 氧化为 ,酸性条件下可将 还原为 。
(2)“氧化”的离子方程式为 ,“氧化”过程中消耗 的量明显偏高的原因是
(1)试剂X为 。 。
(3)取“调节PH”后所得滤液,将PH调至9.4,可得到Co(OH) 沉淀,在空气中850℃煅烧该沉淀
2
(2)检查装置气密性并加入药品后,加热前应进行的操作是 ;实验结束时,在反应管右
得到Co O 的化学方程式为 。
3 4
端可得到紫色 薄片;依次停止加热装置B和C,冷却,继续通入一段时间 的目的是
(4)“提纯”分为萃取和反萃取两步进行。向除杂后的溶液中加入某有机酸萃取剂 发生反应
①冷却 并防止被氧化,② 。
当溶液 处于一定范围内时,测得 萃取率随溶液 的
(3)装置单元D的主要作用是 ;装置F中发生反应的离子方程式为 。
(4)图示装置存在一处缺陷是 。 增大而增大。则反萃取过程中加入的试剂X最好是___________(填序号)。
(5) 产品纯度的测定: A.NaOH B.HNO 3 C.NH 3 ·H 2 O D.H 2 SO 4
I.准确称取0.1000g产品放入锥形瓶,在强碱性条件下,加入过量的30% 溶液和适量蒸馏
(5)“沉钴”中获取草酸钴晶体 的操作为 。
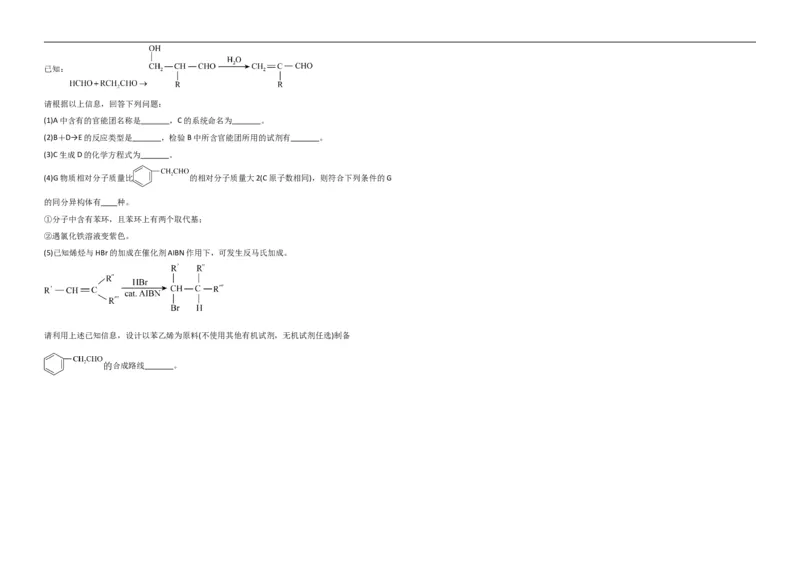
19.(14分)下列为合成聚合物F的路线图:
水,小火加热至溶液变黄绿色,此时铬以 存在,继续加热一段时间;
Ⅱ.向冷却后的锥形瓶中加入过量浓硫酸和浓磷酸(加浓磷酸可防止指示剂提前变色),使 转
化为橙色的 ;
Ⅲ.滴加5滴二苯胺磺酸钠作指示剂,用新配制的 标准溶液滴定,
达滴定终点时消耗标准液体积18.60mL(滴定过程中, 转化为 )。
产品中所含 ( )的质量分数为 。
18.(14分)草酸钴在化学中应用广泛,可用于制备催化剂等。以钻矿[主要成分为 、已知:
请根据以上信息,回答下列问题:
(1)A中含有的官能团名称是 ,C的系统命名为 。
(2)B+D→E的反应类型是 ,检验B中所含官能团所用的试剂有 。
(3)C生成D的化学方程式为 。
(4)G物质相对分子质量比 的相对分子质量大2(C原子数相同),则符合下列条件的G
的同分异构体有 种。
①分子中含有苯环,且苯环上有两个取代基;
②遇氯化铁溶液变紫色。
(5)已知烯烃与HBr的加成在催化剂AIBN作用下,可发生反马氏加成。
请利用上述已知信息,设计以苯乙烯为原料(不使用其他有机试剂,无机试剂任选)制备
的合成路线 。