文档内容
高三化学期末试题
一、选择题:本题共15小题,每小题3分,共45分。每小题只有一个选项符合题意。
1. 化学与生产生活密切相关。下列说法错误的是
A. 饱和 溶液处理锅炉水垢中的 ,发生了沉淀的转化
B. 夏天雷雨过后空气清新,是因为放电时 和 合成了
C. 神舟系列飞船返回舱使用氮化硅耐高温结构材料, 属于共价晶体
D. 可用于污水脱氯 ,是由于其具有还原性
2. 下列有关物质性质的说法正确的是
A. 苯酚和乙醇都能与 溶液反应
B. 的酸性弱于
C. 邻羟基苯甲醛的沸点高于对羟基苯甲醛
D. 酰胺在酸或碱存在并加热的条件下可发生水解反应
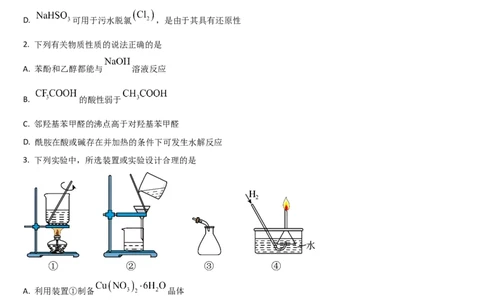
3. 下列实验中,所选装置或实验设计合理的是
A. 利用装置①制备 晶体
B. 利用装置②分离苯酚和水的混合物
C. 利用装置③接收蒸馏实验所得馏分
D. 利用装置④处理氢气尾气
4. 表示阿伏加德罗常数的值。下列说法正确的是
A. 金刚石中含有 键的数目为
B. 含 钠元素的 和 混合物中阴离子的数目为
学科网(北京)股份有限公司C. 的浓硝酸与足量铜反应,转移电子数目为
D. 时, 的 溶液中水电离出的 的数目为
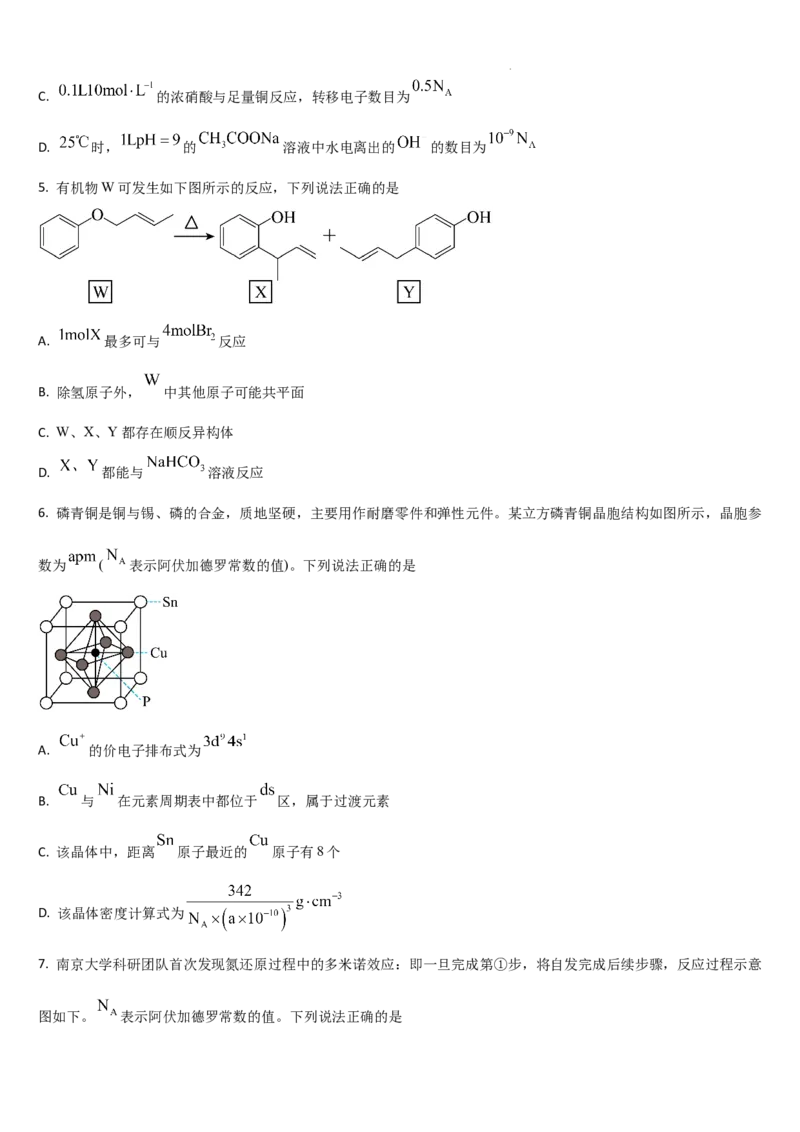
5. 有机物W可发生如下图所示的反应,下列说法正确的是
A. 最多可与 反应
B. 除氢原子外, 中其他原子可能共平面
C. W、X、Y都存在顺反异构体
D. 都能与 溶液反应
6. 磷青铜是铜与锡、磷的合金,质地坚硬,主要用作耐磨零件和弹性元件。某立方磷青铜晶胞结构如图所示,晶胞参
数为 ( 表示阿伏加德罗常数的值)。下列说法正确的是
A. 的价电子排布式为
B. 与 在元素周期表中都位于 区,属于过渡元素
C. 该晶体中,距离 原子最近的 原子有8个
D. 该晶体密度计算式为
7. 南京大学科研团队首次发现氮还原过程中的多米诺效应:即一旦完成第①步,将自发完成后续步骤,反应过程示意
图如下。 表示阿伏加德罗常数的值。下列说法正确的是
学科网(北京)股份有限公司A. 含有 个价电子
B. ①②③步反应均为氧化还原反应
C. 若 参与第②步反应,转移电子数为
D. 整个反应中, 为催化剂, 和 为中间产物
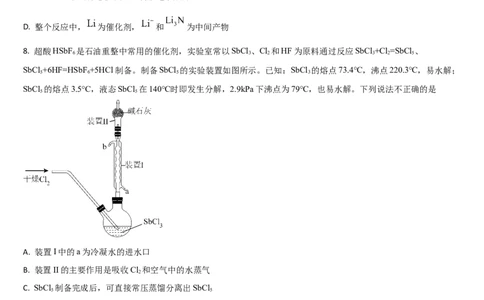
8. 超酸HSbF 是石油重整中常用的催化剂,实验室常以SbCl 、Cl 和HF为原料通过反应SbCl +Cl=SbCl 、
6 3 2 3 2 5
SbCl +6HF=HSbF +5HCl制备。制备SbCl 的实验装置如图所示。已知:SbCl 的熔点73.4℃,沸点220.3℃,易水解;
5 6 5 3
SbCl 的熔点3.5°C,液态SbCl 在140℃时即发生分解,2.9kPa下沸点为79℃,也易水解。下列说法不正确的是
5 5
A. 装置I中的a为冷凝水的进水口
B. 装置II的主要作用是吸收Cl 和空气中的水蒸气
2
C. SbCl 制备完成后,可直接常压蒸馏分离出SbCl
5 5
D. 由SbCl 制备HSbF 时,不能选用玻璃仪器
5 6
9. 已知反应 ,在 时向密闭容器中充入一定量的 气体,平衡时气体混合物
中碘化氢的物质的量分数 为 。测得 和 的关系如图所示。下列结论错误的是
学科网(北京)股份有限公司A. 改变 的初始投入量,平衡时 的物质的量分数 仍为
B. 增大体系压强,平衡不发生移动,平衡常数 不变
C. 温度降低, 、 均减小,平衡向正反应方向移动
D. 温度下降,反应重新达到平衡时,图中表示平衡的点可能是A和D
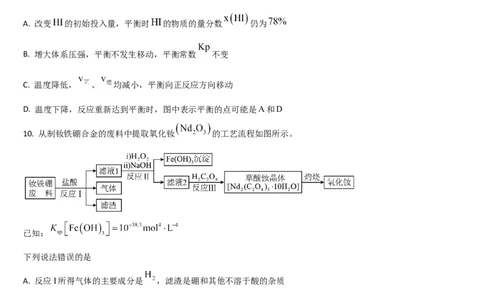
10. 从制钕铁硼合金的废料中提取氧化钕 的工艺流程如图所示。
已知:
下列说法错误的是
A. 反应I所得气体的主要成分是 ,滤渣是硼和其他不溶于酸的杂质
B. 为完全除去滤液1中铁元素,反应II应调节 的最小值为2.9
C. 温度越高,越有利于反应II的进行
D. 反应III中适当增大草酸的浓度,有利于草酸钕晶体的析出
11. NaHe的晶胞结构(与CaF 相似)如图所示,设晶胞边长为anm,阿伏加德罗常数的值为N ,下列说法错误的是
2 2 A
学科网(北京)股份有限公司已知:1号原子的坐标为(0,0,0),3号原子的坐标为(1,1,1)。
A. 2号原子的坐标为( )
B. 晶胞中Na原子与He原子的配位数之比为1∶2
C. 该晶体的密度为 g/cm3
D. 晶胞中Na原子位于He原子围成的正八面体空隙中
12. 下列实验操作对应的现象以及结论都正确且具有因果关系的是
选
实验操作 现象 结论
项
向盛有 含 的 溶液的试管中加入 的 浓溶 层溶
A (无色)
液,振荡 液紫色变浅
向盛有10滴 溶液的试管中滴加3滴
产生黄色沉
B 的 溶液,产生白色沉淀,再向其中滴加3滴
淀
的 溶液
用玻璃棒能取 的 溶液滴在洁净的 试纸颜色无 溶液中的离子
C
明显变化
试纸上 均不发生水解
注射器内气 加压,平衡向生成 气体的
D 将充满 气体的注射器(带塞)的活塞往里推,压缩体积
体颜色变浅 方向移动
A. A B. B C. C D. D
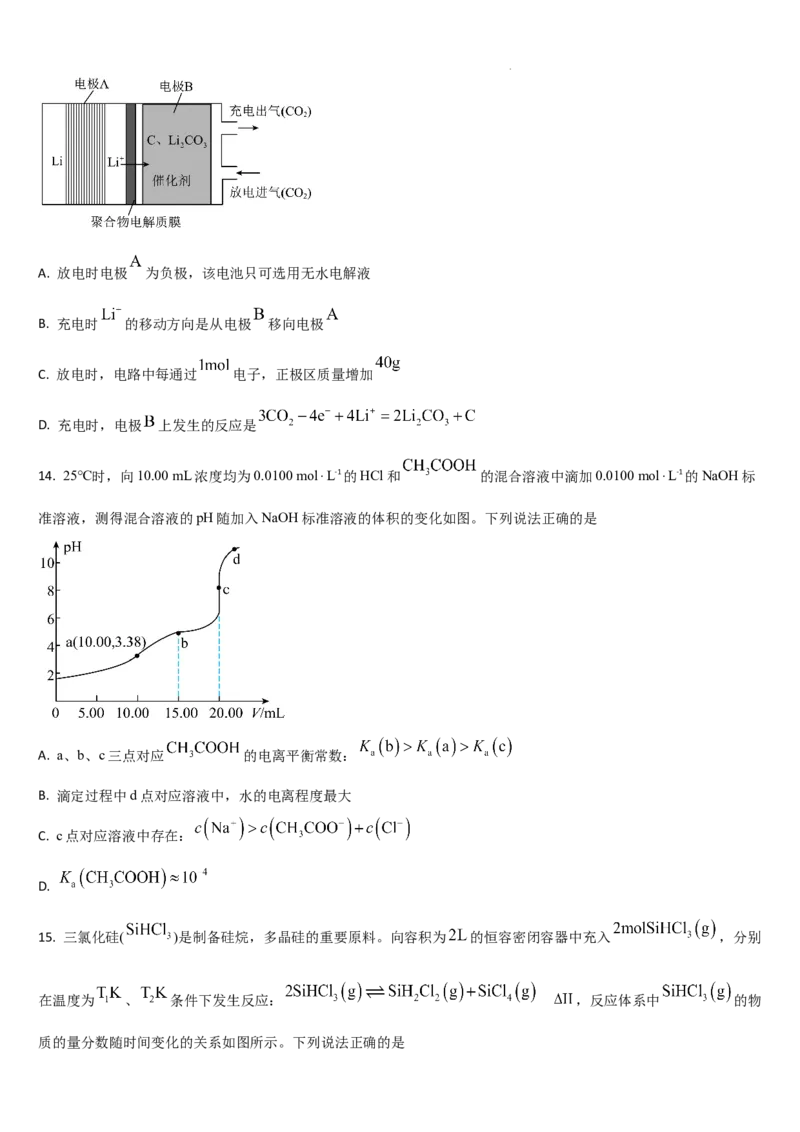
13. 电化学“大气固碳”方法是我国科学家研究发现的,相关装置如图所示。下列说法错误的是
学科网(北京)股份有限公司A. 放电时电极 为负极,该电池只可选用无水电解液
B. 充电时 的移动方向是从电极 移向电极
C. 放电时,电路中每通过 电子,正极区质量增加
D. 充电时,电极 上发生的反应是
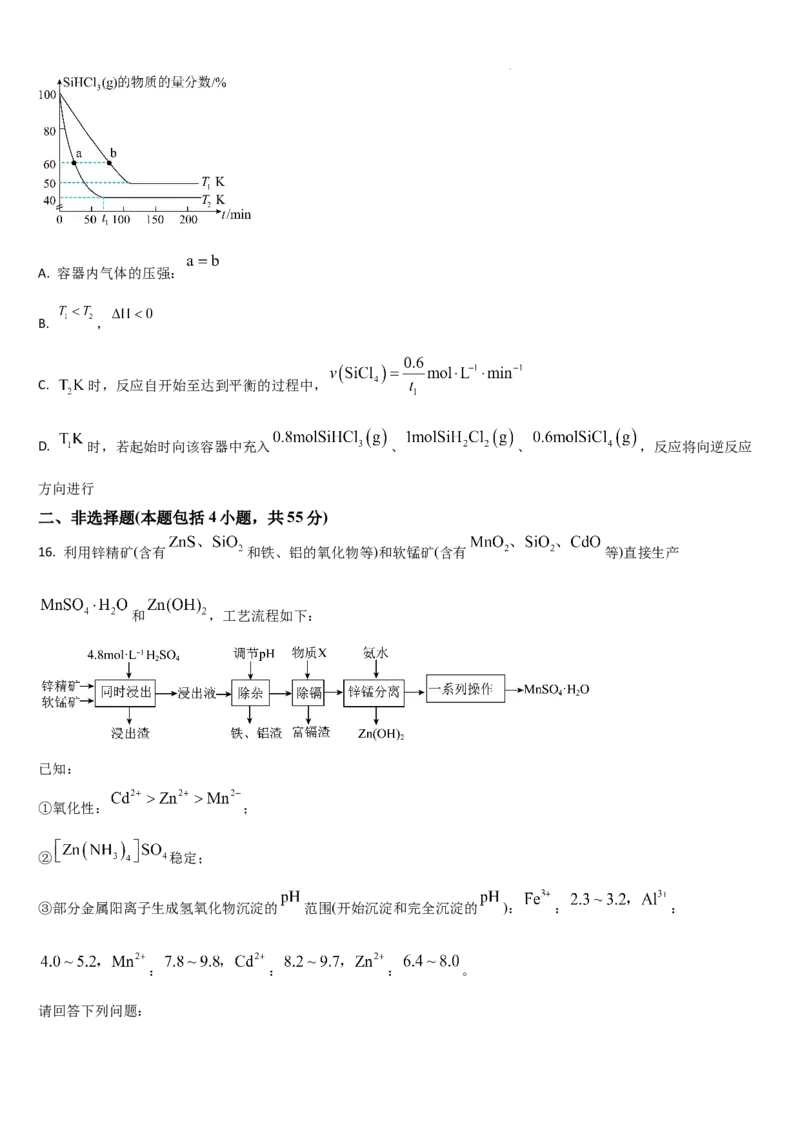
14. 25℃时,向10.00 mL浓度均为0.0100 mol⋅L-1的HCl和 的混合溶液中滴加0.0100 mol⋅L-1的NaOH标
准溶液,测得混合溶液的pH随加入NaOH标准溶液的体积的变化如图。下列说法正确的是
A. a、b、c三点对应 的电离平衡常数:
B. 滴定过程中d点对应溶液中,水的电离程度最大
C. c点对应溶液中存在:
D.
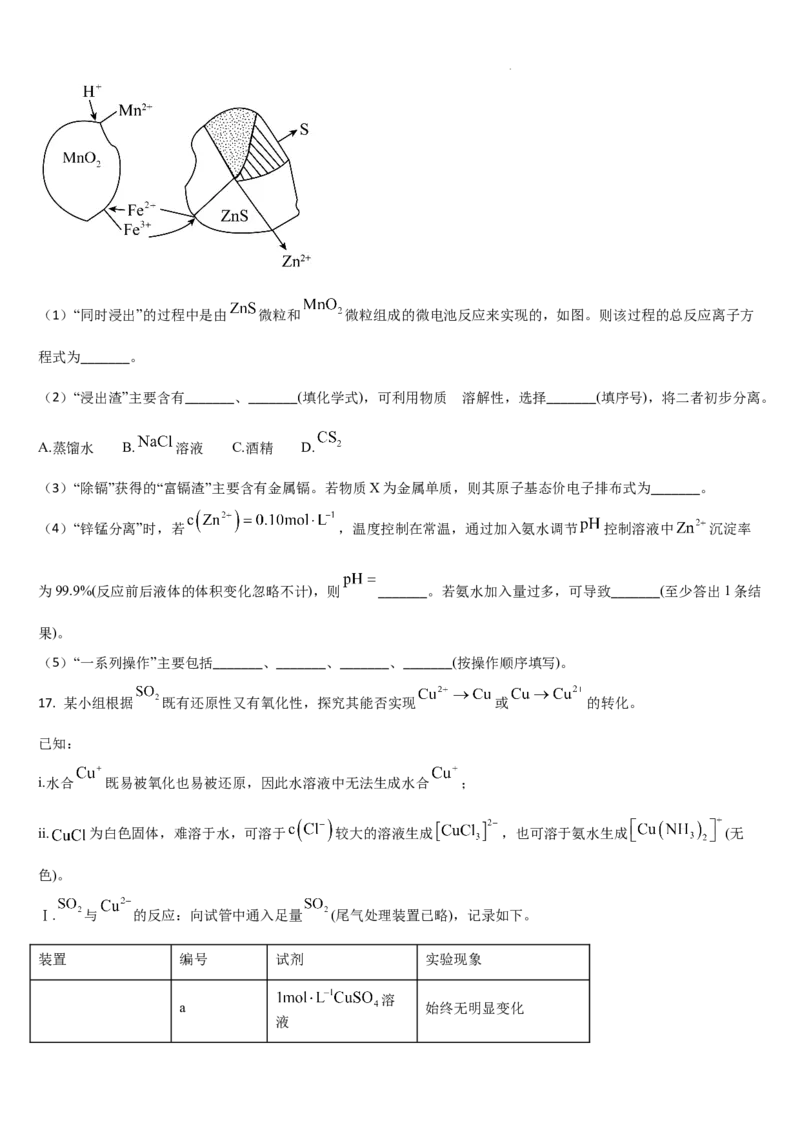
15. 三氯化硅( )是制备硅烷,多晶硅的重要原料。向容积为 的恒容密闭容器中充入 ,分别
在温度为 、 条件下发生反应: ,反应体系中 的物
质的量分数随时间变化的关系如图所示。下列说法正确的是
学科网(北京)股份有限公司A. 容器内气体的压强:
B. ,
C. 时,反应自开始至达到平衡的过程中,
D. 时,若起始时向该容器中充入 、 、 ,反应将向逆反应
方向进行
二、非选择题(本题包括4小题,共55分)
16. 利用锌精矿(含有 和铁、铝的氧化物等)和软锰矿(含有 等)直接生产
和 ,工艺流程如下:
已知:
①氧化性: ;
② 稳定;
③部分金属阳离子生成氢氧化物沉淀的 范围(开始沉淀和完全沉淀的 ): : :
: : : 。
请回答下列问题:
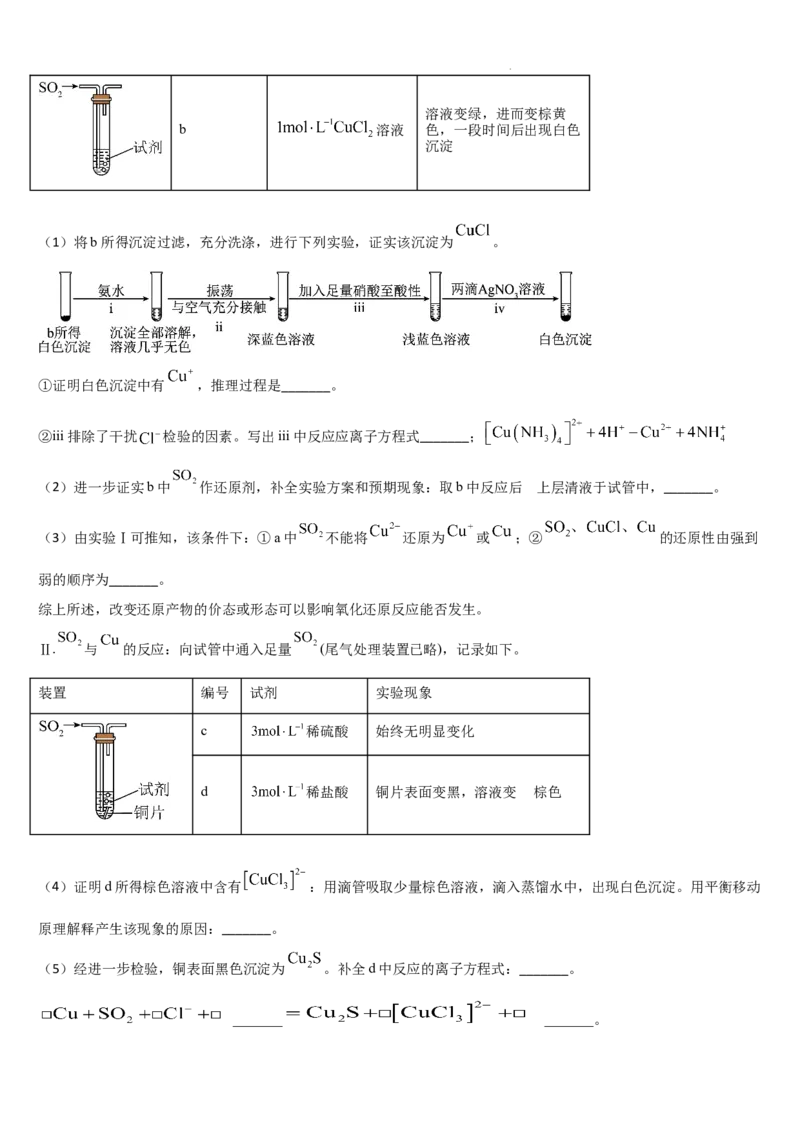
学科网(北京)股份有限公司(1)“同时浸出”的过程中是由 微粒和 微粒组成的微电池反应来实现的,如图。则该过程的总反应离子方
程式为_______。
的
(2)“浸出渣”主要含有_______、_______(填化学式),可利用物质 溶解性,选择_______(填序号),将二者初步分离。
A.蒸馏水 B. 溶液 C.酒精 D.
(3)“除镉”获得的“富镉渣”主要含有金属镉。若物质X为金属单质,则其原子基态价电子排布式为_______。
(4)“锌锰分离”时,若 ,温度控制在常温,通过加入氨水调节 控制溶液中 沉淀率
为99.9%(反应前后液体的体积变化忽略不计),则 _______。若氨水加入量过多,可导致_______(至少答出1条结
果)。
(5)“一系列操作”主要包括_______、_______、_______、_______(按操作顺序填写)。
17. 某小组根据 既有还原性又有氧化性,探究其能否实现 或 的转化。
已知:
i.水合 既易被氧化也易被还原,因此水溶液中无法生成水合 ;
ii. 为白色固体,难溶于水,可溶于 较大的溶液生成 ,也可溶于氨水生成 (无
色)。
Ⅰ. 与 的反应:向试管中通入足量 (尾气处理装置已略),记录如下。
装置 编号 试剂 实验现象
溶
a 始终无明显变化
液
学科网(北京)股份有限公司溶液变绿,进而变棕黄
b 溶液 色,一段时间后出现白色
沉淀
(1)将b所得沉淀过滤,充分洗涤,进行下列实验,证实该沉淀为 。
①证明白色沉淀中有 ,推理过程是_______。
②iii排除了干扰 检验的因素。写出iii中反应应离子方程式_______;
的
(2)进一步证实b中 作还原剂,补全实验方案和预期现象:取b中反应后 上层清液于试管中,_______。
(3)由实验Ⅰ可推知,该条件下:①a中 不能将 还原为 或 ;② 的还原性由强到
弱的顺序为_______。
综上所述,改变还原产物的价态或形态可以影响氧化还原反应能否发生。
Ⅱ. 与 的反应:向试管中通入足量 (尾气处理装置已略),记录如下。
装置 编号 试剂 实验现象
c 稀硫酸 始终无明显变化
d 稀盐酸 铜片表面变黑,溶液变 为棕色
(4)证明d所得棕色溶液中含有 :用滴管吸取少量棕色溶液,滴入蒸馏水中,出现白色沉淀。用平衡移动
原理解释产生该现象的原因:_______。
(5)经进一步检验,铜表面黑色沉淀为 。补全d中反应的离子方程式:_______。
_______ _______。
学科网(北京)股份有限公司(6)与c对比,d能够发生反应的原因是_______。
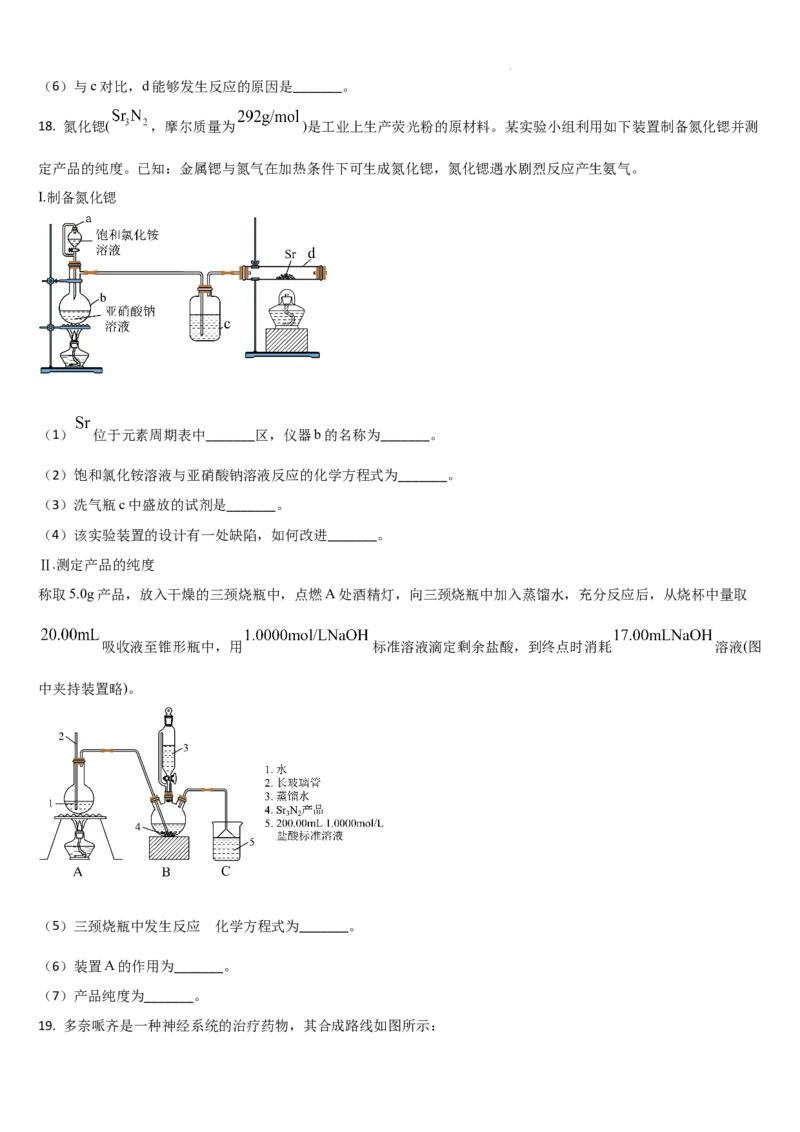
18. 氮化锶( ,摩尔质量为 )是工业上生产荧光粉的原材料。某实验小组利用如下装置制备氮化锶并测
定产品的纯度。已知:金属锶与氮气在加热条件下可生成氮化锶,氮化锶遇水剧烈反应产生氨气。
I.制备氮化锶
(1) 位于元素周期表中_______区,仪器b的名称为_______。
(2)饱和氯化铵溶液与亚硝酸钠溶液反应的化学方程式为_______。
(3)洗气瓶c中盛放的试剂是_______。
(4)该实验装置的设计有一处缺陷,如何改进_______。
Ⅱ.测定产品的纯度
称取5.0g产品,放入干燥的三颈烧瓶中,点燃A处酒精灯,向三颈烧瓶中加入蒸馏水,充分反应后,从烧杯中量取
吸收液至锥形瓶中,用 标准溶液滴定剩余盐酸,到终点时消耗 溶液(图
中夹持装置略)。
的
(5)三颈烧瓶中发生反应 化学方程式为_______。
(6)装置A的作用为_______。
(7)产品纯度为_______。
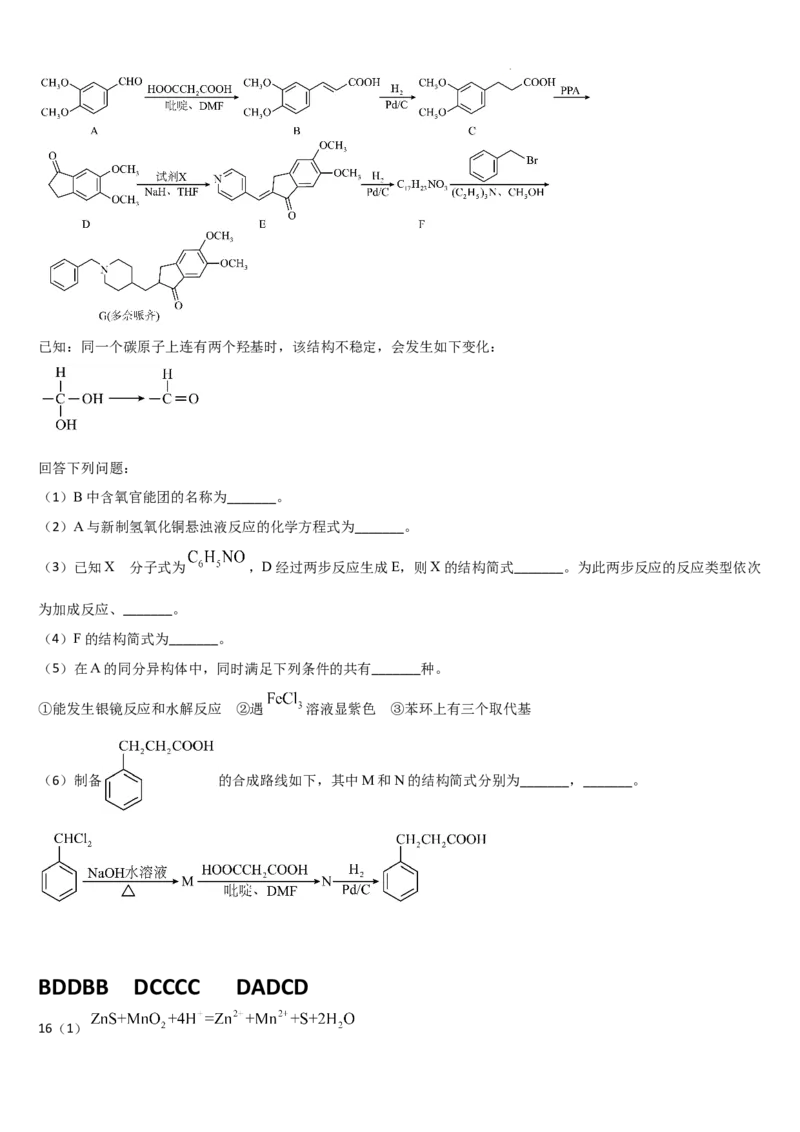
19. 多奈哌齐是一种神经系统的治疗药物,其合成路线如图所示:
学科网(北京)股份有限公司已知:同一个碳原子上连有两个羟基时,该结构不稳定,会发生如下变化:
回答下列问题:
(1)B中含氧官能团的名称为_______。
(2)A与新制氢氧化铜悬浊液反应的化学方程式为_______。
的
(3)已知X 分子式为 ,D经过两步反应生成E,则X的结构简式_______。为此两步反应的反应类型依次
为加成反应、_______。
(4)F的结构简式为_______。
(5)在A的同分异构体中,同时满足下列条件的共有_______种。
①能发生银镜反应和水解反应 ②遇 溶液显紫色 ③苯环上有三个取代基
(6)制备 的合成路线如下,其中M和N的结构简式分别为_______,_______。
BDDBB DCCCC DADCD
16(1)
学科网(北京)股份有限公司(2) ①. SiO ②. S ③. D
2
(3)3d104s2 (4) ①. 7.5 ②. 可能导致Mn2+沉淀使得MnSO ⋅H O的产率降低(或者含Mn2+的溶液中混
4 2
有[Zn(NH ) ]2+)等
3 4
(5) ①. 蒸发浓缩 ②. 冷却结晶 ③. 过滤洗涤 ④. 干燥
17(1) ①. 深蓝色溶液中含 ,是无色溶液中的 被 O 氧化的产物,说明浓氨水溶
2
解出了白色沉淀中的Cu+ ②.
(2)滴加BaCl 溶液,出现白色沉淀,说明 被氧化成
2
(3)Cu>SO >CuCl
2
(4)棕色溶液滴入蒸馏水后离子浓度减小,使 平衡逆向移动,析出CuCl沉淀
(5)
(6) 与 结合成 ,其氧化性弱于SO ,使 Cu 能够被 SO 氧化
2 2
18(1) ①. s ②. 蒸馏烧瓶
(2)
(3)浓硫酸 (4)在d装置后增加一个装有碱石灰的球形干燥管
(5)
(6)利用水蒸气将反应产生的氨气排出,以便被盐酸标准溶液完全吸收
(7)
19(1)醚键、羧基
(2) (3) ①.
②. 消去反应
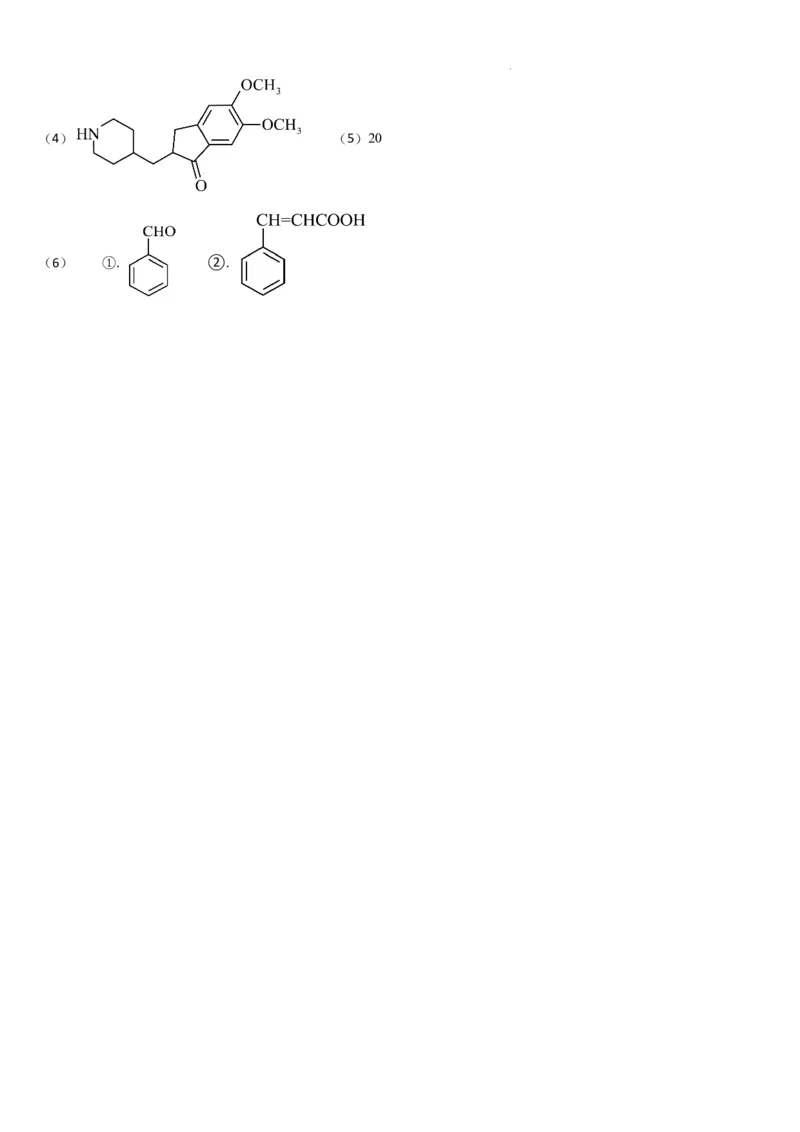
学科网(北京)股份有限公司(4) (5)20
(6) ①. ②.
学科网(北京)股份有限公司