文档内容
哈三中 2024-2025 学年度上学期高三学年期末考试
化学试卷
卷 选择题 共 分
Ⅰ ( 45 )
可能用到的相对原子质量 H1 O16 Na23 Ge73 Hg201 Sb122
一、选择题(每题仅一个选项符合题意,每题3分,共45分)
1.化学与生产生活息息相关,下列说法错误的是
A.水玻璃可以用做木材防火剂,它是一种电解质
B.味精能增加食品的鲜味,是一种常用的增味剂,其主要成分为谷氨酸钠
C.合成氨的反应塔与外加电源的负极相连并维持一定的电压,可以钝化防腐
D.锅炉水垢中含有的CaSO ,可先用Na CO 溶液处理,后用酸除去
4 2 3
2.下列化学用语或表述正确的是
A.CH 的共价键类型:s-p 键
4
B.SO 的价层电子对互斥(VSEPR)模型:
2
σ
C.基态N原子的价层电子排布式:
D.丙炔的键线式:
3.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.标准状况下,11.2LNO和足量O 充分反应,转移电子的数目为N
2 A
B.7.8gNa O 固体中阴离子的数目为0.2N
2 2 A
C.0.1mol·L-1Na SO 溶液中,SO 2-数目小于0.1N
2 3 3 A
D.9gD O所含质子的数目为5N
2 A
4.硫代硫酸钠(Na S O )可用于脱除废水中的Cl 。其工业制备方法为:将一定比例的
2 2 3 2
Na CO 与Na S配成混合溶液,再通入SO ,先有黄色沉淀生成,当黄色沉淀消失时,即
2 3 2 2
生成了Na S O ,同时释放CO 。下列说法错误的是
2 2 3 2
A.制备反应中Na S O 既是氧化产物又是还原产物
2 2 3
B.制备总反应的离子方程式为2S2-+CO 2- +4SO =CO +3S O 2-
3 2 2 2 3
C.产生黄色沉淀的反应中氧化剂与还原剂物质的量之比为2:1
D.将Na S O 脱除Cl 反应设计成原电池时,S O 2-为负极反应物
2 2 3 2 2 3
5.陈述I与陈述II均正确,且具有因果关系的是
选项 陈述I 陈述II
A 晶体中的配位数:CO >H O 键角:CO >H O
2 2 2 2
B 沸点:乙醛>丙烷 乙醛分子间存在氢键
C 酸性:CF COOH<CCl COOH 范德华力:CF COOH<CCl COOH
3 3 3 3
D X射线衍射实验鉴别玻璃仿造的宝石 玻璃是非晶体
高三化学 第1页 共8页
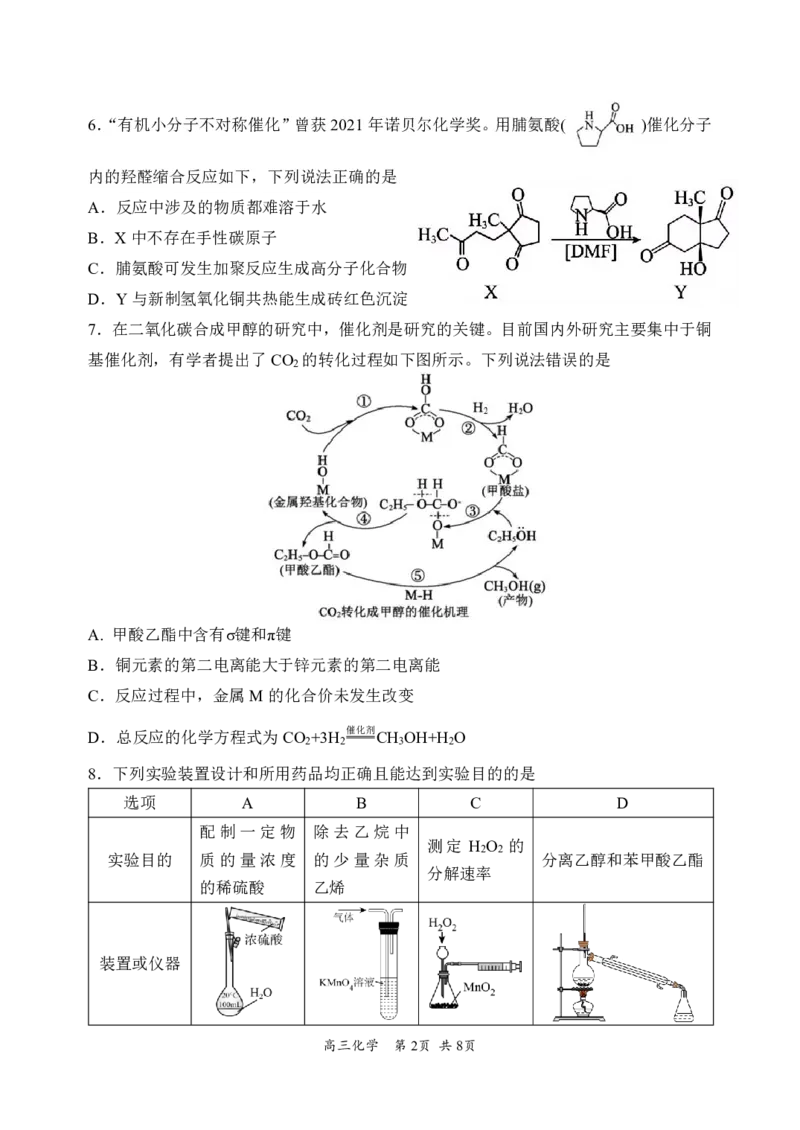
{#{QQABBY6AogiIAAIAARhCAQGACAGQkAAACQgGxAAQMAAACAFABAA=}#}6.“有机小分子不对称催化”曾获2021年诺贝尔化学奖。用脯氨酸( )催化分子
内的羟醛缩合反应如下,下列说法正确的是
A.反应中涉及的物质都难溶于水
B.X中不存在手性碳原子
C.脯氨酸可发生加聚反应生成高分子化合物
D.Y与新制氢氧化铜共热能生成砖红色沉淀
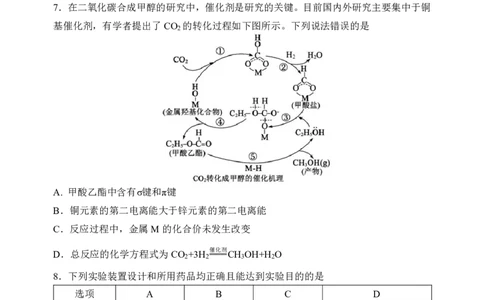
7.在二氧化碳合成甲醇的研究中,催化剂是研究的关键。目前国内外研究主要集中于铜
基催化剂,有学者提出了CO 的转化过程如下图所示。下列说法错误的是
2
A. 甲酸乙酯中含有σ键和π键
B.铜元素的第二电离能大于锌元素的第二电离能
C.反应过程中,金属M的化合价未发生改变
D.总反应的化学方程式为CO +3H 催化剂 CH OH+H O
2 2 3 2
8.下列实验装置设计和所用药品均正确且能达到实验目的的是
选项 A B C D
配制一定物 除去乙烷中
测定 H O 的
2 2
实验目的 质的量浓度 的少量杂质 分离乙醇和苯甲酸乙酯
分解速率
的稀硫酸 乙烯
装置或仪器
高三化学 第2页 共8页
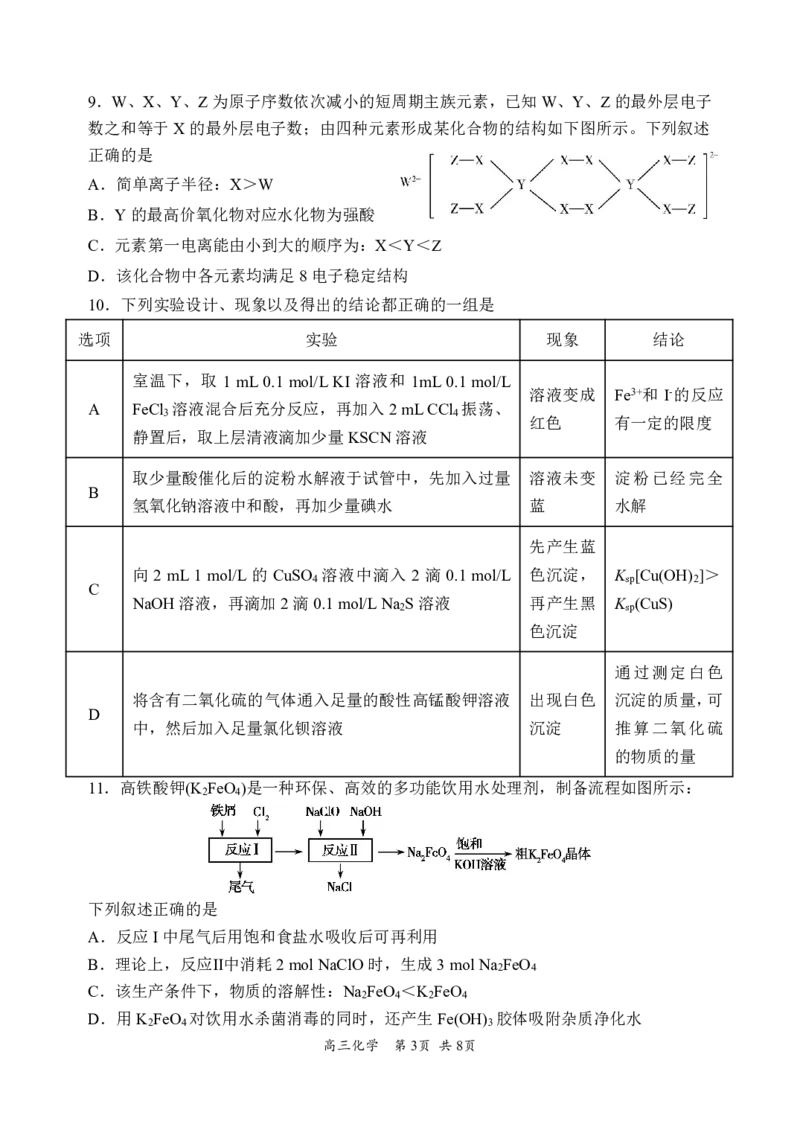
{#{QQABBY6AogiIAAIAARhCAQGACAGQkAAACQgGxAAQMAAACAFABAA=}#}9.W、X、Y、Z为原子序数依次减小的短周期主族元素,已知W、Y、Z的最外层电子
数之和等于X的最外层电子数;由四种元素形成某化合物的结构如下图所示。下列叙述
正确的是
A.简单离子半径:X>W
B.Y的最高价氧化物对应水化物为强酸
C.元素第一电离能由小到大的顺序为:X<Y<Z
D.该化合物中各元素均满足8电子稳定结构
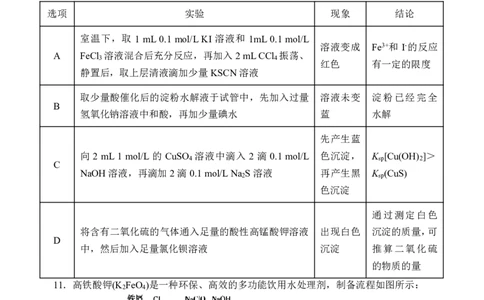
10.下列实验设计、现象以及得出的结论都正确的一组是
选项 实验 现象 结论
室温下,取 1 mL0.1 mol/LKI 溶液和 1mL 0.1 mol/L
溶液变成 Fe3+和 I-的反应
A FeCl 溶液混合后充分反应,再加入2mLCCl 振荡、
3 4
红色 有一定的限度
静置后,取上层清液滴加少量KSCN溶液
取少量酸催化后的淀粉水解液于试管中,先加入过量 溶液未变 淀粉已经完全
B
氢氧化钠溶液中和酸,再加少量碘水 蓝 水解
先产生蓝
向 2 mL1 mol/L 的 CuSO 溶液中滴入 2 滴 0.1 mol/L 色沉淀, K [Cu(OH) ]>
4 sp 2
C
NaOH溶液,再滴加2滴0.1mol/LNa S溶液 再产生黑 K (CuS)
2 sp
色沉淀
通过测定白色
将含有二氧化硫的气体通入足量的酸性高锰酸钾溶液 出现白色 沉淀的质量,可
D
中,然后加入足量氯化钡溶液 沉淀 推算二氧化硫
的物质的量
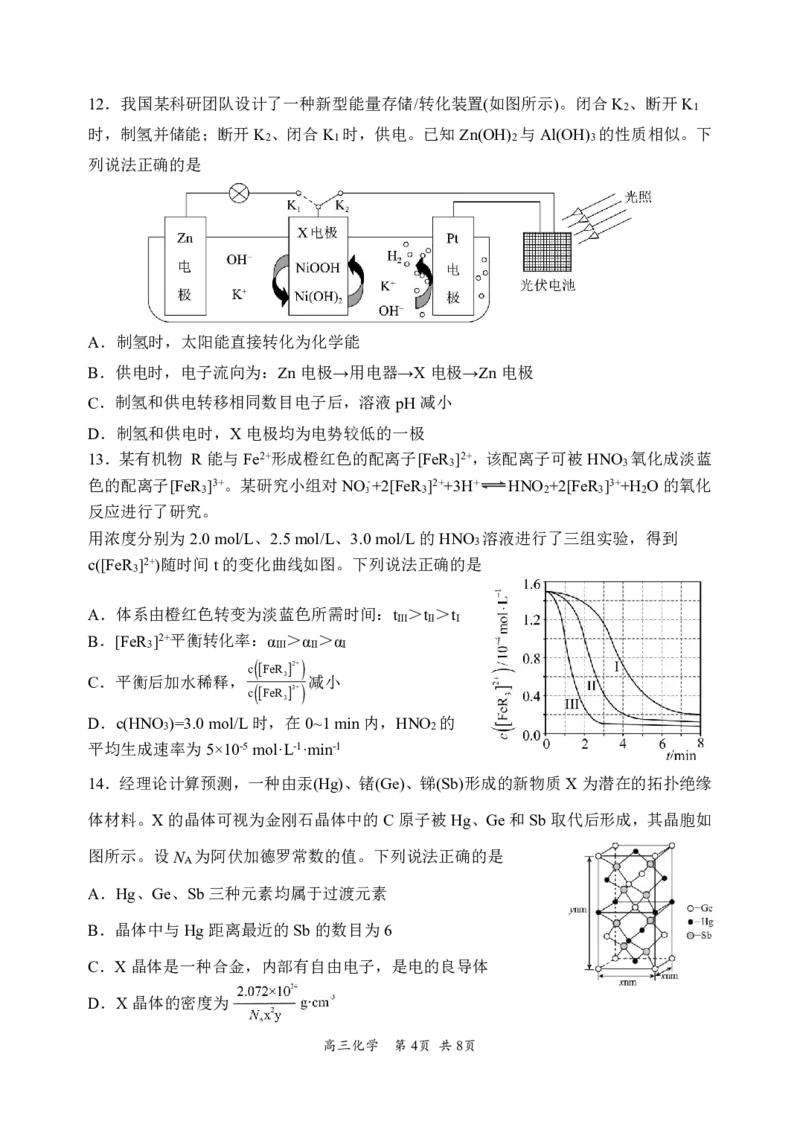
11.高铁酸钾(K FeO )是一种环保、高效的多功能饮用水处理剂,制备流程如图所示:
2 4
下列叙述正确的是
A.反应I中尾气后用饱和食盐水吸收后可再利用
B.理论上,反应Ⅱ中消耗2molNaClO时,生成3molNa FeO
2 4
C.该生产条件下,物质的溶解性:Na FeO <K FeO
2 4 2 4
D.用K FeO 对饮用水杀菌消毒的同时,还产生Fe(OH) 胶体吸附杂质净化水
2 4 3
高三化学 第3页 共8页
{#{QQABBY6AogiIAAIAARhCAQGACAGQkAAACQgGxAAQMAAACAFABAA=}#}12.我国某科研团队设计了一种新型能量存储/转化装置(如图所示)。闭合K 、断开K
2 1
时,制氢并储能;断开K 、闭合K 时,供电。已知Zn(OH) 与Al(OH) 的性质相似。下
2 1 2 3
列说法正确的是
A.制氢时,太阳能直接转化为化学能
B.供电时,电子流向为:Zn电极→用电器→X电极→Zn电极
C.制氢和供电转移相同数目电子后,溶液pH减小
D.制氢和供电时,X电极均为电势较低的一极
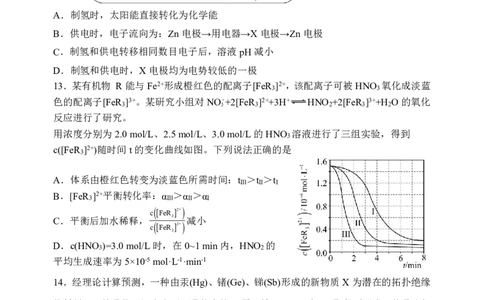
13.某有机物 R能与Fe2+形成橙红色的配离子[FeR ]2+,该配离子可被HNO 氧化成淡蓝
3 3
色的配离子[FeR ]3+。某研究小组对NO-+2[FeR ]2++3H+ HNO +2[FeR ]3++H O的氧化
3 3 3 2 3 2
反应进行了研究。
用浓度分别为2.0mol/L、2.5mol/L、3.0mol/L的HNO 溶液进行了三组实验,得到
3
c([FeR ]2+)随时间t的变化曲线如图。下列说法正确的是
3
A.体系由橙红色转变为淡蓝色所需时间:t >t >t
Ⅲ Ⅱ Ⅰ
B.[FeR ]2+平衡转化率:α >α >α
3 Ⅲ Ⅱ Ⅰ
c
FeR 2+
C.平衡后加水稀释, 3 减小
c
FeR 3+
3
D.c(HNO )=3.0mol/L时,在0~1min内,HNO 的
3 2
平均生成速率为5×10-5mol·L-1·min-1
14.经理论计算预测,一种由汞(Hg)、锗(Ge)、锑(Sb)形成的新物质X为潜在的拓扑绝缘
体材料。X的晶体可视为金刚石晶体中的C原子被Hg、Ge和Sb取代后形成,其晶胞如
图所示。设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.Hg、Ge、Sb三种元素均属于过渡元素
B.晶体中与Hg距离最近的Sb的数目为6
C.X晶体是一种合金,内部有自由电子,是电的良导体
D.X晶体的密度为
高三化学 第4页 共8页
{#{QQABBY6AogiIAAIAARhCAQGACAGQkAAACQgGxAAQMAAACAFABAA=}#}15.乙二胺四乙酸(简称EDTA,可用H Y表示)在化学分析中常用于络合滴定。水溶液中,
4
EDTA常以H Y2+、H Y+、H Y、H Y-、H Y2-、HY3-和Y4-等7种形式存在。常温下,EDTA
6 5 4 3 2
c
Y4
溶液中上述7种微粒的分布分数[如 Y4 ]与溶液pH关系如下左图所示,
含Y微粒浓度和
右图表示EDTA与某金属离子Mm+形成的螯合物的结构。下列说法正确的是
A.曲线e代表HY3-
B.交点Q处pH=8.21
C.pH越小,EDTA与金属离子配位能力越强
D.金属离子Mm+的m=3
Ⅱ卷 非选择题 共 分
( 55 )
二、非选择题(16题14分,17题14分,18题14分,19题13分,共55分)
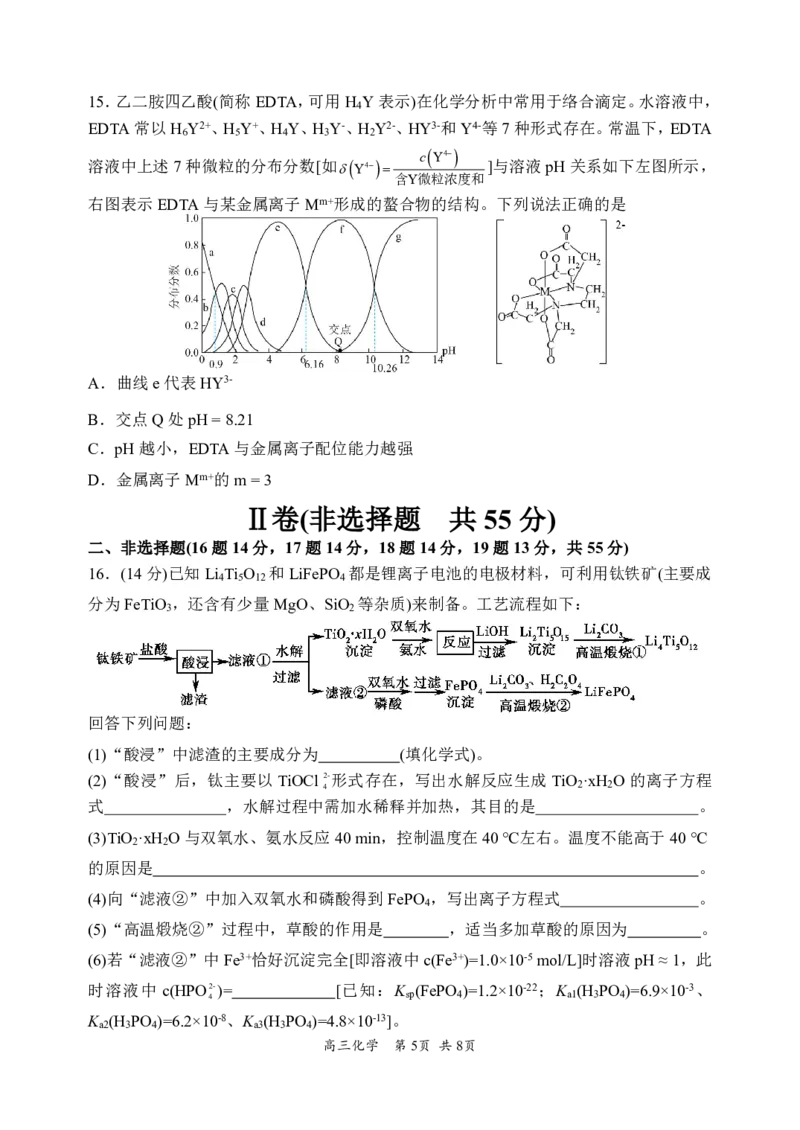
16.(14分)已知Li Ti O 和LiFePO 都是锂离子电池的电极材料,可利用钛铁矿(主要成
4 5 12 4
分为FeTiO ,还含有少量MgO、SiO 等杂质)来制备。工艺流程如下:
3 2
回答下列问题:
(1)“酸浸”中滤渣的主要成分为 (填化学式)。
(2)“酸浸”后,钛主要以TiOCl 2-形式存在,写出水解反应生成TiO ·xH O的离子方程
4 2 2
式 ,水解过程中需加水稀释并加热,其目的是 。
(3)TiO ·xH O与双氧水、氨水反应40min,控制温度在40℃左右。温度不能高于40℃
2 2
的原因是 。
(4)向“滤液②”中加入双氧水和磷酸得到FePO ,写出离子方程式 。
4
(5)“高温煅烧②”过程中,草酸的作用是 ,适当多加草酸的原因为 。
(6)若“滤液②”中Fe3+恰好沉淀完全[即溶液中c(Fe3+)=1.0×10-5mol/L]时溶液pH≈1,此
时溶液中 c(HPO2-)= [已知:K (FePO )=1.2×10-22;K (H PO )=6.9×10-3、
4 sp 4 a1 3 4
K (H PO )=6.2×10-8、K (H PO )=4.8×10-13]。
a2 3 4 a3 3 4
高三化学 第5页 共8页
{#{QQABBY6AogiIAAIAARhCAQGACAGQkAAACQgGxAAQMAAACAFABAA=}#}17.(14分)磺化聚苯乙烯可用于制作高性能离子交换膜。某研究小组探究乙酰基磺酸
(CH COOSO H)制备磺化聚苯乙烯的过程与效果。
3 3
实验Ⅰ.乙酰基磺酸的制备
向装有一定量二氯乙烷溶剂的烧杯中,加入7.6mL乙酸酐[(CH CO) O],控制溶液温度
3 2
在10℃以下,边搅拌边分批加入2.7mL浓硫酸,得到乙酰基磺酸溶液。
(1)制备过程中需使用的玻璃仪器有烧杯、温度计、 、 。
(2)乙酸酐与浓硫酸按物质的量之比1:1反应的化学方程式为 。
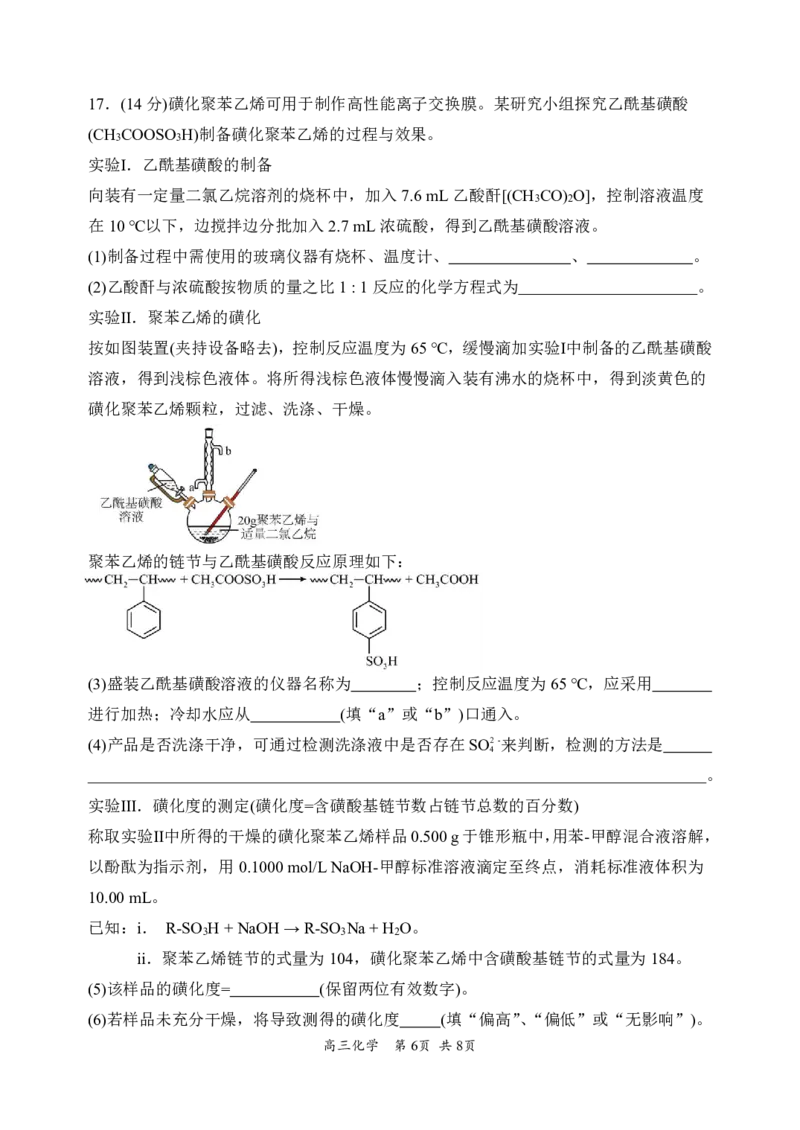
实验Ⅱ.聚苯乙烯的磺化
按如图装置(夹持设备略去),控制反应温度为65℃,缓慢滴加实验Ⅰ中制备的乙酰基磺酸
溶液,得到浅棕色液体。将所得浅棕色液体慢慢滴入装有沸水的烧杯中,得到淡黄色的
磺化聚苯乙烯颗粒,过滤、洗涤、干燥。
聚苯乙烯的链节与乙酰基磺酸反应原理如下:
(3)盛装乙酰基磺酸溶液的仪器名称为 ;控制反应温度为65℃,应采用
进行加热;冷却水应从 (填“a”或“b”)口通入。
(4)产品是否洗涤干净,可通过检测洗涤液中是否存在SO2-来判断,检测的方法是
4
。
实验Ⅲ.磺化度的测定(磺化度=含磺酸基链节数占链节总数的百分数)
称取实验Ⅱ中所得的干燥的磺化聚苯乙烯样品0.500g于锥形瓶中,用苯-甲醇混合液溶解,
以酚酞为指示剂,用0.1000mol/LNaOH-甲醇标准溶液滴定至终点,消耗标准液体积为
10.00mL。
已知:i. R-SO H+NaOH→R-SO Na+H O。
3 3 2
ii.聚苯乙烯链节的式量为104,磺化聚苯乙烯中含磺酸基链节的式量为184。
(5)该样品的磺化度= (保留两位有效数字)。
(6)若样品未充分干燥,将导致测得的磺化度 (填“偏高”、“偏低”或“无影响”)。
高三化学 第6页 共8页
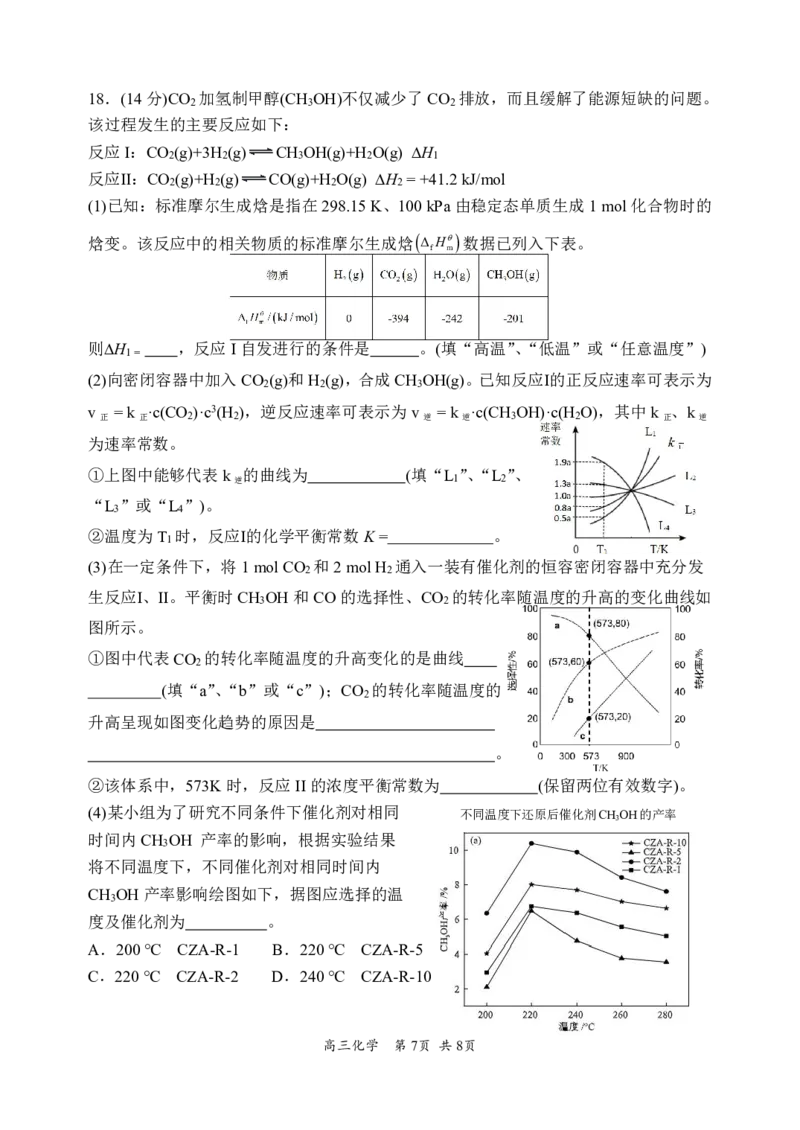
{#{QQABBY6AogiIAAIAARhCAQGACAGQkAAACQgGxAAQMAAACAFABAA=}#}18.(14分)CO 加氢制甲醇(CH OH)不仅减少了CO 排放,而且缓解了能源短缺的问题。
2 3 2
该过程发生的主要反应如下:
反应I:CO (g)+3H (g) CH OH(g)+H O(g) ∆H
2 2 3 2 1
反应Ⅱ:CO (g)+H (g) CO(g)+H O(g) ∆H =+41.2kJ/mol
2 2 2 2
(1)已知:标准摩尔生成焓是指在298.15K、100kPa由稳定态单质生成1mol化合物时的
焓变。该反应中的相关物质的标准摩尔生成焓
Δ
H数据已列入下表。
f m
则∆H ,反应I自发进行的条件是 。(填“高温”、“低温”或“任意温度”)
1=
(2)向密闭容器中加入CO (g)和H (g),合成CH OH(g)。已知反应Ⅰ的正反应速率可表示为
2 2 3
v =k ·c(CO )·c3(H ),逆反应速率可表示为v =k ·c(CH OH)·c(H O),其中k 、k
正 正 2 2 逆 逆 3 2 正 逆
为速率常数。
①上图中能够代表k 的曲线为 (填“L ”、“L ”、
逆 1 2
“L ”或“L ”)。
3 4
②温度为T 时,反应І的化学平衡常数K= 。
1
(3)在一定条件下,将1molCO 和2molH 通入一装有催化剂的恒容密闭容器中充分发
2 2
生反应І、II。平衡时CH OH和CO的选择性、CO 的转化率随温度的升高的变化曲线如
3 2
图所示。
①图中代表CO 的转化率随温度的升高变化的是曲线
2
(填“a”、“b”或“c”);CO 的转化率随温度的
2
升高呈现如图变化趋势的原因是
。
②该体系中,573K时,反应II的浓度平衡常数为 (保留两位有效数字)。
(4)某小组为了研究不同条件下催化剂对相同 不同温度下还原后催化剂CH3OH的产率
时间内CH OH 产率的影响,根据实验结果
3
将不同温度下,不同催化剂对相同时间内
CH OH产率影响绘图如下,据图应选择的温
3
度及催化剂为 。
A.200℃ CZA-R-1 B.220℃ CZA-R-5
C.220℃ CZA-R-2 D.240℃ CZA-R-10
高三化学 第7页 共8页
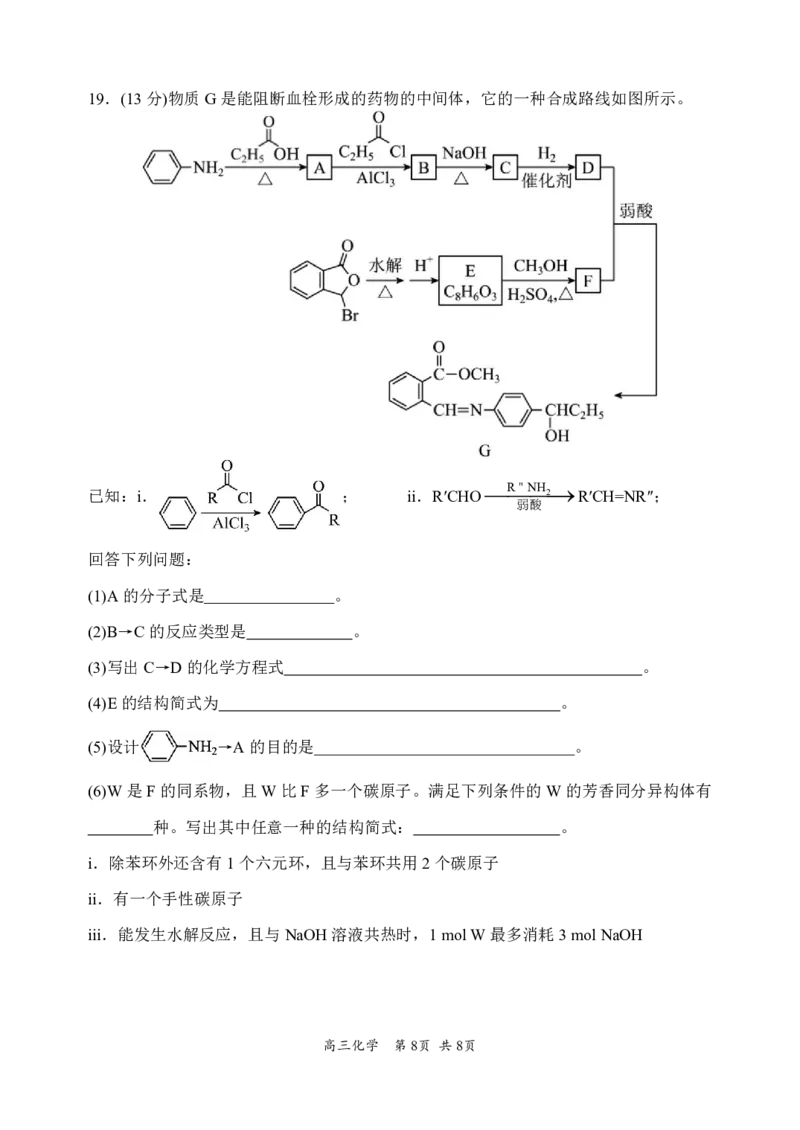
{#{QQABBY6AogiIAAIAARhCAQGACAGQkAAACQgGxAAQMAAACAFABAA=}#}19.(13分)物质G是能阻断血栓形成的药物的中间体,它的一种合成路线如图所示。
已知:i. ; ii.R′CHO R"NH 2 R′CH=NR″;
弱酸
回答下列问题:
(1)A的分子式是 。
(2)B→C的反应类型是 。
(3)写出C→D的化学方程式 。
(4)E的结构简式为 。
(5)设计 →A的目的是 。
(6)W是F的同系物,且W比F多一个碳原子。满足下列条件的W的芳香同分异构体有
种。写出其中任意一种的结构简式: 。
i.除苯环外还含有1个六元环,且与苯环共用2个碳原子
ii.有一个手性碳原子
iii.能发生水解反应,且与NaOH溶液共热时,1molW最多消耗3molNaOH
高三化学 第8页 共8页
{#{QQABBY6AogiIAAIAARhCAQGACAGQkAAACQgGxAAQMAAACAFABAA=}#}