文档内容
2024-2025 学年高二化学上学期期中模拟卷
(考试时间:60分钟 试卷满分:100分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证
号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:第一章~第三章第2节(人教版2019选择性必修1)。
5.难度系数:0.68
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16
第Ⅰ卷(选择题 共 36 分)
一、选择题:本题共12个小题,每小题3分,共36分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.关于化学反应与能量的说法正确的是
A.需要加热的反应都是吸热反应
B.反应物总能量与生成物总能量一定相等
C.断裂化学键要吸收能量
D.燃烧热指的是101kPa时,1mol纯物质完全燃烧生成氧化物时所放出的热量
【答案】C
【解析】A.有的放热反应需要高温条件发生,如铝热反应是放热反应,但需要加热,故A错误;B.化
学反应过程中一定伴随能量的变化,反应物总能量与生成物总能量一定不相等,故B错误;C.形成化学
键放出能量,则断裂化学键需要吸收能量,故C正确;D.燃烧热指的是101kPa时,1mol纯物质完全燃烧
生成稳定的氧化物时所放出的热量,故D错误;答案选C。
2.下列推论正确的是
A. ,则含49 g硫酸的稀硫酸与稀氨水完全反应,放出的
热量小于57.4 kJ
B. ,则碳的燃烧热
C. , ,则 <
D. ,△S>0,则该反应在任何温度下都能自发进行
【答案】A
【解析】A.中和热为稀的强酸和稀的强碱完全反应生成1mol水时放出的热量为57.4kJ,一水合氨是弱
学科网(北京)股份有限公司 学科网(北京)股份有限公司碱,在溶液中的电离时需要是吸热过程,则含49g硫酸的稀硫酸与稀氨水完全反应,放出的热量小于
57.4kJ,故A正确;B.碳的燃烧热为1mol碳完全燃烧生成二氧化碳放出的热量,1mol碳不完全燃烧释放
的能量是110.5kJ,则碳的燃烧热△H小于—110.5k·mol-1,故B错误;C.硫燃烧的反应为放热反应,固态
硫的能量小于气态硫,则固态硫燃烧的反应热△H 大于气态硫燃烧的反应热△H,故C错误;D.该反应
1 2
是熵增的吸热反应,高温条件下反应△H—T△S<0,则反应能自发进行,故D错误;故选A。
3.对于反应 ,下列各数据表示不同条件下的反应速率,其中反应进行得最快的是
A. B.
C. D.
【答案】A
【解析】比较反应率要求单位统一,按照速率比等于系数比转化为同一物质进行比较,我们把速率都转化
为A的反应速率进行比较,A中 ,B中反应速率v(A)= v(B)= ,C中
v(A)= v(C)= ,D中v(A)= v(C)= =0.05mol·L-1·s-1,经过比较,A选项中
反应速率最大;答案选A。
4.常温下0.1mol/L醋酸溶液中存在电离平衡:CH
3
COOH⇌H++CH
3
COO-,下列叙述不正确的是
A.溶液加水稀释或加热均可使CHCOO-的物质的量增多
3
B.溶液中加入少量纯醋酸,平衡向右移动,电离程度增大
C.溶液加水稀释,c(CHCOO-)/[c(CH COOH)・c(OH-)]不变
3 3
D.溶液加水稀释后,溶液中c(CHCOOH)/c(CH COO-)的值减小
3 3
【答案】B
【解析】A.CHCOOH 溶液加水稀释或加热,平衡正向移动,均可使CHCOO-的物质的量增多,A正
3 3
确;B.CHCOOH溶液中加入少量纯醋酸,平衡向右移动,电离程度减小,B错误;C.CHCOOH 溶液
3 3
加水稀释, ,为常数,始终不变,C正确;D.CHCOOH溶液加水稀释,平衡
3
正向移动,醋酸的物质的量减小,醋酸根的物质的量增加,溶液中 ,故比
值减小,D正确;答案选B。
5.实验室利用下列方案探究影响化学反应速率的因素,已知:2 +5HC O+6H+=2Mn2++10CO↑+
2 2 4 2
8HO,有关说法不正确的是
2
实验编号 温度/℃ 酸性KMnO 溶液 草酸(H C O)溶液
4 2 2 4
4 mL 0.01 mol·L- 12 mL 0.01 mol·L-
① 25
1 1
学科网(北京)股份有限公司 学科网(北京)股份有限公司4 mL 0.01 mol·L- 12 mL 0.02 mol·L-
② a
1 1
4 mL 0.01 mol·L- 12 mL 0.01 mol·L-
③ 50
1 1
12 mL 0.01 mol·L-
④ b c
1
A.a=25,实验①②探究的是浓度对于化学反应速率的影响
B.实验①③探究的是温度对化学反应速率的影响
C.实验中需记录溶液颜色变化所需时间
D.若b=25,c=4 mL 0.02 mol·L-1,则实验①④也可用于化学反应速率影响因素的探究
【答案】D
【分析】酸性KMnO 溶液与草酸(H C O)溶液反应生成CO 和锰离子,通过高锰酸钾溶液褪色所需要的时
4 2 2 4 2
间研究影响化学反应速率的因素,所以实验中高锰酸钾钾溶液的浓度应该为定值,控制变量法研究影响化
学反应速率的因素时,只能有一个变量,其它量必须相等。
【解析】A.实验①②研究草酸的浓度对化学反应速率的影响,则温度应该相同,即a=25,故A正确;
B.实验①③中温度不同,c(KMnO )、c(HC O)均相同,故实验①③探究的是温度对化学反应速率的影
4 2 2 4
响,故B正确;C.由于实验过程中酸性KMnO 溶液的浓度相同,通过高锰酸钾钾溶液褪色所需要的时间
4
反映化学反应速率,则实验中需记录溶液颜色变化所需时间,故C正确;D.若b=25,
c=4mL0.02mol•L-1,则实验④中KMnO 过量,溶液无法褪色,则实验①④不能用于化学反应速率影响因素
4
的探究,故D错误。答案选D。
6.下列有关工业合成氨反应: 的说法不正确的是
A.合成氨采取循环操作目的是提高氮气和氢气的利用率
B.除原料气中CO反应: ,适宜低温
高压环境
C.合成塔压强调控在10MPa~30MPa之间,是对生产设备条件和经济成本的综合考虑结果
D.合成塔使用热交换控制体系温度400~500℃左右,主要目的是有利于平衡正向移动
【答案】D
【解析】A.合成氨反应为可逆反应,氮气和氢气不能完全转化为产物NH ,采取循环操作能提高氮气和
3
氢气的利用率,A正确;B.该反应为气体体积减小的放热反应,降低温度或增大压强,均能使平衡正向
移动,故除原料气中CO适宜低温高压环境,B正确;C.增大压强有利于氨的合成,但是压强过大会增加
设备成本,因此合成塔压强调控在10MPa~30MPa之间,是对生产设备条件和经济成本的综合考虑结果,C
正确;D.合成塔使用热交换控制体系温度400~500℃左右,主要目的是使催化剂铁触媒的活性达到最佳
状态,D错误;故选D。
7.将3molA和2.5molB充入2L的恒容密闭容器中,发生的反应:3A(g)+B(g) C(g)+2D(g),5min后反
学科网(北京)股份有限公司 学科网(北京)股份有限公司应达到平衡,测得D的平均反应速率为0.1mol/(L·min),下列结论正确的是
A.A的平均反应速率为0.1mol/(L·min) B.平衡时,C的浓度为0.125mol/L
C.平衡时, 的转化率为 D.平衡时,容器内压强为原来的0.8倍
【答案】C
【分析】5min后反应达到平衡时,D的平均反应速率为0.1mol/(L·min),则D的物质的量为0.1mol/(L·min)
×5min×2L=1mol,由题意可建立如下三段式:
【解析】A.由反应速率之比等于化学计量数之比可知,A的平均反应速率为0.1mol/(L·min) ×
=0.15mol/(L·min),故A错误;B.由三段式数据可知,C的浓度为 =0.25mol/L,故B错误;C.由
三段式数据可知,B的转化率为 ×100%=20%,故C正确;D.由平衡时,容器内压强为可知,平衡
时,容器内压强之比等于气体物质的量之比 = ,故D错误;故选C。
8.向稀氨水中分别加入①蒸馏水、②NH 、③NH Cl(s),并维持室温,相关判断正确的是
3 4
A.加入①之后, 的电离平衡得到促进, 减小
B.加入②之后, 的电离平衡正向移动,电离程度增大
C.加入③之后, 增大, 维持不变
D.升高温度, 的电离平衡得到促进, 减小
【答案】C
【解析】A.加入蒸馏水之后,氨水的电离平衡得到促进,c(OH-)减小,电离常数不变,
, 增大,A错误;B.通入氨气之后,氨水的电离平衡正移,
NH ·H O的电离程度减小,B错误;C.加入固体氯化铵之后,铵根离子浓度增大,氨水的电离平衡逆
3 2
移, 增大, ,温度不变,比值维持不变,C正确;D.电离吸热,升高
温度, 的电离平衡得到促进, 增大,D错误;故选C。
9.水的电离过程为H
2
O⇌H++OH﹣,在不同温度下其离子积为K
w
(25℃)=1.0×10-14,K
w
(35℃)=2.1×10-14,则
学科网(北京)股份有限公司 学科网(北京)股份有限公司下列叙述正确的是
A.c(H+)随着温度的升高而降低
B.在35℃的纯水中时,c(H+)>c(OH﹣)
C.水的电离常数K (25℃)>K (35℃)
w w
D.水的电离是一个吸热过程
【答案】D
【解析】A.水的电离为吸热的过程,升高温度,促进水的电离,c(H+)逐渐增大,A错误;B.纯水为中
性物质,说明c(H+)=c(OH﹣),B错误;C.根据题干信息可知,水的电离常数K (25℃)<K (35℃),C错
w w
误;D.随着温度升高,水的离子积常数逐渐增大,说明升高温度促进水的电离,则水的电离为吸热过
程,D正确;答案选D。
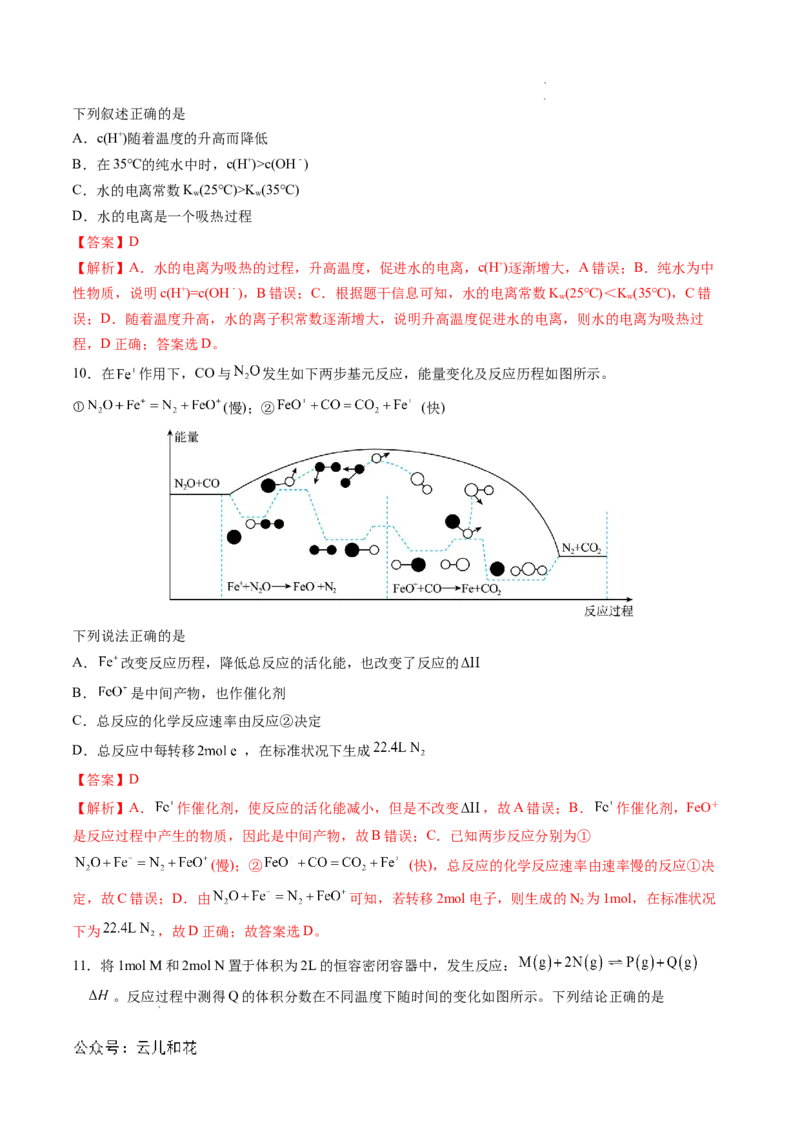
10.在 作用下,CO与 发生如下两步基元反应,能量变化及反应历程如图所示。
① (慢);② (快)
下列说法正确的是
A. 改变反应历程,降低总反应的活化能,也改变了反应的
B. 是中间产物,也作催化剂
C.总反应的化学反应速率由反应②决定
D.总反应中每转移 ,在标准状况下生成
【答案】D
【解析】A. 作催化剂,使反应的活化能减小,但是不改变 ,故A错误;B. 作催化剂,FeO+
是反应过程中产生的物质,因此是中间产物,故B错误;C.已知两步反应分别为①
(慢);② (快),总反应的化学反应速率由速率慢的反应①决
定,故C错误;D.由 可知,若转移2mol电子,则生成的N 为1mol,在标准状况
2
下为 ,故D正确;故答案选D。
11.将1mol M和2mol N置于体积为2L的恒容密闭容器中,发生反应:
。反应过程中测得Q的体积分数在不同温度下随时间的变化如图所示。下列结论正确的是
学科网(北京)股份有限公司 学科网(北京)股份有限公司A. B.温度:
C.温度为 时,M的平衡转化率为50% D.若X、Y两点的平衡常数分别为 、 ,则K c( )+c(OH-)
3
B.点②溶液中:c(Na+)=c(N )+c(HN )
3
C.常温下,K(HN )的数量级为10-4
a 3
D.点③溶液中:c(OH-)=c(H+)+c(HN )
3
【答案】D
【解析】A.点①溶液为HN 与NaN 等浓度的混合溶液,根据电荷守恒可得c(Na+)+c(H+)=c( )+c(OH-),
3 3
学科网(北京)股份有限公司 学科网(北京)股份有限公司溶液pH<7,说明HN 的电离作用大于N的水解作用,所以c(HN )<c(Na+),所以c(HN )+c(H+)<c( )
3 3 3
+c(OH-),故A项错误;
B.点②溶液中存在电荷守恒:c(Na+)+c(H+)=c( )+c(OH-),该点溶液pH=7,则c(H+)= c(OH-),所以
c(Na+)=c( ),则c(Na+)<c( )+c(HN),故B项错误;
3
C.在常温下,0.1 mol/L HN 的pH=2.85,则c(H+)=10-2.85mol/L,K(HN )=
3 a 3
,故K(HN )的数量级为10-5,故C项错误;
a 3
D.点③溶液为NaN 溶液,根据质子守恒可得:c(OH-)=c(H+)+c(HN),故D项正确;
3 3
故本题选D。
第 II 卷(非选择题 共 64 分)
二、非选择题:本题共4个小题,共64分。
13.(14分)回答下列问题。
(1)已知C(石墨,s)=C(金刚石,s)ΔH>0,则稳定性:金刚石 石墨(填“>”“<”)。
(2)甲醇(CHOH)的合成与应用具有广阔的发展前景。
3
在催化剂的作用下,200~300℃时,可用CO 和H 合成CHOH,该反应一般认为可通过如下两个步骤来实
2 2 3
现:
①
②
合成甲醇的热化学方程式为 ;若反应①为慢反应,下列示意图中能体现上述反应能
量变化的是 (填标号)。
(3)向恒容密闭容器中加入适量催化剂,并充入一定量的 和 合成甲醇,经相同反应时间测得
的转化率 与反应温度的变化关系如图所示。
学科网(北京)股份有限公司 学科网(北京)股份有限公司①温度为 时, 的转化率升高,可能原因是 。
②温度为 时, 的转化率降低,可能原因是 。
(4)已知拆开1molH-H键、1molN-H键、1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N 与
2
H 反应生成NH 的热化学方程式是 。
2 3
【答案】(除标明外,每空2分)
(1)<
(2) = (3分) C
(3)反应未达平衡,由 到 温度升高,反应速率加快, 的转化率升高 反应已达平衡,该可逆
反应正反应放热,由 到 温度升高,化学平衡逆向移动, 的转化率降低
(4)N(g)+3H(g) 2NH (g) ΔH=-92 kJ·mol-1(3分)
2 2 3
【解析】(1)焓变为正,为吸热反应,可知石墨能量低,则稳定性:金刚石<石墨,故答案为:<;
(2)根据盖斯定律,合成甲醇的热化学方程=反应①+反应②,即
,而 ;
间接法制备甲醇的反应①吸热,反应②放热,总体放热,反应①活化能较大,C符合题意;
(3)①温度升高反应速率变快所以原因为:反应未达平衡,由T 到T 温度升高,反应速率加快,CO 的
1 2 2
转化率升高;
②反应在T 时达到平衡,且反应为放热反应所以反应已达平衡,该可逆反应正反应放热,由T 到T 温度
2 2 3
升高,化学平衡逆向移动,CO 的转化率降低;
2
(4)在反应 中,断裂3mol H-H键,1mol 键共吸收的能量为:
3×436kJ+946kJ=2254kJ,生成2mol NH ,共形成6mol N-H键,放出的能量为:6×391kJ=2346kJ,吸收的
3
热量少,放出的热量多,该反应为放热反应,放出的热量为:2346kJ-2254kJ=92kJ,故答案为:
。
14.(16分)某课外兴趣小组用 的NaOH标准溶液滴定未知浓度的盐酸溶液,实验操作如
下:①向溶液中加入1~2滴指示剂;②取25.00mL待测溶液放入锥形瓶中;③用氢氧化钠溶液滴定至终
点;④重复以上操作;⑤配制250mL NaOH标准溶液;⑥根据实验数据计算盐酸的物质的量浓度。回答下
列问题:
(1)实验过程中正确的操作顺序是 (填序号),该滴定实验所选指示剂为 。
学科网(北京)股份有限公司 学科网(北京)股份有限公司(2)判断达到滴定终点方法是 。
(3)用上述 的NaOH标准溶液滴定未知浓度的盐酸溶液,读取标准液时,滴定前仰视读
数,滴定后俯视读数,其他操作正确,待测液的浓度 (填“偏大”或“偏小”)。
(4)该小组某一次滴定操作中,碱式滴定管的始终液面如图所示,则本次滴入的NaOH溶液的体积为
mL。
(5)该小组学生某4次实验的有关数据分别记录如表:
NaOH的体积
滴定次数 待测HCl溶液
滴定前刻度 滴定后刻度
第一次 25.00 2.10 28.01
第二次 25.00 1.66 30.50
第三次 25.00 0.25 26.34
第四次 25.00 0 26.00
某同学在处理数据过程中计算得到平均消耗NaOH溶液的体积
。他的计算 (填“合理”或“不合
理”),理由是 。依据表中数据列式计算该HCl溶液的物质的量浓度为 。
【答案】(除标明外,每空2分)
(1)⑤②①③④⑥ 酚酞试液
(2)滴入最后半滴氢氧化钠溶液,指示剂变为浅粉色,且半分钟不褪色
(3)偏小
(4)26
(5)不合理(1分) 第二次滴定时消耗溶液的体积明显偏大,该值应舍去 0.1040mol/L(3分)
【分析】通过设计酸碱中和滴定实验进行滴定测定,并分析滴定误差,计算待测液浓度,据此作答。
【解析】(1)实验操作顺序为:⑤配制250mL标准溶液;②取25.00mL待测溶液放入锥形瓶中;①向溶
液中加入1~2滴指示剂;③用氢氧化钠溶液滴定至终点;④重复以上操作;⑥根据实验数据计算盐酸的物
质的量浓度;该滴定实验为强酸强碱的滴定,所选指示剂为酚酞试液(或甲基橙溶液),答案:
⑤②①③④⑥、酚酞试液;
(2)滴定终点方法为滴入最后半滴氢氧化钠溶液,指示剂变为浅粉色,且半分钟不褪色;
(3)读取标准液时,滴定前仰视读数,滴定后俯视读数,其他操作正确,则标准液的体积读数偏小,测
得待测液的浓度偏小;
学科网(北京)股份有限公司 学科网(北京)股份有限公司(4)根据图中读数进行计算,本次滴入的盐酸体积为26.00mL-0.00mL=26.00mL;
(5)根据4次实验的有关数据可知消耗NaOH溶液的体积分别为28.01mL-2.10 mL=25.91mL、
30.50mL-1.66 mL=28.84mL、26.34mL-0.25mL=26.09mL,26.00mL-0.00 mL=26.00mL,第二次滴定时消耗溶
液的体积明显偏大,该值应舍去,平均体积为26.00mL,计算该HCl溶液的物质的量浓度为
=
0.1040mol/L,答案:不合理;第二次滴定时消耗溶液的体积明显偏大,该值应舍去;0.1040mol/L。
15.(17分)回答下列问题:
(1)已知室温时,0.1 mol·L-1某一元酸CHCOOH在水中有0.1%发生电离,回答下列问题:
3
①该溶液中c(H+)=__________mol·L-1。
②CH COOH的电离平衡常数K=____________。
3
③由水电离出来的c(H+)=__________mol·L-1。
④某温度,纯水中c(H+)=3.0×10-7 mol·L-1,此时在水加入稀硫酸至c(H+)为1.0×10-5 mol·L-1,则此时
溶液中的c(OH-)=__________mol·L-1。
(2)部分弱酸的电离平衡常数如下表:
弱酸 HCOOH HCO HClO
2 3
电离平衡常数/25℃ K=1.77×10-4 K =4.4×10-7,K =4.7×10-11 K=3.0×10-8
1 2
①在相同浓度的HCOOH和HClO的溶液中,溶液导电能力:HCOOH______HClO(填“>”“<”或
“=”,下同);在相同浓度的CO2-和ClO-的溶液中,结合H+的能力CO2-______ClO-。
3 3
②HCO -的电离平衡常数表达式为_____________________。
3
③将少量CO 气体通入NaClO溶液中,写出该反应离子方程式____________________________。
2
【答案】(除标明外,每空2分)
(1)1.0×10-4 1.0×10-7 1.0×10-10 9.0×10-9
(2)> > K= CO+ClO-+HO=HCO -+HClO(3分)
2 2 3
【解析】(1)①0.1 mol·L-1某一元酸CHCOOH在水中有0.1%发生电离,该溶液中c(H+)=0.1 mol·L-
3
1×0.1%=1.0×10-4 mol·L-1;②CHCOOH H++CHCOO-的电离平衡常数K=≈=1.0×10-7;③该溶
3 3
液中H+由CHCOOH电离和水电离之和,由水电离出来的c(H+) =c(OH-) ≈=1.0×10-10;④某温度,纯
3 水 水
水中c(H+)=3.0×10-7 mol·L-1,K =c(H+)×c(OH-)=3.0×10-7×3.0×10-7=9.0×10-14;在水加入稀硫酸至
w
c(H+)为1.0×10-5 mol·L-1,则此时溶液中的c(OH-)===9.0×10-9;(2)①已知K(HCOOH)=1.77×10-
4,K(HClO)=3.0×10-8,所以在相同浓度的HCOOH和HClO的溶液中,HCOOH溶液中离子浓度更大,溶
液导电能力更强;酸性越强相应的结合氢离子的能力越弱,K (H CO)=4.7×10-11,在相同浓度的CO2-和
2 2 3 3
ClO-的溶液中,结合H+的能力CO2->ClO-;故答案为>;>;②HCO - H++CO2-,HCO -的电
3 3 3 3
离平衡常数表达式为K=;③已知K (H CO)>K(HClO)>K (HCO -),将少量CO 气体通入NaClO溶液
1 2 3 2 3 2
中,写出该反应离子方程式CO+ClO-+HO=HCO -+HClO。
2 2 3
16.(17分)随着我国碳达峰、碳中和目标的确定,二氧化碳资源化利用倍受关注。
学科网(北京)股份有限公司 学科网(北京)股份有限公司Ⅰ.以CO 和NH 为原料合成尿素2NH gCO g ⇌ CONH sH OgΔH 87kJ/mol。
2 3 3 2 2 2 2
(1)有利于提高CO 平衡转化率的措施是 (填序号)。
2
A.高温低压 B.低温高压 C.高温高压
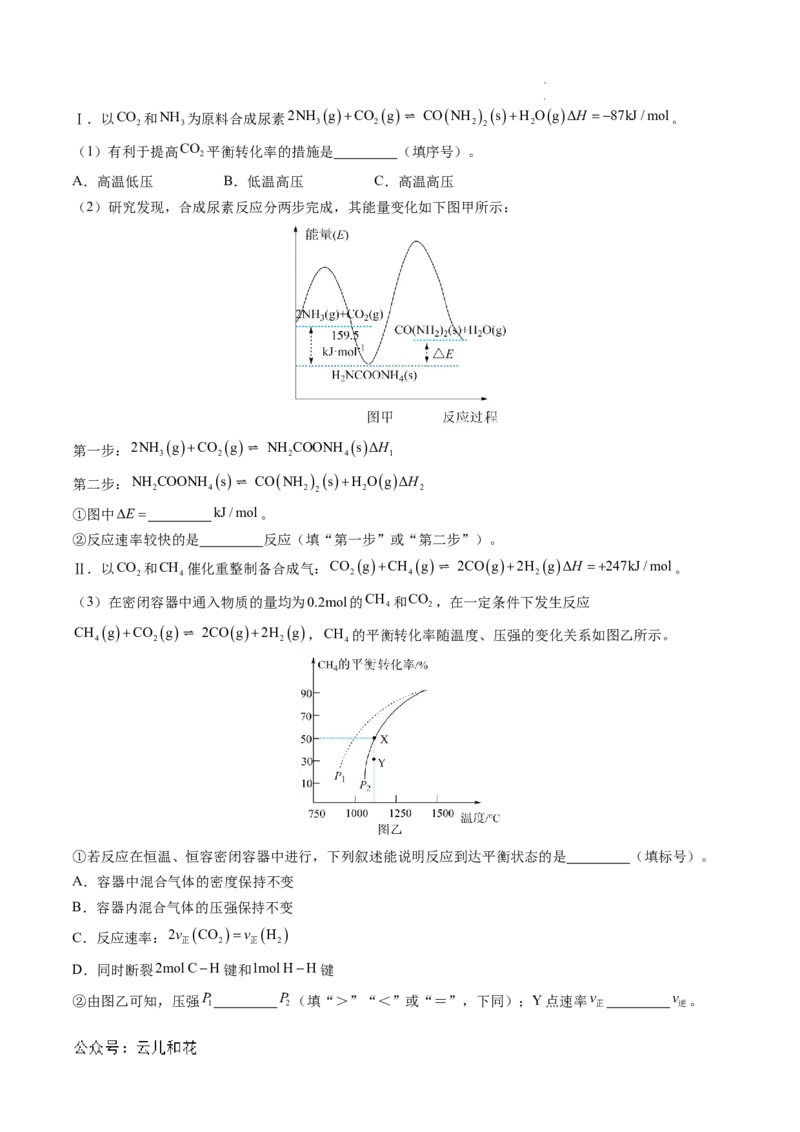
(2)研究发现,合成尿素反应分两步完成,其能量变化如下图甲所示:
第一步:2NH gCO g ⇌ NH COONH sΔH
3 2 2 4 1
第二步:NH COONH s ⇌ CONH sH OgΔH
2 4 2 2 2 2
①图中E kJ/mol。
②反应速率较快的是 反应(填“第一步”或“第二步”)。
Ⅱ.以CO 和CH 催化重整制备合成气:CO gCH g ⇌ 2COg2H gΔH 247kJ/mol。
2 4 2 4 2
(3)在密闭容器中通入物质的量均为0.2mol的CH 和CO ,在一定条件下发生反应
4 2
CH gCO g ⇌ 2COg2H g ,CH 的平衡转化率随温度、压强的变化关系如图乙所示。
4 2 2 4
①若反应在恒温、恒容密闭容器中进行,下列叙述能说明反应到达平衡状态的是 (填标号)。
A.容器中混合气体的密度保持不变
B.容器内混合气体的压强保持不变
C.反应速率:2v CO v H
正 2 正 2
D.同时断裂2mol CH键和1mol HH键
②由图乙可知,压强P P (填“>”“<”或“=”,下同);Y点速率v v 。
1 2 正 逆
学科网(北京)股份有限公司 学科网(北京)股份有限公司③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数K ,则X
p
点对应温度下的K (用含P 的代数式表示)。
p 2
(4)同温下,某研究小组分别在容积相等的两个恒容密闭容器中加入一定量的反应物,控制反应条件使
其仅发生CH CO 重整反应,获得如下效据:
4 2
起始时各物质的物质的量/mol
容器 CH 平衡转 达到平衡时体系 达到平衡时体系能量的
4
编号 CH CO CO H 化率 的压强/MPa 变化
4 2 2
i 1 2 0 0 P 吸收热量:123.5kJ
ii 2 4 0 0
①容器i中反应达到平衡时,生成CO的物质的量为 ,容器ii中反应达到平衡状态过程中吸收的
热量 247kJ(填“>”、“<”或“=”)。
②容器i的容积变为原来的一半,则CH 平衡转化率 (填“>”“<”或“=”)。
4
【答案】(除标明外,每空2分)
(1)B
(2)①72.5 ②第一步(1分)
4
(3)①BD ② <(1分) >(1分) ③ p2
9 2
(4)①1mol < ②=
【解析】(1)由2NH gCO g ⇌ CONH sH OgΔH87kJ/mol可知,该正反应方向为气
3 2 2 2 2
体体积减小的放热反应,因此低温高压有利于平衡正向移动,二氧化碳的转化率提高,故选B。
(2)①已知2NH
3
gCO
2
g ⇌ CONH
2
2
sH
2
OgΔH87kJ/mol,由图可知,E=
159.5kJ/mol-87kJ/mol=72.5kJ/mol;
②由图可知,第一步的活化能比第二步小,活化能越小,反应速率越快,则反应速率较快的是第一步反
应。
(3)①A.在恒温、恒容密闭容器中发生CH gCO g ⇌ 2COg2H g ,参加反应的各组分都是
4 2 2
气体,密度不变不能说明反应达到平衡,A错误;B.反应正向气体体积增大,恒容容器中,压强随着反
应正向进行而增大,压强不变时说明各组分的含量不再变化反应达到平衡,B正确;C.v CO 和
正 2
v H 均表示正反应速率,化学反应速率之比等于化学计量数之比,任意时刻都有2v CO =v H ,
正 2 正 2 正 2
不能说明反应达到平衡,C错误;D.断裂2molC-H键时生成1molH-H键,同时又断裂1molH-H键,正反
应速率等于逆反应速,反应达到平衡,D正确;故选BD;
②CH gCO g ⇌ 2COg2H g 反应正向气体体积增大,增大压强,平衡逆向移动,甲烷的转化
4 2 2
率减小,结合图中信息可知,pv ;
1 2 正 逆
学科网(北京)股份有限公司 学科网(北京)股份有限公司③X点对应温度下甲烷的平衡转化率为50%,可列三段式:
CH g CO g ⇌ 2COg 2H g
4 2 2
起始mol 0.2 0.2 0 0
转化mol 0.1 0.1 0.2 0.2
平衡mol 0.1 0.1 0.2 0.2
0.2 2 0.2 2
p p
0.1+0.1+0.2+0.2 2 0.1+0.1+0.2+0.2 2 4
平衡常数K= = p2。
p 0.1 0.1 9 2
p p
0.1+0.1+0.2+0.2 2 0.1+0.1+0.2+0.2 2
(4)①已知CH (g)+CO (g)=2COg+2H (g)△H=+247kJ/mol,即生成2molCO时放出247kJ热量,容器ⅰ
4 2 2
放出热量123.5kJ,即生成的CO为1mol;容器ii的投料为容器ⅰ的2倍,在恒温恒容的容器中相当于增大
压强,平衡会逆向移动,即生成CO小于2mol,所以放出的热量会小于247kJ;
②容器ⅰ的体积若变成原来的一半,则与容器ii的压强相等,二者为等效平衡,故转化率等于容器ii。
学科网(北京)股份有限公司 学科网(北京)股份有限公司