文档内容
化学试卷
2024-2025 学年下期高 2025 届测试
化 学
考试时间:75分钟 试卷总分:100分
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Ni—59 Zn—65 Ag—108
一、选择题:(本大题共15小题,每题只有一个选项符合题意,每题3分,共45分)
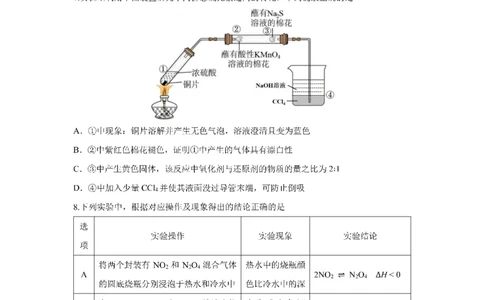
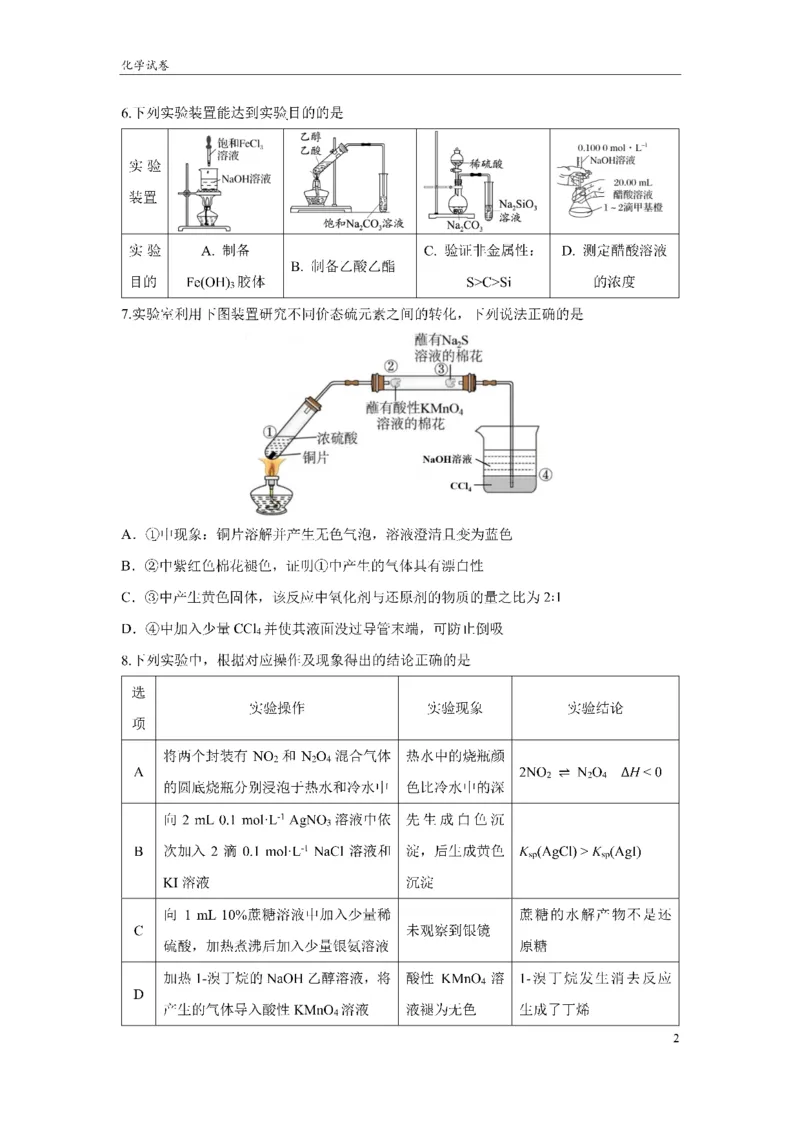
1.化学在生活中有重要作用。下列说法错误的是
A. 味精(谷氨酸钠)可用作食品增味剂 B. 乙醇用于杀菌消毒原理是使微生物蛋白质变性
C. 聚乙烯可用于制作食品包装袋 D. 制作矿泉水瓶的聚酯纤维是纤维素的一种
2.下列化学用语或图示表达正确的是
A.HCl的sp σ电子云: B. 次氯酸的结构式: H—Cl—O
C. 的习惯命名:邻羟基甲苯 D.NH 的VESPR模型:
3
3.下列离子方程式或电极反应式书写正确的是
A.CuSO 溶液除去H S气体:Cu2+ + H S == CuS↓ + 2H+
4 2 2
B. 氨气通入硝酸中反应: 5NH + 3NO— +3H+ == 4N + 9H O
3 3 2 2
C. 中性海水中吸氧腐蚀的正极反应:O + 4H+ + 4e == 2H O
2 2
D. 氯气与水反应:Cl + H O ⇌ 2H+ + Cl— + ClO—
2 2
4.右图表示含某短周期主族元素 X 物质的类别与化合价的对应关系。自然界中的 X 主要存
在于海水中。下列说法错误的是
A.NaX固体与浓硫酸共热可制取a
B.b能使鲜花褪色,说明单质b具有漂白性
C.c的化学式为X O,是d(HXO)的酸酐
2
D.e阴离子XO—的空间构型为正四面体形
4
5.七叶亭是一种植物抗菌素(结构如右图),该分子所有原子共平面。下列说法正确的是
A. 该分子共含有4种官能团
B.1 mol该物质与足量溴水反应,最多消耗2 mol Br
2
C.1 mol该物质与足量氢气反应,最多消耗2 mol H
2
D. 该分子中所有碳原子均为sp2杂化
1化学试卷
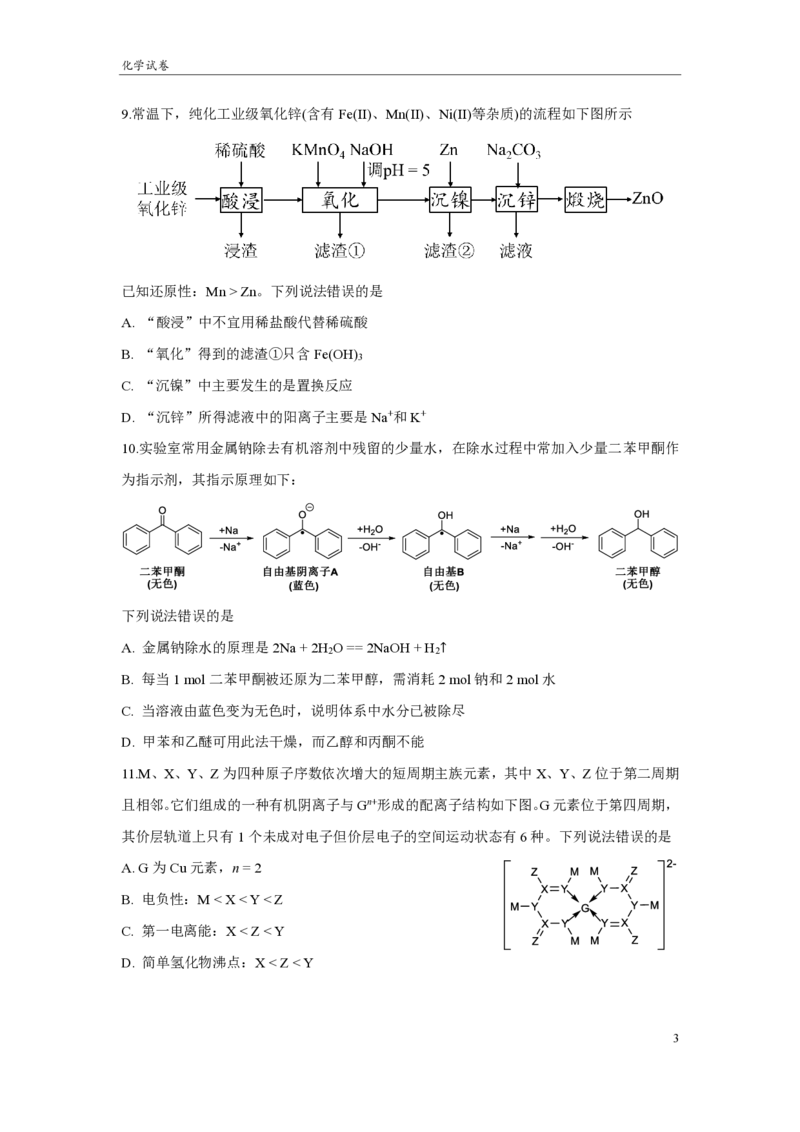
9.常温下,纯化工业级氧化锌(含有Fe(II)、Mn(II)、Ni(II)等杂质)的流程如下图所示
已知还原性:Mn > Zn。下列说法错误的是
A. “酸浸”中不宜用稀盐酸代替稀硫酸
B. “氧化”得到的滤渣①只含Fe(OH)
3
C. “沉镍”中主要发生的是置换反应
D. “沉锌”所得滤液中的阳离子主要是Na+和K+
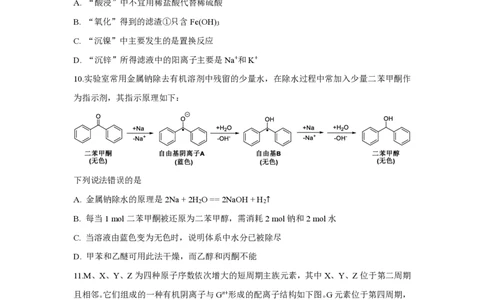
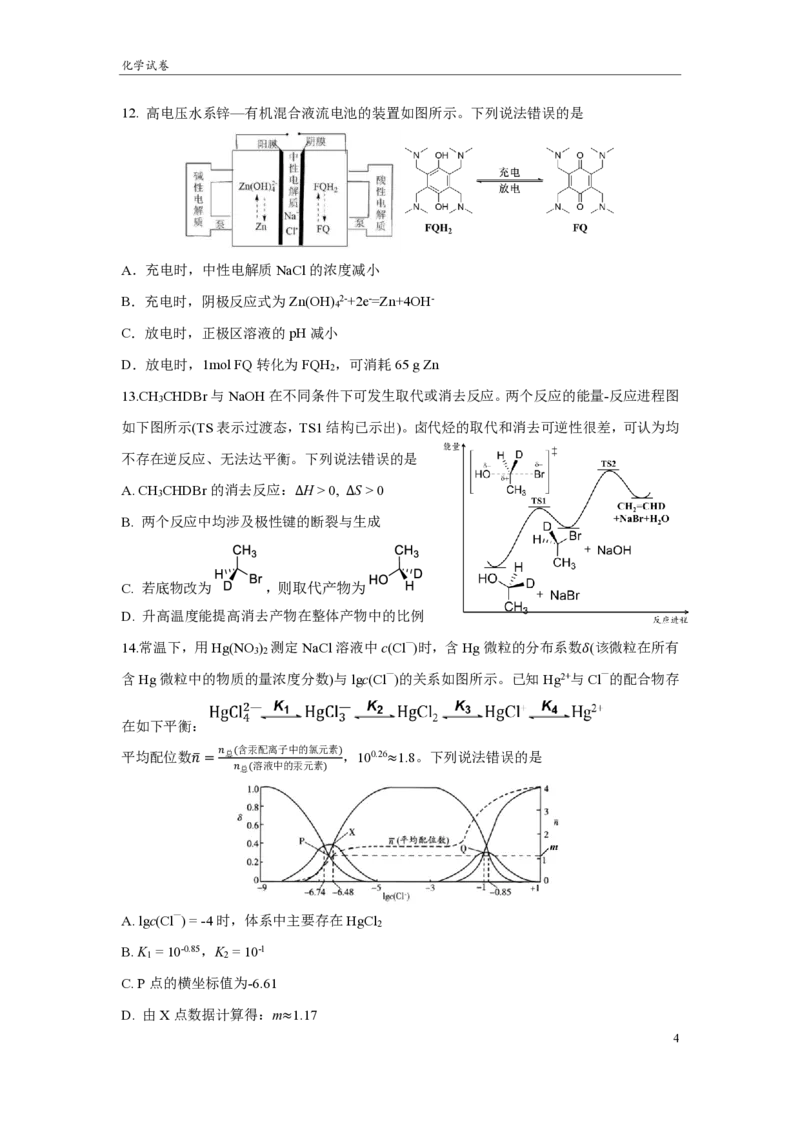
10.实验室常用金属钠除去有机溶剂中残留的少量水,在除水过程中常加入少量二苯甲酮作
为指示剂,其指示原理如下:
下列说法错误的是
A. 金属钠除水的原理是2Na + 2H O == 2NaOH + H ↑
2 2
B. 每当1 mol二苯甲酮被还原为二苯甲醇,需消耗2 mol钠和2 mol水
C. 当溶液由蓝色变为无色时,说明体系中水分已被除尽
D. 甲苯和乙醚可用此法干燥,而乙醇和丙酮不能
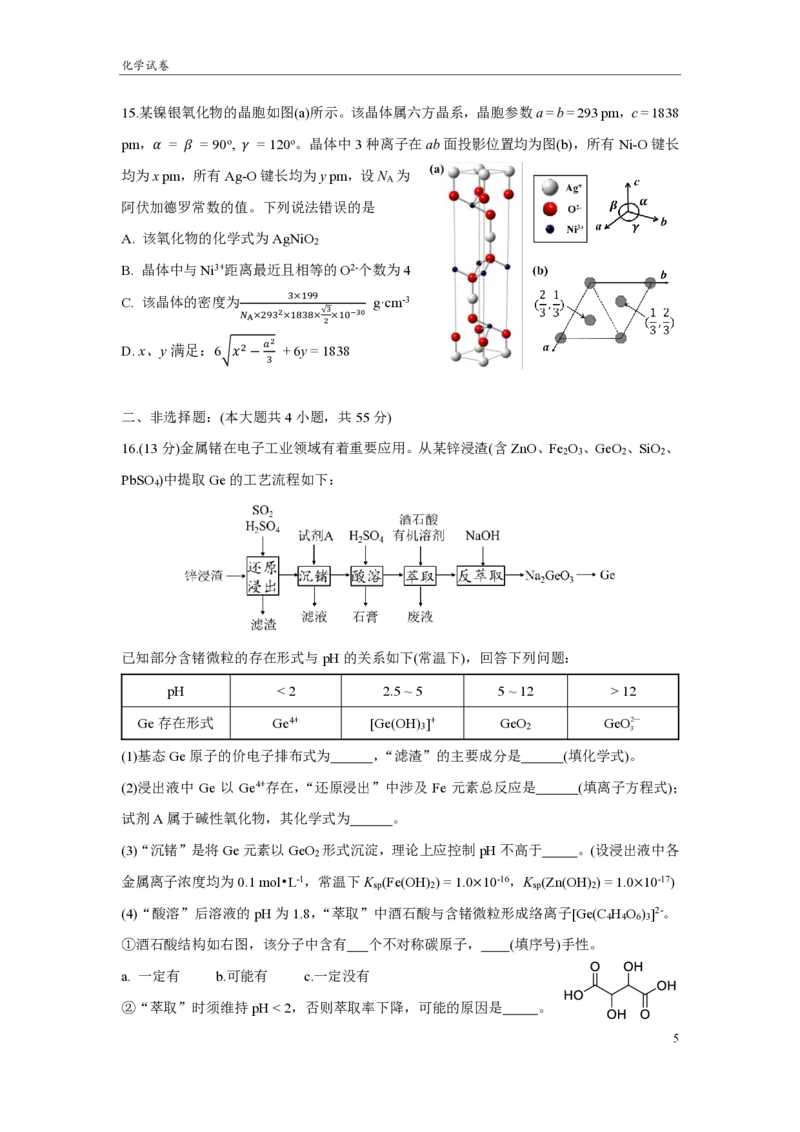
11.M、X、Y、Z为四种原子序数依次增大的短周期主族元素,其中X、Y、Z位于第二周期
且相邻。它们组成的一种有机阴离子与Gn+形成的配离子结构如下图。G元素位于第四周期,
其价层轨道上只有1个未成对电子但价层电子的空间运动状态有6种。下列说法错误的是
A.G为Cu元素,n = 2
B. 电负性:M < X < Y < Z
C. 第一电离能:X < Z < Y
D. 简单氢化物沸点:X < Z < Y
3化学试卷
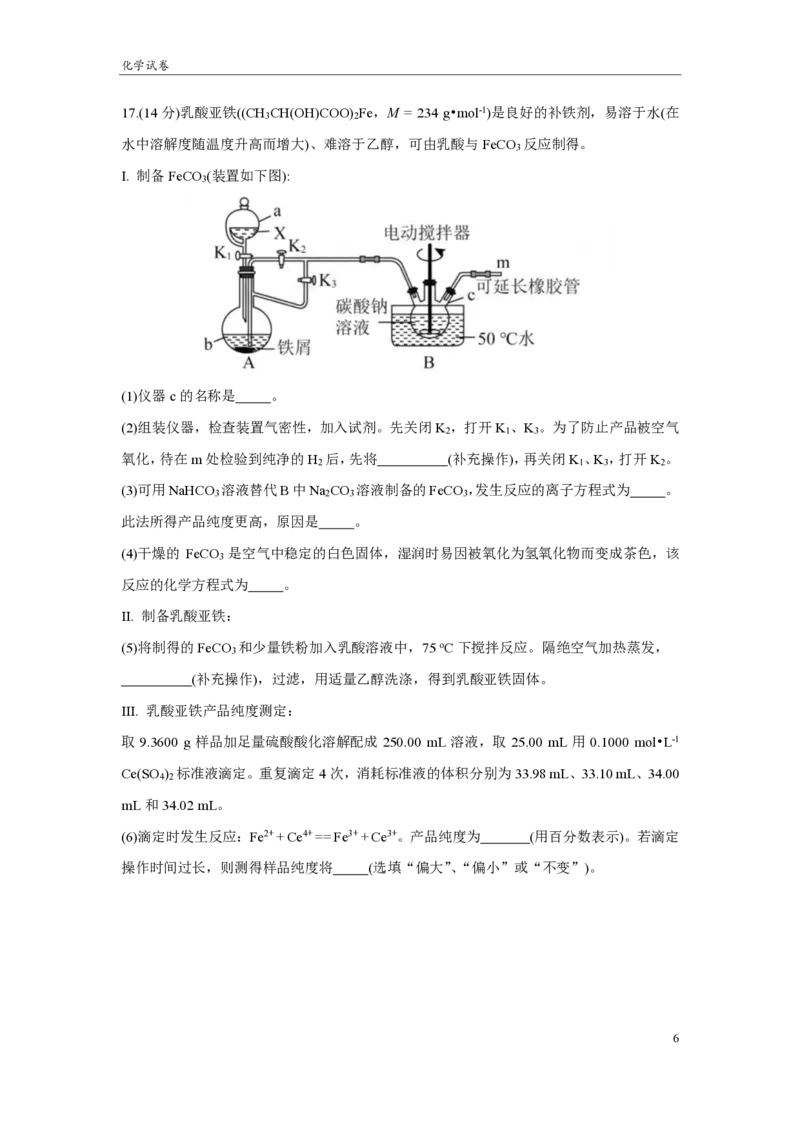
12. 高电压水系锌—有机混合液流电池的装置如图所示。下列说法错误的是
A.充电时,中性电解质NaCl的浓度减小
B.充电时,阴极反应式为Zn(OH) 2+2e=Zn+4OH
4
C.放电时,正极区溶液的pH减小
D.放电时,1mol FQ转化为FQH ,可消耗65 g Zn
2
13.CH CHDBr与NaOH在不同条件下可发生取代或消去反应。两个反应的能量反应进程图
3
如下图所示(TS表示过渡态,TS1结构已示出)。卤代烃的取代和消去可逆性很差,可认为均
不存在逆反应、无法达平衡。下列说法错误的是
A. CH CHDBr的消去反应:ΔH > 0, ΔS > 0
3
B. 两个反应中均涉及极性键的断裂与生成
C. 若底物改为 ,则取代产物为
D. 升高温度能提高消去产物在整体产物中的比例
14.常温下,用Hg(NO ) 测定NaCl溶液中c(Cl—)时,含Hg微粒的分布系数𝛿(该微粒在所有
3 2
含Hg微粒中的物质的量浓度分数)与lgc(Cl—)的关系如图所示。已知Hg2+与Cl—的配合物存
在如下平衡:
平均配位数𝑛̅ =
𝑛总(含汞配离子中的氯元素)
,100.26≈1.8。下列说法错误的是
𝑛总(溶液中的汞元素)
A. lgc(Cl—) = 4时,体系中主要存在HgCl
2
B. K = 100.85,K = 101
1 2
C. P点的横坐标值为6.61
D. 由X点数据计算得:m≈1.17
4化学试卷
15.某镍银氧化物的晶胞如图(a)所示。该晶体属六方晶系,晶胞参数a = b = 293 pm,c = 1838
pm,𝛼 = 𝛽 = 90o, 𝛾 = 120o。晶体中3种离子在ab面投影位置均为图(b),所有NiO键长
均为x pm,所有AgO键长均为y pm,设N 为
A
阿伏加德罗常数的值。下列说法错误的是
A. 该氧化物的化学式为AgNiO
2
B. 晶体中与Ni3+距离最近且相等的O2个数为4
3×199
C. 该晶体的密度为 g·cm3
𝑁A×2932×1838×√
2
3 ×10−30
D. x、y满足:6√𝑥2−
𝑎2
+ 6y = 1838
3
二、非选择题:(本大题共4小题,共55分)
16.(13分)金属锗在电子工业领域有着重要应用。从某锌浸渣(含ZnO、Fe O 、GeO 、SiO 、
2 3 2 2
PbSO )中提取Ge的工艺流程如下:
4
已知部分含锗微粒的存在形式与pH的关系如下(常温下),回答下列问题:
pH < 2 2.5 ~ 5 5 ~ 12 > 12
Ge存在形式 Ge4+ [Ge(OH) ]+ GeO GeO2—
3 2 3
(1)基态Ge原子的价电子排布式为 ,“滤渣”的主要成分是 (填化学式)。
(2)浸出液中 Ge 以 Ge4+存在,“还原浸出”中涉及 Fe 元素总反应是 (填离子方程式);
试剂A属于碱性氧化物,其化学式为 。
(3)““ 沉锗”是将Ge元素以GeO 形式沉淀,理论上应控制pH不高于 。(设浸出液中各
2
金属离子浓度均为0.1 mol•L1,常温下K (Fe(OH) ) = 1.0×1016,K (Zn(OH) ) = 1.0×1017)
sp 2 sp 2
(4)“酸溶”后溶液的pH为1.8,“萃取”中酒石酸与含锗微粒形成络离子[Ge(C H O ) ]2。
4 4 6 3
①酒石酸结构如右图,该分子中含有 个不对称碳原子, (填序号)手性。
a. 一定有 b.可能有 c.一定没有
②“萃取”时须维持pH < 2,否则萃取率下降,可能的原因是 。
5化学试卷
17.(14分)乳酸亚铁((CH CH(OH)COO) Fe,M = 234 g•mol1)是良好的补铁剂,易溶于水(在
3 2
水中溶解度随温度升高而增大)、难溶于乙醇,可由乳酸与FeCO 反应制得。
3
I. 制备FeCO (装置如下图):
3
(1)仪器c的名称是 。
(2)组装仪器,检查装置气密性,加入试剂。先关闭K ,打开K 、K 。为了防止产品被空气
2 1 3
氧化,待在m处检验到纯净的H 后,先将 (补充操作),再关闭K 、K ,打开K 。
2 1 3 2
(3)可用NaHCO 溶液替代B中Na CO 溶液制备的FeCO ,发生反应的离子方程式为 。
3 2 3 3
此法所得产品纯度更高,原因是 。
(4)干燥的 FeCO 是空气中稳定的白色固体,湿润时易因被氧化为氢氧化物而变成茶色,该
3
反应的化学方程式为 。
II. 制备乳酸亚铁:
(5)将制得的FeCO 和少量铁粉加入乳酸溶液中,75 oC下搅拌反应。隔绝空气加热蒸发,
3
(补充操作),过滤,用适量乙醇洗涤,得到乳酸亚铁固体。
III. 乳酸亚铁产品纯度测定:
取 9.3600 g 样品加足量硫酸酸化溶解配成 250.00 mL 溶液,取 25.00 mL 用 0.1000 mol•L1
Ce(SO ) 标准液滴定。重复滴定4次,消耗标准液的体积分别为33.98 mL、33.10 mL、34.00
4 2
mL和34.02 mL。
(6)滴定时发生反应:Fe2+ + Ce4+ == Fe3+ + Ce3+。产品纯度为 (用百分数表示)。若滴定
操作时间过长,则测得样品纯度将 (选填“偏大”、“偏小”或“不变”)。
6化学试卷
18.(14分)工业上以合成气(含CO、H 和少量CO )为原料制备二甲醚(DME),涉及反应如下:
2 2
①CO(g) + 2H (g) ⇌ CH OH(g) ΔH = 90.2 kJ•mol1
2 3 1
②2CH OH(g) ⇌ CH OCH (g) + H O(g) ΔH = 24.5 kJ•mol1
3 3 3 2 2
③CO(g) + H O(g) ⇌ CO (g) + H (g)
2 2 2
(1)反应2CO(g) + 4H (g) ⇌ CH OCH (g) + H O(g) ΔH = kJ•mol1。
2 3 3 2 3
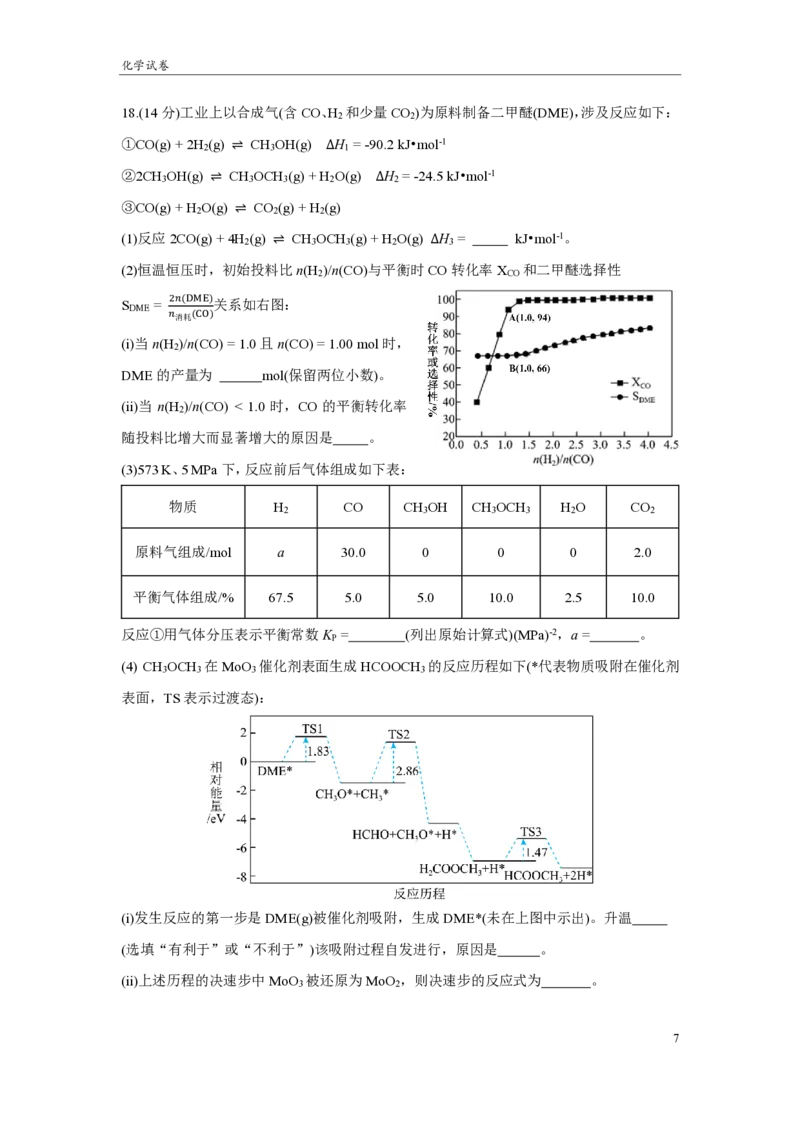
(2)恒温恒压时,初始投料比n(H )/n(CO)与平衡时CO转化率X 和二甲醚选择性
2 CO
2𝑛(DME)
S = 关系如右图:
DME
𝑛消耗(CO)
(i)当n(H )/n(CO) = 1.0且n(CO) = 1.00 mol时,
2
DME的产量为 mol(保留两位小数)。
(ii)当 n(H )/n(CO) < 1.0 时,CO 的平衡转化率
2
随投料比增大而显著增大的原因是 。
(3)573 K、5 MPa下,反应前后气体组成如下表:
物质 H CO CH OH CH OCH H O CO
2 3 3 3 2 2
原料气组成/mol a 30.0 0 0 0 2.0
平衡气体组成/% 67.5 5.0 5.0 10.0 2.5 10.0
反应①用气体分压表示平衡常数K = (列出原始计算式)(MPa)2,a = 。
P
(4) CH OCH 在MoO 催化剂表面生成HCOOCH 的反应历程如下(*代表物质吸附在催化剂
3 3 3 3
表面,TS表示过渡态):
(i)发生反应的第一步是DME(g)被催化剂吸附,生成DME*(未在上图中示出)。升温
(选填“有利于”或“不利于”)该吸附过程自发进行,原因是 。
(ii)上述历程的决速步中MoO 被还原为MoO ,则决速步的反应式为 。
3 2
7化学试卷
19.(14分)科学家在1933年首次成功合成了金刚烷(C H ),但直到1962年才首次合成出
10 16
其同分异构体扭曲烷。其合成路线如下:
已知:① ;
② ,一级醇(RCH OH)比二级醇(R1R2CHOH)更易发生此反应
2
回答下列问题:
(1)化合物A含有的含氧官能团名称是 ,A→B的反应类型是 。
(2) B→C中三乙胺(N(CH CH ) )的作用是 。
2 3 3
(3) D→E的离子方程式为 。
(4)试写出G的结构简式 。
(5) G→H转化过程中的两步反应顺序不能调换,原因是 。
(6)“扭曲烷” (选填“具有”或“不具有”)对映异构体。
(7)满足下列条件的A的同分异构体共有 种。
①能与FeCl 发生显色反应;②苯环上只有3个取代基;③1 mol该物质最多消耗2 mol NaOH
3
其中核磁共振氢谱显示4组峰且峰面积比为1:2:2:9的结构是 (任填一种)。
8