文档内容
2025-2026 学年高二化学上学期第一次月考卷
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证
号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:第1章~第2章第2节(人教版2019选择性必修1)。
5.难度系数:0.67
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16
第Ⅰ卷(选择题 共 48 分)
一、选择题:本题共16小题,每小题3分,共48分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.为响应国家双碳目标,科学家积极研发新的能源,能源的应用场景如图,下列有关说法错误的是
A.太阳能是可再生能源
B.氢能属于清洁能源
C.图中涉及的能源转化形式为太阳能 电能 光能
D.电动汽车行驶时,能源转化形式为电能 化学能 动能
【答案】D
【解析】A.常见的可再生能源:太阳能、风能、水能、地热能、生物质能等,即太阳能是可再生能
源,故A正确;
B.氢气燃烧生成水,没有污染,属于清洁能源,故B正确;
C.图中利用太阳能发电,电能使灯泡发光,能量转化形式为太阳能 电能 光能,故C正确;
D.电动汽车行驶时,能源转化形式为化学能 电能 动能,故D错误;
答案选D。
2.下列有关中和热和燃烧热的说法中,正确的是
1 / 15
学科网(北京)股份有限公司A.反应热就是热量
B.在稀溶液中, 和 完全中和时放出的热量小于
C. 溶液与稀 溶液恰好完全反应时,放出 的热量
D.已知 所以,C的燃烧热是220.7
【答案】B
【解析】A.在一定温度下,化学反应吸收或放出的热量叫做反应热,A错误;B.醋酸为弱电解质,
电离吸热,在稀溶液中, 和 完全中和时放出的热量小于 ,B正确;
C.中和热是指强酸和强碱的稀溶液反应生成 水所释放的热量,所以 的 与稀
溶液恰好完全反应时放出 的热量,C错误;D.C的燃烧热是C完全燃烧生成 所放
出的热量,D错误;故选B。
3.下列关于热化学方程式的描述或结论正确的是( )
选项 已知热化学方程式 有关描述或结论
A 3O(g)===2O(g) ΔH=+242.6 kJ·mol-1 氧气的能量比臭氧的高
2 3
B C H(g)===C H(g)+CH(g) ΔH>0 丙烷比乙烯稳定
3 8 2 4 4
NaOH(aq)+HCl(aq)===NaCl(aq)+HO(l) 含10.0 g NaOH的稀溶液与稀盐酸
2
C
ΔH=-57.3 kJ·mol-1 完全中和,放出的热量约为14.3 kJ
①2C(石墨,s)+2O(g)===2CO(g) ΔH;
2 2 1
D ΔH>ΔH
1 2
②2C(石墨,s)+O(g)===2CO(g) ΔH
2 2
【答案】A
【解析】由给出的热化学方程式可知,该反应为吸热反应,故臭氧的能量比氧气的高,A项错误;丙
烷吸收能量,分解为乙烯和甲烷两种物质,无法比较反应物与生成物之一的稳定性,B项错误;由已知
热化学方程式可知1 mol NaOH与HCl完全反应放出57.3 kJ热量,故含10.0 g NaOH的稀溶液与稀盐酸
完全反应放出的热量约为14.3 kJ,C项正确;ΔH 、ΔH 均小于0,燃烧越充分放出的热量越多,ΔH越
1 2
小,故ΔH<ΔH,D项错误。
1 2
4.下列措施或事实不能用勒夏特列原理解释的是
A.将 球浸泡在热水中颜色加深
B.配制 溶液时,向溶液中加入少量铁粉
C.用饱和食盐水除去氯气中的少量 气体
D.工业上生产硫酸的过程中,使用过量的空气以提高 的利用率
【答案】B
【解析】A.反应2NO (g) NO(g)是放热反应,温度升高,平衡逆向移动,NO 浓度增大,容器内颜
2 2 4 2
色加深,能用勒夏特列原理解释,A不符合题意;B.配制 溶液时,向溶液中加入少量铁粉是为
了防止Fe2+被氧化,与平衡移动无关,不能用勒夏特列原理解释,B符合题意;C.用饱和食盐水除去
氯气中的少量 气体,原因是饱和食盐水中氯离子浓度较高,使平衡Cl+H O H++Cl-+HClO逆向
2 2
2 / 15
学科网(北京)股份有限公司进行,从而降低Cl 的溶解度,可以用勒夏特列原理解释,C不符合题意;D.工业上生产硫酸的过程
2
中,使用过量的空气可以使2SO +O 2SO 正向移动,提高 的利用率,能用勒夏特列原理解
2 2 3
释,D不符合题意;故选B。
5.工业上由CO 和H 合成气态甲醇的热化学方程式为CO(g)+3H(g)=CH OH(g)+HO(g) ΔH<0。已知
2 2 2 2 3 2
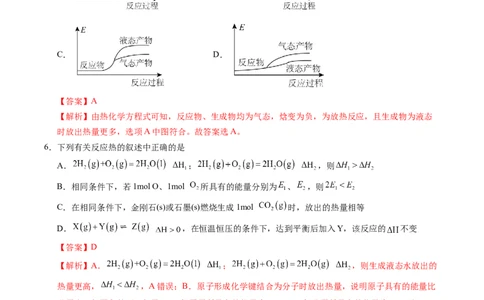
该反应是放热反应。下列表示合成甲醇的反应的能量变化示意图正确的是
A. B.
C. D.
【答案】A
【解析】由热化学方程式可知,反应物、生成物均为气态,焓变为负,为放热反应,且生成物为液态
时放出热量更多,选项A中图符合。故答案选A。
6.下列有关反应热的叙述中正确的是
A. ; ,则
B.相同条件下,若1mol O、1mol 所具有的能量分别为 、 ,则
C.在相同条件下,金刚石(s)或石墨(s)燃烧生成1mol 时,放出的热量相等
D. ,在恒温恒压的条件下,达到平衡后加入Y,该反应的 不变
【答案】D
【解析】A. ; ,则生成液态水放出的
热量更高, ,A错误;B.原子形成化学键结合为分子时放出热量,说明原子具有的能量比
分子多。相同条件下,如果1mol氧原子所具有的能量为E,1mol氧分子所具有的能量为E,则2E>
1 2 1
E,B错误;C.石墨转化为金刚石是一个吸热过程,则金刚石的能量比石墨高,金刚石(s)或石墨(s)燃
2
烧生成1mol 时,金刚石放出的热量多,C错误;D.一定条件下,反应热与平衡移动无关,与
化学计量数及物质的状态有关,D正确; 故选D。
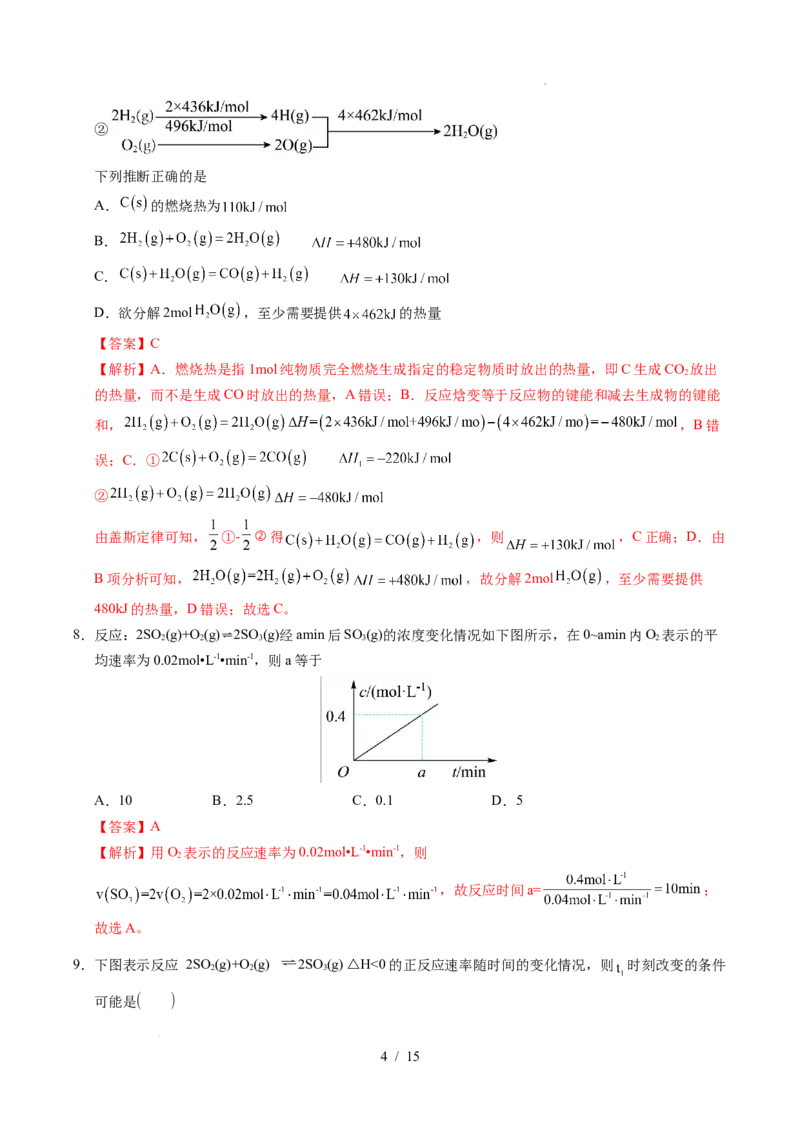
7.C和 在生产、生活、科技中是重要的燃料。已知:
①
3 / 15
学科网(北京)股份有限公司②
下列推断正确的是
A. 的燃烧热为
B.
C.
D.欲分解2mol ,至少需要提供 的热量
【答案】C
【解析】A.燃烧热是指1mol纯物质完全燃烧生成指定的稳定物质时放出的热量,即C生成CO 放出
2
的热量,而不是生成CO时放出的热量,A错误;B.反应焓变等于反应物的键能和减去生成物的键能
和, ,B错
误;C.①
②
由盖斯定律可知, ①- ②得 ,则 ,C正确;D.由
B项分析可知, ,故分解2mol ,至少需要提供
480kJ的热量,D错误;故选C。
8.反应:2SO
2
(g)+O
2
(g)⇌2SO
3
(g)经amin后SO
3
(g)的浓度变化情况如下图所示,在0~amin内O
2
表示的平
均速率为0.02mol•L-1•min-1,则a等于
A.10 B.2.5 C.0.1 D.5
【答案】A
【解析】用O 表示的反应速率为0.02mol•L-1•min-1,则
2
,故反应时间a= ;
故选A。
9.下图表示反应 2SO (g)+O(g) 2SO (g) △H<0的正反应速率随时间的变化情况,则 时刻改变的条件
2 2 3
可能是( )
4 / 15
学科网(北京)股份有限公司A.降低温度 B.减小压强 C.减小 的浓度 D.加入催化剂
【答案】A
【分析】由图知在t 时刻v 减小,反应正向进行,重新平衡时的速率小于原平衡速率,新平衡时反应
1 正
物浓度比原来小。
【解析】A.该反应的正反应是放热反应,降低温度,正逆反应速率都减小,平衡正向移动,则反应物
浓度减小,A符合题意;B.减小压强,平衡逆向移动,最终正反应速率比减小压强后起始的速率大,
B不符合题意;C.减小三氧化硫浓度,平衡正向移动,但改变条件瞬间,正反应速率不变,C不符合
题意;D.加入催化剂,正逆反应速率均增大,最终正反应速率比原来的大,D不符合图象;故选A。
10.已知反应2NO + 2H = N + 2H O的速率方程为υ= kc2(NO)· c(H )(k为速率常数),其反应历程如下:
2 2 2 2
① 2NO + H → N +H O 慢;② HO + H → 2H O 快
2 2 2 2 2 2 2 2
下列说法不正确的是
A.升高温度,可提高反应①、②的反应速率
B.c (NO) 、c(H )增大相同的倍数,对总反应的反应速率的影响程度相同
2
C.该反应的快慢主要取决于反应①
D.可逆反应使用催化剂加快反应速率时,正逆反应的活化能均减小
【答案】B
【解析】A.升高温度,物质的内能增加,活化分子数目增加,有效碰撞次数增加,化学反应速率加
快,故升高温度,可提高反应①、②的速率,A正确;B.根据速率方程为:υ=kc2(NO)· c(H )可知:
2
c(NO)的改变对化学反应速率的影响大于c(H )的改变对化学反应速率的影响,故c(NO)、c(H )增大相
2 2
同的倍数,对总反应的反应速率的影响程度不相同,B错误;C.对于多步反应,总反应速率由慢反
应决定,根据已知信息可知反应①是慢反应,反应②是快反应,所以该反应的快慢主要取决于慢反应
①,C正确;D.催化剂可以提高活化分子百分数,加快反应速率,使用催化剂加快反应速率时,正
逆反应的活化能均减小,D正确;故合理选项是B。
11. 分解的能量变化曲线如图所示。下列有关判断不正确的是
5 / 15
学科网(北京)股份有限公司A.该反应为吸热反应
B.过程Ⅰ使用了催化剂,加快了反应速率
C.过程Ⅱ逆反应的活化能
D.催化剂通过参与反应改变反应历程、改变反应的活化能来改变化学反应速率
【答案】C
【解析】A.由图可知,改反应中反应物的总能量低于生成物的总能量,为吸热反应,A正确;
B.由图可知,过程Ⅰ的活化能低于过程Ⅱ,说明过程Ⅰ使用了催化剂,加快了反应速率,B正确;
C.由图可知,过程Ⅱ逆反应的活化能 -12.5 =172.5 ,C错误;
D.催化剂通过参与反应改变反应历程、改变反应的活化能来改变化学反应速率,D正确;
故选C。
12.某温度下,密闭容器中发生反应 。下列说法正确的是
A.当4v(NH ) =6v(H O) 时,反应达到平衡状态
3 正 2 逆
B.当12个N-H键断裂的同时有12个O-H键形成,反应达到平衡状态
C.升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小
D.其他条件不变,仅将容器体积扩大一倍,再次达到平衡时,NO(g)的平衡浓度减小
【答案】D
【解析】A.当4v(NH ) =6v(H O) 时,正逆反应速率不相等,反应未达平衡状态,A错误;B.N-H
3 正 2 逆
键断裂和O-H键形成均为正反应速率,无法判断正逆反应速率是否相等,B错误;C.升高温度,正
逆反应速率均增大,反应正向放热,平衡逆向移动,C错误;D.其他条件不变,仅将容器的体积扩
大一倍,NO(g)的浓度瞬间变为原浓度的一半,平衡正向移动,再次达到平衡时,NO(g)的平衡浓度最
终比原平衡时浓度小,D正确;故选D。
13.已知O(g)+2Cl(g) 2ClO(g) ΔH>0,在三个恒温、恒容的密闭容器中分别充入1 mol O 与2 mol
2 2 2 2
Cl,测得平衡时O 的转化率如下表:
2 2
容器编
温度/℃ 容器体积/L 平衡时 转化率 平衡时压强
号
① 200 V 50% p
1 1
② 200 V 70% p
2 2
③ 350 V 50% p
3 3
6 / 15
学科网(北京)股份有限公司下列说法正确的是
A.起始反应速率:①>② B.平衡时压强:p>p
1 2
C.容器体积:V①,选项A错误;B.②平衡时O 转化率比①大,说明平衡时②中气体的物
1 2 2
质的量比①少,又温度相同,则②中压强大,所以平衡时压强:p < p ,选项B错误;C.③和①O
1 2 2
转化率相同,又该反应为吸热反应,③的温度高,平衡向正反应方向移动,所以达到③的压强则平衡
向逆反应方向移动,即③的压强小于①,所以③的体积大于①,VY
1 2
C.平衡常数:K < K < K
a b c
D.适当降低温度,NO 的平衡转化率增大
2
【答案】D
【解析】A.该反应为放热反应,升高温度,平衡逆向进行,NO 平衡转化率降低,该反应为气体物
2
质的量减少反应,增大压强,平衡正向进行,NO 平衡转化率增大,根据图像可知,X代表温度,Y
2
代表压强,故A错误;B.在温度相同时,增大压强,平衡正向进行,NO 平衡转化率增大,根据图
2
像,推出Y>Y,故B错误;C.利用“放热反应,升高温度,平衡常数减小”,该反应为放热反
2 1
应,三点中,c温度最高,平衡常数最小,故C错误;D.该反应为放热反应,降低温度,平衡正向
移动,NO 平衡转化率增大,故D正确;答案为D。
2
15.上海交通大学仇毅翔等研究了不同含金化合物催化乙烯加氢[ ]的反应
历程如下图所示:
7 / 15
学科网(北京)股份有限公司下列说法正确的是
A.该反应的焓变:
B.催化乙烯加氢效果较好的催化剂是
C.稳定性:过渡态1>过渡态2
D.催化剂可以改变速率,但不能改变平衡转化率
【答案】D
【解析】A.焓变等于生成物的总能量减去反应物的总能量,由题干图示反应物、生成物的总能量可知
,故A错误;B.由图可知, 对应的活化能小,则催
化效果好,故B错误;C.由图可知,过渡态1所处状态能量高于状态2,两种过渡态物质中较稳定的
是过渡态2,则稳定性:过渡态1<过渡态2,故C错误;D.催化剂只能改变反应历程,降低反应活化
能,加快反应速率,但不影响平衡移动,故D正确;故选D。
16.在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如表所示,下列说法不正确的是
物质 X Y Z
初始浓度
1 2 0
平衡浓度
0.5 0.5 1
A.反应可表示为
B.Y的平衡转化率为75%,化学平衡常数为16
C.反应前后气体总压强之比为3:2
D.增大压强,平衡会正向移动,反应的平衡常数增大
【答案】D
【解析】A.根据表中数据可知,该反应X,Y,Z的转化量关系为1:3:2,则该反应可以表示为
,A项正确;B.反应达到平衡时,Y的转化率为 ,平衡
常数为 ,B项正确;C.反应前后压强之比为 ,为3:
2,C项正确;D.K与温度有关,增大压强,该反应平衡会正向移动,反应的平衡常数不变,D项错
8 / 15
学科网(北京)股份有限公司误;答案选D。
第 II 卷(非选择题 共 52 分)
二、非选择题:本题共4小题,共52分。
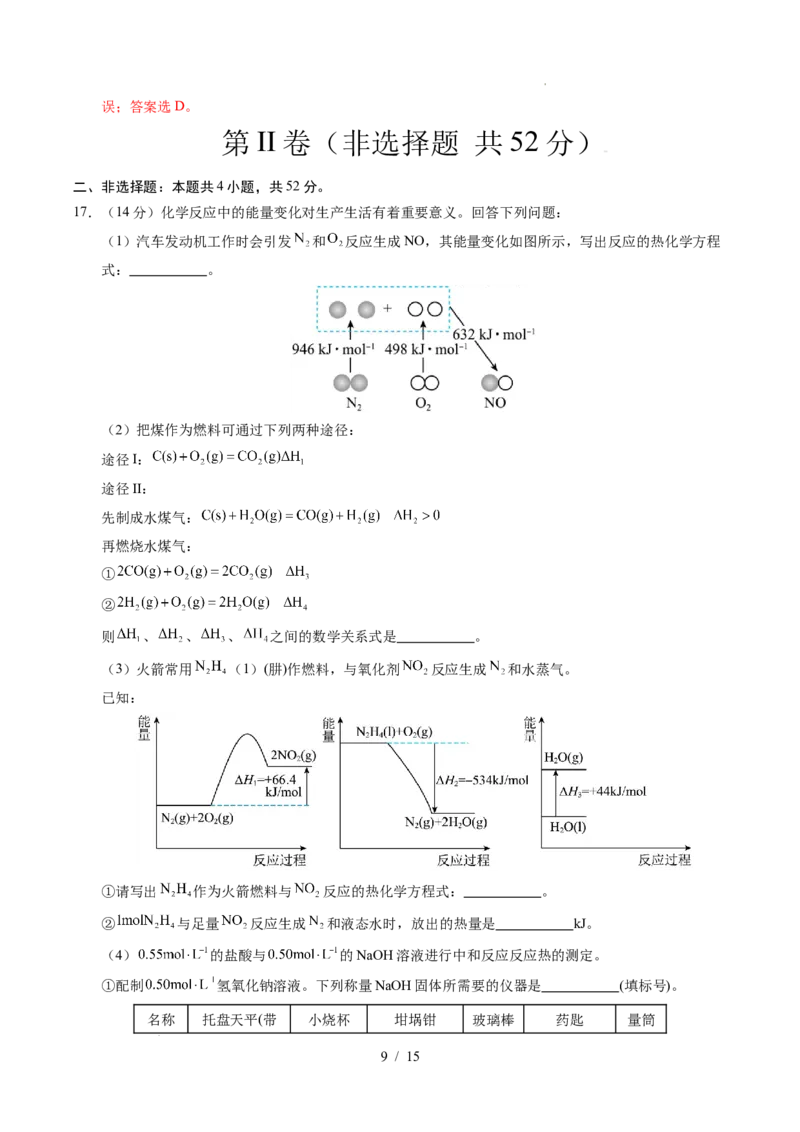
17.(14分)化学反应中的能量变化对生产生活有着重要意义。回答下列问题:
(1)汽车发动机工作时会引发 和 反应生成NO,其能量变化如图所示,写出反应的热化学方程
式: 。
(2)把煤作为燃料可通过下列两种途径:
途径I:
途径II:
先制成水煤气:
再燃烧水煤气:
①
②
则 、 、 、 之间的数学关系式是 。
(3)火箭常用 (1)(肼)作燃料,与氧化剂 反应生成 和水蒸气。
已知:
①请写出 作为火箭燃料与 反应的热化学方程式: 。
② 与足量 反应生成 和液态水时,放出的热量是 kJ。
(4) 的盐酸与 的NaOH溶液进行中和反应反应热的测定。
①配制 氢氧化钠溶液。下列称量NaOH固体所需要的仪器是 (填标号)。
名称 托盘天平(带 小烧杯 坩埚钳 玻璃棒 药匙 量筒
9 / 15
学科网(北京)股份有限公司砝码)
仪器
选项 a b c d e f
②中和反应反应热的测定。利用如图所示装置进行中和反应反应热的测定,缺少一种必要的仪器,其
仪器名称为 ,该仪器的作用是 。
③实验中若将 的盐酸与 的 溶液反应改用 的
盐酸与 的NaOH溶液进行反应,若实验操作均正确,则理论上两次实验所放出的热
量 (填“相等”或“不相等”,下同),所求中和反应反应热的数值 。
【答案】(除标明外,每空2分)
(1)
(2)
(3) 655.2
(4)①abe ②玻璃搅拌器(1分) 搅拌,使酸、碱快速完全反应(1分)
③不相等(1分) 相等(1分)
【解析】(1)该反应的反应热=反应物总键能-生成物总键能=
,故该反应的热化学方程式为 ;
(2)依据盖斯定律,反应C(s)+O(g)=CO (g)可由途径Ⅱ的反应+ (①+②)得到,则其焓变ΔH=ΔH +
2 2 1 2
(ΔH +ΔH );
3 4
(3)①已知(1)
(2)
根据盖斯定律:②×2-①可得: (l)+ (g)=3N(g)+4HO(g)
2 2
=2×(-534kJ/mol)-66.4kJ/mol=-1134.4kJ/mol,故 作为火箭燃料与 反应的热化学方程式为
;
10 / 15
学科网(北京)股份有限公司②由上一问可知, 与足量 反应生成 和气态水(2mol)时,放出热量
,由图可知, ,故生成液态水时放出的热量为
;
(4)①称量NaOH固体需要用托盘天平,NaOH固体具有腐蚀性,应放在小烧杯内进行称量,同时需
要用药匙量取NaOH固体,故选abe;
②中和反应反应热的测定,需要用环形玻璃搅拌棒将酸碱混合均匀充分反应;
③反应放出的热量和所用酸以及碱的量的多少有关,并若用60mL0.50mol/L盐酸跟50mL0.55mol/
LNaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但是中和热的均是
强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,所以测得中和热数值相等。
18.(12分)研究小组利用 溶液和酸性 溶液的反应来探究外界条件改变对化学反应速率的
影响,实验如下:
参加反应的物质
实验 溶液颜色褪至无
溶液(含硫酸) 溶液
实验序号
温度/K 色时所需时间/s
V/mL c/mol·L V/mL c/mol·L V/mL
① 290 2 0.02 4 0.1 0 6
② 2 0.02 3 0.1 8
③ 315 2 0.02 0.1 1
回答下列问题:
(1)通过实验①、②,可探究 的改变对反应速率的影响,其中 。
(2)通过实验 (填实验序号)可探究温度变化对化学反应速率的影响,由实验②中数据可
知 。
(3)实验过程中,发现反应开始一段时间溶液褪色不明显,不久后迅速褪色。甲同学认为是反应放
热导致溶液温度升高所致,重做实验②,测定反应过程中不同时间的温度,结果如下:
时间/s 0 2 4 6 8 10
温度/K 290 291 291 291.5 292 292
①结合实验目的与表中数据,得出的结论是 。
②你猜想可能是 的影响。若证明你的猜想,除了酸性高锰酸钾溶液和草酸溶液外,还需
要选择的最佳试剂是 (填标号)。
A.硫酸钾 B.水 C.二氧化锰 D.硫酸锰
【答案】(除标明外,每空2分)
(1)反应物浓度(1分) l(1分)
11 / 15
学科网(北京)股份有限公司(2)②、③
(3)温度不是反应速率突然加快的原因 催化剂( ) D
【解析】(1)通过观察实验①、②的数据可知T、V 未知,但实验①、②中所用的 溶液的体
1 1
积不同,根据控制变量法的原则,T 应为290K,变量为 溶液的浓度,此外两组实验溶液的总
1
体积应保持一致确两组实验中其他溶液的浓度相同,故V=1,故答案为:反应物浓度;l;(2)根据
1
控制变量法的原则,V=1,所以可通过实验②、③探究温度变化对化学反应速率的影响,反应原理为
1
,实验②中所用的 溶液的物质的量为
, 溶液的物质的量为 ,
溶液过量,8s内消耗的 溶液的物质的量为 ,此时溶液的总体积
为 ,所以8s 内 ,故答案为:②、③;
;(3)不同时间下,温度升高的程度很小,所以温度不是反应速率突然加快的
原因,随着反应的进行,锰离子的浓度逐渐增加,可催化该反应,为了验证锰离子的催化效果,但又
不引进其他的杂质离子,可选择的最佳试剂是硫酸锰,故答案为:温度不是反应速率突然加快的原
因;催化剂( );D;
19.(12分)研究 之间的转化具有重要意义。回答下列问题:
已知:
将一定量 气体充入恒容的密闭容器中,控制反应温度为 。
(1)下列可以作为反应达到平衡的判据是___________(填标号)。
A.气体的压强不变 B.
C.K不变 D.容器内颜色不变
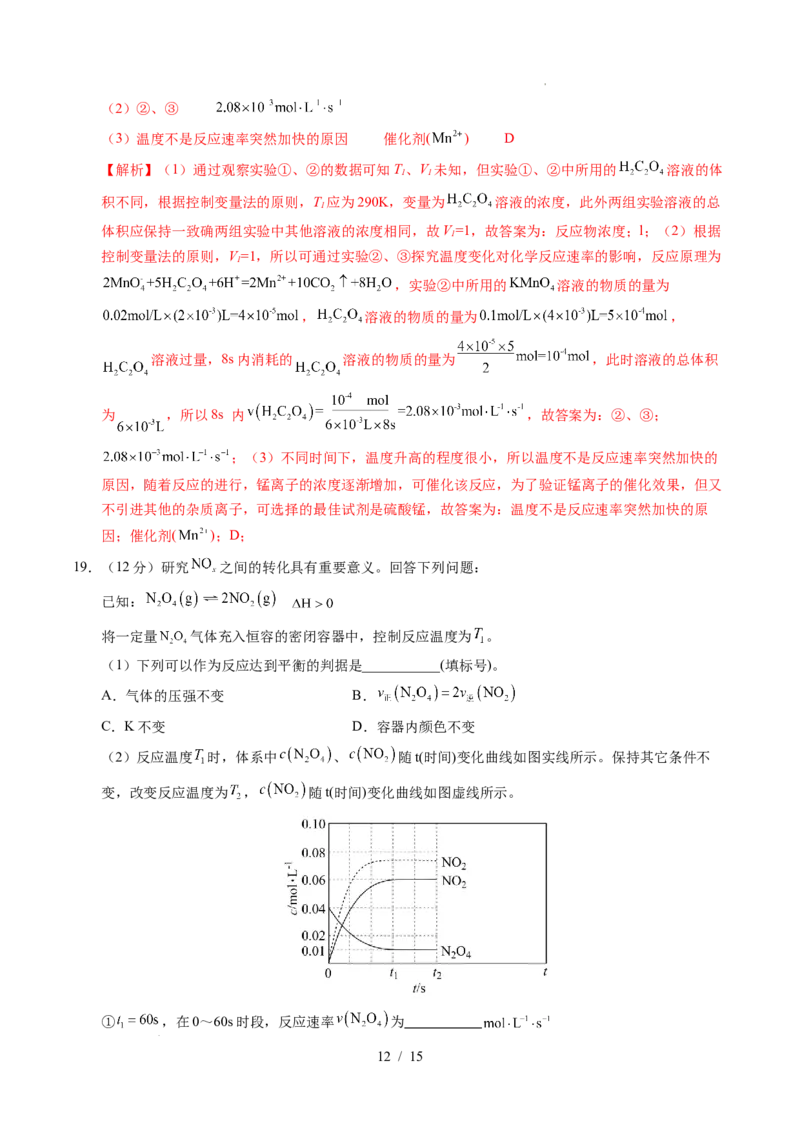
(2)反应温度 时,体系中 、 随t(时间)变化曲线如图实线所示。保持其它条件不
变,改变反应温度为 , 随t(时间)变化曲线如图虚线所示。
① ,在0~60s时段,反应速率 为
12 / 15
学科网(北京)股份有限公司②反应温度为 (填“大于”或“小于”) 。
③温度 时反应达平衡后,将反应容器的容积减少一半,平衡向 (填“正反应”或“逆反
应”)方向移动。
④ 时刻反应达到平衡,混合气体平衡总压强为p, 气体的平衡转化率为75%,则反应
的平衡常数 。(用平衡分压代替平衡浓度计算,分压=总压×物
质的量分数)。
(3)NO氧化反应: 分两步进行,其反应过程能量变化示意图如图。
Ⅰ.
Ⅱ.
决定NO氧化反应速率的步骤是 (填“Ⅰ”或“Ⅱ”)。
【答案】(每空2分)
(1)ABD
(2)① ②大于 ③逆反应方向 ④
(3)Ⅱ
【解析】(1)A.反应后气体分子数增大,气体的压强不变,表面反应达到平衡;
B. 代表四氧化二氮的消耗和生成速率相等,反应达到平衡;
C.K只与稳定有关,K不变不可以说明反应达到平衡;
D.容器内颜色不变,说明反应物和生成物浓度不再变化,反应达到平衡;
故选:ABD;
(2)① ,在0~60s时段,反应速率 为
;
②反应吸热,升高温度平衡正向移动,二氧化氮浓度增大,反应温度为 大于 。
③温度 时反应达平衡后,将反应容器的容积减少一半,平衡向体积减少的方向移动,平衡向逆反应
方向移动。
④ 时刻反应达到平衡,混合气体平衡总压强为p, 气体的平衡转化率为75%,设起始四氧化二
13 / 15
学科网(北京)股份有限公司氮的物质的量为amol,
;
(3)决定NO氧化反应速率的步骤是活化能最大的步骤,是反应 Ⅱ。
20.(14分)亚硝酰氯(ClNO)是有机合成中的重要试剂,可通过反应:2NO(g)+Cl (g) 2 ClNO(g)制
2
得。回答下列问题:
(1)一定温度下,将等物质的量的NO与Cl 置于恒容密闭容器中发生反应。下列选项中可判断反应
2
达到平衡状态的是___________(填标号)。
A.混合气体的密度保持不变
B.混合气体的平均相对分子质量不变
C.NO和Cl 的物质的量之比保持不变
2
D.每消耗1molNO的同时生成1molClNO
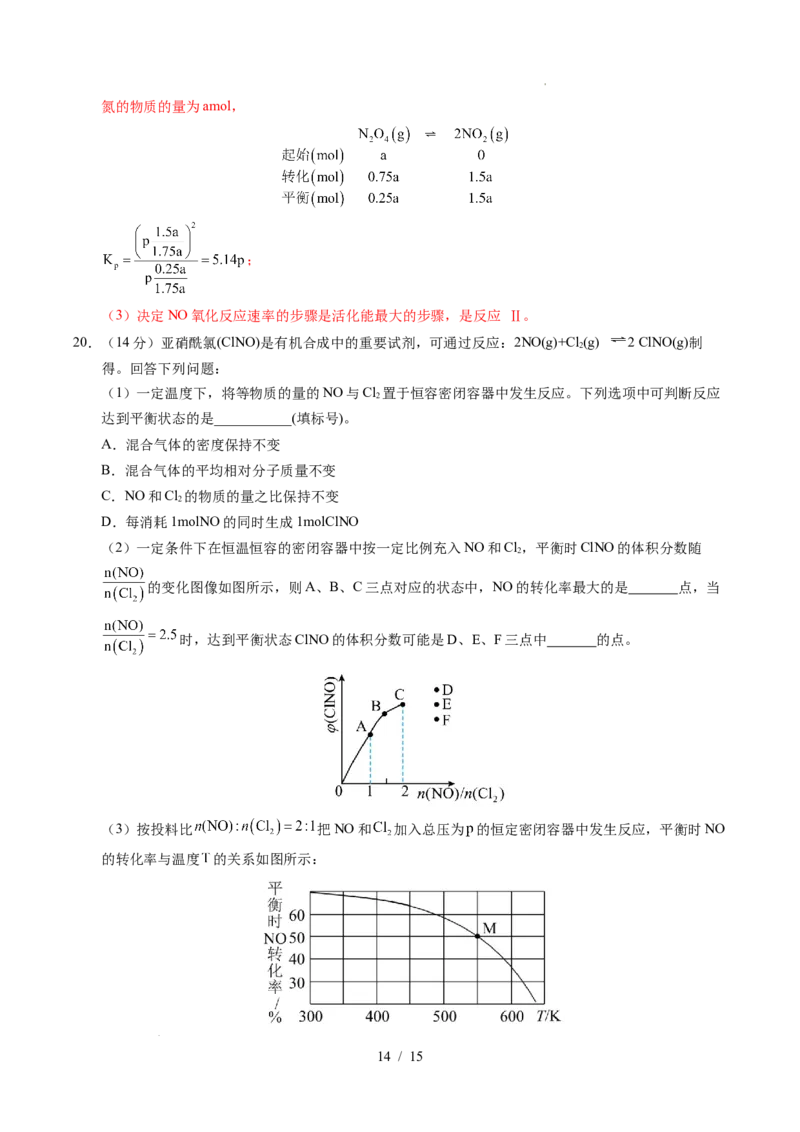
(2)一定条件下在恒温恒容的密闭容器中按一定比例充入NO和Cl,平衡时ClNO的体积分数随
2
的变化图像如图所示,则A、B、C三点对应的状态中,NO的转化率最大的是 点,当
时,达到平衡状态ClNO的体积分数可能是D、E、F三点中 的点。
(3)按投料比 把NO和 加入总压为 的恒定密闭容器中发生反应,平衡时NO
的转化率与温度 的关系如图所示:
14 / 15
学科网(北京)股份有限公司①该反应的 0(填“>”“<”或“=”)。判断理由是 。
②在 压强条件下,M点时容器内NO的体积分数为 。
③若反应一直保持在 压强条件下进行,则M点的分压平衡常数 (用含 的表达式表
示,用平衡分压代替平衡浓度计算,分压 总压 体积分数)。
【答案】(每空2分)
(1)BC
(2)A F
(3)①< NO平衡转化率随温度的升高而减少,说明升温平衡逆移,故正反应为放热反应
②40% ③5/P
【解析】(1)A.混合气体质量恒定,密闭容器恒容,故密度始终保持不变,密度不能作为判断平衡
的依据,故A错误;B.混合气体的平均摩尔质量为 ,混合气体总质量守恒,该反应前后气体
化学计量数之和不相等,混合气体总物质的量在变化,当混合气体的平均相对分子质量不变,说明反
应达到平衡状态,故B正确;C.NO与Cl 等物质的量充入反应容器,而两者按照2∶1转化,故当NO
2
和Cl 的物质的量之比保持不变,说明反应达到平衡状态,故C正确;D.反应的任意时刻,每消耗
2
1molNO的同时均生成1molClNO,不能说明达到平衡状态,故D错误;故选BC;
(2)①n(NO)/n(Cl )比值越小,NO的转化率越大,故NO转化率最大的是A点;
2
②当反应物的物质的量之比等于化学计量数之比时,生成物的体积分数最大,当 时,
ClNO的体积分数较C点减小,故应该是F点;
(3)①由图乙可知,随温度升高,平衡时NO的转化率降低,则该反应为放热反应,ΔH<0;
②假设反应开始时,n(NO)=2mol、n(Cl )=1mol,M点平衡时NO的转化率为50%,根据三段式可得,
2
平衡时n(NO)=1mol、n(Cl )=0.5mol、n(ClNO)=1mol,故M点时容器内NO的体积分数=
2
;
③根据分压平衡常数Kp的定义,将数据代入可得 。
15 / 15
学科网(北京)股份有限公司