文档内容
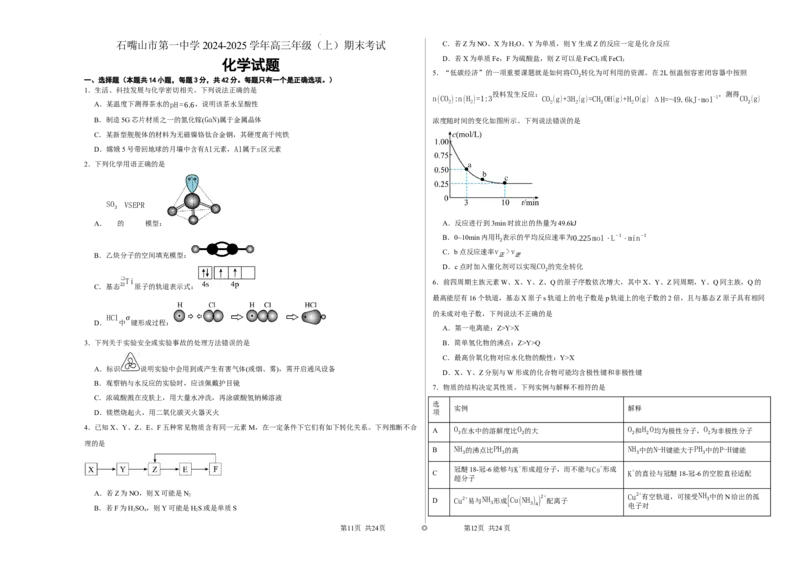
石嘴山市第一中学 2024-2025 学年高三年级(上)期末考试 C.若Z为NO、X为HO、Y为单质,则Y生成Z的反应一定是化合反应
2
化学试题
D.若X为单质Fe,F为硫酸盐,则Z可以是FeCl
2
或FeCl
3
5.“低碳经济”的一项重要课题就是如何将CO 转化为可利用的资源。在2L恒温恒容密闭容器中按照
2
一、选择题(本题共14小题,每题3分,共42分。每题只有一个是正确选项。)
1.生活、科技发展与化学密切相关。下列说法正确的是
投料发生反应: ,测得
n(CO ):n(H )=1:3 CO (g)+3H (g)=CH OH(g)+H O(g) ΔH=-49.6kJ·mol-1 CO (g)
A.某温度下测得茶水的pH=6.6,说明该茶水呈酸性 2 2 2 2 3 2 2
B.制造5G芯片材质之一的氮化镓(GaN)属于金属晶体 浓度随时间的变化如图所示。下列说法错误的是
C.某新型舰舰体的材料为无磁镍铬钛合金钢,其硬度高于纯铁
D.嫦娥5号带回地球的月壤中含有Al元素,Al属于s区元素
2.下列化学用语正确的是
SO VSEPR
3
A. 的 模型: A.反应进行到3min时放出的热量为49.6kJ
B.0~10min内用H 表示的平均反应速率为0.225mol⋅L−1 ⋅min−1
2
C.b点反应速率v >v
B.乙炔分子的空间填充模型: 正 逆
D.c点时加入催化剂可以实现CO 的完全转化
2
❑Ti 6.前四周期主族元素W、X、Y、Z、Q的原子序数依次增大,其中X、Y、Z同周期,Y、Q同主族,Q的
C.基态22 原子的轨道表示式:
最高能层有16个轨道,基态X原子s轨道上的电子数是p轨道上的电子数的2倍,且与基态Z原子具有相同
的未成对电子数,下列说法不正确的是
HCl σ
D. 中 键形成过程:
A.第一电离能:Z>Y>X
3.下列关于实验安全或实验事故的处理方法错误的是 B.简单氢化物的沸点:Z>Y>Q
C.最高价氧化物对应水化物的酸性:Y>X
A.标识 说明实验中会用到或产生有害气体(或烟、雾),需开启通风设备
D.X、Y、Z分别与W形成的化合物可能均含极性键和非极性键
B.观察钠与水反应的实验时,应该佩戴护目镜
7.物质的结构决定其性质。下列实例与解释不相符的是
C.浓硫酸溅在皮肤上,用大量水冲洗,再涂碳酸氢钠稀溶液
选
实例 解释
D.镁燃烧起火,用二氧化碳灭火器灭火 项
4.已知X、Y、Z、E、F五种常见物质含有同一元素M,在一定条件下它们有如下转化关系。下列推断不合 A O 在水中的溶解度比O 的大 O 和H O均为极性分子,O 为非极性分子
3 2 2 2 2
理的是
B NH 的沸点比PH 的高 NH 中的N-H键能大于PH 中的P-H键能
3 3 3 3
冠醚18-冠-6能够与K+形成超分子,而不能与Cs+形成
C K+的直径与冠醚18-冠-6的空腔直径适配
超分子
A.若Z为NO,则X可能是N 2 D Cu2+易与NH 形成[Cu(NH ) ) 2+ 配离子 Cu2+有空轨道,可接受NH 3 中的N给出的孤
3 3 4 电子对
B.若F为HSO ,则Y可能是HS或是单质S
2 4 2
第11页 共24页 ◎ 第12页 共24页
学科网(北京)股份有限公司A.A B.B C.C D.D
8.常温下,下列各组离子在指定溶液中一定能大量共存的是()
A.水电离出的 的溶液: 、 、 、
c(H+ )⋅c(OH− )=10−22 K+ Na+ SO2− S O2−
4 2 3
B.澄清透明溶液: 、 、 、
M g2+ Cu2+ Cl− SO2−
4
C.使酚酞变红色的溶液: 、 、 、
N H+ K+ AlO− NO−
4 2 3
D.含 的溶液: 、 、 、
0.1mol⋅L−1KI Fe3+ Na+ NO− Cl−
3
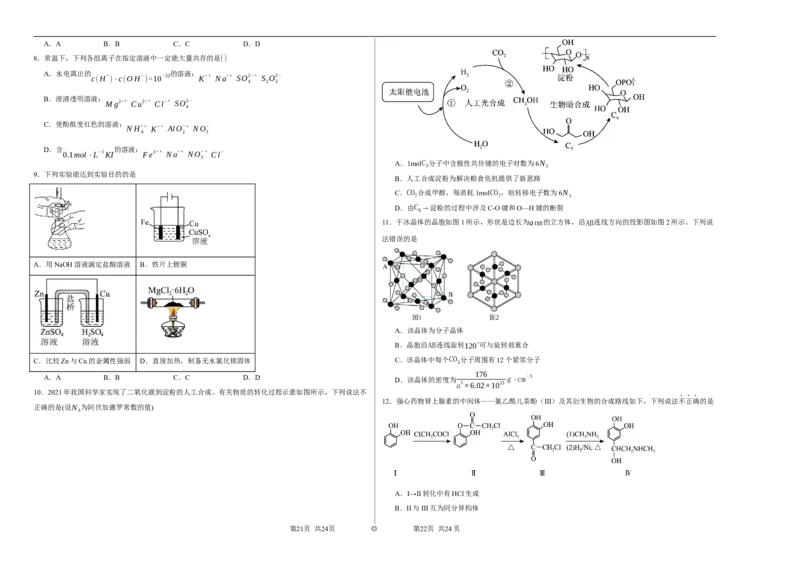
A.1molC 分子中含极性共价键的电子对数为6N
3 A
9.下列实验能达到实验目的的是
B.人工合成淀粉为解决粮食危机提供了新思路
C.CO 合成甲醇,每消耗1molCO ,则转移电子数为6N
2 2 A
D.由C →淀粉的过程中涉及C-O键和O—H键的断裂
6
11.干冰晶体的晶胞如图1所示,形状是边长为anm的立方体,沿AB连线方向的投影图如图2所示。下列说
法错误的是
A.用NaOH溶液滴定盐酸溶液 B.铁片上镀铜
A.该晶体为分子晶体
B.晶胞沿AB连线旋转120∘可与旋转前重合
C.比较Zn与Cu的金属性强弱 D.直接加热,制备无水氯化镁固体 C.该晶体中每个CO 分子周围有12个紧邻分子
2
176
A.A B.B C.C D.D
D.该晶体的密度为
g⋅cm−3
a3×6.02×1023
10.2021年我国科学家实现了二氧化碳到淀粉的人工合成。有关物质的转化过程示意如图所示,下列说法不
12.强心药物肾上腺素的中间体——氯乙酰儿茶酚(III)及其衍生物的合成路线如下,下列说法不正确的是
正确的是(设N 为阿伏加德罗常数的值)
A
A.I→II转化中有HCl生成
B.II与III互为同分异构体
第21页 共24页 ◎ 第22页 共24页C.1mol IV能与3molNaOH反应 B.M点:
2c(A−)=c(Na+)+c(H+)
C.当 时,
D.预测可以发生反应 V(HA)=10mL c(OH−)=c(H+)+c(HA)+c(A−)
13.含 的废水在废水处理过程中与臭氧发生反应会产生 。模拟在 上电催化处理 的示 D.N点:
Br− BrO− RuCu/CNT BrO− c(Na+)>c(A−)>c(OH−)>c(H+)>c(HA)
3 3
意图如图所示,下列说法正确的是
二、非选择题(本题共58分。)
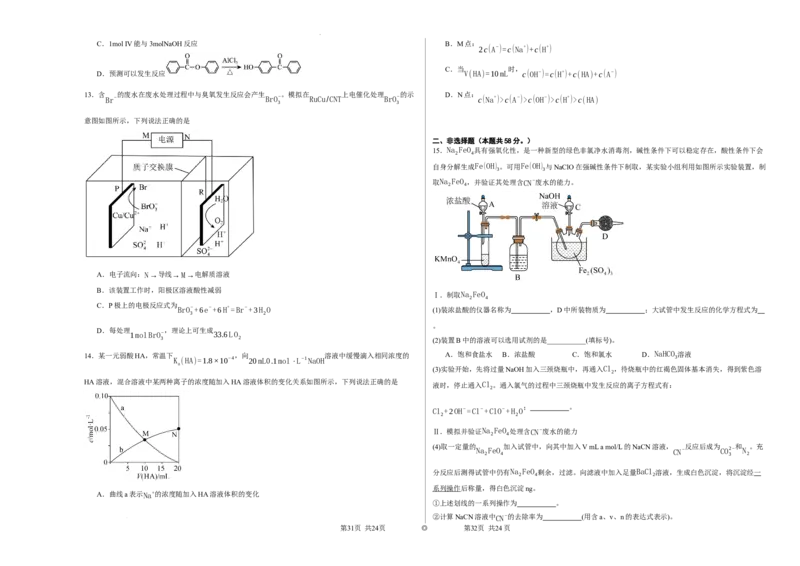
15.Na FeO 具有强氧化性,是一种新型的绿色非氯净水消毒剂,碱性条件下可以稳定存在,酸性条件下会
2 4
自身分解生成Fe(OH) 。可用Fe(OH) 与NaClO在强碱性条件下制取,某实验小组利用如图所示实验装置,制
3 3
取Na FeO ,并验证其处理含CN−废水的能力。
2 4
A.电子流向:N→导线→M→电解质溶液
B.该装置工作时,阳极区溶液酸性减弱
Ⅰ.制取Na FeO
2 4
C.P极上的电极反应式为
BrO−+6e−+6H+=Br−+3H O (1)装浓盐酸的仪器名称为 ,D中所装物质为 ;大试管中发生反应的化学方程式为
3 2
。
D.每处理 ,理论上可生成
1molBrO− 33.6LO
3 2 (2)装置B中的溶液可以选用试剂的是___________(填标号)。
14.某一元弱酸HA,常温下 ,向 溶液中缓慢滴入相同浓度的 A.饱和食盐水 B.浓盐酸 C.饱和氯水 D.NaHCO 溶液
K (HA)=1.8×10−4 20mL0.1mol⋅L−1NaOH 3
a
(3)实验开始,先将过量NaOH加入三颈烧瓶中,再通入Cl ,待烧瓶中的红褐色固体基本消失,得到紫色溶
2
HA溶液,混合溶液中某两种离子的浓度随加入HA溶液体积的变化关系如图所示,下列说法正确的是
液时,停止通入Cl 。通入氯气的过程中三颈烧瓶中发生反应的离子方程式有:
2
; 。
Cl +2OH−=Cl−+ClO−+H O
2 2
Ⅱ.模拟并验证Na FeO 处理含CN−废水的能力
2 4
(4)取一定量的 加入试管中,向其中加入V mL a mol/L的NaCN溶液, 反应后成为 和 。充
Na FeO CN− CO2− N
2 4 3 2
分反应后测得试管中仍有Na FeO 剩余,过滤。向滤液中加入足量BaCl 溶液,生成白色沉淀,将沉淀经一
2 4 2
系列操作后称量,得白色沉淀ng。
A.曲线a表示Na+的浓度随加入HA溶液体积的变化
①上述划线的一系列操作为 。
②计算NaCN溶液中CN−的去除率为 (用含a、v、n的表达式表示)。
第31页 共24页 ◎ 第32页 共24页
学科网(北京)股份有限公司(5)Na FeO 作为高效的水处理剂,请说出其优点为 。 分子(填“极性”或“非极性”)。
2 4
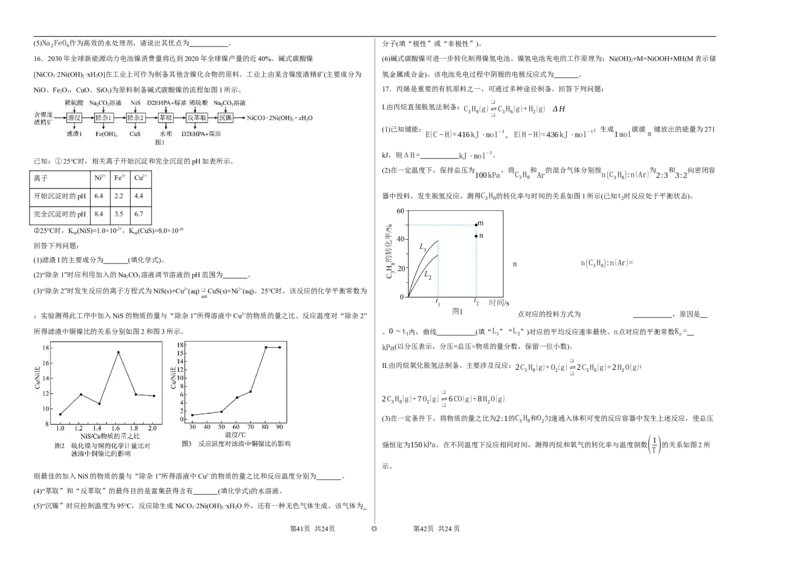
16.2030年全球新能源动力电池镍消费量将达到2020年全球镍产量的近40%。碱式碳酸镍 (6)碱式碳酸镍可进一步转化制得镍氢电池。镍氢电池充电的工作原理为:Ni(OH) +M=NiOOH+MH(M表示储
2
[NiCO·2Ni(OH) ·xH O]在工业上可作为制备其他含镍化合物的原料。工业上由某含镍废渣精矿(主要成分为 氢金属或合金)。该电池充电过程中阴极的电极反应式为 。
3 2 2
NiO、Fe O,CuO、SiO)为原料制备碱式碳酸镍的流程如图1所示。 17.丙烯是重要的有机原料之一,可通过多种途径制备。回答下列问题:
2 3 2
❑
Ⅰ.由丙烷直接脱氢法制备:C H (g)⇌ C H (g)+H (g) ΔH
3 8 3 6 2
❑
(1)已知键能: ;生成 碳碳 键放出的能量为271
E(C−H)=416kJ⋅mol−1、E(H−H)=436kJ⋅mol−1 1mol π
kJ,则ΔH= kJ⋅mol−1。
已知:①25℃时,相关离子开始沉淀和完全沉淀的pH如表所示。
(2)在一定温度下,保持总压为 ,将 和 的混合气体分别按 为 和 向密闭容
100kPa C H Ar n(C H ):n(Ar) 2:3 3:2
离子 Ni2+ Fe3+ Cu2+ 3 8 3 8
开始沉淀时的pH 6.4 2.2 4.4 器中投料,发生脱氢反应,测得C H 的转化率与时间的关系如图1所示(已知t 时反应处于平衡状态)。
3 8 2
完全沉淀时的pH 8.4 3.5 6.7
②25℃时,K (NiS)=1.0×10-27,K (CuS)=8.0×10-35
sp sp
回答下列问题:
(1)滤渣I的主要成分为 (填化学式)。 m n(C H ):n(Ar)=
3 8
(2)“除杂1”时应利用加入的NaCO 溶液调节溶液的pH范围为 。
2 3
(3)“除杂2”时发生反应的离子方程式为NiS(s)+Cu2+(aq)❑CuS(s)+Ni2+(aq)。25℃时,该反应的化学平衡常数为
⇌
;实验测得此工序中加入NiS的物质的量与“除杂1”所得溶液中Cu2+的物质的量之比、反应温度对“除杂2” 点对应的投料方式为 ,原因是
所得滤渣中铜镍比的关系分别如图2和图3所示。 。0∼t 内,曲线 (填“L ”“L ”)对应的平均反应速率最快。n点对应的平衡常数K =
1 1 2 p
kPa(以分压表示,分压=总压×物质的量分数,保留一位小数)。
❑
Ⅱ.由丙烷氧化脱氢法制备。主要涉及反应:2C H (g)+O (g)⇌2C H (g)+2H O(g) ;
3 8 2 3 6 2
❑
❑
2C H (g)+7O (g)⇌6CO(g)+8H O(g)
3 8 2 2
❑
(3)在一定条件下,将物质的量之比为2:1的C H 和O 匀速通入体积可变的反应容器中发生上述反应,使总压
3 8 2
(1)
强恒定为150kPa。在不同温度下反应相同时间,测得丙烷和氧气的转化率与温度倒数 的关系如图2所
T
示。
则最佳的加入NiS的物质的量与“除杂1”所得溶液中Cu2+的物质的量之比和反应温度分别为 。
(4)“萃取”和“反萃取”的最终目的是富集获得含有 (填化学式)的水溶液。
(5)“沉镍”时应控制温度为95℃,反应除生成NiCO·2Ni(OH) ·xH O外,还有一种无色气体生成。该气体为
3 2 2
第41页 共24页 ◎ 第42页 共24页(4)E中官能团的名称为 。
(5)F的同分异构体中,能发生银镜反应,且苯环上有五个取代基的结构有 种,其中核磁共振氢
谱有4组峰的结构简式为 。
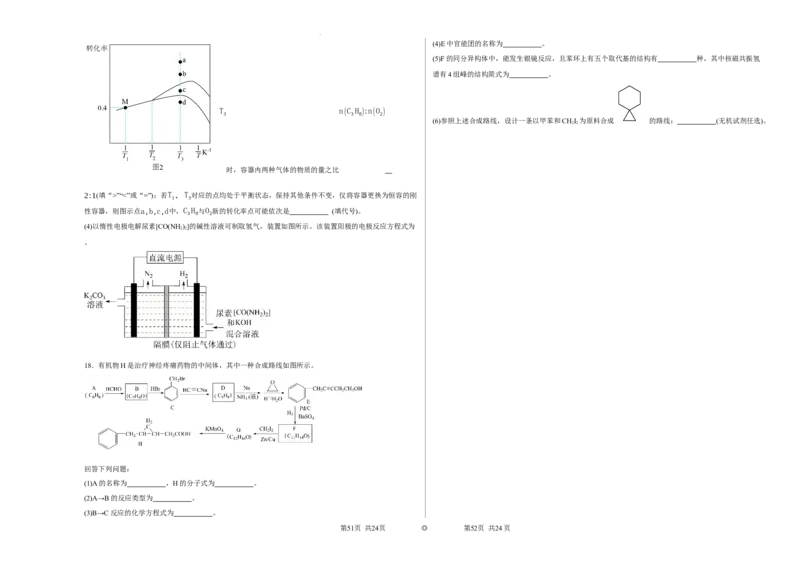
T n(C H ):n(O )
3 3 8 2
(6)参照上述合成路线,设计一条以甲苯和CHI 为原料合成 的路线: (无机试剂任选)。
2 2
时,容器内两种气体的物质的量之比
2:1(填“>”“<”或“=”);若T 、T 对应的点均处于平衡状态,保持其他条件不变,仅将容器更换为恒容的刚
1 3
性容器,则图示点a,b,c,d中,C H 与O 新的转化率点可能依次是 (填代号)。
3 8 2
(4)以惰性电极电解尿素[CO(NH)]的碱性溶液可制取氢气,装置如图所示。该装置阳极的电极反应方程式为
2 2
。
18.有机物H是治疗神经疼痛药物的中间体,其中一种合成路线如图所示。
回答下列问题:
(1)A的名称为 ,H的分子式为 。
(2)A→B的反应类型为 。
(3)B→C反应的化学方程式为 。
第51页 共24页 ◎ 第52页 共24页
学科网(北京)股份有限公司