文档内容
2025-2026 学年上期高 2026 届 10 月阶段性测试
化学 试卷
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 K-39 Ca-40 Fe-56
一、选择题:本题共15 小题,每小题 3 分,共45 分。每小题给出的四个选项中,只有一项是符合题目要
求的。
1. 化学与能源、材料、食品、医药等联系紧密,下列说法正确的是
A.乙烯、硫酸、化肥等属于精细化学品,医药、农药、食品添加剂属于大宗化学品
B.碳化硅抗氧化且耐高温,可用作固体电解质
C.低压法制得的低密度聚乙烯可用于生产薄膜、绝缘材料等产品
D.氯化镁、硫酸钙、葡萄糖酸-δ-内酯等都是制作豆腐常用的凝固剂
2.物质的性质决定其用途,下列与物质性质相关的说法正确的是
A.油脂产生“哈喇”味,因其发生了氧化反应 B.某溶液焰色试验呈黄色,说明其溶质是钠盐
C.金属锂保存在盛有煤油的广口试剂瓶中 D.高锰酸钾与苯酚应存放在同一药品柜中
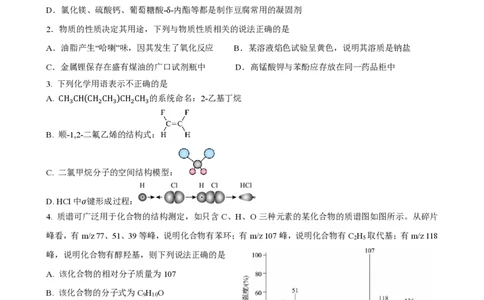
3. 下列化学用语表示不正确的是
A. CH CH(CH CH )CH CH 的系统命名:2-乙基丁烷
3 2 3 2 3
B. 顺-1,2-二氟乙烯的结构式:
C. 二氯甲烷分子的空间结构模型:
D.HCl中𝜎键形成过程:
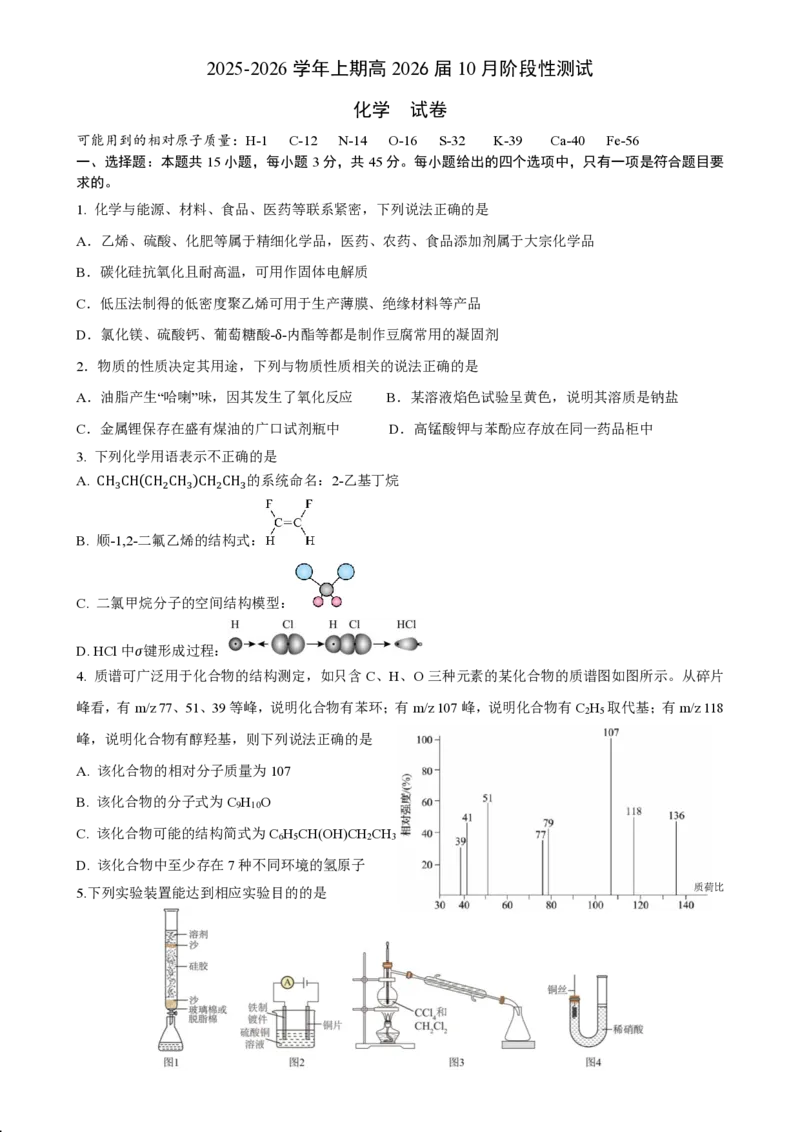
4. 质谱可广泛用于化合物的结构测定,如只含C、H、O三种元素的某化合物的质谱图如图所示。从碎片
峰看,有m/z 77、51、39等峰,说明化合物有苯环;有m/z 107峰,说明化合物有C H 取代基;有m/z 118
2 5
峰,说明化合物有醇羟基,则下列说法正确的是
A. 该化合物的相对分子质量为107
B. 该化合物的分子式为C H O
9 10
C. 该化合物可能的结构简式为C H CH(OH)CH CH
6 5 2 3
D. 该化合物中至少存在7种不同环境的氢原子
5.下列实验装置能达到相应实验目的的是 质荷比10.下列事实与所给解释不相符的是
选项 事实 解释
A 原子光谱是离散的谱线 原子核外电子的能量是量子化的
B 铂在王水中的溶解性大于浓硝酸 王水的氧化性更强
C 淀粉—聚丙烯酸钠树脂具有强大的吸水和保水能力 —COONa具有强亲水性
D 纳米铅晶体的熔点低于普通金属铅 纳米铅晶体的比表面积大
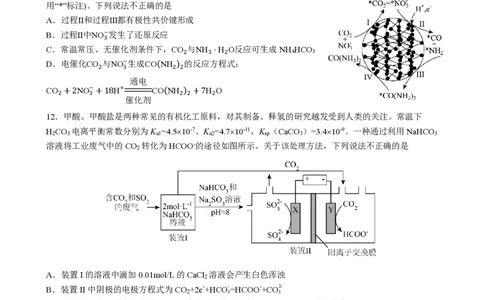
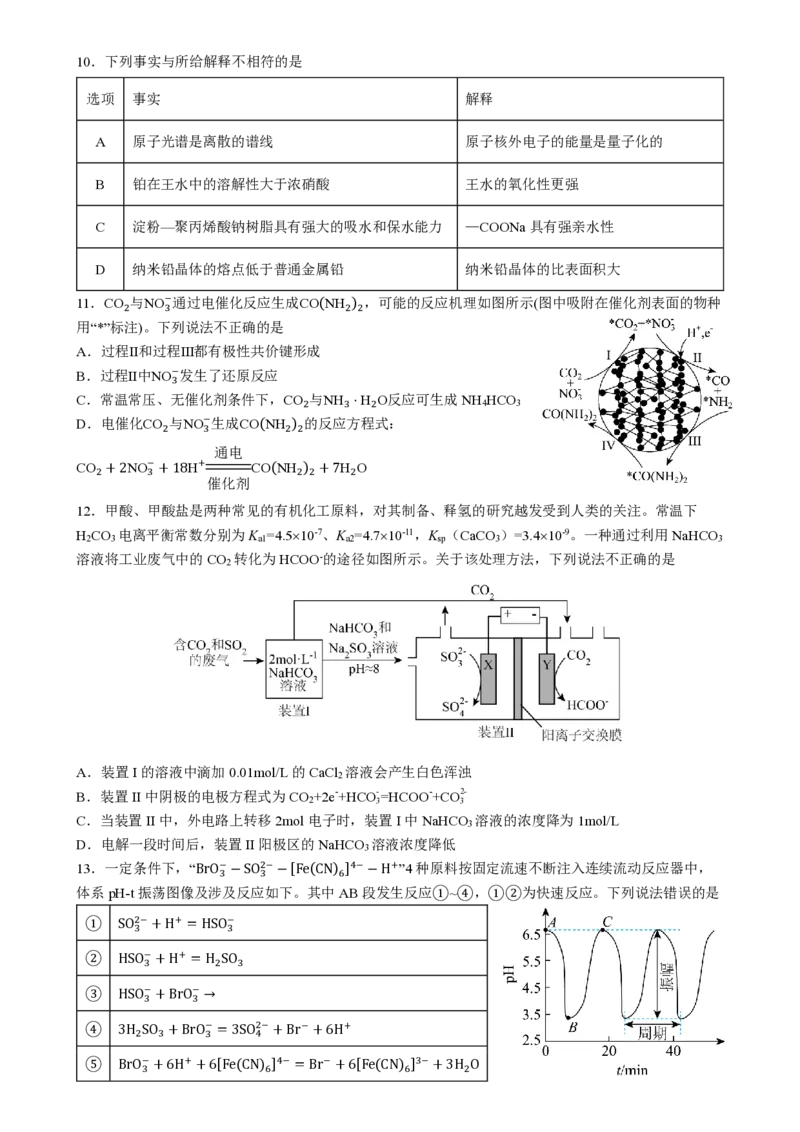
11.CO 与NO−通过电催化反应生成CO(NH ) ,可能的反应机理如图所示(图中吸附在催化剂表面的物种
2 3 2 2
用“*”标注)。下列说法不正确的是
A.过程Ⅱ和过程Ⅲ都有极性共价键形成
B.过程Ⅱ中NO−发生了还原反应
3
C.常温常压、无催化剂条件下,CO 与NH ⋅H O反应可生成NH HCO
2 3 2 4 3
D.电催化CO 与NO−生成CO(NH ) 的反应方程式:
2 3 2 2
通电
CO +2NO−+18H+ CO(NH ) +7H O
2 3 2 2 2
催化剂
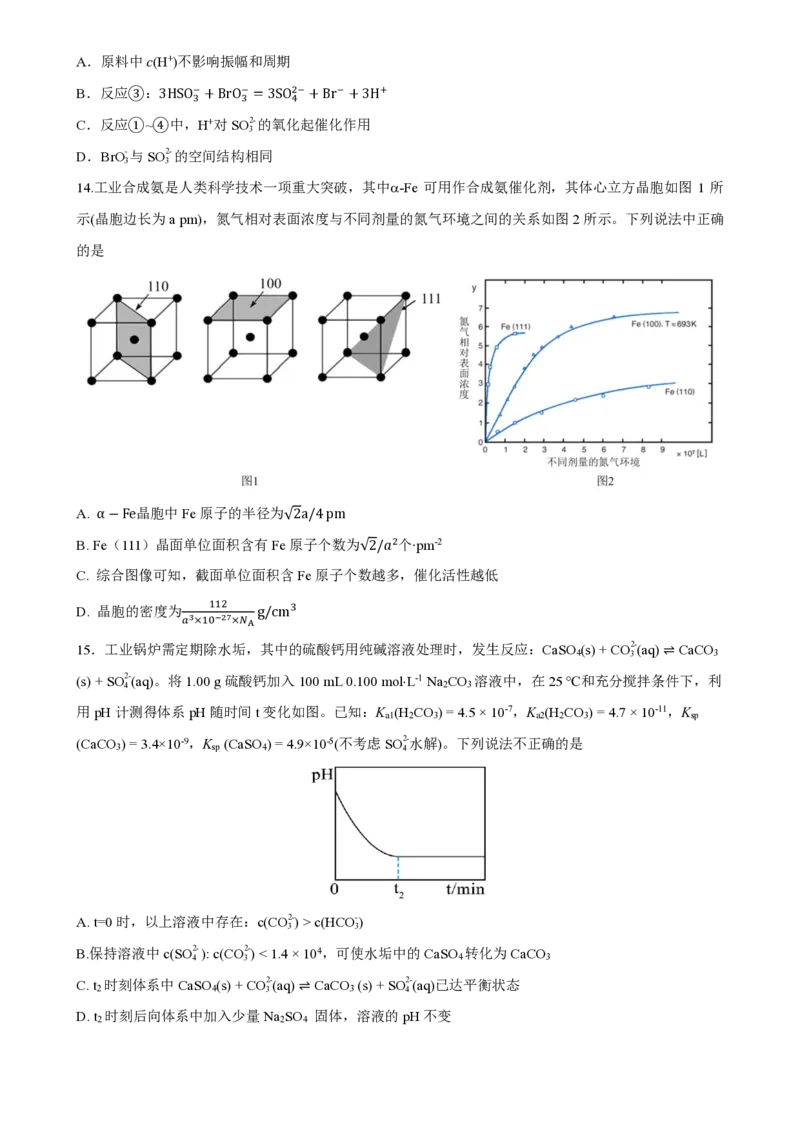
12.甲酸、甲酸盐是两种常见的有机化工原料,对其制备、释氢的研究越发受到人类的关注。常温下
H CO 电离平衡常数分别为K =4.510-7、K =4.710-11,K (CaCO )=3.410-9。一种通过利用NaHCO
2 3 a1 a2 sp 3 3
溶液将工业废气中的CO 转化为HCOO-的途径如图所示。关于该处理方法,下列说法不正确的是
2
A.装置I的溶液中滴加0.01mol/L的CaCl 溶液会产生白色浑浊
2
B.装置II中阴极的电极方程式为CO +2e-+HCO- =HCOO-+CO2-
2 3 3
C.当装置II中,外电路上转移2mol电子时,装置I中NaHCO 溶液的浓度降为1mol/L
3
D.电解一段时间后,装置II阳极区的NaHCO 溶液浓度降低
3
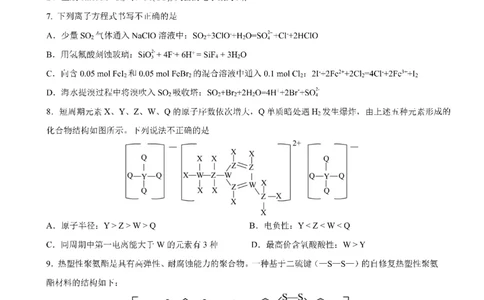
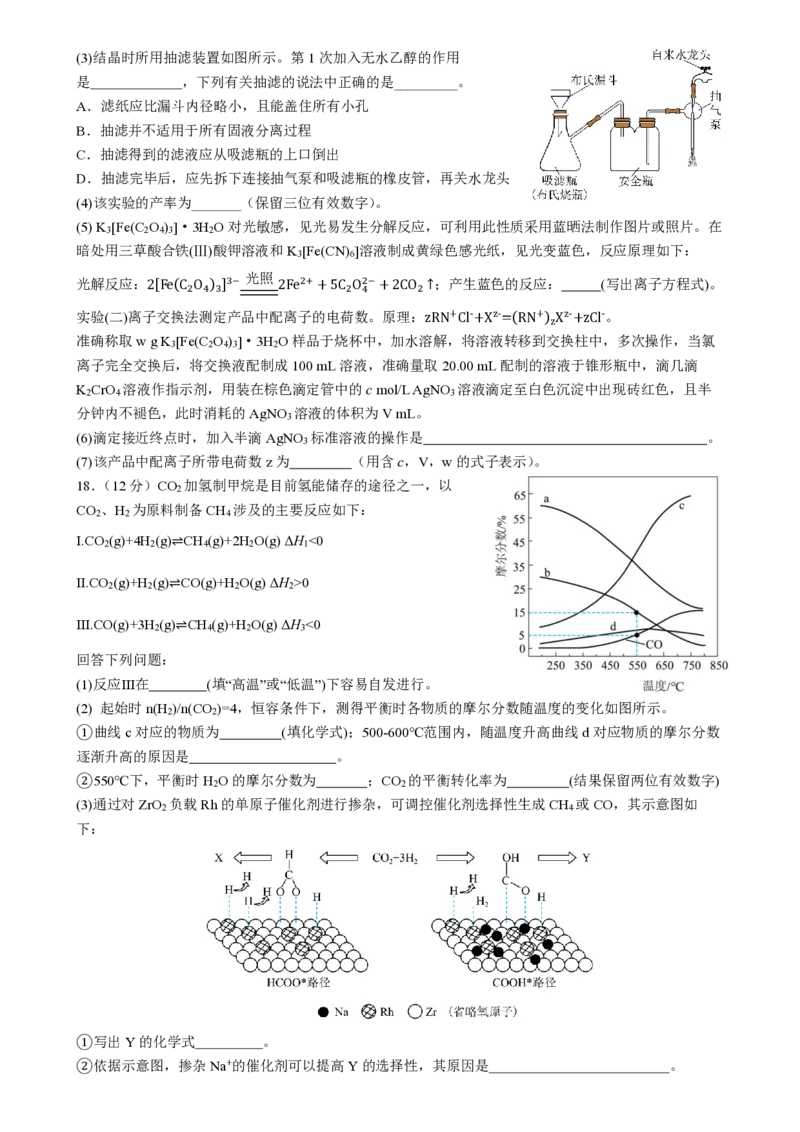
13.一定条件下,“BrO−−SO2−−[Fe(CN) ]4−−H+”4种原料按固定流速不断注入连续流动反应器中,
3 3 6
体系pH-t振荡图像及涉及反应如下。其中AB段发生反应①~④,①②为快速反应。下列说法错误的是
① SO2−+H+ =HSO−
3 3
② HSO−+H+ =H SO
3 2 3
③ HSO−+BrO− →
3 3
④ 3H SO +BrO− =3SO2−+Br−+6H+
2 3 3 4
⑤ BrO−+6H++6[Fe(CN) ]4− =Br−+6[Fe(CN) ]3−+3H O
3 6 6 2A.原料中c(H+)不影响振幅和周期
B.反应③:3HSO−+BrO− =3SO2−+Br−+3H+
3 3 4
C.反应①~④中,H+对SO2- 的氧化起催化作用
3
D.BrO- 与SO2- 的空间结构相同
3 3
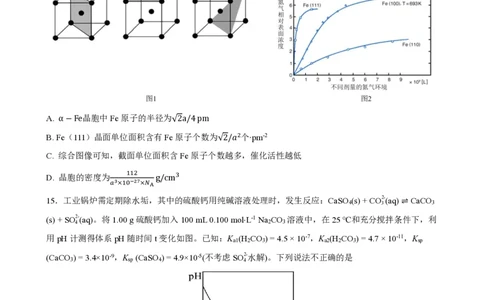
14.工业合成氨是人类科学技术一项重大突破,其中-Fe 可用作合成氨催化剂,其体心立方晶胞如图 1 所
示(晶胞边长为a pm),氮气相对表面浓度与不同剂量的氮气环境之间的关系如图2所示。下列说法中正确
的是
A. α−Fe晶胞中Fe原子的半径为√2a/4 pm
B.Fe(111)晶面单位面积含有Fe原子个数为√2/𝑎2个∙pm-2
C. 综合图像可知,截面单位面积含Fe原子个数越多,催化活性越低
D. 晶胞的密度为 112 g/cm3
𝑎3×10−27×𝑁A
15.工业锅炉需定期除水垢,其中的硫酸钙用纯碱溶液处理时,发生反应:CaSO (s) + CO2-(aq) ⇌ CaCO
4 3 3
(s)+ SO2-(aq)。将1.00 g硫酸钙加入100 mL 0.100 molL-1 Na CO 溶液中,在25 ℃和充分搅拌条件下,利
4 2 3
用pH计测得体系pH随时间t变化如图。已知:K (H CO ) = 4.5 × 10-7,K (H CO ) = 4.7 × 10-11,K
a1 2 3 a2 2 3 sp
(CaCO ) = 3.4×10-9,K (CaSO ) = 4.9×10-5(不考虑SO2-水解)。下列说法不正确的是
3 sp 4 4
A.t=0时,以上溶液中存在:c(CO2-) > c(HCO-)
3 3
B.保持溶液中c(SO2- ): c(CO2-) < 1.4 × 104,可使水垢中的CaSO 转化为CaCO
4 3 4 3
C.t 时刻体系中CaSO (s) + CO2-(aq) ⇌ CaCO (s) + SO2-(aq)已达平衡状态
2 4 3 3 4
D.t 时刻后向体系中加入少量Na SO 固体,溶液的pH不变
2 2 4二、非选择题:本题共 4小题,共55分。
16. (12分)电解铜的阳极泥中含PtTe、PdSe、Pt、Pd、Au、Cu等物质,以该阳极泥为原料,分离和回
收Au、Pt、Pd、Cu等金属或其化合物的工艺流程如图所示:
已知:
①PtTe中Pt为+2价,“氧化焙烧”时,阳极泥中的化合态Pt、Pd均转化为单质。
② (NH ) PtCl 易溶于水,(NH ) PtCl、(NH ) PdCl 难溶于水;③K (NH ) PdCl =9.910−8;
4 2 4 4 2 6 4 2 6 sp 4 2 6
回答下列问题:
(1)写出 Te的价电子排布式: 。
52
(2)“氧化焙烧”中,PtTe发生反应的化学方程式为 。
(3)滤液b溶质的主要成分是 (填化学式)。
(4)“氯浸”工艺中,金属 P 、t P d 、 A u 被氧化为配离子:PtCl 2−、PdCl 2−、AuCl −。
6 6 4
①Pd→PdCl 2−的转化中氧化剂与还原剂的物质的量之比为 。
6
②“分金”加入过量草酸的作用,除析出金属Au外,还有 。
(5) “沉钯”之前,测得溶液中c
PdCl
2−
=0.1molL−1,加入等体积的
0 6
N H
4
C l 溶液充分反应,测得反应后
混合液中c
PdCl
2−
=1.110−6molL−1,则初始加入
6
N H
4
C l 溶液的浓度为 m o l L − 1 (忽略溶液混合时
的体积变化)。
17.(16分)某实验小组设计实验制备三草酸合铁(Ⅲ)酸钾晶体{K [Fe(C O ) ]·3H O}(M=491g/mol)并
3 2 4 3 2
测定其配离子电荷数。
实验(一)制备K [Fe(C O ) ]·3H O。简易制备流程如下:
3 2 4 3 2
I. FeC O ·2H O的合成: 在100 mL烧杯中先加4.00 g FeSO •7H O、2滴3.00 mol/L H SO 溶液和30
2 4 2 4 2 2 4
mL水,搅拌均匀,再加入10 mL K C O 饱和溶液,过滤、洗涤,得到黄色沉淀FeC O ·2H O;
2 2 4 2 4 2
II. FeC O ·2H O的氧化[FeC O ·2H O被氧化时有Fe(OH) 生成]:在黄色沉淀中加入12 mL K C O 饱
2 4 2 2 4 2 3 2 2 4
和溶液,搅拌均匀,滴加10 mL 10%双氧水,继续搅拌,直至溶液转变为深红棕色并伴有大量细小的气
泡产生,然后在沸水浴中浓缩溶液至体积约20 mL;
III. K [Fe(C O ) ]·3H O产品的提纯:在浓缩溶液中加入K C O 溶液和H C O 溶液。结晶时,在溶液中
3 2 4 3 2 2 2 4 2 2 4
加入10 mL无水乙醇,搅拌均匀,将溶液微热,冷却结晶,抽滤。再用10 mL无水乙醇洗涤产品,最终
得到4.91 g产品。
(1)浓缩溶液时可除去 (填化学式)。
(2)提纯三草酸合铁(Ⅲ)酸钾时,添加K C O 溶液和H C O 溶液的目的是 。
2 2 4 2 2 4(3)结晶时所用抽滤装置如图所示。第1次加入无水乙醇的作用
是 ,下列有关抽滤的说法中正确的是_________。
A.滤纸应比漏斗内径略小,且能盖住所有小孔
B.抽滤并不适用于所有固液分离过程
C.抽滤得到的滤液应从吸滤瓶的上口倒出
D.抽滤完毕后,应先拆下连接抽气泵和吸滤瓶的橡皮管,再关水龙头
(4)该实验的产率为_______(保留三位有效数字)。
(5) K [Fe(C O ) ]·3H O对光敏感,见光易发生分解反应,可利用此性质采用蓝晒法制作图片或照片。在
3 2 4 3 2
暗处用三草酸合铁(Ⅲ)酸钾溶液和K [Fe(CN) ]溶液制成黄绿色感光纸,见光变蓝色,反应原理如下:
3 6
光解反应:2[Fe(C O ) ]3−
光照
2Fe2++5C O2−+2CO ↑;产生蓝色的反应: (写出离子方程式)。
2 4 3 2 4 2
实验(二)离子交换法测定产品中配离子的电荷数。原理:zRN+Cl-+Xz-=(RN+) Xz-+zCl-。
z
准确称取w g K [Fe(C O ) ]·3H O样品于烧杯中,加水溶解,将溶液转移到交换柱中,多次操作,当氯
3 2 4 3 2
离子完全交换后,将交换液配制成100 mL溶液,准确量取20.00 mL配制的溶液于锥形瓶中,滴几滴
K CrO 溶液作指示剂,用装在棕色滴定管中的c mol/L AgNO 溶液滴定至白色沉淀中出现砖红色,且半
2 4 3
分钟内不褪色,此时消耗的AgNO 溶液的体积为V mL。
3
(6)滴定接近终点时,加入半滴AgNO 标准溶液的操作是 。
3
(7)该产品中配离子所带电荷数z为 (用含c,V,w的式子表示)。
18.(12分)CO 加氢制甲烷是目前氢能储存的途径之一,以
2
CO 、H 为原料制备CH 涉及的主要反应如下:
2 2 4
Ⅰ.CO (g)+4H (g)⇌CH (g)+2H O(g) ΔH <0
2 2 4 2 1
Ⅱ.CO (g)+H (g)⇌CO(g)+H O(g) ΔH >0
2 2 2 2
Ⅲ.CO(g)+3H (g)⇌CH (g)+H O(g) ΔH <0
2 4 2 3
回答下列问题:
(1)反应Ⅲ在 (填“高温”或“低温”)下容易自发进行。
(2) 起始时n(H )/n(CO )=4,恒容条件下,测得平衡时各物质的摩尔分数随温度的变化如图所示。
2 2
①曲线c对应的物质为 (填化学式);500-600℃范围内,随温度升高曲线d对应物质的摩尔分数
逐渐升高的原因是 。
②550℃下,平衡时H O的摩尔分数为 ;CO 的平衡转化率为 (结果保留两位有效数字)
2 2
(3)通过对ZrO 负载Rh的单原子催化剂进行掺杂,可调控催化剂选择性生成CH 或CO,其示意图如
2 4
下:
①写出Y的化学式 。
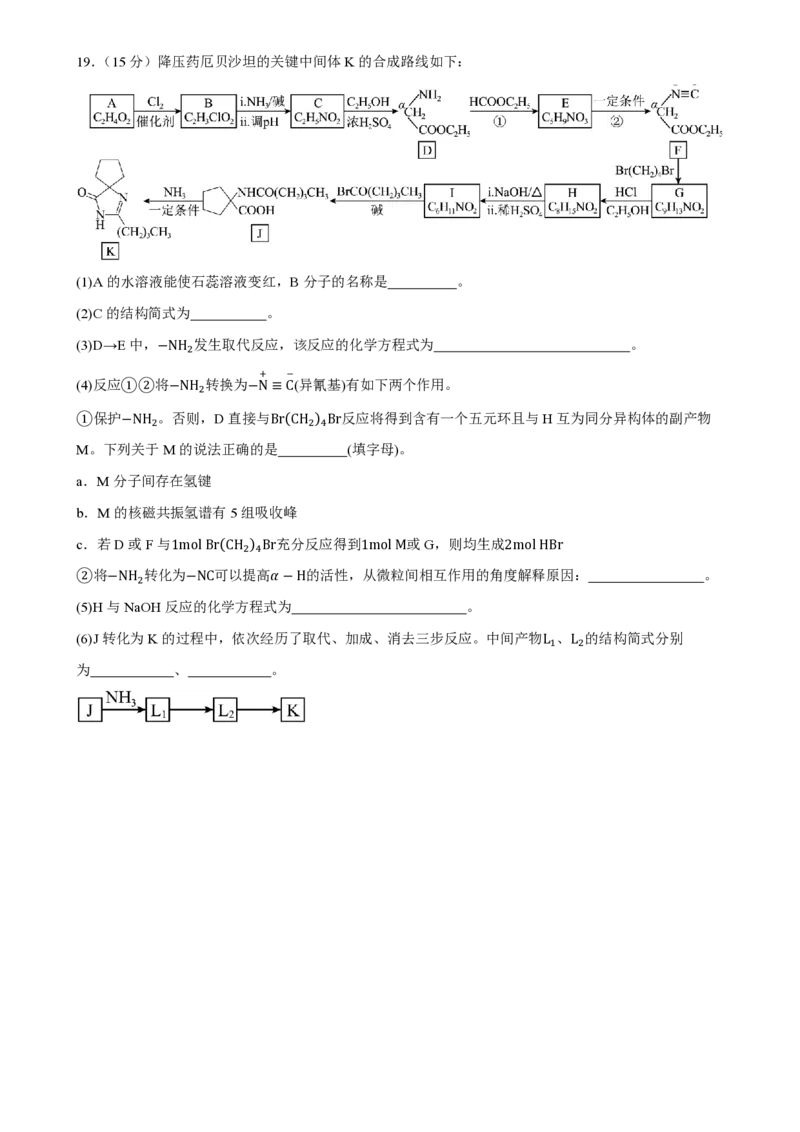
②依据示意图,掺杂Na+的催化剂可以提高Y的选择性,其原因是 。19.(15分)降压药厄贝沙坦的关键中间体K的合成路线如下:
(1)A的水溶液能使石蕊溶液变红,B分子的名称是 。
(2)C的结构简式为 。
(3)D→E中,−NH 发生取代反应,该反应的化学方程式为 。
2
+ −
(4)反应①②将−NH 转换为−N≡C(异氰基)有如下两个作用。
2
①保护−NH 。否则,D直接与Br(CH ) Br反应将得到含有一个五元环且与H互为同分异构体的副产物
2 2 4
M。下列关于M的说法正确的是 (填字母)。
a.M分子间存在氢键
b.M的核磁共振氢谱有5组吸收峰
c.若D或F与1mol Br(CH ) Br充分反应得到1mol M或G,则均生成2mol HBr
2 4
②将−NH 转化为−NC可以提高𝛼−H的活性,从微粒间相互作用的角度解释原因: 。
2
(5)H与NaOH反应的化学方程式为 。
(6)J转化为K的过程中,依次经历了取代、加成、消去三步反应。中间产物L 、L 的结构简式分别
1 2
为 、 。