文档内容
山东省名校考试联盟2024-2025学年高三下学期3月高考模
拟考试 化学试题
学校:___________姓名:___________班级:___________考号:___________
一、未知
1.山东历史文化底蕴深厚、地理位置优越、物产丰富,下列说法错误的是
A.临沂大青山锰矿含大量氧化锰,可用铝热法冶炼
B.龙山文化遗址的蛋壳黑陶高柄杯,可用黏土经一系列物理变化制得
C.潍坊风筝骨架材料可用竹篾制作,竹篾主要成分为纤维素
D.东营黄河三角洲的形成与胶体聚沉有关
2.物质性质决定用途,两者对应关系错误的是
A.FeO为黑色粉末状固体,可用于制作打印机的墨粉
B. 具有良好的光学性能,可用于制作光导纤维
C. 受到撞击时能迅速产生大量 ,可用于汽车安全气囊的气体发生剂
D.抗坏血酸具有还原性,可用作水果罐头中的抗氧化剂
3.下列化学用语正确的是
A. 的系统命名:2-甲基-3-苯基丙酸
B.邻羟基苯甲醛中的氢键可以表示为
C.天然橡胶的反式结构简式为
D. 分子中 键的形成
4.下列描述错误的是
A. 的VSEPR模型为正八面体 B. : 大于 ;
C. 是含有极性键的极性分子 D.1mol金刚砂中含有4mol 键
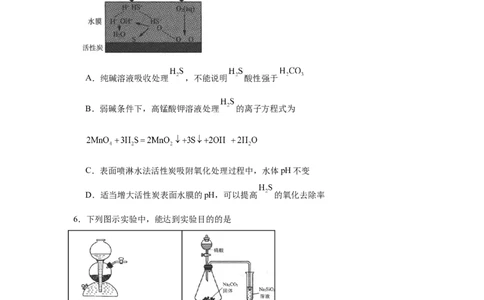
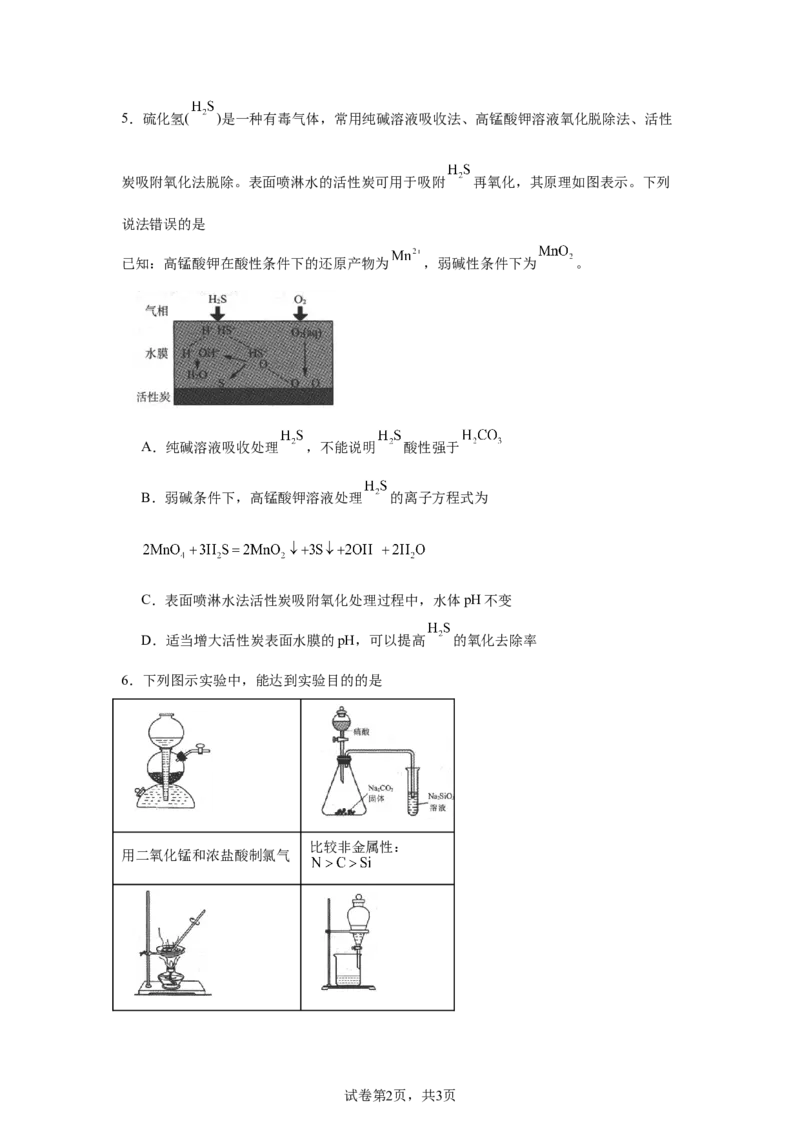
试卷第1页,共3页5.硫化氢( )是一种有毒气体,常用纯碱溶液吸收法、高锰酸钾溶液氧化脱除法、活性
炭吸附氧化法脱除。表面喷淋水的活性炭可用于吸附 再氧化,其原理如图表示。下列
说法错误的是
已知:高锰酸钾在酸性条件下的还原产物为 ,弱碱性条件下为 。
A.纯碱溶液吸收处理 ,不能说明 酸性强于
B.弱碱条件下,高锰酸钾溶液处理 的离子方程式为
C.表面喷淋水法活性炭吸附氧化处理过程中,水体pH不变
D.适当增大活性炭表面水膜的pH,可以提高 的氧化去除率
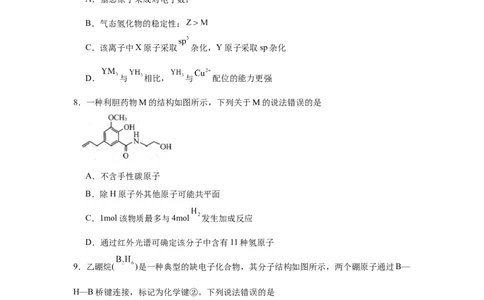
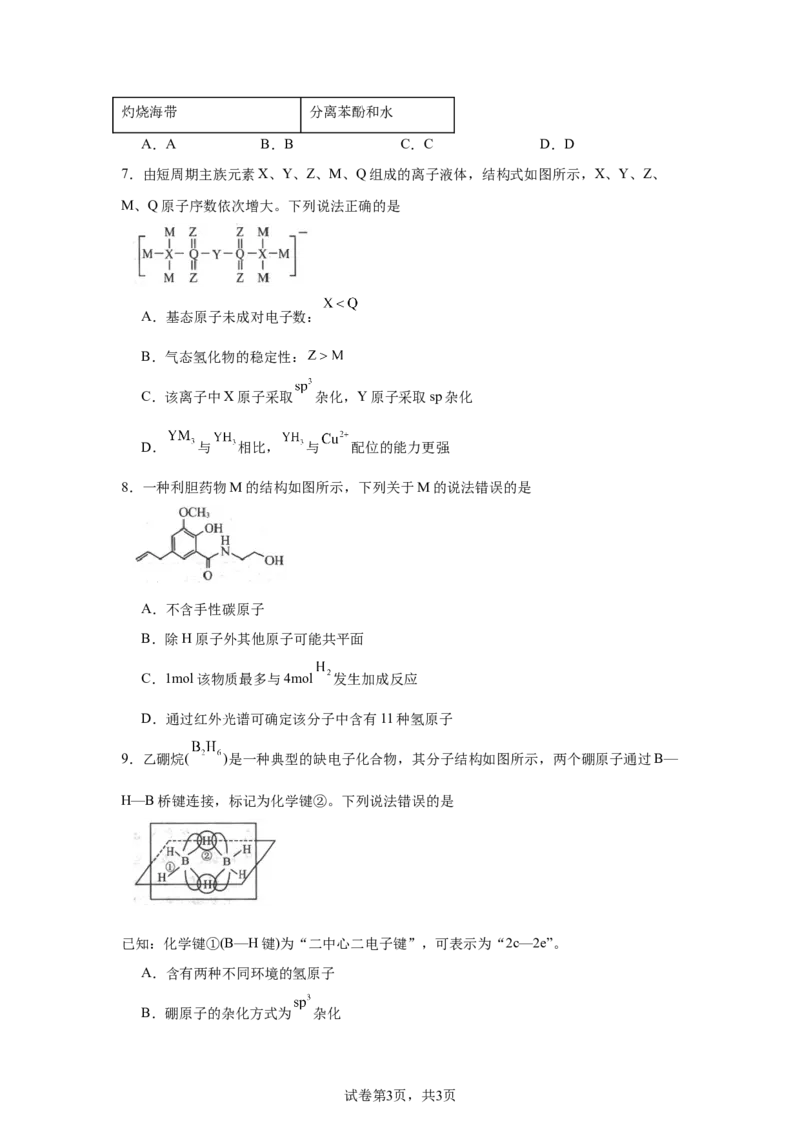
6.下列图示实验中,能达到实验目的的是
比较非金属性:
用二氧化锰和浓盐酸制氯气
试卷第2页,共3页灼烧海带 分离苯酚和水
A.A B.B C.C D.D
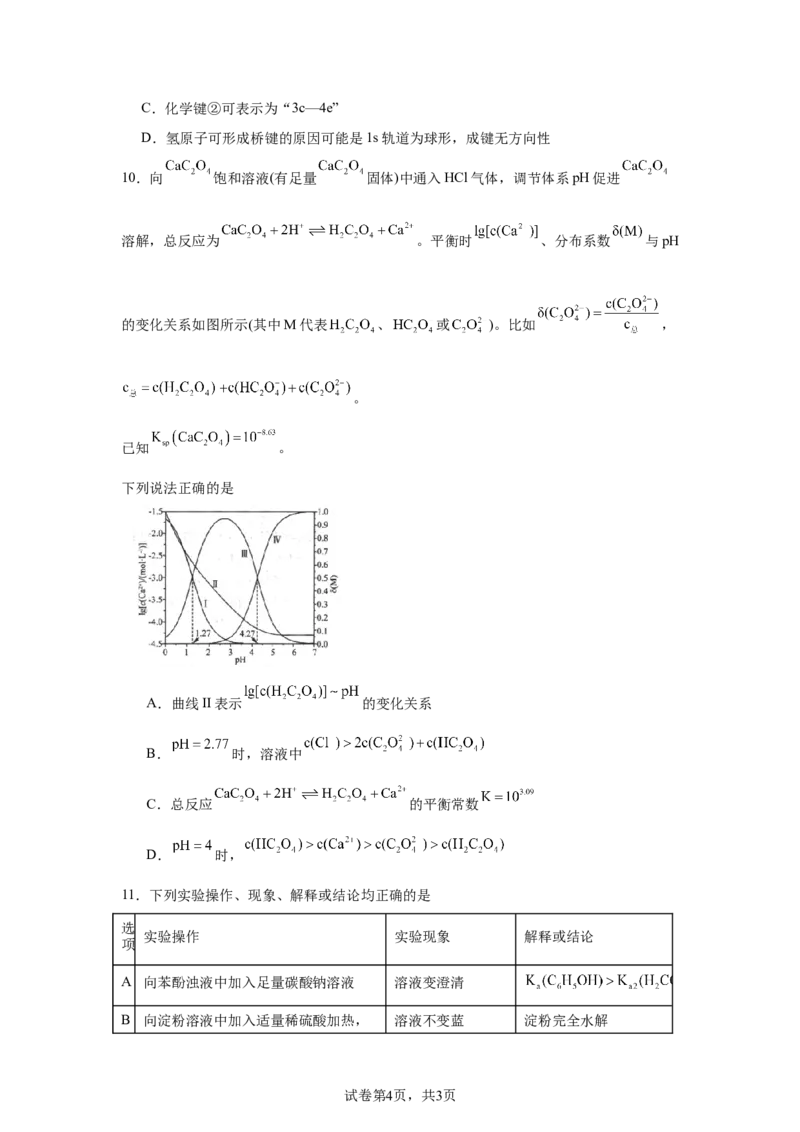
7.由短周期主族元素X、Y、Z、M、Q组成的离子液体,结构式如图所示,X、Y、Z、
M、Q原子序数依次增大。下列说法正确的是
A.基态原子未成对电子数:
B.气态氢化物的稳定性:
C.该离子中X原子采取 杂化,Y原子采取sp杂化
D. 与 相比, 与 配位的能力更强
8.一种利胆药物M的结构如图所示,下列关于M的说法错误的是
A.不含手性碳原子
B.除H原子外其他原子可能共平面
C.1mol该物质最多与4mol 发生加成反应
D.通过红外光谱可确定该分子中含有11种氢原子
9.乙硼烷( )是一种典型的缺电子化合物,其分子结构如图所示,两个硼原子通过B—
H—B桥键连接,标记为化学键②。下列说法错误的是
已知:化学键①(B—H键)为“二中心二电子键”,可表示为“2c—2e”。
A.含有两种不同环境的氢原子
B.硼原子的杂化方式为 杂化
试卷第3页,共3页C.化学键②可表示为“3c—4e”
D.氢原子可形成桥键的原因可能是1s轨道为球形,成键无方向性
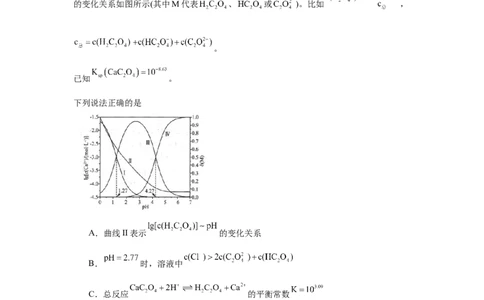
10.向 饱和溶液(有足量 固体)中通入HCl气体,调节体系pH促进
溶解,总反应为 。平衡时 、分布系数 与pH
的变化关系如图所示(其中M代表 、 或 )。比如 ,
。
已知 。
下列说法正确的是
A.曲线II表示 的变化关系
B. 时,溶液中
C.总反应 的平衡常数
D. 时,
11.下列实验操作、现象、解释或结论均正确的是
选
实验操作 实验现象 解释或结论
项
A 向苯酚浊液中加入足量碳酸钠溶液 溶液变澄清
B 向淀粉溶液中加入适量稀硫酸加热, 溶液不变蓝 淀粉完全水解
试卷第4页,共3页冷却后加入NaOH溶液至碱性,再滴
加少量碘水
用洁净的铂丝在酒精灯上灼烧至无
C 火焰呈黄色 该溶液为钠盐溶液
色,再蘸取某溶液,进行焰色试验
一段时间 甲池的出现蓝色沉 相同介质中,负极的
D 淀,乙池的无明显 腐蚀速率大于阴极的
现象 腐蚀速率
后,分别取铁电极附近溶液于2支试
管中,均滴加铁氰化钾溶液
A.A B.B C.C D.D
12.己二酸是工业上最有应用价值的脂肪族二元羧酸。我国科学家合成了四氧化三钴/石墨
炔( )复合电催化剂,利用该催化剂实现了己二酸的高效绿色制备,工作原理如
图所示,下列说法错误的是
A.a极电势高于b极
B.制备己二酸的电极反应式为
C.该装置工作一段时间后,b极区需补充水
D.该装置工作中至少涉及三种能量转化形式
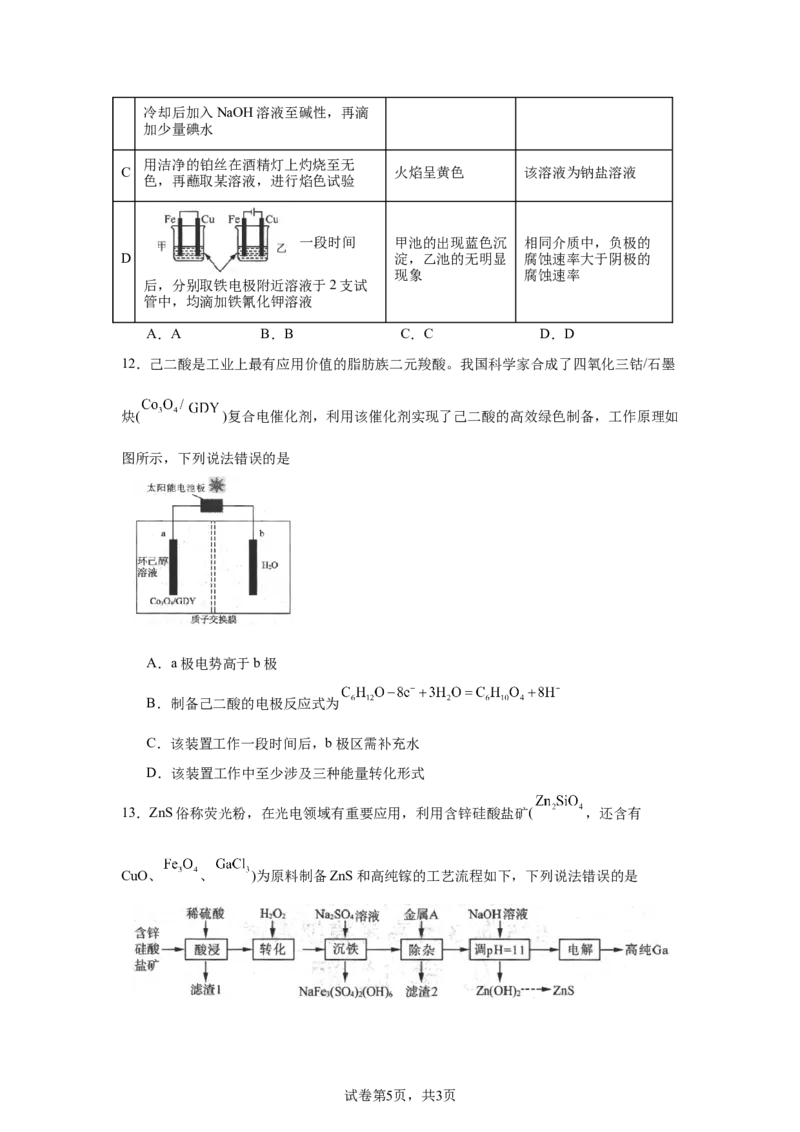
13.ZnS俗称荧光粉,在光电领域有重要应用,利用含锌硅酸盐矿( ,还含有
CuO、 、 )为原料制备ZnS和高纯镓的工艺流程如下,下列说法错误的是
试卷第5页,共3页已知:①镓及其化合物性质类似于铝,溶液中的氯离子会影响镓电解析出;
② ;
③ 时, 开始溶解; 时, 。
A.“滤渣1”的主要成分为
B.“电解”操作中,阴极电极反应式为
C.金属A为Zn,目的是置换
D.“沉铁”的离子反应为
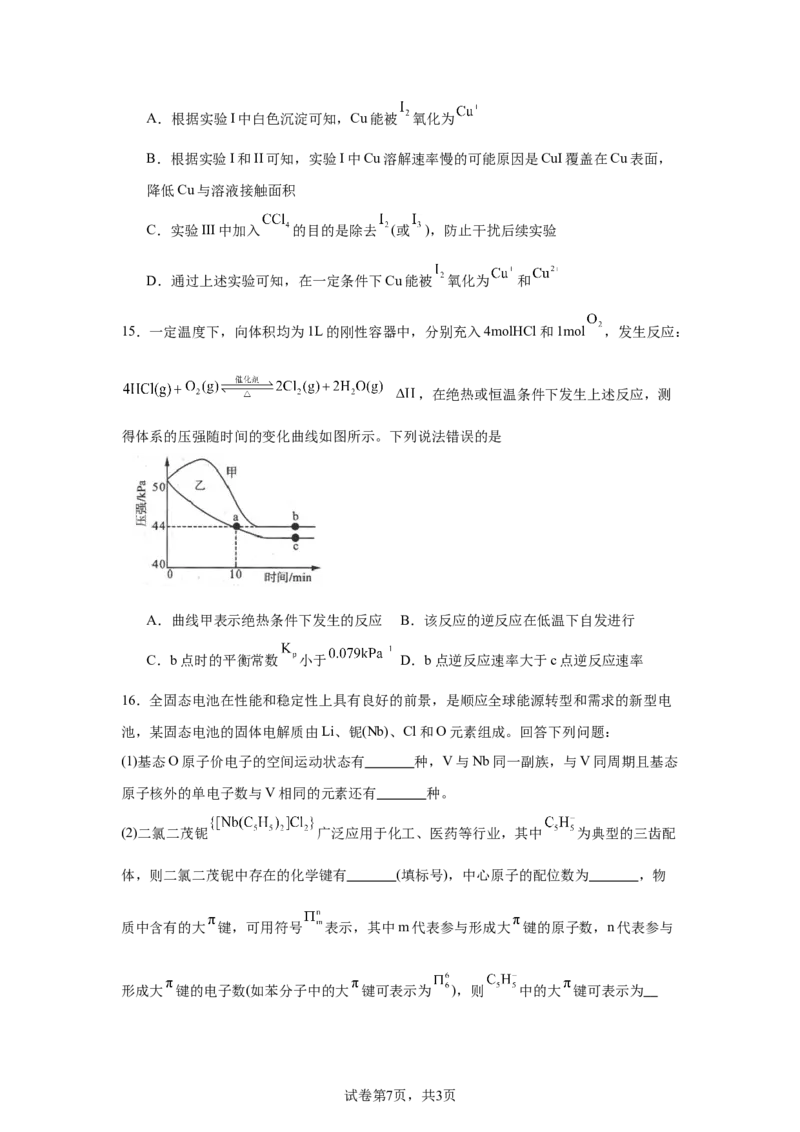
14.某化学兴趣小组探究Cu被 氧化的产物,实验记录如下:
编
实验操作 实验现象
号
实 极少量的 溶解,溶液变为浅红色;充分反应后,红色的铜粉转
验I 化为白色沉淀,溶液仍为浅红色
实
完全溶解,溶液为深红棕色;红色的铜粉快速溶解,充分反应
验
后,溶液仍为深红棕色
II
实 深红棕色溶液加 后分层,下层溶液显紫红色,上层溶液无
验 色;无色溶液中滴加浓氨水,无明显现象,静置一段时间后溶液
III 变为深蓝色
已知:① 易溶于KI溶液,发生反应 (红棕色), 和 氧化性几乎相同;
② (蓝色); (无色); (无色)易被空气氧化。
下列说法错误的是
试卷第6页,共3页A.根据实验I中白色沉淀可知,Cu能被 氧化为
B.根据实验I和II可知,实验I中Cu溶解速率慢的可能原因是CuI覆盖在Cu表面,
降低Cu与溶液接触面积
C.实验III中加入 的目的是除去 (或 ),防止干扰后续实验
D.通过上述实验可知,在一定条件下Cu能被 氧化为 和
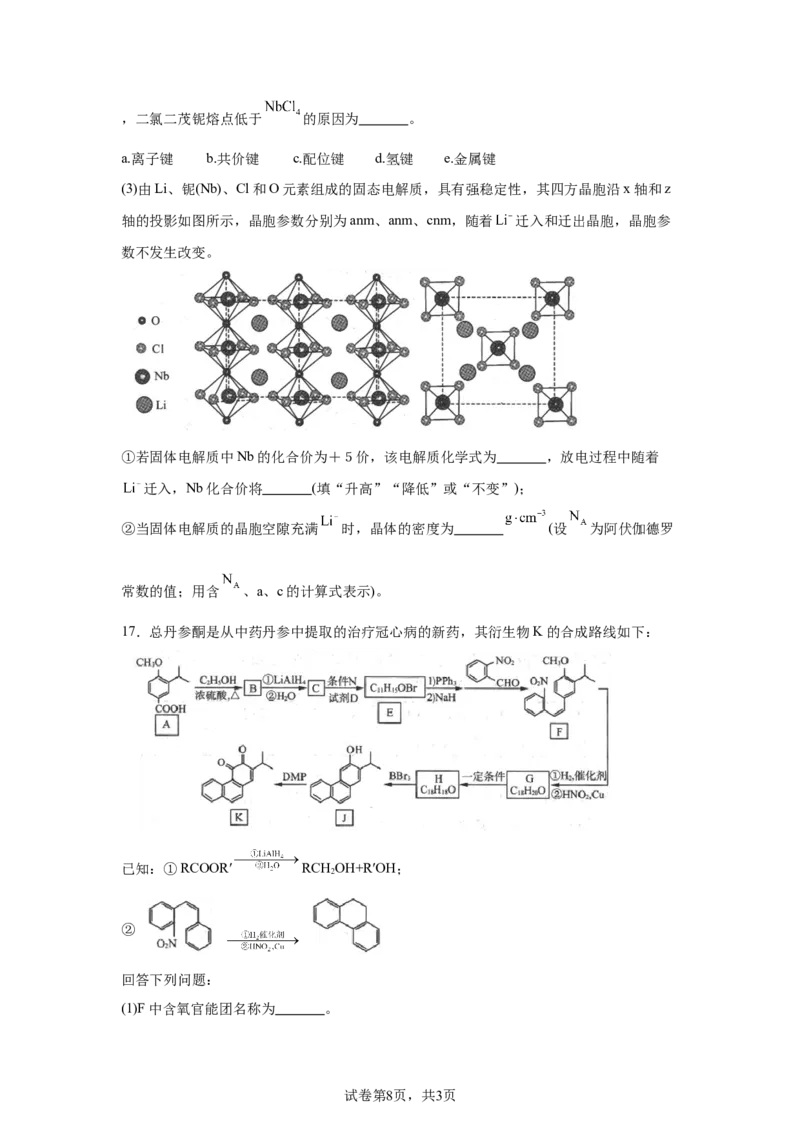
15.一定温度下,向体积均为1L的刚性容器中,分别充入4molHCl和1mol ,发生反应:
,在绝热或恒温条件下发生上述反应,测
得体系的压强随时间的变化曲线如图所示。下列说法错误的是
A.曲线甲表示绝热条件下发生的反应 B.该反应的逆反应在低温下自发进行
C.b点时的平衡常数 小于 D.b点逆反应速率大于c点逆反应速率
16.全固态电池在性能和稳定性上具有良好的前景,是顺应全球能源转型和需求的新型电
池,某固态电池的固体电解质由Li、铌(Nb)、Cl和O元素组成。回答下列问题:
(1)基态O原子价电子的空间运动状态有 种,V与Nb同一副族,与V同周期且基态
原子核外的单电子数与V相同的元素还有 种。
(2)二氯二茂铌 广泛应用于化工、医药等行业,其中 为典型的三齿配
体,则二氯二茂铌中存在的化学键有 (填标号),中心原子的配位数为 ,物
质中含有的大 键,可用符号 表示,其中m代表参与形成大 键的原子数,n代表参与
形成大 键的电子数(如苯分子中的大 键可表示为 ),则 中的大 键可表示为
试卷第7页,共3页,二氯二茂铌熔点低于 的原因为 。
a.离子键 b.共价键 c.配位键 d.氢键 e.金属键
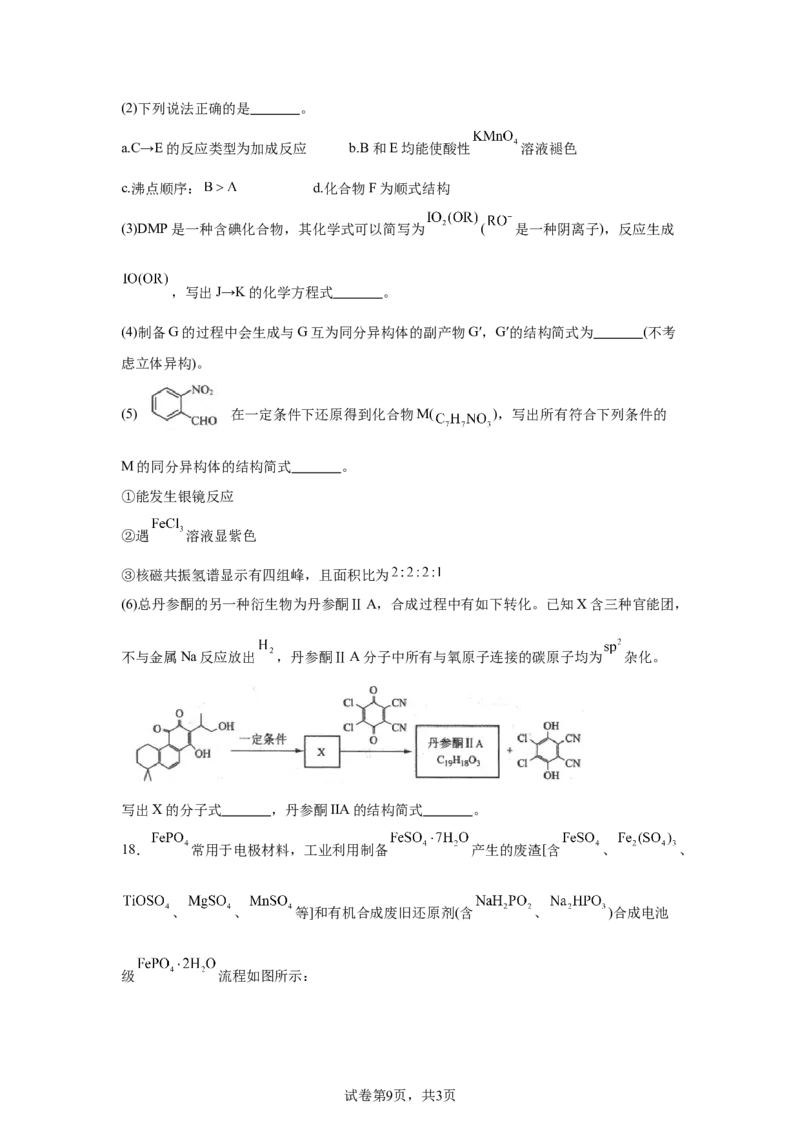
(3)由Li、铌(Nb)、Cl和O元素组成的固态电解质,具有强稳定性,其四方晶胞沿x轴和z
轴的投影如图所示,晶胞参数分别为anm、anm、cnm,随着 迁入和迁出晶胞,晶胞参
数不发生改变。
①若固体电解质中Nb的化合价为+5价,该电解质化学式为 ,放电过程中随着
迁入,Nb化合价将 (填“升高”“降低”或“不变”);
②当固体电解质的晶胞空隙充满 时,晶体的密度为 (设 为阿伏伽德罗
常数的值;用含 、a、c的计算式表示)。
17.总丹参酮是从中药丹参中提取的治疗冠心病的新药,其衍生物K的合成路线如下:
已知:①RCOOR′ RCHOH+R′OH;
2
②
回答下列问题:
(1)F中含氧官能团名称为 。
试卷第8页,共3页(2)下列说法正确的是 。
a.C→E的反应类型为加成反应 b.B和E均能使酸性 溶液褪色
c.沸点顺序: d.化合物F为顺式结构
(3)DMP是一种含碘化合物,其化学式可以简写为 ( 是一种阴离子),反应生成
,写出J→K的化学方程式 。
(4)制备G的过程中会生成与G互为同分异构体的副产物G′,G′的结构简式为 (不考
虑立体异构)。
(5) 在一定条件下还原得到化合物M( ),写出所有符合下列条件的
M的同分异构体的结构简式 。
①能发生银镜反应
②遇 溶液显紫色
③核磁共振氢谱显示有四组峰,且面积比为
(6)总丹参酮的另一种衍生物为丹参酮ⅡA,合成过程中有如下转化。已知X含三种官能团,
不与金属Na反应放出 ,丹参酮ⅡA分子中所有与氧原子连接的碳原子均为 杂化。
写出X的分子式 ,丹参酮IIA的结构简式 。
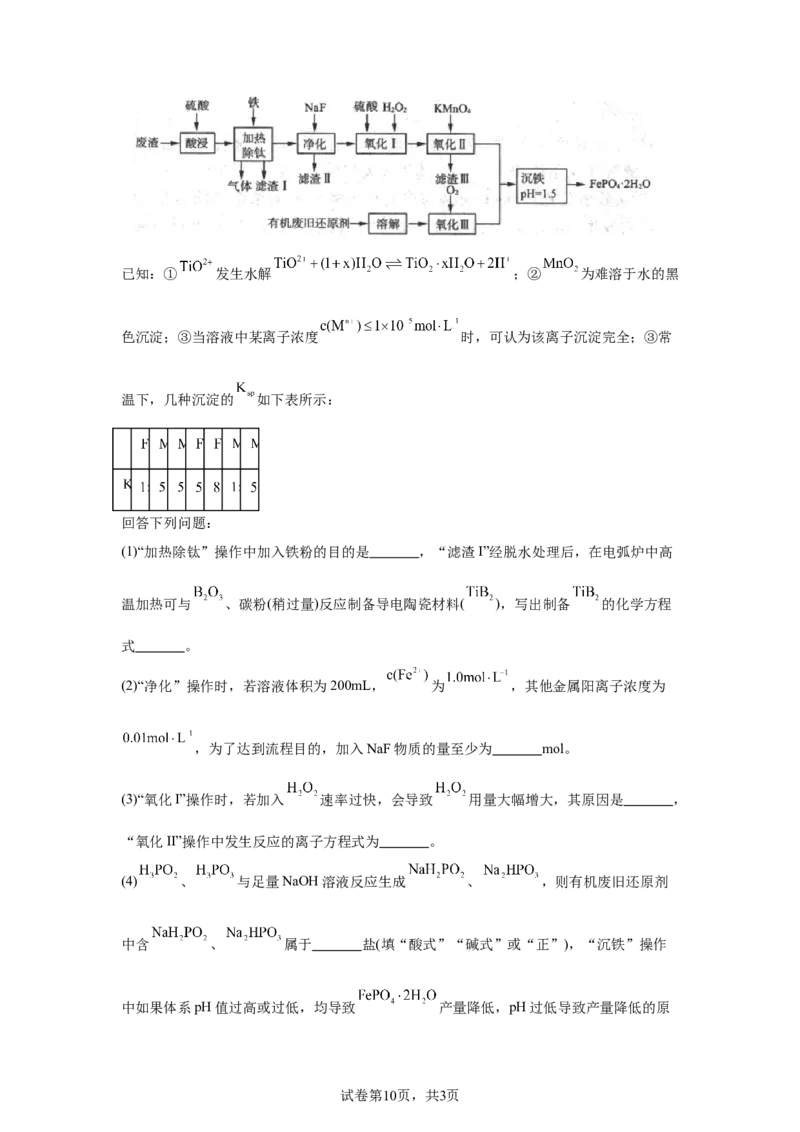
18. 常用于电极材料,工业利用制备 产生的废渣[含 、 、
、 、 等]和有机合成废旧还原剂(含 、 )合成电池
级 流程如图所示:
试卷第9页,共3页已知:① 发生水解 ;② 为难溶于水的黑
色沉淀;③当溶液中某离子浓度 时,可认为该离子沉淀完全;③常
温下,几种沉淀的 如下表所示:
回答下列问题:
(1)“加热除钛”操作中加入铁粉的目的是 ,“滤渣I”经脱水处理后,在电弧炉中高
温加热可与 、碳粉(稍过量)反应制备导电陶瓷材料( ),写出制备 的化学方程
式 。
(2)“净化”操作时,若溶液体积为200mL, 为 ,其他金属阳离子浓度为
,为了达到流程目的,加入NaF物质的量至少为 mol。
(3)“氧化I”操作时,若加入 速率过快,会导致 用量大幅增大,其原因是 ,
“氧化II”操作中发生反应的离子方程式为 。
(4) 、 与足量NaOH溶液反应生成 、 ,则有机废旧还原剂
中含 、 属于 盐(填“酸式”“碱式”或“正”),“沉铁”操作
中如果体系pH值过高或过低,均导致 产量降低,pH过低导致产量降低的原
试卷第10页,共3页因是 。“沉铁”后的余液中含有大量的 , 溶解度与温度关系如图所
示,从余液中提取 的操作是 。
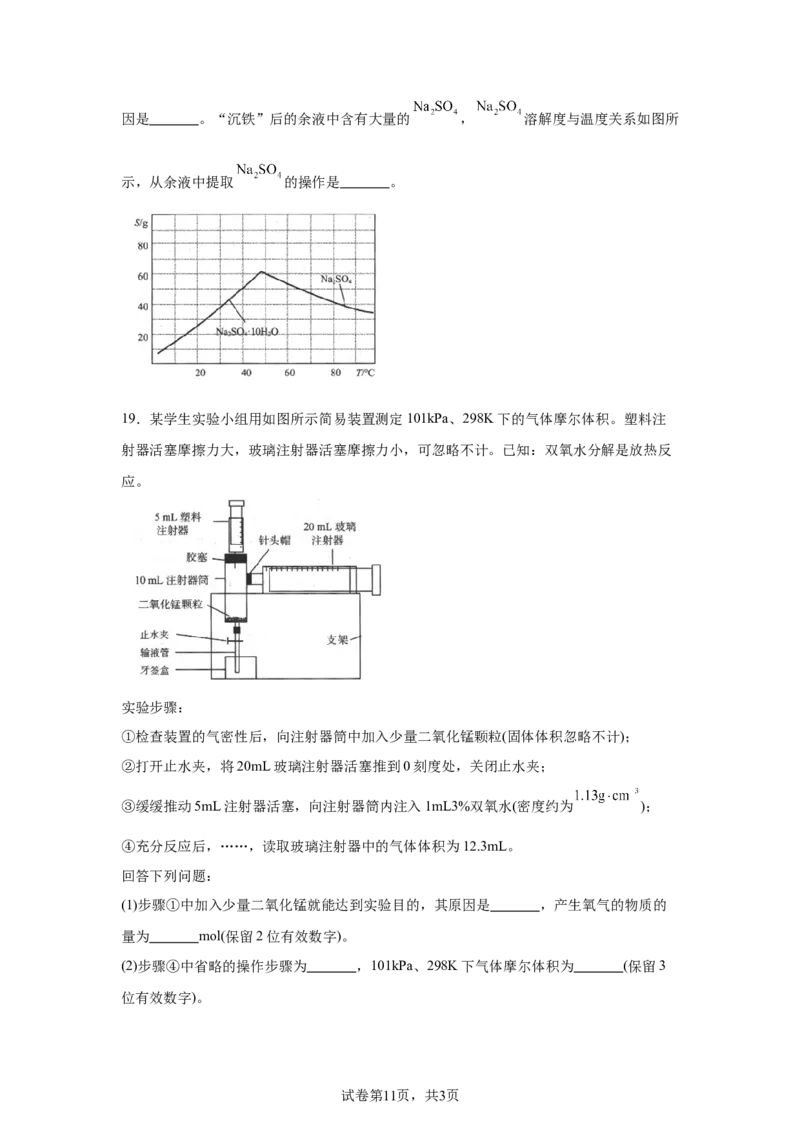
19.某学生实验小组用如图所示简易装置测定101kPa、298K下的气体摩尔体积。塑料注
射器活塞摩擦力大,玻璃注射器活塞摩擦力小,可忽略不计。已知:双氧水分解是放热反
应。
实验步骤:
①检查装置的气密性后,向注射器筒中加入少量二氧化锰颗粒(固体体积忽略不计);
②打开止水夹,将20mL玻璃注射器活塞推到0刻度处,关闭止水夹;
③缓缓推动5mL注射器活塞,向注射器筒内注入1mL3%双氧水(密度约为 );
④充分反应后,……,读取玻璃注射器中的气体体积为12.3mL。
回答下列问题:
(1)步骤①中加入少量二氧化锰就能达到实验目的,其原因是 ,产生氧气的物质的
量为 mol(保留2位有效数字)。
(2)步骤④中省略的操作步骤为 ,101kPa、298K下气体摩尔体积为 (保留3
位有效数字)。
试卷第11页,共3页(3)若反应器中不再产生气泡,立即读取玻璃注射器中的气体体积,则测定的101kPa、
298K下的氧气的气体摩尔体积 (填“偏大”“偏小”或“无影响”)。
(4)另一化学实验小组提出 分解与浓度密切相关,随着浓度降低分解速率降低,当浓
度低于一定程度,不再发生分解,同时其浓度随着放置时间也会发生改变。因此提出新的
实验方案:
I.利用排水法收集VmL101kPa、298K下的氧气,将其缓慢通入稍过量 碱性悬浊
液,反应生成 ;
II.向反应后悬浊液加入稍过量KI溶液,再加硫酸酸化,在暗处静置5min,将其配成
500mL溶液,取出25.00mL于碘量瓶中,然后加入几滴淀粉试液,用
标准溶液滴定生成的 ( )。
①配成500mL溶液时需要的主要玻璃仪器有烧杯、玻璃棒、 ,则达到滴定终点时
消耗 溶液的体积为amL,则101kPa、298K下气体摩尔体积为 ;
②下列操作导致101kPa、298K下气体摩尔体积偏大的是 (填标号)。
a.步骤I中,氧气通入速率太快
b.步骤II中,配制500mL溶液时,仰视定容
c.步骤II中,滴定前滴定管尖嘴有气泡,滴定结束后尖嘴没有气泡
20.甲烷催化氧化偶联制乙烯是提高甲烷附加值的一项重要研究课题,其涉及的反应如下:
反应I.
反应II.
已知:① 的选择性 ;② :用平衡分压代替平衡浓度
计算;分压 总压 物质的量分数。
回答下列问题:
试卷第12页,共3页(1)反应III: 的 ,反应III能
够自发进行的原因是 。
(2)向刚性容器中充入4mol 和2mol ,起始压强为 、温度为TK条件下发
生反应I、反应II,达到平衡后,测得反应体系总压强为 , 的分压为
,则 的选择性为 ,反应I的分压表示的平衡常数
(用含 代数式表示),若再向刚性容器中充入一定量的 ,重新达平衡后,则分
压 将 (填“增大”“减小”或“不变”), 将 (填“增大”
“减小”或“不变”)。
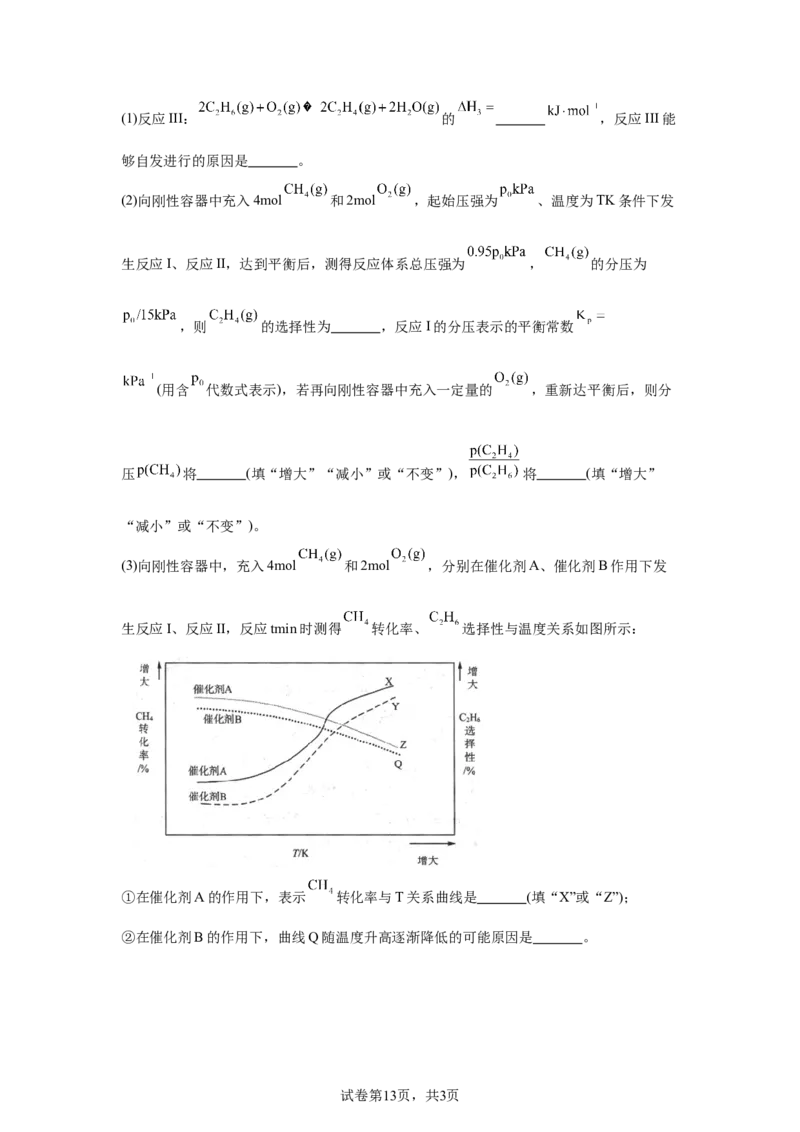
(3)向刚性容器中,充入4mol 和2mol ,分别在催化剂A、催化剂B作用下发
生反应I、反应II,反应tmin时测得 转化率、 选择性与温度关系如图所示:
①在催化剂A的作用下,表示 转化率与T关系曲线是 (填“X”或“Z”);
②在催化剂B的作用下,曲线Q随温度升高逐渐降低的可能原因是 。
试卷第13页,共3页