文档内容
高途高中·化学
点睛卷
2024
浙江省-------------------------------- 高途高中化学点睛卷 -----------------------------------
绝密 启用前
【高途】2024年浙江省普通高中学业水平选择性考试模拟测试卷
化 学
本试卷共10页,21小题,满分100分,考试用时90分钟
可能用到的相对原子质量:
H—1 C—12 N—14 O—16 Na—23 Cl—35.5 K—39 Fe—56 Ag—108
一、选择题(本大题共16小题,每小题3分,共48分。每小题列出的四个备选项中只有一个是符
合题目要求的,不选、多选、错选均不得分)
1.下列物质中属于碱性氧化物的是( )
A.HCl B.CO C.NO D.CaO
2.硫酸钡在医疗上常用作消化系统X射线检查的内服药剂,下列说法不正确的是( )
A.Ba元素位于周期表s区 B.所有钡盐都能使蛋白质变性
C.硫酸钡属于强电解质 D.硫酸根离子的空间构型是四面体
3.下列化学用语或图示表达正确的是( )
A.中子数为19的硫原子:19S B.BF 的空间结构模型:
16 3
C.N
2
的电子式:NN D.基态氮原子价层电子轨道表示式:
4.物质的性质决定用途,下列两者对应关系不正确的是( )
A.SiO 能把光的强弱转变为电流的强弱,故SiO 用作光导纤维
2 2
B.Na CO 溶液水解显碱性,油脂碱性条件下水解程度大,故工业上用纯碱去油污
2 3
C. 尾气中CO有还原性,NO 有氧化性,在催化剂作用下转化为CO 和N ,故可用三元催化器处理汽车尾气
x 2 2
D.SO 使溴水或酸性KMnO 溶液褪色,说明SO 有还原性
2 4 2
5.下列关于元素及其化合物的性质说法不正确的是( )
A.Na可与熔融TiCl 反应制取金属Ti B.铁与硫反应易生成硫化铁
4
C.浓硝酸在见光或受热时会发生分解 D.Mg与CO 反应可生成C
2
6.已知反应:2Fe3 3ClO 10OH=2FeO2 3Cl 5H O,下列说法正确的是( )
4 2
A.ClO是还原剂 B.H O是氧化产物
2
C.Fe3发生还原反应 D.生成1molFeO2离子转移3mol电子
4
试卷第2页-------------------------------- 高途高中化学点睛卷 -----------------------------------
7.下列反应的离子方程式表示不正确的是( )
电解
A.用惰性电极电解氯化镁溶液:2Cl 2H O Cl H 2OH
2 2 2
B.明矾溶液中加入过量NaOH溶液:Al3 4OH=Al OH
4
C. 稀硫酸滴入Na S O 溶液中:2H++S O2-=SO +S+H O
2 2 3 2 3 2 2
D.NH HSO 溶液中逐滴加入足量的Ba(OH) 溶液:
4 3 2
NH++HSO-+Ba2++2OH-=BaSO +NH H O+H O
4 3 3 3 2 2
8.下列叙述中正确的是( )
A.乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色
B.向鸡蛋清溶液中加入浓(NH ) SO 溶液,产生沉淀,加水后沉淀溶解
4 2 4
C.分馏、干馏都是物理变化,裂化、裂解都是化学变化
D.糖类、油脂和蛋白质都属于高分子化合物
9.药物中间体X结构如图,下列说法正确的是( )
A.分子中存在手性碳原子
B.分子中所有原子可能共平面
C.1mol该物质与足量H 反应,最多可消耗6mol H
2 2
D.1mol该物质与足量NaOH溶液反应,最多可消耗3mol NaOH
10.短周期主族元素X、Y、Z、R的原子序数依次增大,X是地壳中含量最高的元
素,单质Z在X单质中燃烧火焰呈黄色,R基态原子p能级有一对成对电子。下列说法正确的是( )
A.电负性:X>R>Z>Y B.X与Z组成的化合物肯定含有共价键
C.原子半径:Z>R>X>Y D.气态氢化物的稳定性:X>Y>R
11.锂电池在航空航天领域应用广泛,Li-CO 电池供电的反应机理如图所示,下列说法正确的是( )
2
A.X方向为电流方向 B.交换膜M为阴离子交换膜
C.正极的电极反应式:4Li++4e-+3CO =2Li CO +C D.可采用LiNO 水溶液作为电解质溶液
2 2 3 3
试卷第3页-------------------------------- 高途高中化学点睛卷 -----------------------------------
12.已知:NF 的结构式可以表示为 。一定条件下,氨与氟气发生反应:
3
一定条件
4NH 3F NF 3NH F。下列有关说法错误的是( )
3 2 3 4
A.除F 外,反应物和生成物均为共价化合物 B.NF 中各原子均满足8电子稳定结构
2 3
C.NF 中只含极性共价键 D.NH F中既含有离子键又含有共价键
3 4
13.钡餐造影检查是以医用硫酸钡作为造影剂,口服后随着人体消化管道的蠕动,涂抹在胃肠道内管壁及充
填在管腔内,在X线照射下与周围器官形成明显对比,可以观察胃、食管等器官的外形、大小、位置、扩张性
及蠕动波情况,进而显示消化道有无病变。
已知:常温下,K (BaCO )=5.0×10-9,K (BaSO )=1.0×10-10;H CO 的电离平衡常数K =4.5×10-7,
sp 3 sp 4 2 3 a1
K =5.6×10-11;饱和BaCO 溶液pH约为9.6,人体胃液pH约为2;H SO 的一级电离是完全电离,二级电离电离
a2 3 2 4
常数K =1.0×10-2。结合信息,以下推断不正确的是( )
a2
A.BaSO 在胃液中的溶解度大于1.0×10-5mol·L-1
4
B.若每次加入1L1mol·L-1的Na CO 溶液,至少需要4次加入才能将0.1molBaSO 全部转化为BaCO
2 3 4 3
C.饱和BaCO 溶液通入少量CO 后溶液中:c(CO 2-)<c(HCO -)
3 2 3 3
D.若误服BaCO ,医学上可采用适当浓度的Na SO 溶液洗胃或静脉缓注Na SO 溶液实现解毒
3 2 4 2 4
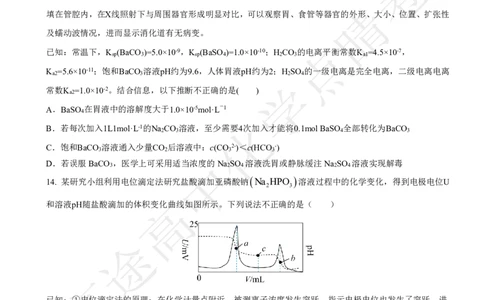
14.
某研究小组利用电位滴定法研究盐酸滴加亚磷酸钠
Na HPO
溶液过程中的化学变化,得到电极电位U
2 3
和溶液pH随盐酸滴加的体积变化曲线如图所示。下列说法不正确的是( )
已知:①电位滴定法的原理:在化学计量点附近,被测离子浓度发生突跃,指示电极电位也发生了突跃,进
而确定滴定终点。
②亚磷酸 H PO 是二元弱酸,其电离常数分别是K 101.4,K 106.7
3 3 al a2
A.a点对应溶液的溶质为NaH PO 和NaCl,pH7
2 3
B.第二次电极电位突跃发生的化学反应为:NaH PO HCl H PO NaCl
2 3 3 3
C.c点对应的溶液中可能存在:c
H
c
OH
c
H
PO
2c
HPO2
2 3 3
D.水的电离程度:a>b
试卷第4页-------------------------------- 高途高中化学点睛卷 -----------------------------------
15.氯胺是由氯气遇到氨气反应生成的一类化合物,是常用的饮用水二级消毒剂,主
要包括一氯胺、二氯胺和三氯胺(NH Cl、NHCl 和NCl )。已知部分化学键的键能和化学反
2 2 3
应的能量变化如表和图所示。下列说法正确的是( )
化学键 N-H N-Cl H-Cl
键能(kJ/mol) 391.3 x 431.8
A.NH (g)2Cl (g) NHCl (g)2HCl(g) ΔH 22.6kJmol1
3 2 2
B.反应过程中的H 1405.6kJmol1
2
C.选用合适的催化剂,可降低反应过程中的H 值
D.表中的x=191.2
16.下列实验方案设计、现象与结论均正确的是( )
目的 方案设计 现象与结论
检验火柴头中是否含有氯
将几根未燃过的火柴头浸入水中,稍后取少量 若有白色沉淀产生,说明
A
元素(ClO) 溶液于试管中,加入稀HNO 、AgNO 溶液 火柴头中含有氯元素
3 3 3
取适量NaOH、1-溴丁烷、无水乙醇,共热,
酸性KMnO 溶液紫红色
B 检验1-溴丁烷消去产物 4
将产生的气体直接通入酸性KMnO 溶液中
4 褪去,有1-丁烯生成
向麦芽糖样品溶液X中加入银氨溶液,水浴加 产生银镜,X中麦芽糖已发
C 检验X中麦芽糖是否水解
热 生水解
溶液变蓝,氧化性:NO -
D 证明NO -氧化性强于I 向KI溶液中加入NaNO 溶液,再滴加淀粉溶液 2
2 2 2
>I
2
A.A B.B C.C D.D
二、非选择题(本大题共5小题,共52分)
17. (10分)根据物质结构与性质的内在联系,回答下列问题:
(1) BCl 和NCl 中心原子的杂化方式分别为________和_______。第一电离能介于B、N之间的第二周期元素有
____
3 __种。3
(2) 卤化物CsICl 受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为____(写化学式)。解释X的
熔点比Y高的2原因_____。
试卷第5页-------------------------------- 高途高中化学点睛卷 -----------------------------------
(3)下列说法正确的是___________。
A. 基态Na 的电子有10种空间运动状态
+
B.每个氯离子周围与它最近且等距的氯离子有12个
C.NaCl晶体的密度为ρg cm ,图示晶胞Na 与Cl 的距离d 58.5 pm
3 2ρNA
3 + −
D.
配合物的稳定性不仅与⋅配体有关,还与中心原子的所带电=荷等因素有关
18.(10分)固体化合物X有三种元素组成。某学习小组开展如下探究实验:
请回答:
(1)组成X的元素有_______,X的化学式为_______。
(2)化合物X与液态氨也能发生类似的反应,请写出相应的化学方程式_________________________。
(3)固体A能溶于NaHF 的水溶液,产物中含一种正八面体的负三价阴离子,写出其相应的离子方程式_______
2
(4)红褐色固体B在真空条件灼烧,反应完全后生成黑色粉末(纯净物),黑色粉末的成分可能是_______,并用
实验验证的方案是_______。
19.(10分)当今,世界多国相继规划了碳达峰、碳中和的时间节点。因此,研发二氧化碳利用技术,降低空
气中二氧化碳含量成为研究热点。
(1)工业上用二氧化碳催化加氢可合成乙醇,其反应原理为:
2CO
2
(g)+6H
2
(g)CH
3
CH
2
OH(g)+3H
2
O(g) H。
△
温度/K 400 500
平衡常数K 9 5.3
通过表格中的数值可以推断:该反应在______(填“高温”、“低温”或“任何温度”)下能自发进行。
试卷第6页-------------------------------- 高途高中化学点睛卷 -----------------------------------
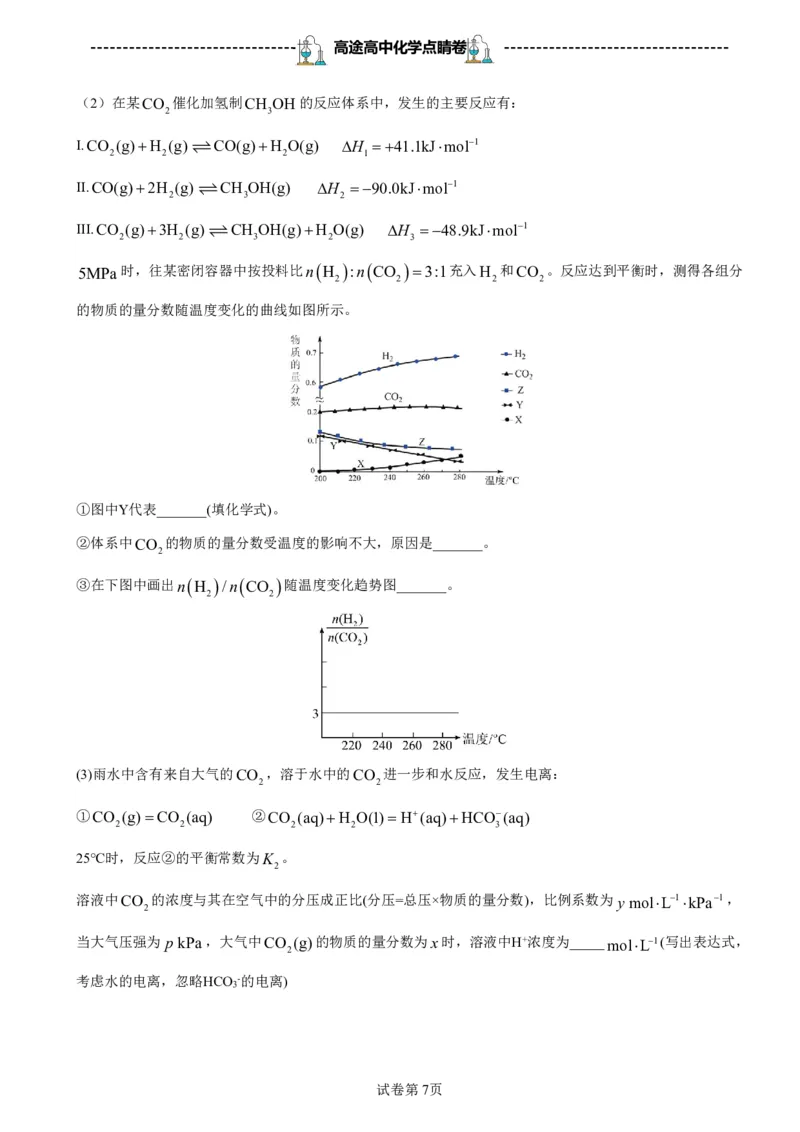
(2)在某CO 催化加氢制CH OH的反应体系中,发生的主要反应有:
2 3
I.CO (g)H (g) CO(g)H O(g) H 41.1kJmol1
2 2 2 l
II.CO(g)2H (g) CH OH(g) H 90.0kJmol1
2 3 2
III.CO (g)3H (g) CH OH(g)H O(g) H 48.9kJmol1
2 2 3 2 3
5MPa时,往某密闭容器中按投料比n H :n CO 3:1充入H 和CO 。反应达到平衡时,测得各组分
2 2 2 2
的物质的量分数随温度变化的曲线如图所示。
①图中Y代表_______(填化学式)。
②体系中CO 的物质的量分数受温度的影响不大,原因是_______。
2
③在下图中画出n H /n CO 随温度变化趋势图_______。
2 2
(3)雨水中含有来自大气的CO ,溶于水中的CO 进一步和水反应,发生电离:
2 2
①CO (g)CO (aq) ②CO (aq)H O(1)H(aq)HCO(aq)
2 2 2 2 3
25℃时,反应②的平衡常数为K 。
2
溶液中CO 的浓度与其在空气中的分压成正比(分压=总压×物质的量分数),比例系数为
y
molL1kPa1,
2
当大气压强为 p kPa,大气中CO (g)的物质的量分数为x时,溶液中H+浓度为_____molL1(写出表达式,
2
考虑水的电离,忽略HCO -的电离)
3
试卷第7页-------------------------------- 高途高中化学点睛卷 -----------------------------------
20.(10分)叠氮化钾能促进难以萌发的种子发育,在新作物育种中应用广泛,实验室制备KN 流程如下。回
3
答下列问题:
I.制备KN :
3
已知:
①制备亚硝酸异丙酯在烧杯中进行;
②制备KN 的D、E和F阶段均在图甲装置中完成。
3
(1)KN 属于__________(填“离子化合物”或“共价化合物”)。
3
(2)仪器A的名称为______,仪器B的作用是______________。
(3)仪器A中发生反应时,CH CHONO与水合肼在碱性条件下,重新生成CH CHOH(异丙醇),该反应
3 2 3 2
的化学方程式为______________________。
(4)关于上述流程中各步骤的说法,错误的是______(填标号)。
A.步骤D还需要的仪器是容量瓶和胶头滴管
B.制备亚硝酸异丙酯时用冰盐浴的目的是防止反应过于剧烈
C.步骤F加入无水乙醇的目的是促进KN 的溶解
3
试卷第8页-------------------------------- 高途高中化学点睛卷 -----------------------------------
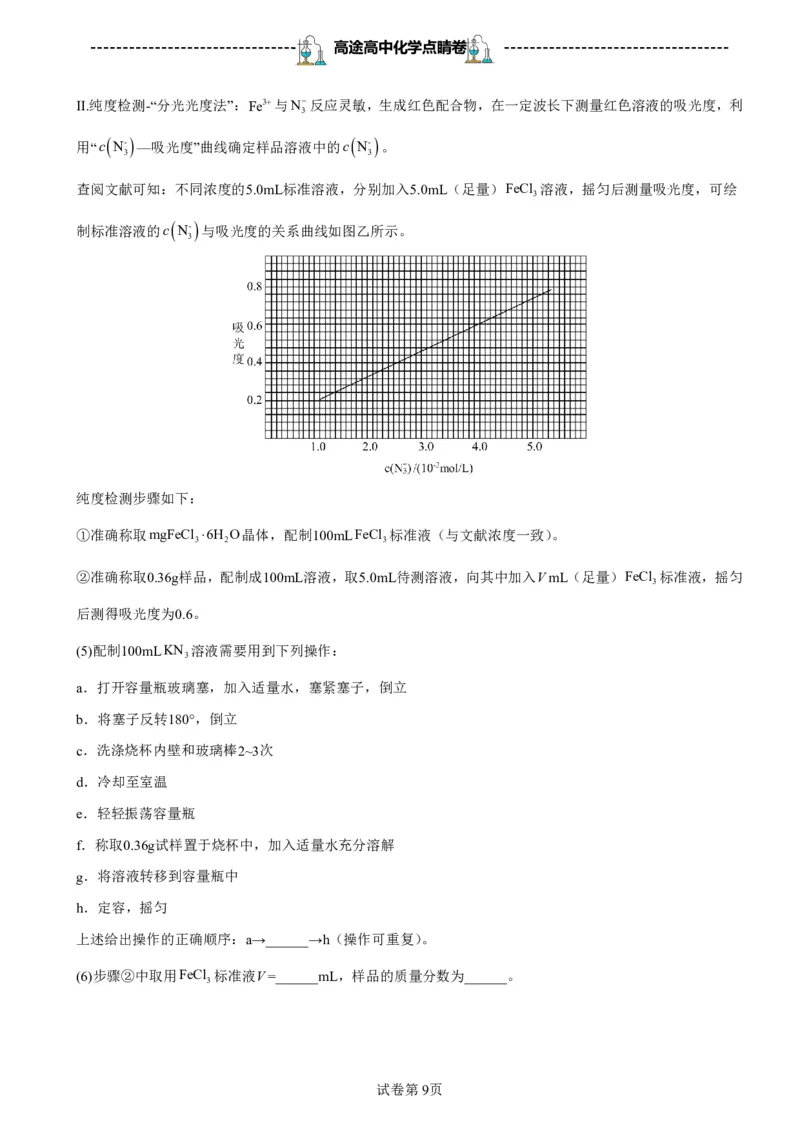
II.纯度检测-“分光光度法”:Fe3与N反应灵敏,生成红色配合物,在一定波长下测量红色溶液的吸光度,利
3
用“c
N-
—吸光度”曲线确定样品溶液中的c
N-
。
3 3
查阅文献可知:不同浓度的5.0mL标准溶液,分别加入5.0mL(足量)FeCl 溶液,摇匀后测量吸光度,可绘
3
制标准溶液的c
N-
与吸光度的关系曲线如图乙所示。
3
纯度检测步骤如下:
①准确称取mgFeCl 6H O晶体,配制100mLFeCl 标准液(与文献浓度一致)。
3 2 3
②准确称取0.36g样品,配制成100mL溶液,取5.0mL待测溶液,向其中加入VmL(足量)FeCl 标准液,摇匀
3
后测得吸光度为0.6。
(5)配制100mLKN 溶液需要用到下列操作:
3
a.打开容量瓶玻璃塞,加入适量水,塞紧塞子,倒立
b.将塞子反转180°,倒立
c.洗涤烧杯内壁和玻璃棒2~3次
d.冷却至室温
e.轻轻振荡容量瓶
f.称取0.36g试样置于烧杯中,加入适量水充分溶解
g.将溶液转移到容量瓶中
h.定容,摇匀
上述给出操作的正确顺序:a→______→h(操作可重复)。
(6)步骤②中取用FeCl 标准液V=______mL,样品的质量分数为______。
3
试卷第9页-------------------------------- 高途高中化学点睛卷 -----------------------------------
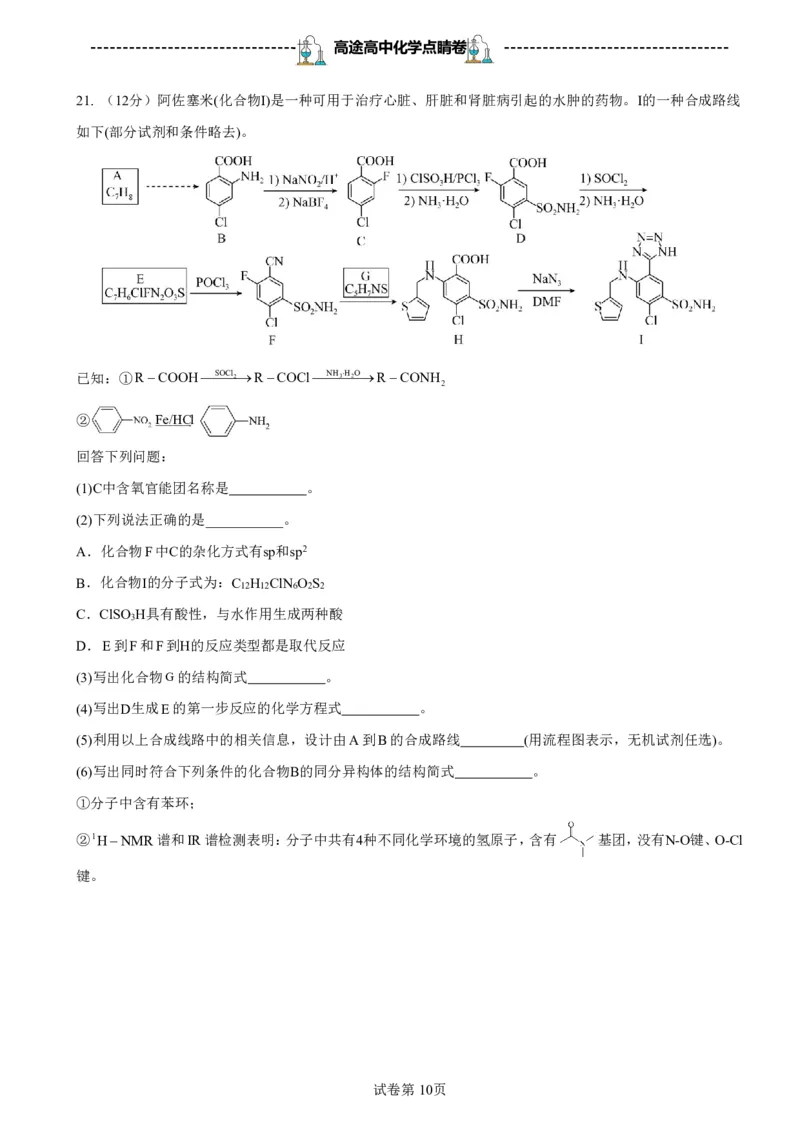
21. (12分)阿佐塞米(化合物Ⅰ)是一种可用于治疗心脏、肝脏和肾脏病引起的水肿的药物。Ⅰ的一种合成路线
如下(部分试剂和条件略去)。
已知:①RCOOHSOCl2RCOClNH3H2ORCONH
2
② Fe/HCl
回答下列问题:
(1)C中含氧官能团名称是 。
(2)下列说法正确的是___________。
A.化合物F中C的杂化方式有sp和sp2
B.化合物I的分子式为:C H ClN O S
12 12 6 2 2
C.ClSO H具有酸性,与水作用生成两种酸
3
D.E到F和F到H的反应类型都是取代反应
(3)写出化合物G的结构简式 。
(4)写出D生成E的第一步反应的化学方程式 。
(5)利用以上合成线路中的相关信息,设计由A到B的合成路线 (用流程图表示,无机试剂任选)。
(6)写出同时符合下列条件的化合物B的同分异构体的结构简式 。
①分子中含有苯环;
②1HNMR谱和IR谱检测表明:分子中共有4种不同化学环境的氢原子,含有 基团,没有N-O键、O-Cl
键。
试卷第10页-------------------------------- 高途高中化学点睛卷 -----------------------------------
【高途】2024年浙江省普通高中学业水平选择性考试模拟测试卷
化学参考答案
1、【答案】D
【分析】碱性氧化物,是指与酸反应生成一种盐和水(除了盐和水以外不包括其它物质)的化合物。
【详解】A.HCl不属于氧化物,故A错误;
B.CO不能与酸反应生成盐和水,故B错误;
C.NO不能与酸反应生成盐和水,故C错误;
D.CaO能与酸反应生成盐和水,属于碱性氧化物,故D正确;故选D。
2、【答案】B
【详解】A.Ba元素位于第ⅡA族,周期表s区,A正确;
B. 可溶性钡盐都能使蛋白质变性,硫酸钡不溶于水,不能使蛋白质变性,B错误;
C. 硫酸钡溶于水能完全电离,属于强电解质,C正确;
D. 硫酸根离子的中心原子键电子对为4,孤电子对为1 6242 =0,空间构型是四面体,D正确;故选
2
B。
3、【答案】B
【分析】根据核素表示判断A,利用杂化轨道理论判断分子中中心原子的杂化类型,根据VSEPR判断分子的
空间构型;根据电子式的定义判断氮气的电子式书写;
【详解】A.中子数为19的硫原子:35S,故A不正确;
16
B.BF 的空间结构模型根据杂化轨道理论,B原子采用sp2杂化,属于平面三角形,故B正确;
3
C.N 的电子式根据最外层电子进行判断::NN:,故C不正确;
2
D.基态氮原子价层电子轨道表示式: ,故D不正确;故选B。
4、【答案】A
【详解】A.SiO 并不能把光的强弱转变为电流的强弱,SiO 用作光导纤维是因为其对光有很好的反射性,
2 2
故A错误;
B.Na CO 溶液中存在碳酸根的水解而显碱性,油脂在碱性条件下水解为甘油和高级脂肪酸盐,甘油和高级
2 3
脂肪酸盐无法重新生成油脂,所以油脂碱性条件下水解程度大,故B正确;
C.汽车尾气中含有CO、NO 等有毒气体,CO有还原性,NO 有氧化性,二者发生氧化还原反应转化为
x x
无污染的为CO 和N ,故C正确。
2 2
试卷第11页-------------------------------- 高途高中化学点睛卷 -----------------------------------
D.SO 使溴水或酸性KMnO 溶液褪色,说明SO 有还原性,故D正确。故选A。
2 4 2
5.【答案】 B
【详解】
A. 金属Na具有强还原性,能与熔融TiCl 反应制取金属Ti,故A正确;
4
B. 铁是变价金属,与氧化性较弱的硫单质共热反应生成硫化亚铁,故B错误;
C. 浓硝酸不稳定,在见光或受热时分解生成二氧化氮,氧气和水,故C正确;
D.Mg在CO 中发生燃烧反应生成MgO和C,故D正确。故选B。
2
6、【答案】D
【详解】
分析方程式中元素化合价可知:Fe从+3→+6,Cl从+1→-1;故Fe3+作还原剂,被氧化,发
生氧化反应,得到氧化产物FeO2- ;ClO 作氧化剂,被还原,发生还原反应,得到还原产
4
物Cl ,生成1molFeO2-离子转移3mol电子,故答案选D。
4
7、【答案】A
A. 用惰性电极电解氯化镁溶液时会生成Mg(OH) 沉淀,离子方程式为:
2
电解
Mg2+2Cl2H O Cl H Mg(OH) ,A项错误;
2 2 2 2
B. 明矾中加入过量NaOH,铝离子与氢氧根离子反应生成Al(OH),离子方程式为Al3 4OH=Al OH
4 4
,B正确;
C. 稀硫酸滴入Na S O 溶液中离子方程式为:2H S O2 SO SH O,C正确;
2 2 3 2 3 2 2
D.NH HSO 溶液中逐滴加入足量的Ba(OH) 溶液生成亚硫酸钡沉淀和一水合氨,D正确。故选A。
4 3 2
8、【答案】B
【详解】A.乙烯、氯乙烯分子中含有不饱和的碳碳双键,可以使酸性高锰酸钾溶液褪色。聚乙烯分子中没有
不饱和键,不能使酸性高锰酸钾溶液褪色,A项错误;
B.鸡蛋清属于蛋白质,浓的(NH ) SO 盐溶液会使蛋白质的溶解度降低从而从溶液中析出,当加水之后,盐
4 2 4
析出的沉淀又可重新溶解,B项正确;
C.干馏是固体或有机物在隔绝空气条件下加热分解的反应过程,是化学变化,C项错误;
D.糖类中单糖、二糖及油脂的相对分子质量在10000以下,不属于高分子,而蛋白质属于高分子化合物,D
项错误;故选B。
9、【答案】C
【详解】A.由结构简式可知,X分子中不含有连有4个不同原子或原子团的手性碳原子,故A错误;
试卷第12页-------------------------------- 高途高中化学点睛卷 -----------------------------------
B.由结构简式可知,X分子中含有空间构型为四面体形的饱和碳原子,则分子中所有原子不可能共平面,故
B错误;
C.由结构简式可知,X分子中含有的苯环、碳碳双键一定条件下能与氢气发生加成反应,则1molX分子最多
可消耗6mol氢气,故C正确;
D.由结构简式可知,X分子中含有的羧基和酯基能与氢氧化钠溶液反应,则1molX分子最多可消耗2mol氢氧
化钠,故D错误;故选C。
10、【答案】C
【分析】短周期主族元素X、Y、Z、R的原子序数依次增大,X是地壳中含量最高的元素,则X为O,单质Z在
X单质中燃烧火焰呈黄色,则Z为Na,Y为F,R基态原子p能级有一对成对电子,则R为S。
【详解】A.根据同周期从左到右电负性逐渐增大,同主族从上到下电负性逐渐减小,因此电负性:F>O>S>Na
,故A错误;
B.X与Z组成的化合物Na O中不含共价键,故B错误;
2
C.电子层数越多,原子半径越大;电子层数相同,核电荷数越大,原子半径越小,则原子半径:Na>S>O>F
,故C正确;
D.根据非金属性越强,其气态氢化物越稳定,因此气态氢化物的稳定性:HF>H O>H S,故D错误。
2 2
故选C。
11、【答案】C
【详解】A.Li为原电池的负极,电子从Li电极经导线流向CO 电极,所以X方向为电子方向,A错误;
2
B.离子交换膜需要Li+通过,所以M为阳离子交换膜,B错误;
C.正极为CO 生成C单质,电极反应式:4Li++4e-+3CO =2Li CO +C,C正确;
2 2 2 3
D.Li为活泼金属,能与水反应,所以该电池不能用水性电解质,D错误;
故选C。
12、【答案】A
【详解】A.NH F为离子化合物,A错误;
4
B.NF 中N和F共用电子对,均满足8电子稳定结构,B正确;
3
C.NF 中N和F共用电子对,N和F对电子对的吸引能力不同,形成极性共价键,C正确;
3
D.NH+和F之间形成离子键,NH+内部N和H之间形成共价键,D正确;
4 4
故选A。
试卷第13页-------------------------------- 高途高中化学点睛卷 -----------------------------------
13、【答案】B
【详解】A项,根据沉淀溶解平衡BaSO (s) Ba2+(aq)+SO 2-(aq),K (BaSO )=1.0×10-10知纯水中
4 4 sp 4
K BaSO c Ba2+ c SO2- 11010
,
c Ba2+ =c SO2- K BaSO =110-5mol/L
,在胃液中因H+
sp 4 4 4 sp 4
和SO 2-结合(硫酸二级电离不完全),使平衡正向移动,溶解度增大,故A正确;B项,向BaSO 中加入Na CO
4 4 2 3
c SO2- K BaSO 110-10 1
溶液,发生反应:BaSO (s)+CO 2-(aq) BaCO (s)+SO 2-(aq),K= 4 = sp 4 = ,
4 3 3 4 c CO2- K BaCO 510-9 50
3 sp 3
若每次加入1L1mol/L的Na CO 溶液能处理BaSO 的物质的量为xmol,K= c SO2 4 - = x 1 得出x= 1 ,将
2 3 4
c
CO2-
1-x 50 51
3
0.1
=5.1
0.1molBaSO 处理需要加入 1 ,至少需要加入6次,故B错误;C项,饱和BaCO 溶液pH约为9.6,饱和BaCO
4 3 3
51
溶液存在BaCO (s) Ba2+(aq)+CO 2-(aq),K (BaCO )=5.0×10-9,碳酸根水解生成碳酸氢根,
3 3 sp 3
c
CO2-
c
H+
c
CO2-
K 5.61011
K 3 5.61011,得出 3 a2 5.6101.4 1,此时c(CO 2-)<c(HCO -)
a2
c
HCO-
c
HCO-
c
H+ 109.6 3 3
3 3
,通入少量CO 后,溶液中CO 2-发生反应减少,HCO -增多,c(CO 2-)<c(HCO -),故C正确;D项,若误服BaCO
2 3 3 3 3 3
,根据BaCO (s)+SO 2-(aq) BaSO (s))+CO 2-(aq),K (BaSO )=1.0×10-10c(Cl-),故
2 3 3
c(H+)b;故D说法正确;
试卷第14页-------------------------------- 高途高中化学点睛卷 -----------------------------------
答案为C。
15、【答案】D
【详解】A.根据图中物质转化关系,NH (g)+Cl (g)=N(g)+3H(g)+2Cl(g) H =1416.9kJ•mol-1,设Cl—Cl
3 2 1
△
键键能为ykJ•mol-1,则有1416.9kJmol-1=(3391.3+y)kJmol-1,解得y=243。再根据方程式
NH (g)+Cl (g)=NH Cl(g)+HCl(g) H=11.3kJ•mol-1 可求得N-Cl键能为191.2kJ•mol-1;
3 2 2
△
计算所给反应NH (g)+2Cl (g)=NHCl (g)+2HCl(g) 相应焓变值,
3 2 2
ΔH=3391.3+2243-(391.3+2191.2+2431.8)kJmol1 22.6kJmol1,则A错误;
B. H=反应物键能和 - 生成物键能和,可得生成物总键能为1416.9kJmol-1-11.3kJmol-1=1405.6 kJmol-1
,气△态原子成键形成1molNH Cl气体和1molHCl气体放出能量,则反应过程中的 H =-1405.6kJ•mol-1,B错
2 2
误; △
C.选用合适的催化剂,可降低反应过程中的活化能,但反应物总能量、生成物总能量没有改变、不改变H
值,C错误;
D.由A可知x=191.2,D正确;故选D。
16、【答案】D
A. 溶液中氯酸根离子不能和银离子生成氯化银沉淀,方案设计、现象与结论不正确,故A错误;
B. 乙醇也能使高锰酸钾溶液褪色,应先用水除去乙醇,再通入酸性高锰酸钾溶液检验消去产物1-丁烯,故B
错误;
C. 麦芽糖也是还原性糖,能够与银氨溶液反应,产生银镜,不能说明麦芽糖发生了水解,C错误;
D. 向KI溶液中加入NaNO 溶液,再滴加淀粉溶液,变蓝,说明溶液中有碘单质生成,则NO -将I-氧化成I ,
2 2 2
NO -的氧化性强于I ,D正确;故选D。
2 2
17、【答案】(1)sp2 sp3 3
(2)CsCl CsCl为离子晶体,熔融克服离子键,而ICl为分子晶体,熔融只需克服分子间作用力
(3)BD
【解析】(1)BCl 中心B原子的价层电子对数为3,B原子采用sp2杂化,NCl 中心N原子的价层电子对数为4,
N原子采用sp3杂化3;B、N位于同周期,同周期元素第一电离能从左到右呈增3大趋势,但IIA、IIIA和VA、VIA
异常,因此第一电离能介于B、N之间的元素有Be、C、O三种,故答案为:sp2;sp3;3;
(2)卤化物CsICl 受热发生非氧化还原反应,生成CsCl和ICl两种物质,其中CsCl为离子晶体,则无色晶体为
CsCl,红棕色液体2为ICl,CsCl为离子晶体,熔融克服离子键,而ICl为分子晶体,熔融只需克服分子间作用力
,故答案为:CsCl;CsCl为离子晶体,熔融克服离子键,而ICl为分子晶体,熔融只需克服分子间作用力;
试卷第15页-------------------------------- 高途高中化学点睛卷 -----------------------------------
(3)A. 基态Na 的核外电子排布为:1s22s22p6,核外电子有5种空间运动状态,A错;
+
B. 以氯离子为观察对象,可知其周围与它最近且等距的氯离子有12个,B正确;
M
C.据“均摊法”,晶胞中含 个Na+、 个Cl-,设晶胞边长为acm,则晶体密度为N 4Ag
a3
1 1 1
cm = g cm =ρg 1 cm 2× , 4 则 + a 1 = =4 cm, 8 晶 × 胞 8+ Na 6× 与 2 C = l 的 4 距离为晶胞边长的一半为:d= a = ⋅
−3 4 a × 3 5 N 8A.5 −3 3 3 4× ρN 58A.5 + − 1
⋅ ⋅ 2 2×
cm= pm,C错误;
3 4× ρN 58A.5 1 3 4× ρN 58A.5 10
D.配合物中中2×心原子所×带1的0电荷会影响配位键的形成,故配合物的稳定性不仅与配体有关,还与中心原子的
所带电荷等因素有关,故正确;
故答案为:BD;
18、【答案】(1)Fe、Cl、O FeOCl(或FeCl Fe O )
3 2 3
(2)FeOCl2NH FeONH NH Cl(写成3FeOCl6NH FeNH 3NH ClFe O 或
3 2 4 3 2 3 4 2 3
FeCl Fe O 6NH FeNH 3NH ClFe O )
3 2 3 3 2 3 4 2 3
(3)FeOOH3HF FeF32H O(或FeOH Fe O 9HF 3FeF36H O)
2 6 2 3 2 3 2 6 2
(4)Fe或FeO或Fe O ;
3 4
取适量固体于试管中,加入足量盐酸使固体溶解,若产生气泡,则是Fe;如不产生气泡,向溶液中加入少量
KSCN溶液,若出现血红色溶液,则是Fe O ;若无上述现象,说明是FeO。
3 4
16g
【分析】红褐色固体B为Fe O ,物质的量为 =0.1mol,铁元素物质的量为0.2mol,氧元素物质的量为
2 3
160g/mol
1.8g
0.3mol,固体A灼烧生成Fe O 和水,水的质量为17.8g-16.0g=1.8g,水的物质的量为 =0.1mol,氢元素
2 3
18g/mol
物质的量为0.2mol,氧元素物质的量为0.1mol,固体A中Fe、H、O的原子个数比为:0.2mol:0.2mol:0.4mol=1:1:2
,A的化学式为:FeO(OH),化合物X中有铁元素0.2mol,质量为11.2g,无色气体A通入到足量硝酸酸化的硝
28.7g
酸银溶液中产生白色沉淀B为AgCl,物质的量为 =0.2mol,无色气体A为HCl,化合物X中含氯元素
143.5g/mol
0.2mol,质量为7.1g,X中另一种元素的质量为21.5g-11.2g-7.1g=3.2g,Fe、Cl原子个数比为0.2mol:0.2mol=1:1
3.2g
,依据正负化合价代数和为0的原则,另一种元素不能为氢元素,应为氧元素,物质的量为 =0.2mol,
16g/mol
则X的化学式为:FeOCl(或FeCl ·Fe O )。
3 2 3
(1)由分析可知,X的化学式为:FeOCl,组成X的元素有Fe、O、Cl。
(2)FeOCl与水反应生成FeO(OH)和HCl,则FeOCl与液态氨反应的化学方程式为:
FeOCl+2NH =FeO(NH )+NH Cl(或3FeOCl6NH FeNH 3NH ClFe O 或
3 2 4 3 2 3 4 2 3
试卷第16页-------------------------------- 高途高中化学点睛卷 -----------------------------------
FeCl Fe O 6NH FeNH 3NH ClFe O )。
3 2 3 3 2 3 4 2 3
(3)由分析可知,A的化学式为:FeO(OH),FeO(OH) 能溶于NaHF 的水溶液,产物中含一种正八面体的负
2
三价阴离子,则其中心原子价层电子对数为6,阴离子为FeF3-,反应的离子方程式为:
6
FeOOH3HF FeF32H O(或FeOH Fe O 9HF 3FeF36H O)。
2 6 2 3 2 3 2 6 2
(4)红褐色固体B为Fe O ,真空条件灼烧,反应完全后生成黑色粉末(纯净物),依据元素守恒,黑色粉末的
2 3
成分可能是Fe或FeO或Fe O ,铁能与盐酸反应生成氢气,Fe O 能与盐酸反应生成铁离子,FeO能与盐酸反应
3 4 3 4
生成亚铁离子,因此检验固体成分的方案为:取适量固体于试管中,加入足量盐酸使固体溶解,若产生气泡
Fe O
,则是Fe;如不产生气泡,向溶液中加入少量KSCN溶液,若出现血红色溶液,则是 3 4;若无上述现象,
说明是FeO。
CH OH
19、【答案】(1) 低温 (2) ① 3 ② 温度升高时,反应I吸热反应正向进行的程度和反应III放热反
K pxy+K
应逆向进行的程度相差不大 ③ (3) 2 W
【详解】
(1)温度升高平衡常数K减小,则为放热反应, H<0,该反应是气体体积缩小的反应,则 S<0, H-T S<0
,反应才能自发进行,则 H<0,其正反应在低温△下能自发进行; △ △ △
(2)①△H <0, H <0△,即生成甲醇的反应均为放热反应,所以温度升高平衡时甲醇的物质的量分数应减
3 2
小, H >0,生成△CO的反应为吸热反应,所以随温度升高CO平衡时的物质的量分数会变大,二者共同作用
1
导致水△蒸气减小幅度小于甲醇,所以Z代表H O,Y代表CH OH,X代表CO,故答案为:CH OH;
2 3 3
②依据主要反应的化学方程式可知,反应Ⅲ消耗CO ,反应Ⅰ逆向产生CO ,最终体系内CO 的物质的量分数与
2 2 2
上述两个反应进行的程度相关。由于 H <0而 H >0,根据勒夏特列原理,温度改变时,反应Ⅲ和反应Ⅰ平
3 1
衡移动方向相反,且平衡移动程度相近△,导致体△系内CO 的物质的量分数受温度的影响不大;故答案为:温度
2
升高时,反应I吸热反应正向进行的程度和反应III放热反应逆向进行的程度相差不大;
③其他条件相同下,升高温度,反应I吸热反应正向进行的程度和反应III放热反应逆向进行的程度相差不大,
即n(CO )基本不变,反应II为放热反应,升高温度平衡逆向移动,n(H )增大,则nH /nCO 随温度升高而
2 2 2 2
试卷第17页-------------------------------- 高途高中化学点睛卷 -----------------------------------
增大,图示为: 。
c H+ c(HCO-)
(3)由题可知,①CO (g) CO (aq),②CO (aq)+H O(l) H+(aq)+HCO-(aq),K = 3 ,又因为溶
2 2 2 2 3 2 cCO
2
⇌ ⇌
液中CO 的浓度与其在空气中的分压成正比,则c(CO )=y(mol•L-1•kPa-1)•p(CO )=p•x•y,在忽略HCO-的电离时
2 2 2 3
c H+ c H+ -c OH- c2 H+ -K
,c(H+)-c(OH-)=c(HCO 3 -),而c(H+)•c(OH-)=K w ,所以K 2 = cCO = cCO w ,可得
2 2
c(H+)= K pxy+K mol•L-1,故答案为: K pxy+K ;
2 W 2 W
20、【答案】(1) 离子化合物 (2) 三颈烧瓶;冷凝回流兼平衡气压
水浴加热
(3)CH CHONO+N H H O+KOH CH CHOH+KN +3H O
3 2 2 4 2 3 2 3 2
(4)AC (5)b、f、d、g、c、g、e (6)5.0 90%
【分析】将KOH溶解在无水乙醇中,冷却后与85%水合肼、亚硝酸异丙酯混合反应,在70~80℃条件下回流1-2h
,之后加入无水乙醇降低KN 的溶解度,同时冰盐浴冷却析出KN 晶体,抽滤得到粗品,然后多次用无水乙醇
3 3
和乙醚洗涤,最后烘干即可得叠氮化钾产品。
【详解】(1)KN 属于离子化合物,由钾离子和叠氮酸根离子构成。
3
(2)根据仪器A的结构特点可知其为三颈烧瓶;仪器B为球形冷凝管,其作用为冷凝回流兼平衡气压。
(3)仪器A中发生反应时, CH CHONO与水合肼在碱性条件下,重新生成CH CHOH (异丙醇),该
3 2 3 2
水浴加热
反应的化学方程式为CH CHONO+N H H O+KOH CH CHOH+KN +3H O 。
3 2 2 4 2 3 2 3 2
(4)A.步骤D为将65gKOH溶解在300mL~400mL无水乙醇中,需要称量固体和量取乙醇,故步骤D还需要的
仪器是天平、500mL量筒、胶头滴管,故选项A错误;
B. 制备亚硝酸异丙酯的反应放热,用冰盐浴可以降低温度,防止反应过于剧烈,故B正确;
C. KN 微溶于乙醇,加入无水乙醇可以降低其溶解度,促使KN 结晶析出,得到细小均匀的颗粒,提高产率
3 3
,故C错误;
故选AC。
(5)配制一定物质的量浓度的溶液一般需经过检漏、计算、称量、溶解、转移(移液前要先冷却至室温)、
洗涤、定容、摇匀等步骤,所以顺序为a、b、f、d、g、c、g、e、 h。
试卷第18页-------------------------------- 高途高中化学点睛卷 -----------------------------------
(6)根据文献记载,不同浓度的5.0mLNaN 标准溶液,分别加入5.0mL(足量)FeCl 标准溶液可得吸光度曲线
3 3
图,所以取用的标准氯化铁溶液的体积为5mL;根据曲线图,吸光度0.6对应的c N- 为4.0×10-2mol•L-1,则
3
0.360g产品中含有KN 3 的质量为4.0×10-2mol·L-1×0.1L×81g·mol-1=0.324g,纯度为0.324g 100%=90% 。
0.360g
21、【答案】(1)羧基 (2)AC (3) (4) +SOCl +SO +HCl
2 2
(5)
(6)
【详解】根据B的结构简式和A的分子式可知A是甲苯,D生成E发生已知信息的反应,则E的结构简式为
,F和G发生取代反应生成H,根据F和H的结构简式可知G的结构简式为 。
(1)根据C的结构简式可知C中含氧官能团为羧基。
(2)A项,F中氰基(-C≡N)中的C为sp杂化,苯环中的C原则为sp2杂化,故A正确;B项,I的分子式为C H ClN O S
12 11 6 2 2
,B错误;C项,ClSO H具有酸性,与水作用生成两种酸ClSO H+H O=H SO +HCl,C正确;D项,由
3 3 2 2 4
E( )到F( )是通过三氯氧磷(POCl )使酰胺基脱水形成氰基,可以视为消除反应,非取
3
代反应,D错误;故选AC。
(3)联系F、H的结构和G的分子式,容易判断反应为取代反应,掉下HF分子,所以G的结构简式为 。
(4)结合题给信息,羧基可与氯化亚砜发生取代反应生成酰氯, +SOCl → +SO +HCl。
2 2
(5)甲苯转化为2-氨基-4-氯苯甲酸,羧基显然由甲基氧化而来,氨基由硝基还原而来,硝基、氯原子都由苯的
硝化和苯的氯代而来,考虑官能团引入的先后顺序和苯环上取代基定位效应,应先引入硝基、氯原子,再氧
试卷第19页-------------------------------- 高途高中化学点睛卷 -----------------------------------
化甲基,最后还原硝基,否则硝基和氯原子取代位置会错位、氨基可能被氧化:
。
(6)苯环与酰胺基 的组合可以为 和 ,此时还有一个O和一个Cl,考虑分子中4中不同环境H
原子和没有N-O键、Cl-O键的前提下,插入一个O的可能结构为 。再放上一个Cl原子
即可得解 、 、 、 。
试卷第20页