文档内容
绝密 启用前
★
2024 年高考考前信息必刷卷(江苏专用)05
化 学
(考试时间:75分钟 试卷满分:100分)
预测 2024 年高考江苏卷化学试题继续保持以往风格,试卷结构和试题难度保持相对稳定,难度适中,
试题立足于高中化学主干内容,强调化学与科技、生产、生活的亲密联系。在考查化学科基本知识、基本技
能的同时实现了对化学学科素养的全面考查。
单选题13小题,集中体现了对高中化学主干与核心知识的考查,特别是元素化合物、化学实验、化
学反应原理等主干知识,高频考点有化学用语(第2题)、实验基本操作(第3题)、物质性质与用途
(第7题)、有机物的结构与性质(第9题)、多平衡图像分析(第13题)等。对于非选择题,兼顾考
查金属与非金属,第14题为钼精矿制备金属钼、第16题为蚀刻废液制备CuO,第17题为NOx、CO为
情境考查化学反应原理综合问题,题型注意工业情境与化学知识的融合,注重语言表达能力和化学计算能
力的考查。
试卷突出了对元素化合物、化学实验以及化学反应原理内容的考查,还呈现了江苏卷特有的 1 拖 3 题
型,江苏很少单独考查元素化合物知识,一般融入到化学实验、工艺流程、物质结构、基本概念等模块中考
查,第12、13题考查了电离平衡的应用、多平衡体系的分析,为选择题的压轴题型。第15题以为药物中间
体的合成为背景考查有机化学知识。第17题的考查反应原理综合应用。
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Cl 35.5 Ca 40 Mn 55 Cu 64 I
127 La 139
第 卷(选择题 共 分)
Ⅰ 39
一、选择题:本题共13小题,每小题3分,共39分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
微信 公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx0021.在各种防疫防控措施中,化学知识起了重要作用,下列说法正确的是
A.用药皂洗手能有效防止病毒传染,药皂中的苯酚能杀菌消毒
B.将“84”消毒液(有效成分为NaClO)与盐酸混合使用,可提升消毒效果
C.双氧水、酒精、过氧乙酸等消毒液均可以将病毒氧化而达到消毒的目的
D.医用防护服的核心材料是微孔聚四氟乙烯薄膜,其单体四氟乙烯属于烯烃
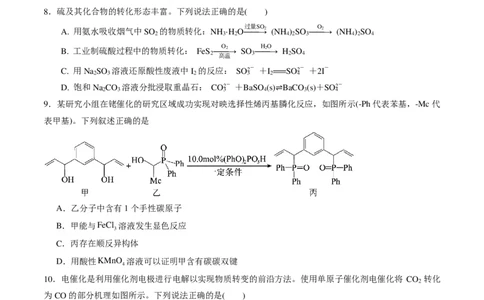
2.反应CH +2H S===CS +4H 可以除去天然气中的H S。下列说法正确的是( )
4 2 2 2 2
·· ·· ··
A. H S为极性分子 B. CS 的电子式为· S · C · S ·
2 2 · ·· ·E AA··AE ·EAE AA··AE EA·E
C. CH 的空间构型为平面正方形 D.反应中CH 仅作还原剂
4 4
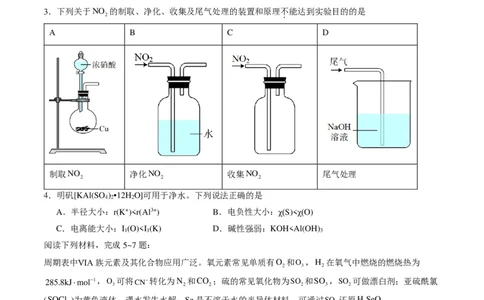
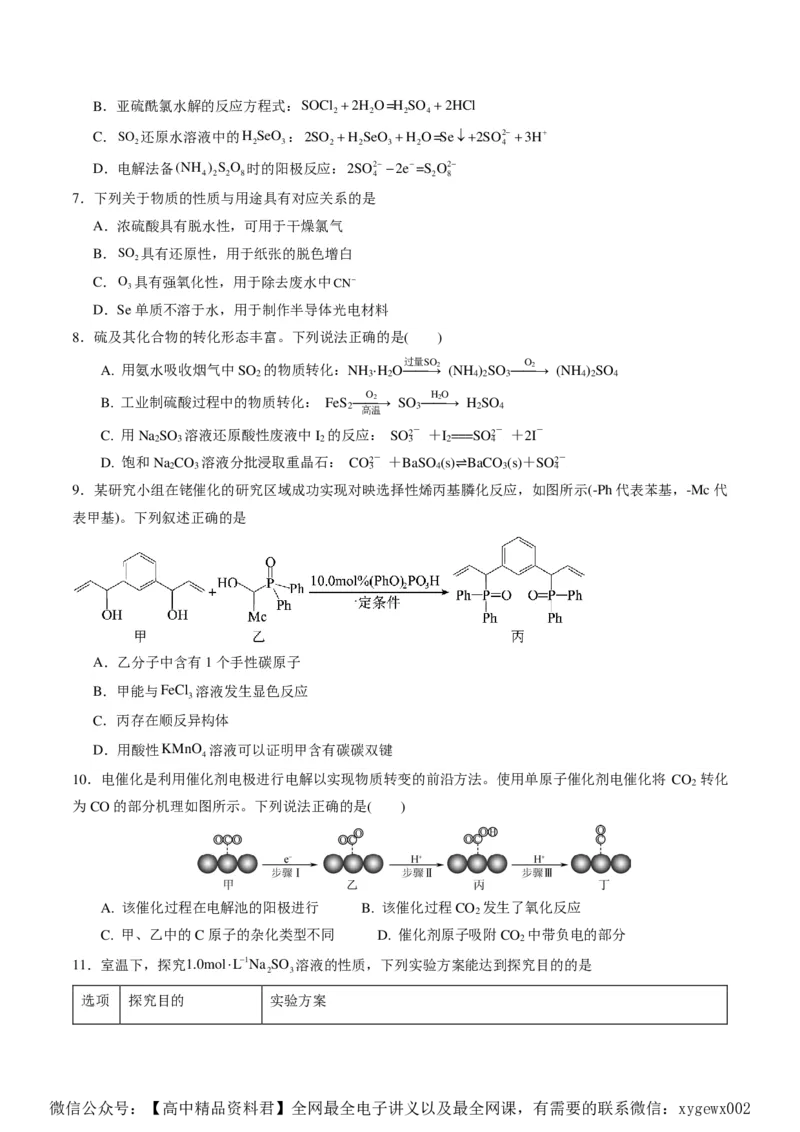
3.下列关于NO
2
的制取、净化、收集及尾气处理的装置和原理不
.
能达到实验目的的是
A B C D
制取NO 净化NO 收集NO 尾气处理
2 2 2
4.明矾[KAl(SO ) •12H O]可用于净水。下列说法正确的是
4 2 2
A.半径大小:r(K+)c ( HCO−)
2 2 3 3
B.KOH完全转化为KHCO 时,溶液中存在:K (H CO )⋅K (H CO )0
2 6 2 2 4 2 1
反应Ⅱ:C H (g)+2CO (g) 4CO(g)+3H (g) ΔH >0
2 6 2 2 2
一定条件下,向容积为1.0L的容器中通入2molC H 和3molCO ,若仅考虑上述反应,C H 平衡转化率和
2 6 2 2 6
平衡时C H 的选择性随温度、压强的关系如图所示,L、L 代表不同压强下乙烷的平衡转化率。
2 4 1 2
已知:
微信 公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002生成C H 消耗C H的量
C H 的选择性= 2 4 2 6 ×100%
2 4 C H的总消耗量
2 6
下列说法正确的是
A.压强L >L
1 2
n(CO)
B.压强为L 、温度为T时,反应达平衡时,混合气体中 =2
1 n(C H )
2 4
( )
n C H
C.一定温度下,增大 2 6 可提高C H 的平衡转化率
n ( CO ) 2 6
2
D.反应C H (g)+2CO(g)+3H (g) 2C H (g)+2H O(g) ΔH=ΔH -2ΔH
2 6 2 2 4 2 2 1
二、非选择题:本题共4小题,共61分。
14.(15分)金属钼(Mo)在工业和国防建设中有重要的作用,钼元素的常见化合价为+4、+5、+6.由钼精
矿(主要成分是MoS )制备钼单质和钼酸钠晶体(Na MoO ·2H O),部分流程如图所示。
2 2 4 2
(1)钼精矿在空气中焙烧时,主要反应的化学方程式为 。
(2)操作1是加入碳酸钠溶液碱浸、过滤。在25℃时,碱浸液中,c(MoO2-)=0.80mol/L,
4
c(SO2-)=0.05mol/L,在结晶前需加入Ba(OH) 固体以除去溶液中的SO2-。当BaMoO 开始沉淀时,SO2-的
4 2 4 4 4
去除率是 (用百分数表示)。
[已知,在25℃时,K (BaMoO )=4.0×10−8,K (BaSO )=1.0×10−10,操作过程中溶液的体积和温度变化可忽
sp 4 sp 4
略不计]
(3)操作3中,经过滤可得钼酸固体。检验钼酸是否洗涤干净的操作为 。
(4)在碱性条件下,向钼精矿中加入NaClO溶液也可以制备Na MoO ,同时生成SO2-,该反应的离子方
2 4 4
程式为 。
(5)钼单质晶体的一个晶胞如图所示。该晶胞为立方体,Mo原子位于顶点和面心。请在图中用短线连接
Mo原子A以及与其距离最近且等距的Mo原子 。
15.(15分)氯霉素(H)的一种合成路线如下:
微信 公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002回答下列问题:
(1)氯霉素分子中碳原子的杂化轨道类型为 。
(2)G→H的反应类型为 。
(3)D的分子式为C H BrO ,其结构简式为 。
10 11 2
(4)E的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式 。
①芳香族化合物 ②分子中含有3种不同化学环境的氢原子
(5)写出以乙烯为主要原料制备 的合成路线流程图 (无机试剂和有机溶剂任用,合
成路线流程图示例见本题题干)。
16.(15分)已知:Cu(OH) +2OH−= [ Cu(OH) ]2−,氢氧化铜悬浊液受热易分解生成CuO。蚀刻含铜电
2 4
路板有多种方法,用蚀刻废液可制备CuO。
(1)酸性蚀刻液法(过氧化氢-盐酸法)。
①用过氧化氢和盐酸蚀刻含铜电路板时发生的离子反应方程式为 。
②反应后有气泡产生,且反应一段时间后,随着溶液变蓝,产生气泡的速率加快,可能的原因是 。
[ ]
(2)碱性蚀刻液法。碱性含铜蚀刻液主要成分为 Cu(NH ) Cl 、氨水、氯化铵等。蚀刻过程中,
3 4 2
[ Cu(NH
3
)
4
] Cl
2
与电路板上的铜发生反应生成
Cu(NH
3
)
2
Cl,失去蚀刻能力,通入空气可恢复蚀刻能力。
①1mol [ Cu(NH ) ] Cl 中σ键的数目为 。
3 4 2
②蚀刻能力恢复的化学方程式为 。
(3)酸性蚀刻废液与碱性蚀刻废液混和可析出3Cu(OH) ⋅CuCl 沉淀,pH在4~5之间易生成氢氧化铜胶
2 2
体。酸性蚀刻废液与碱性蚀刻废液混和反应装置如图1所示。不同pH时,铜元素回收率如图2所示。
①为减少Cu(OH) 胶体形成而影响后续操作,溶液A为 (选填“酸性”或“碱性”)蚀刻废液。
2
微信 公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002②pH>7.5时,铜元素回收率下降的原因为 。
(4)设计从酸性蚀刻废液中制备氧化铜的实验方案。向一定质量的酸性蚀刻废液中 。(实验中必
.
须
.
使用的试剂:20%NaOH溶液、硝酸银溶液、稀硝酸、蒸馏水)
17.(16分)NO 、CO是重要污染物,处理NO 、CO等污染物对建设美丽中国具有重要意义。回答下
x x
列问题。
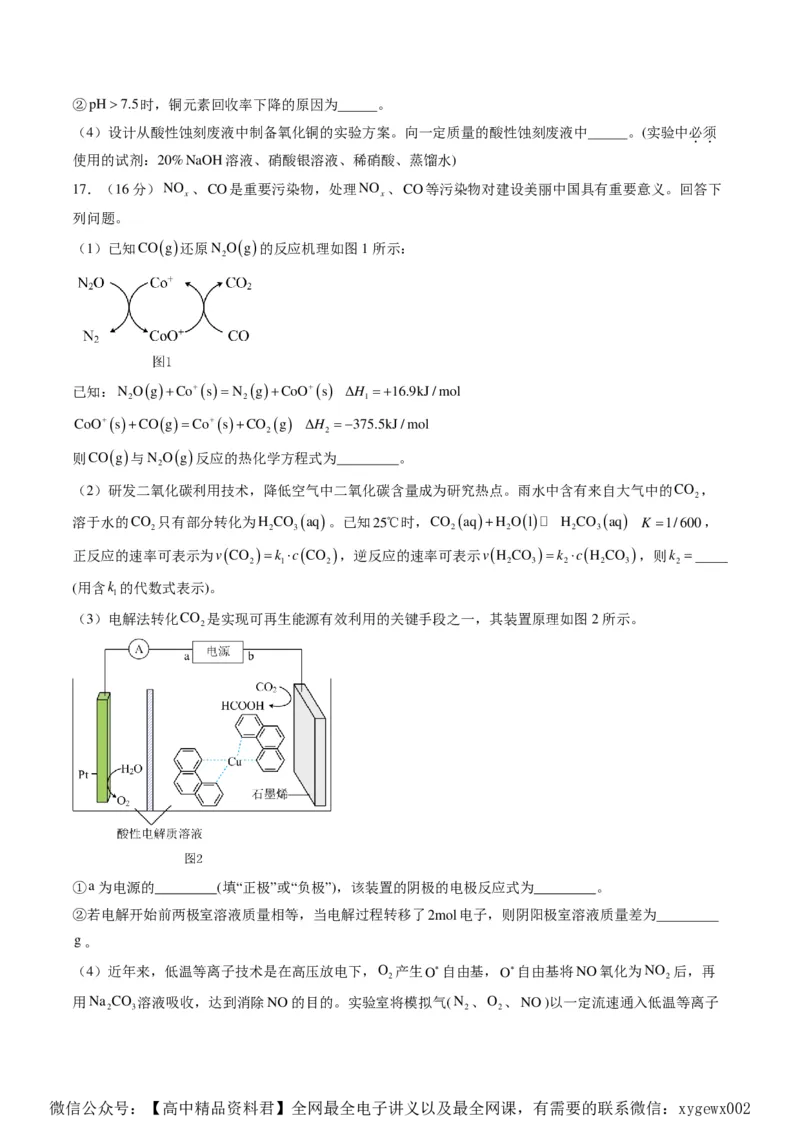
(1)已知CO(g)还原N O(g)的反应机理如图1所示:
2
已知:N O(g)+Co+(s)=N (g)+CoO+(s) ΔH =+16.9kJ/mol
2 2 1
CoO+(s)+CO(g)=Co+(s)+CO (g) ΔH =−375.5kJ/mol
2 2
则CO(g)与N O(g)反应的热化学方程式为 。
2
(2)研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。雨水中含有来自大气中的CO ,
2
溶于水的CO 只有部分转化为H CO (aq)。已知25℃时,CO (aq)+H O(l) H CO (aq) K =1/600,
2 2 3 2 2 2 3
正反应的速率可表示为v(CO )=k ⋅c(CO ),逆反应的速率可表示v(H CO )=k ⋅c(H CO ),则k =
2 1 2 2 3 2 2 3 2
(用含k 的代数式表示)。
1
(3)电解法转化CO 是实现可再生能源有效利用的关键手段之一,其装置原理如图2所示。
2
①a为电源的 (填“正极”或“负极”),该装置的阴极的电极反应式为 。
②若电解开始前两极室溶液质量相等,当电解过程转移了2mol电子,则阴阳极室溶液质量差为
g。
(4)近年来,低温等离子技术是在高压放电下,O 产生O∗自由基,O∗自由基将NO氧化为NO 后,再
2 2
用Na CO 溶液吸收,达到消除NO的目的。实验室将模拟气(N 、O 、NO)以一定流速通入低温等离子
2 3 2 2
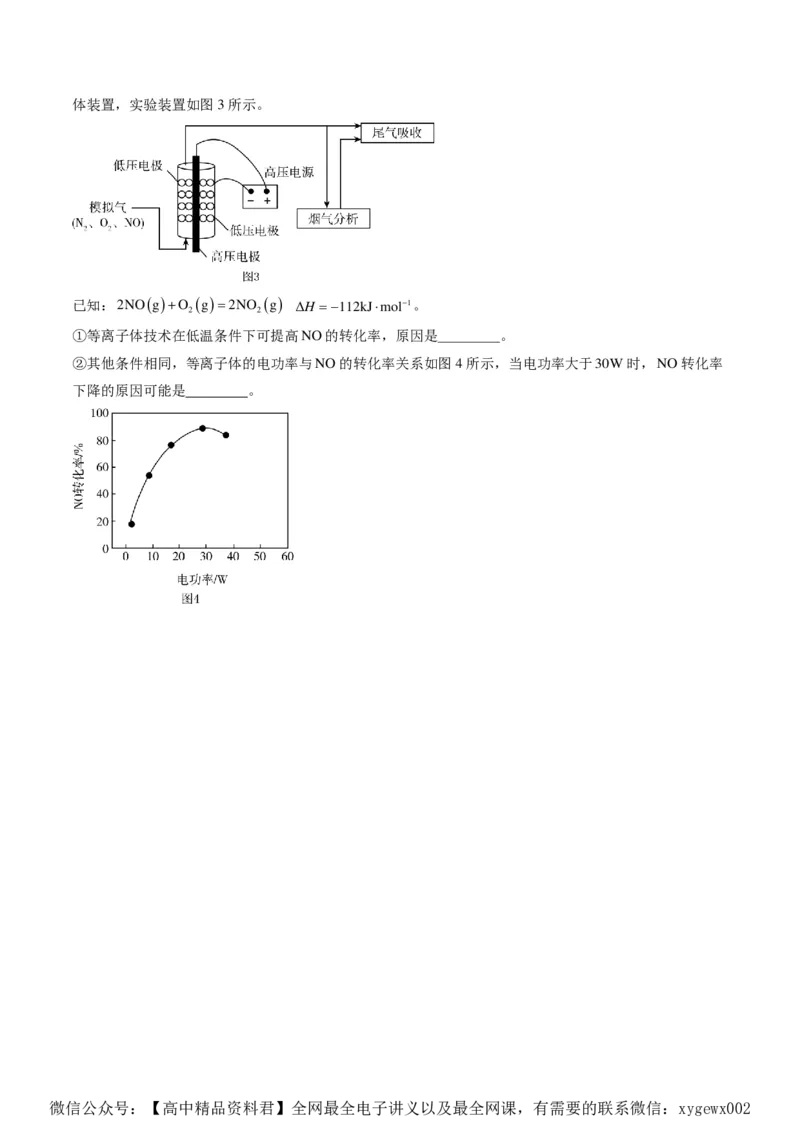
微信 公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002体装置,实验装置如图3所示。
已知:2NO(g)+O (g)=2NO (g) ΔH =−112kJ⋅mol−1。
2 2
①等离子体技术在低温条件下可提高NO的转化率,原因是 。
②其他条件相同,等离子体的电功率与NO的转化率关系如图4所示,当电功率大于30W时,NO转化率
下降的原因可能是 。
微信 公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002