文档内容
专题24 氯及其化合物 卤素
1.【2023年6月浙江卷】探究卤族元素单质及其化合物的性质,下列方案设计、现象和结论都正确的是
实验方案 现象 结论
分层,下层由紫红色 碘在浓 溶液中的溶解
往碘的 溶液中加入等体积浓 溶液,振
A 变为浅粉红色, 能力大于在 中的溶
荡
上层呈棕黄色
解能力
B 用玻璃棒蘸取次氯酸钠溶液点在 试纸上 试纸变白 次氯酸钠溶液呈中性
向 溶液中先滴加4滴 转化为 ,
先产生白色沉淀,再
C 溶液,再滴加4滴 溶解度小于 溶
产生黄色沉淀
溶液 解度
取两份新制氯水,分别滴加 溶液和淀粉 前者有白色沉淀,后 氯气与水的反应存在限
D
溶液 者溶液变蓝色 度
2.【2023年湖北卷】下列化学事实不符合“事物的双方既相互对立又相互统一”的哲学观点的是
A.石灰乳中存在沉淀溶解平衡
B.氯气与强碱反应时既是氧化剂又是还原剂
C.铜锌原电池工作时,正极和负极同时发生反应
D.Li、Na、K的金属性随其核外电子层数增多而增强
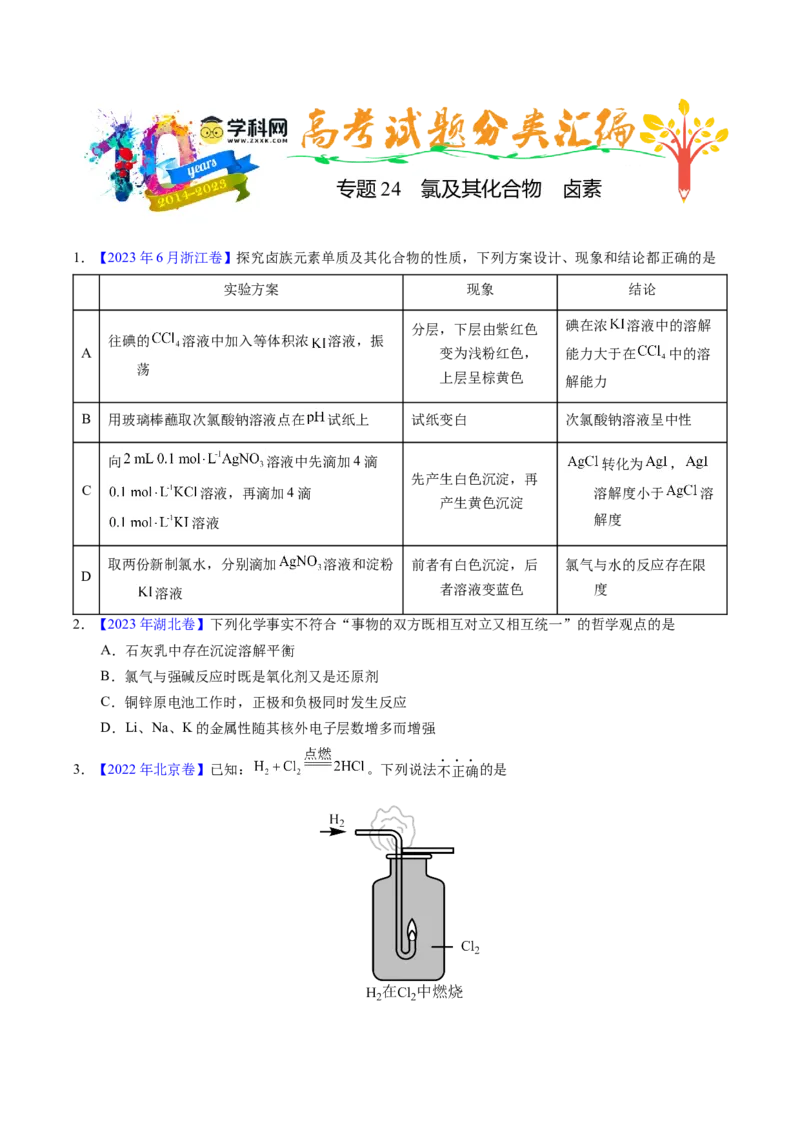
3.【2022年北京卷】已知: 。下列说法不正确的是A. 分子的共价键是 键, 分子的共价键是 键
B.燃烧生成的 气体与空气中的水蒸气结合呈雾状
C.停止反应后,用蘸有浓氨水的玻璃棒靠近集气瓶口产生白烟
D.可通过原电池将 与 反应的化学能转化为电能
4.【2022年重庆卷】下列叙述正确的是
A.Cl 和Br 分别与Fe2+反应得到Cl-和Br-
2 2
B.Na和Li分别在O 中燃烧得到NaO和LiO
2 2 2
C.1molSO 与1molNO 分别通入1L水中可产生相同浓度的HSO 和HNO
3 2 2 4 3
D.0.1mol•L-1醋酸和0.1mol•L-1硼酸分别加入适量NaCO 中均可得到CO 和HO
2 3 2 2
5.(2021·辽宁真题)下列说法正确的是
A. (标准状况)与水充分反应转移 电子
B. 和 均可通过化合反应得到
C.将蘸有浓氨水和浓硫酸的玻璃棒相互靠近,有白烟产生
D. 与 溶液反应:
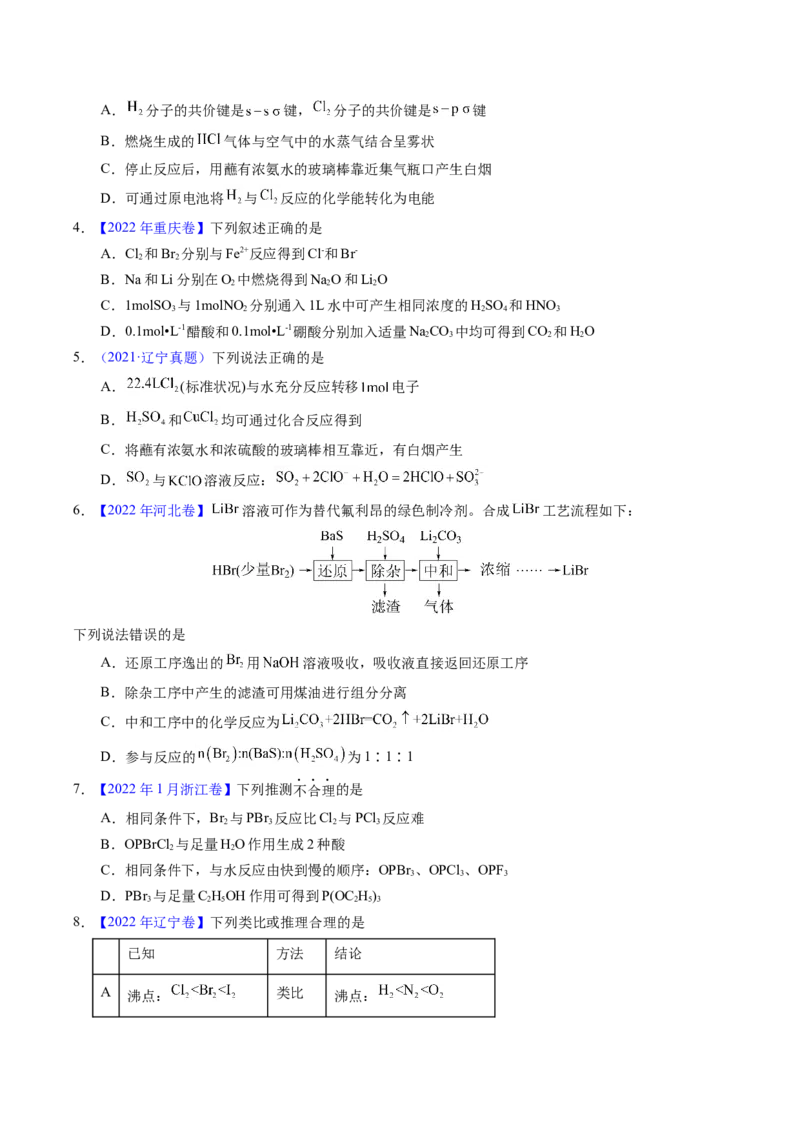
6.【2022年河北卷】 溶液可作为替代氟利昂的绿色制冷剂。合成 工艺流程如下:
下列说法错误的是
A.还原工序逸出的 用 溶液吸收,吸收液直接返回还原工序
B.除杂工序中产生的滤渣可用煤油进行组分分离
C.中和工序中的化学反应为
D.参与反应的 为1∶1∶1
7.【2022年1月浙江卷】下列推测不合理的是
A.相同条件下,Br 与PBr 反应比Cl 与PCl 反应难
2 3 2 3
B.OPBrCl 与足量HO作用生成2种酸
2 2
C.相同条件下,与水反应由快到慢的顺序:OPBr 、OPCl 、OPF
3 3 3
D.PBr 与足量C HOH作用可得到P(OC H)
3 2 5 2 5 3
8.【2022年辽宁卷】下列类比或推理合理的是
已知 方法 结论
A 沸点: 类比 沸点:B 酸性: 类比 酸性:
C 金属性: 推理 氧化性:
D : 推理 溶解度:
9.【2022年海南卷】依据下列实验,预测的实验现象正确的是
选项 实验内容 预测的实验现象
A 溶液中滴加NaOH溶液至过量 产生白色沉淀后沉淀消失
B 溶液中滴加KSCN溶液 溶液变血红色
C AgI悬浊液中滴加NaCl溶液至过量 黄色沉淀全部转化为白色沉淀
D 酸性 溶液中滴加乙醇至过量 溶液紫红色褪去
10.【2022年6月浙江卷】下列说法正确的是
A.工业上通过电解六水合氯化镁制取金属镁
B.接触法制硫酸时,煅烧黄铁矿以得到三氧化硫
C.浓硝酸与铁在常温下不能反应,所以可用铁质容器贮运浓硝酸
D.“洁厕灵”(主要成分为盐酸)和“84消毒液”(主要成分为次氯酸钠)不能混用
11.(2021.6·浙江真题)关于化合物 的性质,下列推测不合理的是
A.具有强氧化性 B.与 溶液反应可生成两种钠盐
C.与盐酸作用能产生氯气 D.水解生成盐酸和硝酸
12.(2021·广东真题)化学创造美好生活。下列生产活动中,没有运用相应化学原理的是
选项 生产活动 化学原理
A 用聚乙烯塑料制作食品保鲜膜 聚乙烯燃烧生成 和
B 利用海水制取溴和镁单质 可被氧化、 可被还原
C 利用氢氟酸刻蚀石英制作艺术品 氢氟酸可与 反应
D 公园的钢铁护栏涂刷多彩防锈漆 钢铁与潮湿空气隔绝可防止腐蚀
13.(2020·天津高考真题)在全国人民众志成城抗击新冠病毒期间,使用的“84消毒液”的主要有效成
分是
A.NaOH B.NaCl C.NaClO D.NaCO
2 3
14.(2016·全国高考真题)化学在生活中有着广泛的应用,下列对应关系错误的是( )化学性质 实际应用
A. Al (SO ) 和小苏打反应 泡沫灭火器灭火
2 4 3
B. 铁比铜金属性强 FeCl 腐蚀Cu刻制印刷电路板
3
C. 次氯酸盐具有氧化性 漂白粉漂白织物
D. HF与SiO 反应 氢氟酸在玻璃器皿上刻蚀标记
2
15.(2020·全国高考真题)国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,乙醚、75%乙醇、含氯消
毒剂、过氧乙酸(CHCOOOH)、氯仿等均可有效灭活病毒。对于上述化学药品,下列说法错误的是
3
A.CHCHOH能与水互溶
3 2
B.NaClO通过氧化灭活病毒
C.过氧乙酸相对分子质量为76
D.氯仿的化学名称是四氯化碳
16.(2015·北京高考真题)某消毒液的主要成分为NaClO,还含有一定量的NaOH,下列用来解释事实的
方程式中不合理的是(已知:饱和NaClO溶液的pH约为11)
A.该消毒液可用NaOH溶液吸收Cl 制备:Cl +2OH-=Cl-+ ClO-+ H O
2 2 2
B.该消毒液的pH约为12:ClO-+ H O HClO+ OH-
2
C.该消毒液与洁厕灵(主要成分为HCl)混用,产生Cl:2H++ Cl-+ ClO-= Cl ↑+H O
2 2 2
D.该消毒液加白醋生成HClO,可增强漂白作用:CHCOOH+ ClO-= HClO+CH COO—
3 3
17.(2015·浙江高考真题)下列说法正确的是( )
A.为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可
B.做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸。如果在沸腾前发现忘记加沸石,应立即停
止加热,冷却后补加
C.在未知溶液中滴加BaCl 溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶液中存在SO 2
2 4
-或SO 2-
3
D.提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤、干燥的方法
故答案选B。
18.(2016·上海高考真题)向新制氯水中加入少量下列物质,能增强溶液漂白能力的是( )
A.碳酸钙粉末 B.稀硫酸 C.氯化钙溶液 D.二氧化硫水溶液
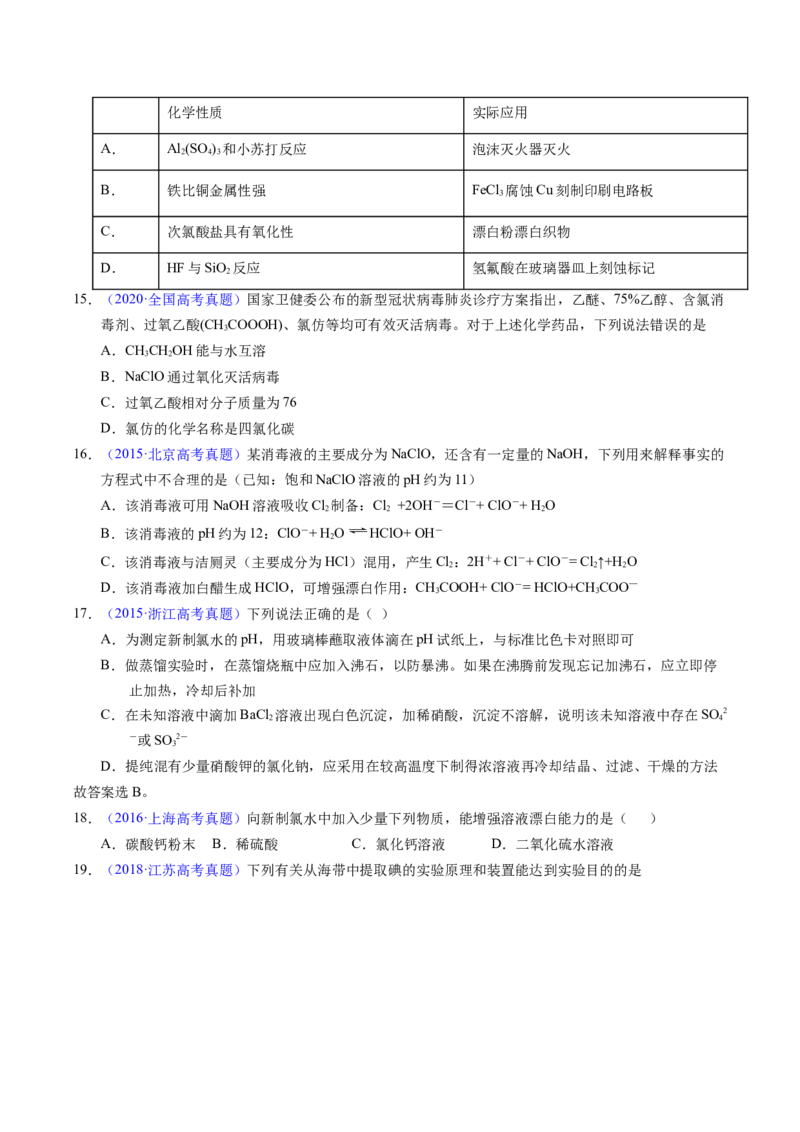
19.(2018·江苏高考真题)下列有关从海带中提取碘的实验原理和装置能达到实验目的的是A.用装置甲灼烧碎海带
B.用装置乙过滤海带灰的浸泡液
C.用装置丙制备用于氧化浸泡液中I−的Cl
2
D.用装置丁吸收氧化浸泡液中I−后的Cl 尾气
2
20.(2016·上海高考真题)下列化工生产过程中,未涉及氧化还原反应的是( )
A.海带提碘 B.氯碱工业
C.氨碱法制碱 D.海水提溴
21.(2015·山东高考真题)下列由实验现象得出的结论正确的是
操作及现象 结论
A 向AgCl悬浊液中加入NaI溶液时出现黄色沉淀。 Ksp(AgCl)< Ksp(AgI)
B 向某溶液中滴加氯水后再加入KSCN溶液,溶液呈红色。 溶液中一定含有Fe2+
向NaBr溶液中滴入少量氯水和苯,振荡、静置,溶液上层
C Br—还原性强于Cl—
呈橙红色。
加热盛有NH Cl固体的试管,试管底部固体消失,试管口
4
D NH Cl固体可以升华
4
有晶体凝结。
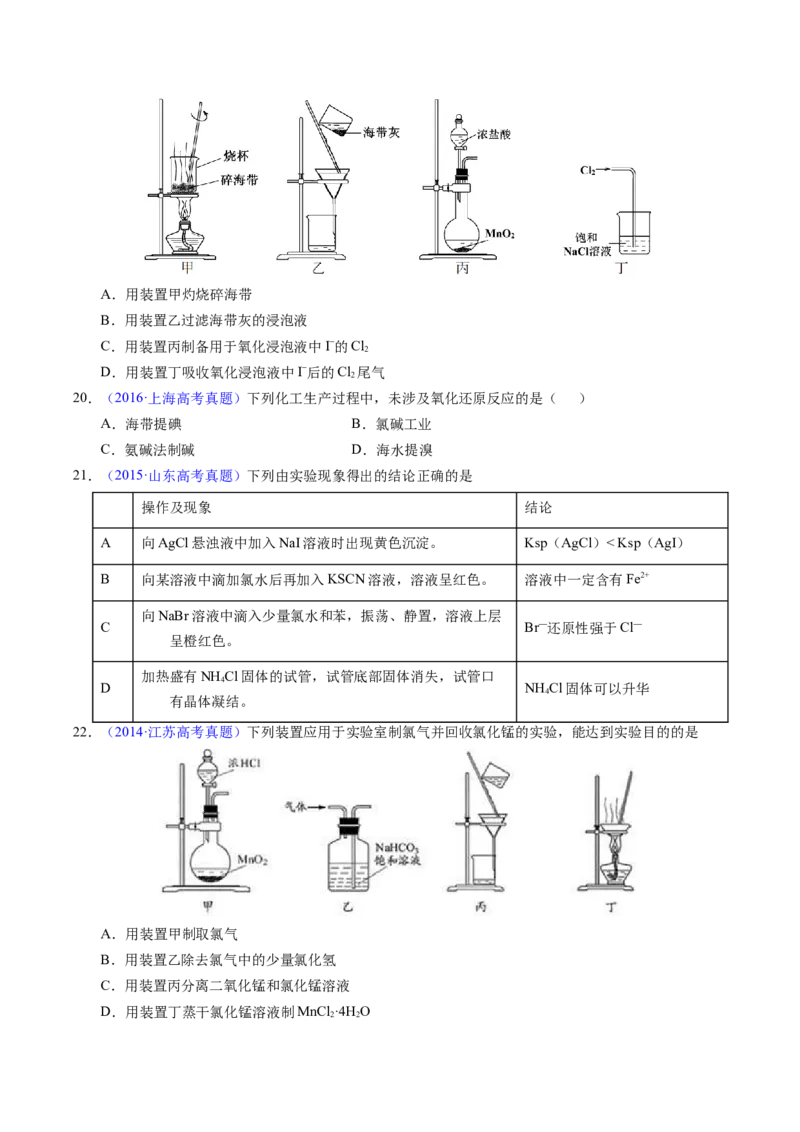
22.(2014·江苏高考真题)下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的的是
A.用装置甲制取氯气
B.用装置乙除去氯气中的少量氯化氢
C.用装置丙分离二氧化锰和氯化锰溶液
D.用装置丁蒸干氯化锰溶液制MnCl ·4H O
2 223.(2014·江苏高考真题)在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是
A.氯水的颜色呈浅绿色,说明氯水中含有Cl
2
B.向氯水中滴加硝酸酸化的AgNO 溶液,产生白色沉淀,说明氯水中含有Cl-
3
C.向氯水中加入NaHCO 粉末,有气泡产生,说明氯水中含有H+
3
D.向FeCl 溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO
2
24.(2014·海南高考真题)下列关于物质应用的说法错误的是
A.玻璃容器可长期盛放各种酸 B.纯碱可用于清洗油污
C.浓氨水可检验氯气管道漏气 D.NaS可除去污水中的Cu2+
2
25.(2019·海南高考真题)能正确表示下列反应的离子方程式为( )
A.向FeBr 溶液中通入过量Cl:2Fe2++Cl=2Fe3++2Cl-
2 2 2
B.向碳酸钠溶液中通入少量CO:CO2-+CO +H O=2HCO -
2 3 2 2 3
C.向碘化钾溶液中加入少量双氧水:3HO+I-=IO -+3H O
2 2 3 2
D.向硫化钠溶液中通入过量SO :2S2-+5SO+2H O=3S↓+4HSO -
2 2 2 3
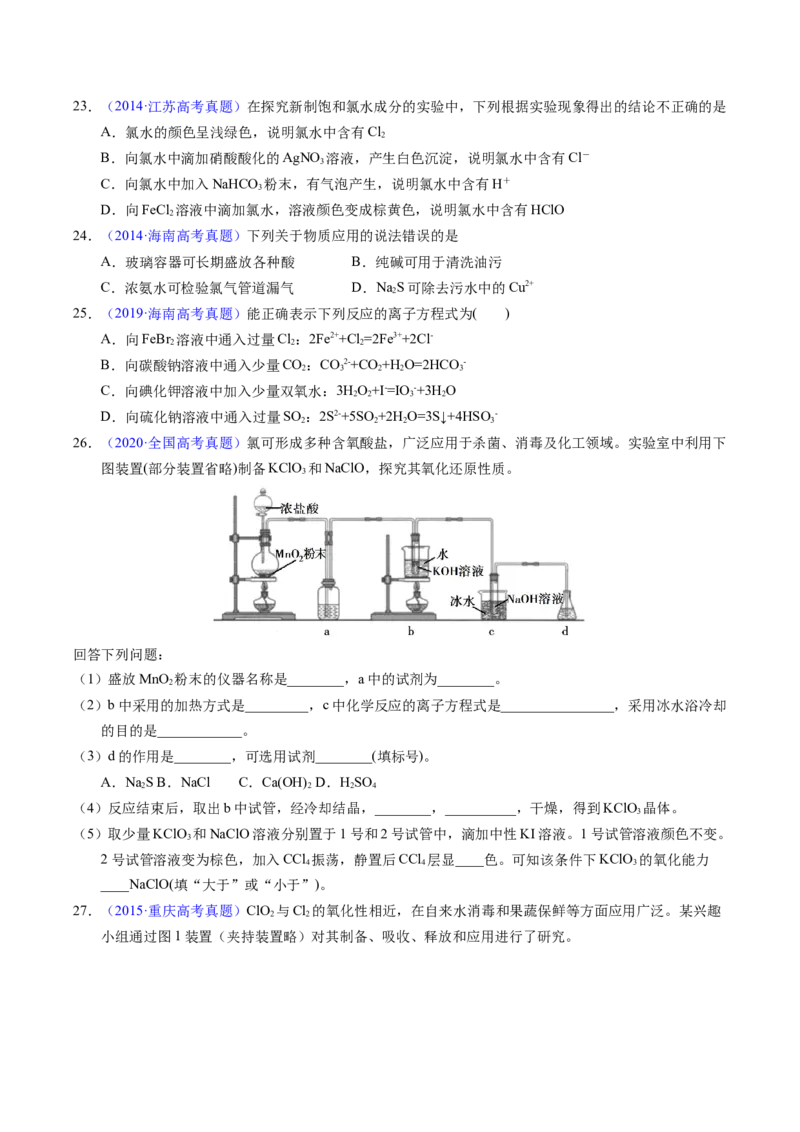
26.(2020·全国高考真题)氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下
图装置(部分装置省略)制备KClO 和NaClO,探究其氧化还原性质。
3
回答下列问题:
(1)盛放MnO 粉末的仪器名称是________,a中的试剂为________。
2
(2)b中采用的加热方式是_________,c中化学反应的离子方程式是________________,采用冰水浴冷却
的目的是____________。
(3)d的作用是________,可选用试剂________(填标号)。
A.NaS B.NaCl C.Ca(OH) D.HSO
2 2 2 4
(4)反应结束后,取出b中试管,经冷却结晶,________,__________,干燥,得到KClO 晶体。
3
(5)取少量KClO 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。
3
2号试管溶液变为棕色,加入CCl 振荡,静置后CCl 层显____色。可知该条件下KClO 的氧化能力
4 4 3
____NaClO(填“大于”或“小于”)。
27.(2015·重庆高考真题)ClO 与Cl 的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣
2 2
小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。(1)仪器D的名称是____。安装F中导管时,应选用图2中的_____。
(2)打开B的活塞,A中发生反应:2NaClO+4HCl=2ClO ↑+Cl↑+2NaCl+2HO。为使ClO 在D中被稳定
3 2 2 2 2
剂充分吸收,滴加稀盐酸的速度宜____(填“快”或“慢”)。
(3)关闭B的活塞,ClO 在D中被稳定剂完全吸收生成NaClO,此时F中溶液的颜色不变,则装置C的
2 2
作用是_____。
(4)已知在酸性条件下NaClO 可发生反应生成NaCl并释放出ClO ,该反应的离子方程式为____,在
2 2
ClO 释放实验中,打开E的活塞,D中发生反应,则装置F的作用是______。
2
(5)已吸收ClO 气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO 的浓度随时间的变化如图3所示。若将其
2 2
用于水果保鲜,你认为效果较好的稳定剂是_______,原因是_________。
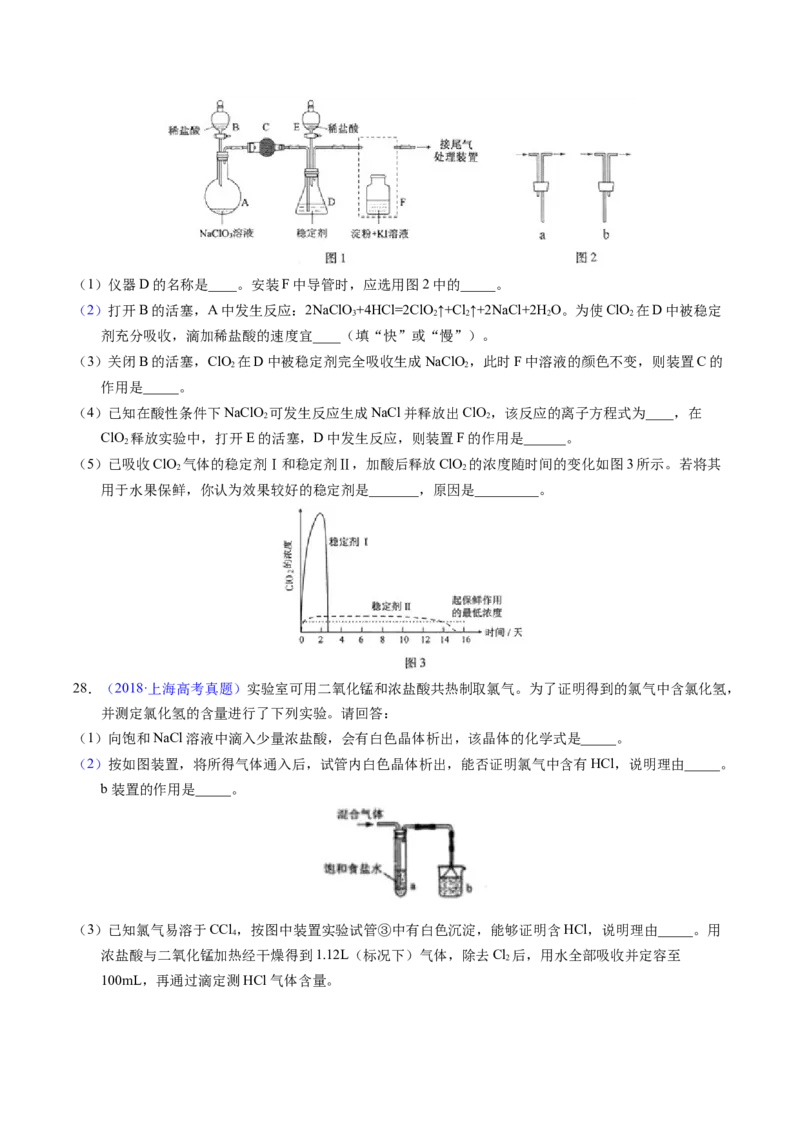
28.(2018·上海高考真题)实验室可用二氧化锰和浓盐酸共热制取氯气。为了证明得到的氯气中含氯化氢,
并测定氯化氢的含量进行了下列实验。请回答:
(1)向饱和NaCl溶液中滴入少量浓盐酸,会有白色晶体析出,该晶体的化学式是_____。
(2)按如图装置,将所得气体通入后,试管内白色晶体析出,能否证明氯气中含有HCl,说明理由_____。
b装置的作用是_____。
(3)已知氯气易溶于CCl ,按图中装置实验试管③中有白色沉淀,能够证明含HCl,说明理由_____。用
4
浓盐酸与二氧化锰加热经干燥得到1.12L(标况下)气体,除去Cl 后,用水全部吸收并定容至
2
100mL,再通过滴定测HCl气体含量。(4)定容所需要仪器有烧杯、玻璃棒、________和_____。
(5)取定容后溶液20.00mL,加入2滴酚酞试液,用0.0250mol/L标准NaOH溶液滴定,当______即为滴
定终点,消耗NaOH溶液19.20mL,则得到的气体中氯化氢的体积含量是______。
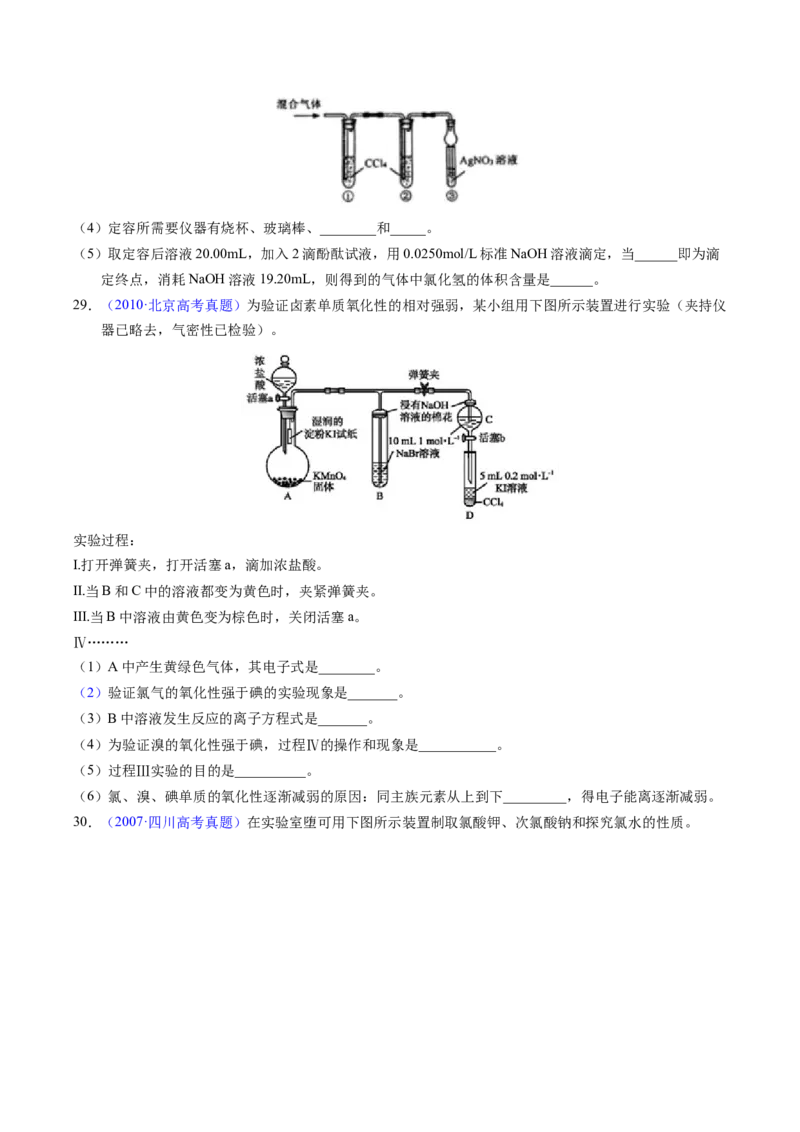
29.(2010·北京高考真题)为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪
器已略去,气密性已检验)。
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕色时,关闭活塞a。
Ⅳ………
(1)A中产生黄绿色气体,其电子式是________。
(2)验证氯气的氧化性强于碘的实验现象是_______。
(3)B中溶液发生反应的离子方程式是_______。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是___________。
(5)过程Ⅲ实验的目的是__________。
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下_________,得电子能离逐渐减弱。
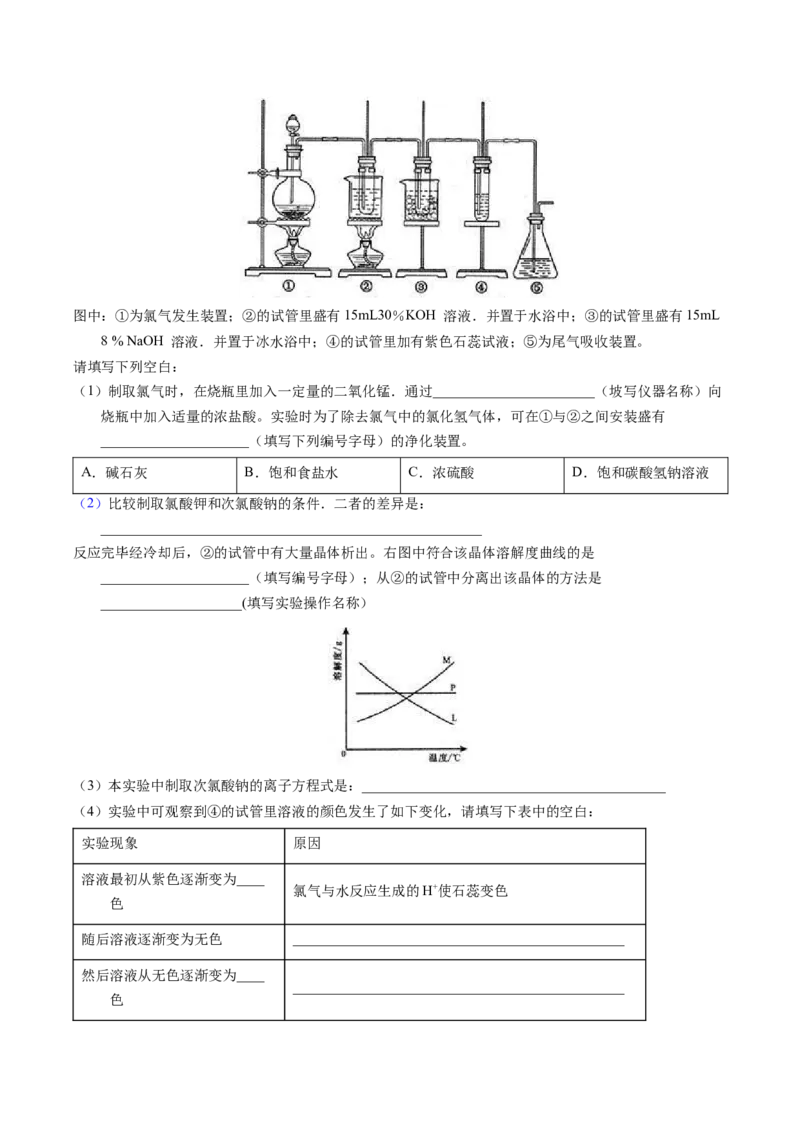
30.(2007·四川高考真题)在实验室堕可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。图中:①为氯气发生装置;②的试管里盛有15mL30%KOH 溶液.并置于水浴中;③的试管里盛有15mL
8 % NaOH 溶液.并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰.通过_______________________(坡写仪器名称)向
烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有
_____________________(填写下列编号字母)的净化装置。
A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液
(2)比较制取氯酸钾和次氯酸钠的条件.二者的差异是:
______________________________________________________
反应完毕经冷却后,②的试管中有大量晶体析出。右图中符合该晶体溶解度曲线的是
_____________________(填写编号字母);从②的试管中分离出该晶体的方法是
____________________(填写实验操作名称)
(3)本实验中制取次氯酸钠的离子方程式是:___________________________________________
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
实验现象 原因
溶液最初从紫色逐渐变为____
氯气与水反应生成的H+使石蕊变色
色
随后溶液逐渐变为无色 _______________________________________________
然后溶液从无色逐渐变为____
_______________________________________________
色31.(2016·浙江高考真题)Cl 与NaOH溶液反应可生成NaCl、NaClO和NaClO(Cl-和ClO-)的比值与反应
2 3
的温度有关,用24gNaOH配成的250mL溶液,与Cl 恰好完全反应(忽略Cl 与水的反应、盐类的水
2 2
解及溶液体积变化):
(1)NaOH溶液的物质的量浓度_____mol·L-1;
(2)某温度下,反应后溶液中c(Cl-)=6c(ClO-),则溶液中c(ClO-) =_____mol·L-1。