文档内容
专题42 反应热计算——盖斯定律
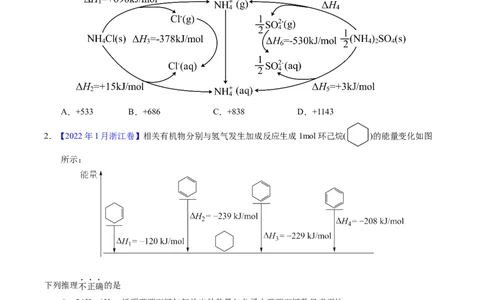
1.【2022年重庆卷】“千畦细浪舞晴空”,氮肥保障了现代农业的丰收。为探究(NH )SO 的离子键强弱,
4 2 4
设计如图所示的循环过程,可得△H/(kJ•mol-1)为
4
A.+533 B.+686 C.+838 D.+1143
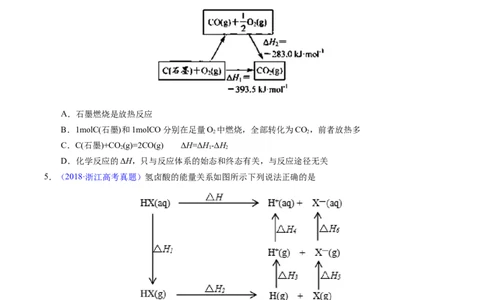
2.【2022年1月浙江卷】相关有机物分别与氢气发生加成反应生成1mol环己烷( )的能量变化如图
所示:
下列推理不正确的是
A.2ΔH≈ΔH,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
1 2
B.ΔH<ΔH,说明单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定
2 3
C.3ΔH<ΔH,说明苯分子中不存在三个完全独立的碳碳双键
1 4
D.ΔH-ΔH <0,ΔH-ΔH >0,说明苯分子具有特殊稳定性
3 1 4 3
3.(2021.6·浙江真题)相同温度和压强下,关于反应的 ,下列判断正确的是A. B.
C. D.
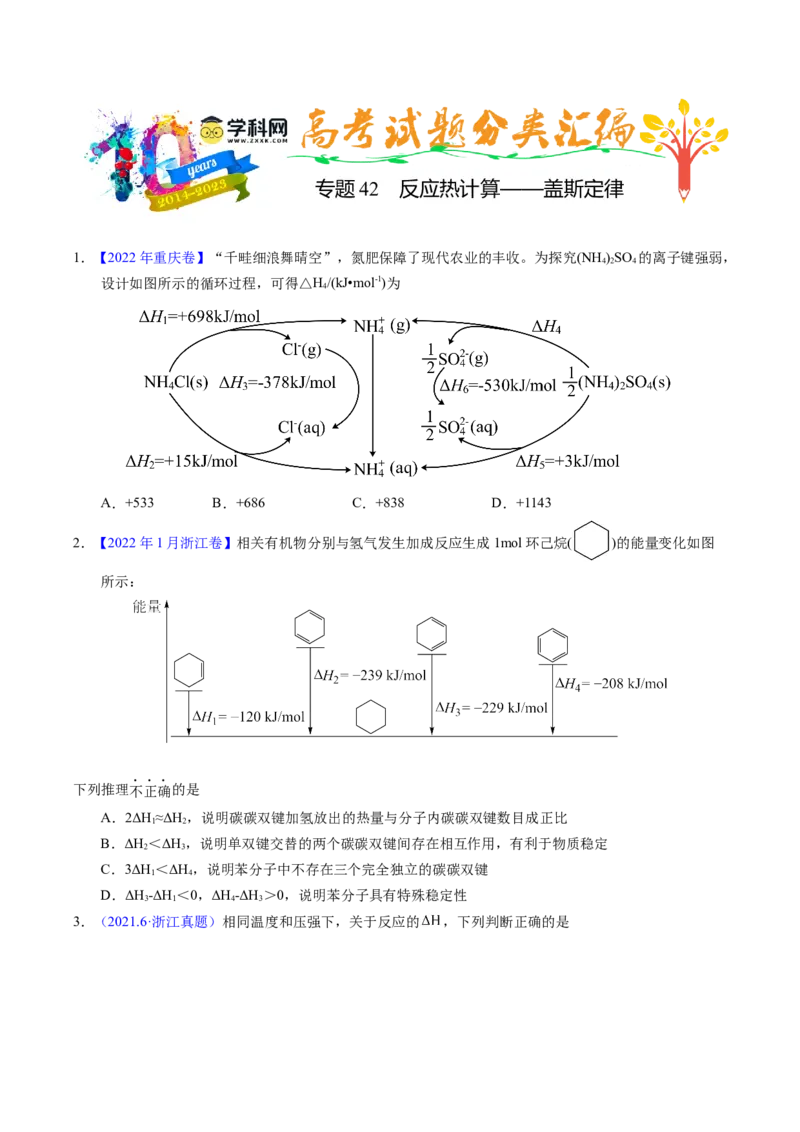
4.(2020·北京高考真题)依据图示关系,下列说法不正确的是
A.石墨燃烧是放热反应
B.1molC(石墨)和1molCO分别在足量O 中燃烧,全部转化为CO,前者放热多
2 2
C.C(石墨)+CO (g)=2CO(g) ΔH=ΔH-ΔH
2 1 2
D.化学反应的ΔH,只与反应体系的始态和终态有关,与反应途径无关
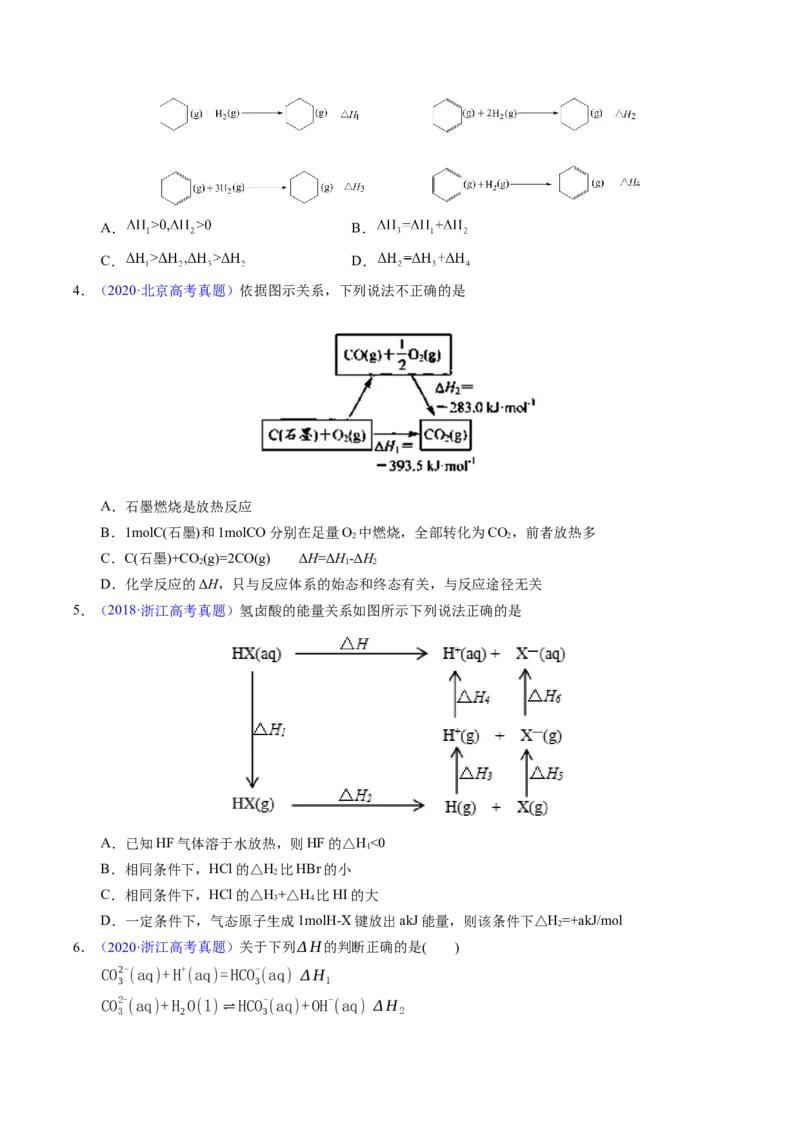
5.(2018·浙江高考真题)氢卤酸的能量关系如图所示下列说法正确的是
A.已知HF气体溶于水放热,则HF的△H<0
1
B.相同条件下,HCl的△H 比HBr的小
2
C.相同条件下,HCl的△H+△H 比HI的大
3 4
D.一定条件下,气态原子生成1molH-X键放出akJ能量,则该条件下△H=+akJ/mol
2
6.(2020·浙江高考真题)关于下列ΔH的判断正确的是( )
CO2- (aq)+H+ (aq)=HCO- (aq) ΔH
3 3 1
CO
3
2- (aq)+H
2
O(l)⇌ HCO
3
- (aq)+OH- (aq) ΔH
2OH- (aq)+H+ (aq)=H O(l) ΔH
2 3
OH- (aq)+CH COOH(aq)=CH COO- (aq)+H O(l) ΔH
3 3 2 4
A.ΔH <0 ΔH <0 B.ΔH <ΔH C.ΔH <0 ΔH >0
1 2 1 2 3 4
D.ΔH >ΔH
3 4
7.(2015·重庆高考真题)黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:S(s)+2KNO
3
(s)+3C(s)=KS(s)+N (g)+3CO (g) ΔH=x kJ·mol-1
2 2 2
已知碳的燃烧热ΔH=a kJ·mol-1
1
S(s)+2K(s)=KS(s) ΔH=b kJ·mol-1
2 2
2K(s)+N (g)+3O (g)=2KNO(s) ΔH=c kJ·mol-1
2 2 3 3
则x为
A.3a+b-c B.c+3a-b C.a+b-c D.c+a-b
8.(2017·浙江高考真题)根据 体系的能量循环图:
下列说法正确的是:
A. >0 B.
C. D.
9.(2014·江苏高考真题)已知:C(s)+O(g)=CO(g) △H
2 2 1
CO(g)+C(s)=2CO(g) △H
2 2
2CO(g)+O(g)=2CO(g) △H
2 2 3
4Fe(s)+3O(g)=2Fe O(s) △H
3 2 3 4
3 CO(g)+Fe O(s)=3CO(g)+2Fe(s) △H
2 3 2 5
下列关于上述反应焓变的判断正确的是
A.△H>0,△H<0
1 3
B.△H>0,△H>0
2 4
C.△H=△H+△H
1 2 3
D.△H=△H+△H
3 4 5
10.(2008·宁夏高考真题)已知H(g)、C H(g)和C HOH(1)的燃烧热分别是-285.8kJ·mol-1、-
2 2 4 2 5
1411.0kJ·mol-1和-1366.8kJ·mol-1,则由C H(g)和HO(l)反应生成C HOH(l)的△H为( )
2 4 2 2 5
A.-44.2kJ·mol-1 B.+44.2kJ·mlo-1
C.-330kJ·mol-1 D.+330kJ·mlo-1
11.(2013·全国高考真题)在1200℃时,天然气脱硫工艺中会发生下列反应①HS(g)+ O(g)=SO(g)+HO(g) △H
2 2 2 2 1
②2HS(g)+SO (g)= S(g)+2HO(g) △H
2 2 2 2 2
③HS(g)+ O(g)=S(g)+H O(g) △H
2 2 2 3
④2S(g) =S (g) △H
2 4
则△H 的正确表达式为( )
4
A.△H=2/3(△H+△H-3△H)
4 1 2 3
B.△H=2/3(3△H-△H-△H)
4 3 1 2
C.△H=3/2(△H+△H-3△H)
4 1 2 3
D.△H=3/2(△H-△H-3△H)
4 1 2 3
12.(2014·全国高考真题)室温下,将1mol的CuSO ·5H O(s)溶于水会使溶液温度降低,热效应为△H,
4 2 1
将1mol的CuSO (s)溶于水会使溶液温度升高,热效应为△H;CuSO ·5H O受热分解的化学方程式为:
4 2 4 2
CuSO ·5H O(s) CuSO (s)+5HO(l),热效应为△H。则下列判断正确的是
4 2 4 2 3
A.△H>△H B.△H<△H
2 3 1 3
C.△H+△H=△H D.△H+△H>△H
1 3 2 1 2 3
13.(2013·海南高考真题)已知下列反应的热化学方程式:
6C(s)+5H(g)+3N(g)+9O(g)=2C H(ONO)(l);ΔH
2 2 2 3 5 2 3 1
2 H (g)+ O (g)= 2H O(g);ΔH
2 2 2 2
C(s)+ O (g)=CO (g);ΔH
2 2 3
则反应4C H(ONO)(l)= 12CO(g)+10HO(g) + O (g) +6N (g)的ΔH为
3 5 2 3 2 2 2 2
A.12ΔH+5ΔH -2ΔH B.2ΔH-5ΔH -12ΔH
3 2 1 1 2 3
C.12ΔH-5ΔH -2ΔH D.ΔH-5ΔH -12ΔH
3 2 1 1 2 3
14.(2018·浙江高考真题)已知:
下列说法正确的是
A.∆H<0,∆H<0,∆H<∆H B.6∆H+∆H+∆H-∆H=0
1 2 3 4 1 2 3 4
C.-6∆H+∆H+∆H-∆H=0 D.-6∆H+∆H-∆H+∆H=0
1 2 3 4 1 2 3 4
15.(2019·浙江高考真题)MgCO 和CaCO 的能量关系如图所示(M=Ca、Mg):
3 3
M2+(g)+CO2-(g) M2+(g)+O2−(g)+CO(g)
3 2已知:离子电荷相同时,半径越小,离子键越强。下列说法不正确的是
A.ΔH(MgCO )>ΔH(CaCO)>0
1 3 1 3
B.ΔH(MgCO )=ΔH(CaCO)>0
2 3 2 3
C.ΔH(CaCO)-ΔH(MgCO )=ΔH(CaO)-ΔH(MgO)
1 3 1 3 3 3
D.对于MgCO 和CaCO ,ΔH+ΔH>ΔH
3 3 1 2 3
16.【2022年全国乙卷】油气开采、石油化工、煤化工等行业废气普遍含有的硫化氢,需要回收处理并加
以利用。回答下列问题:
(1)已知下列反应的热化学方程式:
①
②
③
计算 热分解反应④ 的 ________ 。
17.【2023年全国甲卷】甲烷选择性氧化制备甲醇是一种原子利用率高的方法。回答下列问题:
(1)已知下列反应的热化学方程式:
①
②
反应③ 的 。
18.【2023年全国乙卷】硫酸亚铁在工农业生产中有许多用途,如可用作农药防治小麦黑穗病,制造磁性
氧化铁、铁催化剂等。回答下列问题:
(2)已知下列热化学方程式:
则 的 。
19.【2023年山东卷】一定条件下,水气变换反应 的中间产物是 。为探究
该反应过程,研究 水溶液在密封石英管中的分子反应:
Ⅰ.
Ⅱ.
研究发现,在反应Ⅰ、Ⅱ中, 仅对反应Ⅰ有催加速作用;反应Ⅰ速率远大于反应Ⅱ,近似认为反应Ⅰ
建立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问题:(1)一定条件下,反应Ⅰ、Ⅱ的焓变分别为 、 ,则该条件下水气变换反应的焓变 (用
含 的代数式表示)。
20.【2023年湖北卷】纳米碗 是一种奇特的碗状共轭体系。高温条件下, 可以由 分子
经过连续5步氢抽提和闭环脱氢反应生成。 的反应机理和能量变化如
下:
回答下列问题:
(1)已知 中的碳氢键和碳碳键的键能分别为 和 ,H-H键能为
。估算 的 。
21.【2023年湖北卷】聚苯乙烯是一类重要的高分子材料,可通过苯乙烯聚合制得。
Ⅰ.苯乙烯的制备
(1)已知下列反应的热化学方程式:
①
②
③
计算反应④ 的 ;
22.【2023年1月浙江卷】“碳达峰·碳中和”是我国社会发展重大战略之一, 还原 是实现“双
碳”经济的有效途径之一,相关的主要反应有:Ⅰ:
Ⅱ:
请回答:
(2)反应 的 。
23.【2023年6月浙江卷】水煤气变换反应是工业上的重要反应,可用于制氢。
水煤气变换反应:
该反应分两步完成:
请回答:
(1) 。
24.(2021·福建真题)化学链燃烧( )是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃烧方
式相比,避免了空气和燃料的直接接触,有利于高效捕集 。基于 载氧体的甲烷化学链
燃烧技术示意图如下。
空气反应器与燃料反应器中发生的反应分别为:
①
②
(1)反应 _______ 。
25.(2021·辽宁真题)苯催化加氢制备环己烷是化工生产中的重要工艺,一定条件下,发生如下反应:
Ⅰ.主反应: (g)+3H
2
(g)⇌ (g) ∆H
1
<0
Ⅱ.副反应: (g) ⇌ (g) ∆H 2 >0
回答下列问题:(1)已知:Ⅲ.
Ⅳ.2 (g)+15O
2
(g)⇌12CO
2
(g)+6H
2
O(l) ∆H
4
Ⅴ. (g)+9O(g)=6CO (g)+6HO(l) ∆H
2 2 2 5
则 _______(用 、 和 表示)。
26.【2021年江苏卷】甲烷是重要的资源,通过下列过程可实现由甲烷到氢气的转化。
(2)CH 与CO 重整的主要反应的热化学方程式为
4 2
反应I:CH(g)+CO (g)=2CO(g)+2H(g) ΔH=246.5kJ·mol-1
4 2 2
反应II:H(g)+CO (g)=CO(g)+HO(g) ΔH=41.2kJ·mol-1
2 2 2
反应III:2CO(g)=CO(g)+C(s) ΔH=-172.5kJ·mol-1
2
①在CH 与CO 重整体系中通入适量HO(g),可减少C(s)的生成,反应3CH(g)+CO (g)+2HO(g)=4CO(g)
4 2 2 4 2 2
+8H (g)的ΔH=___。
2
27.【2022年湖北卷】自发热材料在生活中的应用日益广泛。某实验小组为探究“ ”体系
的发热原理,在隔热装置中进行了下表中的五组实验,测得相应实验体系的温度升高值( )随时间(t)
的变化曲线,如图所示。
回答下列问题:
(1)已知:
①
②
③
则 的 ___________ 。
28.【2022年全国甲卷】金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前生产钛的方法
之一是将金红石 转化为 ,再进一步还原得到钛。回答下列问题:
(1) 转化为 有直接氯化法和碳氯化法。在 时反应的热化学方程式及其平衡常数如下:
(ⅰ)直接氯化:
(ⅱ)碳氯化:
①反应 的 为_______ , _______Pa。29.(2012·江苏高考真题)铝是地壳中含量最高的金属元素,其单质及合金在生产生活中的应用日趋广泛。
(1)真空碳热还原-氯化法可实现由铝土矿制备金属铝,其相关反应的热化学方程式如下:
Al O(s)+AlCl (g)+3C(s)=3AlCl(g)+3CO(g) △H=a kJ·mol-1
2 3 3
3AlCl(g)=2Al(l)+AlCl (g) △H=b kJ·mol-1
3
①反应Al O(s)+3C(s)=2Al(l)+3CO(g)的△H=________kJ·mol-1(用含a、b 的代数式表示)。
2 3
②Al C 是反应过程中的中间产物。Al C 与盐酸反应(产物之一是含氢量最高的烃)的化学方程式为
4 3 4 3
____________________________________________。
30.(2020·山东高考真题)探究CHOH合成反应化学平衡的影响因素,有利于提高CHOH的产率。以
3 3
CO、H 为原料合成CHOH涉及的主要反应如下:
2 2 3
Ⅰ.
Ⅱ.
Ⅲ.
回答下列问题:
(1) _________ 。
31.(2017·全国高考真题)[2017·新课标Ⅲ]砷(As)是第四周期ⅤA族元素,可以形成As S、As O、
2 3 2 5
HAsO 、HAsO 等化合物,有着广泛的用途。回答下列问题:
3 3 3 4
(3)已知:As(s)+ H(g)+2O(g)=HAsO (s) ΔH
2 2 3 4 1
H(g)+ O(g)=HO(l) ΔH
2 2 2 2
2As(s)+ O(g) =As O(s) ΔH
2 2 5 3
则反应As O(s) +3H O(l)= 2H AsO (s)的ΔH =_________。
2 5 2 3 4
32.(2009·山东高考真题)运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
(2)O(g)= O+(g)+e- H=1175.7kJ·mol-1
2 2 1
PtF(g)+ e-1 PtF-(g) H= -771.1 kJ·mol-1
6 6 2
O+PtF-(s)=O+(g)+PtF - H=482.2 kJ·mol-1
2 6 2 6 3
则反应O(g)+ PtF (g) = O+PtF- (s)的 H=_____________ kJ·mol-1。
2 6 2 6
(3)在25℃下,向浓度均为0.1 mol·L-1的MgCl 和CuCl 混合溶液中逐滴加入氨水,先生成__________
2 2
33.(2016·全国高考真题)联氨(又称联肼,NH,无色液体)是一种应用广泛的化工原料,可用作火箭
2 4
燃料,回答下列问题:
(3)①2O(g)+N (g)=N O(l) △H
2 2 2 4 1
②N(g)+2H (g)=N H(l) △H
2 2 2 4 2
③O(g)+2H (g)=2H O(g) △H
2 2 2 3④2NH(l) + N O(l)= 3N (g)+ 4H O(g) △H=-1048.9kJ/mol
2 4 2 4 2 2 4
上述反应热效应之间的关系式为△H=________________,联氨和NO 可作为火箭推进剂的主要原因为
4 2 4
_________________________________________________。
34.(2018·江苏高考真题)NO (主要指NO和NO )是大气主要污染物之一。有效去除大气中的NO 是
x 2 x
环境保护的重要课题。
(1)用水吸收NO 的相关热化学方程式如下:
x
2NO (g)+HO(l) HNO(aq)+HNO (aq) ΔH=−116.1 kJ·mol−1
2 2 3 2
3HNO(aq) HNO(aq)+2NO(g)+HO(l) ΔH=75.9 kJ·mol−1
2 3 2
反应3NO (g)+HO(l) 2HNO(aq)+NO(g)的ΔH=___________kJ·mol−1。
2 2 3
35.(2013·江苏高考真题)磷是地壳中含量较为丰富的非金属元素,主要以难溶于水的磷酸盐如
Ca (PO ) 等形式存在。它的单质和化合物在工农业生产中有着重要的应用。
3 4 2
(1)白磷(P )可由Ca (PO )、焦炭和SiO 在一定条件下反应获得。相关热化学方程式如下:
4 3 4 2 2
2Ca (PO )(s)+10C(s)= 6CaO(s)+P (s)+10CO(g) △H="+3359.26" kJ·mol-1
3 4 2 4 1
CaO(s)+SiO (s)= CaSiO (s) △H=-89.61 kJ·mol-1
2 3 2
2Ca (PO )(s)+6SiO (s)+10C(s)= 6CaSiO (s)+P(s)+10CO(g) △H
3 4 2 2 3 4 3
则△H= kJ·mol-1。
3