文档内容
专题44 化学反应机理与反应历程
1.【2023年全国新课标卷】“肼合成酶”以其中的 配合物为催化中心,可将 与 转化为
肼( ),其反应历程如下所示。
下列说法错误的是
A. 、 和 均为极性分子
B.反应涉及 、 键断裂和 键生成
C.催化中心的 被氧化为 ,后又被还原为
D.将 替换为 ,反应可得
【答案】D
【解析】A.NH OH,NH ,HO的电荷分布都不均匀,不对称,为极性分子,A正确;B.由反应历程可
2 3 2
知,有N-H,N-O键断裂,还有N-H键的生成,B正确;C.由反应历程可知,反应过程中,
Fe2+先失去电子发生氧化反应生成Fe3+,后面又得到电子生成Fe2+,C正确;D.由反应历程可知,反
应过程中,生成的NH NH 有两个氢来源于NH ,所以将NH OH替换为ND OD,不可能得到
2 2 3 2 2
ND ND ,得到ND NH 和HDO,D错误;故选D。
2 2 2 2
2.【2023年广东卷】催化剂Ⅰ和Ⅱ均能催化反应 。反应历程(下图)中,M为中间产物。其它
条件相同时,下列说法不正确的是
A.使用Ⅰ和Ⅱ,反应历程都分4步进行B.反应达平衡时,升高温度,R的浓度增大
C.使用Ⅱ时,反应体系更快达到平衡 D.使用Ⅰ时,反应过程中M所能达到的最高浓度更大【答案】C
【解析】A.由图可知两种催化剂均出现四个波峰,所以使用Ⅰ和Ⅱ,反应历程都分4步进行,A正确;
B.由图可知该反应是放热反应,所以达平衡时,升高温度平衡向左移动,R的浓度增大,B正确;
C.由图可知Ⅰ的最高活化能小于Ⅱ的最高活化能,所以使用Ⅰ时反应速率更快,反应体系更快达到
平衡,C错误;D.由图可知在前两个历程中使用Ⅰ活化能较低反应速率较快,后两个历程中使用Ⅰ
活化能较高反应速率较慢,所以使用Ⅰ时,反应过程中M所能达到的最高浓度更大,D正确;故选
C。
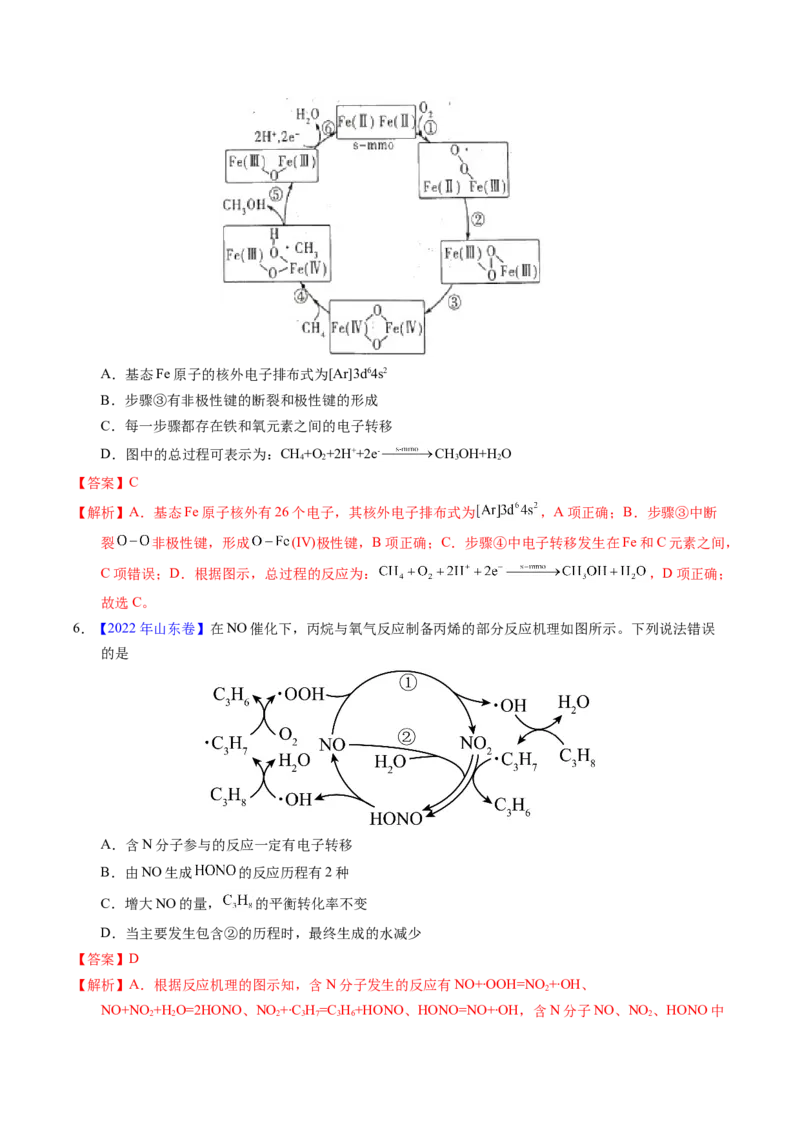
3.【2023年湖北卷】 是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合
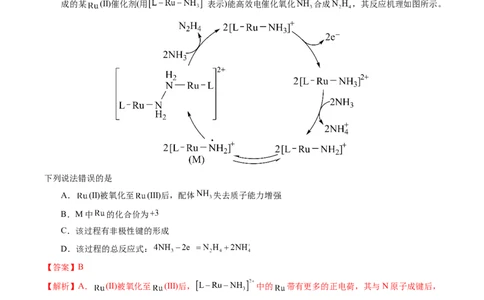
成的某 (Ⅱ)催化剂(用 表示)能高效电催化氧化 合成 ,其反应机理如图所示。
下列说法错误的是
A. (Ⅱ)被氧化至 (Ⅲ)后,配体 失去质子能力增强
B.M中 的化合价为
C.该过程有非极性键的形成
D.该过程的总反应式:
【答案】B
【解析】A. (Ⅱ)被氧化至 (Ⅲ)后, 中的 带有更多的正电荷,其与N原子成键后,
吸引电子的能力比 (Ⅱ)强,这种作用使得配体 中的 键极性变强且更易断裂,因此其
失去质子( )的能力增强,A说法正确;B. (Ⅱ)中 的化合价为+2,当其变为 (Ⅲ)后,
的化合价变为+3, (Ⅲ)失去2个质子后,N原子产生了1个孤电子对, 的化合价不变;M为
,当 变为M时,N原子的孤电子对拆为2个电子并转移给 1个电
子,其中 的化合价变为 ,因此,B说法不正确;C.该过程M变为
时,有 键形成, 是非极性键,C说法正确;D.从整个过程来看, 4个 失去了2个电子后生成了1个 和2个 , (Ⅱ)是催化剂,因此,该过程
的总反应式为 ,D说法正确;综上所述,本题选B。
4.【2023年1月浙江卷】标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下[已知
和 的相对能量为0],下列说法不正确的是
A.
B.可计算 键能为
C.相同条件下, 的平衡转化率:历程Ⅱ>历程Ⅰ
D.历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:
【答案】C
【解析】对比两个历程可知,历程Ⅱ中增加了催化剂,降低了反应的活化能,加快了反应速率。A.催化
剂能降低活化能,但是不能改变反应的焓变,因此 ,A正确;B.已知 的相对
能量为0,对比两个历程可知, 的相对能量为 ,则 键能为
,B正确;C.催化剂不能改变反应的平衡转化率,因此相同条件下, 的平衡转
化率:历程Ⅱ=历程Ⅰ,C错误;D.活化能越低,反应速率越快,由图像可知,历程Ⅱ中第二步反应
的活化能最低,所以速率最快的一步反应的热化学方程式为:
,D正确;故答案为:C。
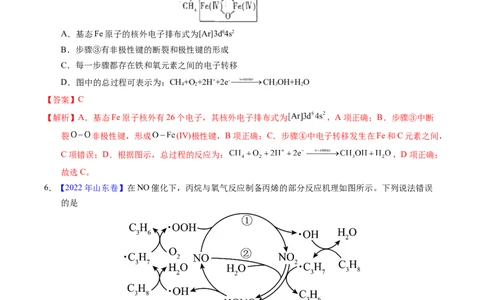
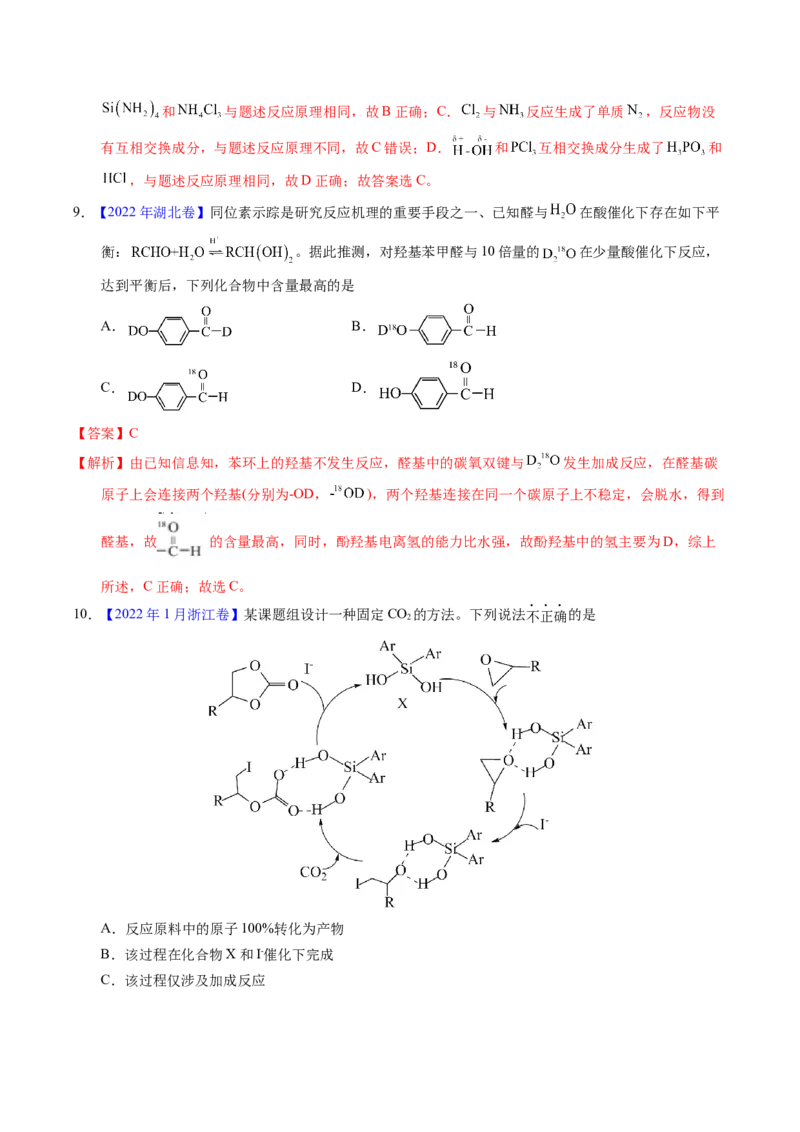
5.(2021·湖北真题)甲烷单加氧酶(s—mmo)含有双核铁活性中心,是O 氧化CH 生成CHOH的催化剂,
2 4 3
反应过程如图所示。下列叙述错误的是A.基态Fe原子的核外电子排布式为[Ar]3d64s2
B.步骤③有非极性键的断裂和极性键的形成
C.每一步骤都存在铁和氧元素之间的电子转移
D.图中的总过程可表示为:CH+O +2H++2e- CHOH+H O
4 2 3 2
【答案】C
【解析】A.基态Fe原子核外有26个电子,其核外电子排布式为 ,A项正确;B.步骤③中断
裂 非极性键,形成 (Ⅳ)极性键,B项正确;C.步骤④中电子转移发生在Fe和C元素之间,
C项错误;D.根据图示,总过程的反应为: ,D项正确;
故选C。
6.【2022年山东卷】在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误
的是
A.含N分子参与的反应一定有电子转移
B.由NO生成 的反应历程有2种
C.增大NO的量, 的平衡转化率不变
D.当主要发生包含②的历程时,最终生成的水减少
【答案】D
【解析】A.根据反应机理的图示知,含N分子发生的反应有NO+∙OOH=NO+∙OH、
2
NO+NO +H O=2HONO、NO +∙C H=C H+HONO、HONO=NO+∙OH,含N分子NO、NO 、HONO中
2 2 2 3 7 3 6 2N元素的化合价依次为+2价、+4价、+3价,上述反应中均有元素化合价的升降,都为氧化还原反应,
一定有电子转移,A项正确;B.根据图示,由NO生成HONO的反应历程有2种,B项正确;C.
NO是催化剂,增大NO的量,C H 的平衡转化率不变,C项正确;D.无论反应历程如何,在NO催
3 8
化下丙烷与O 反应制备丙烯的总反应都为2C H+O 2C H+2H O,当主要发生包含②的历程时,
2 3 8 2 3 6 2
最终生成的水不变,D项错误;答案选D。
7.【2022年湖南卷】甲基丙烯酸甲酯是合成有机玻璃的单体。
旧法合成的反应:
新法合成的反应:
下列说法错误的是(阿伏加德罗常数的值为 )
A. 的电子式为
B.新法没有副产物产生,原子利用率高
C. 的 溶液中 的微粒数小于
D. 的作用是降低反应的活化能,使活化分子数目增多,百分数不变
【答案】D
【解析】A.氢氰酸为共价化合物,结构式为H—C≡N,电子式为 ,故A正确;B.由方程式可
知,新法合成甲基丙烯酸甲酯的反应为没有副产物生成,原子利用率为100的化合反应,故B正确;
C.硫酸氢铵是强酸弱碱的酸式盐,铵根离子在溶液中会发生水解反应,所以1L0.05mol/L的硫酸氢铵
溶液中铵根离子的数目小于0.05mol/L×1L×N mol—1=0.05N ,故C正确;D.由方程式可知,钯为新法
A A
合成甲基丙烯酸甲酯的催化剂,能降低反应的活化能,使活化分子的数目和百分数都增大,故D错误;
故选D。
8.【2022年辽宁卷】 、 均可自耦电离: 、 。
下列反应与 CHCHOH+HBr原理不同的是
3 2
A. B.
C. D.
【答案】C
【解析】A.根据题目信息可知, 和 互相交换成分生成 和 。由
可得, 与 互相交换成分生成 和 ,与题述反应原理相
同,A正确;B.由于 可自电离, 可写为 , 与 交换成分生成和 与题述反应原理相同,故B正确;C. 与 反应生成了单质 ,反应物没
有互相交换成分,与题述反应原理不同,故C错误;D. 和 互相交换成分生成了 和
,与题述反应原理相同,故D正确;故答案选C。
9.【2022年湖北卷】同位素示踪是研究反应机理的重要手段之一、已知醛与 在酸催化下存在如下平
衡: 。据此推测,对羟基苯甲醛与10倍量的 在少量酸催化下反应,
达到平衡后,下列化合物中含量最高的是
A. B.
C. D.
【答案】C
【解析】由已知信息知,苯环上的羟基不发生反应,醛基中的碳氧双键与 发生加成反应,在醛基碳
原子上会连接两个羟基(分别为-OD, ),两个羟基连接在同一个碳原子上不稳定,会脱水,得到
醛基,故 的含量最高,同时,酚羟基电离氢的能力比水强,故酚羟基中的氢主要为D,综上
所述,C正确;故选C。
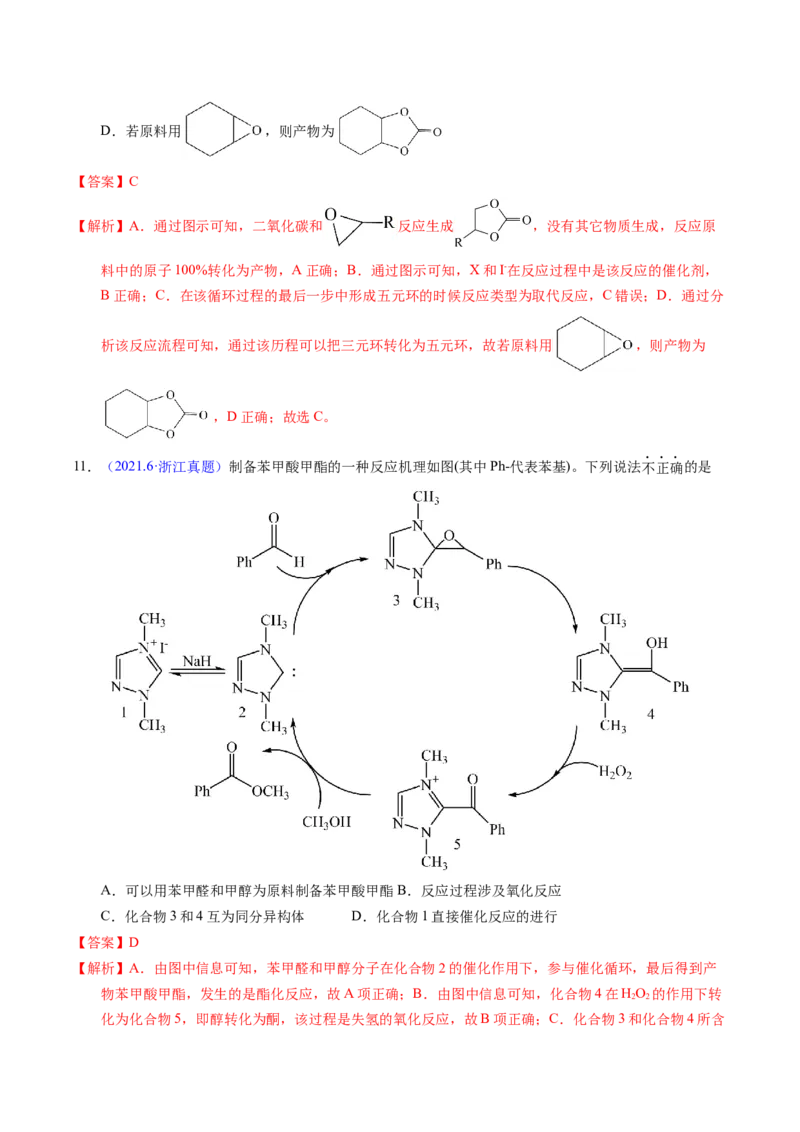
10.【2022年1月浙江卷】某课题组设计一种固定CO 的方法。下列说法不正确的是
2
A.反应原料中的原子100%转化为产物
B.该过程在化合物X和I-催化下完成
C.该过程仅涉及加成反应D.若原料用 ,则产物为
【答案】C
【解析】A.通过图示可知,二氧化碳和 反应生成 ,没有其它物质生成,反应原
料中的原子100%转化为产物,A正确;B.通过图示可知,X和I-在反应过程中是该反应的催化剂,
B正确;C.在该循环过程的最后一步中形成五元环的时候反应类型为取代反应,C错误;D.通过分
析该反应流程可知,通过该历程可以把三元环转化为五元环,故若原料用 ,则产物为
,D正确;故选C。
11.(2021.6·浙江真题)制备苯甲酸甲酯的一种反应机理如图(其中Ph-代表苯基)。下列说法不正确的是
A.可以用苯甲醛和甲醇为原料制备苯甲酸甲酯B.反应过程涉及氧化反应
C.化合物3和4互为同分异构体 D.化合物1直接催化反应的进行
【答案】D
【解析】A.由图中信息可知,苯甲醛和甲醇分子在化合物2的催化作用下,参与催化循环,最后得到产
物苯甲酸甲酯,发生的是酯化反应,故A项正确;B.由图中信息可知,化合物4在HO 的作用下转
2 2
化为化合物5,即醇转化为酮,该过程是失氢的氧化反应,故B项正确;C.化合物3和化合物4所含原子种类及数目均相同,结构不同,两者互为同分异构体,故C项正确;D.由图中信息可知,化合
物1在NaH的作用下形成化合物2,化合物2再参与催化循环,所以直接催化反应进行的是化合物
2,化合物1间接催化反应的进行,故D项错误;综上所述,说法不正确的是D项,故答案为D。
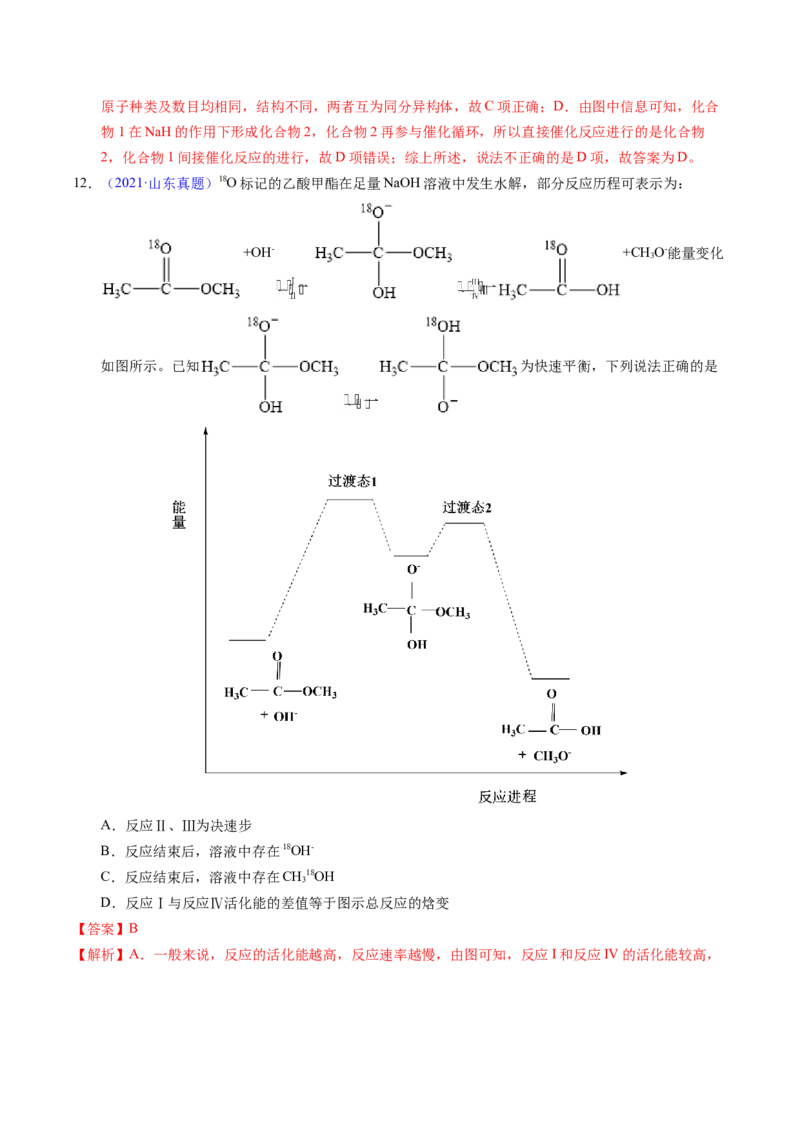
12.(2021·山东真题)18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为:
+OH- +CH O-能量变化
3
如图所示。已知 为快速平衡,下列说法正确的是
A.反应Ⅱ、Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CH18OH
3
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
【答案】B
【解析】A.一般来说,反应的活化能越高,反应速率越慢,由图可知,反应I和反应IV的活化能较高,因此反应的决速步为反应I、IV,故A错误;B.反应I为加成反应,而 与
为快速平衡,反应II的成键和断键方式为 或
,后者能生成18OH-,因此反应结束后,溶液中存在18OH-,故B正确;C.反
应III的成键和断键方式为 或 ,因此反应结束后溶液中
不会存在CH18H,故C错误;D.该总反应对应反应物的总能量高于生成物总能量,总反应为放热反
3
应,因此 和CHO-的总能量与 和OH-的总能量之差等于图
3
示总反应的焓变,故D错误;综上所述,正确的是B项,故答案为B。
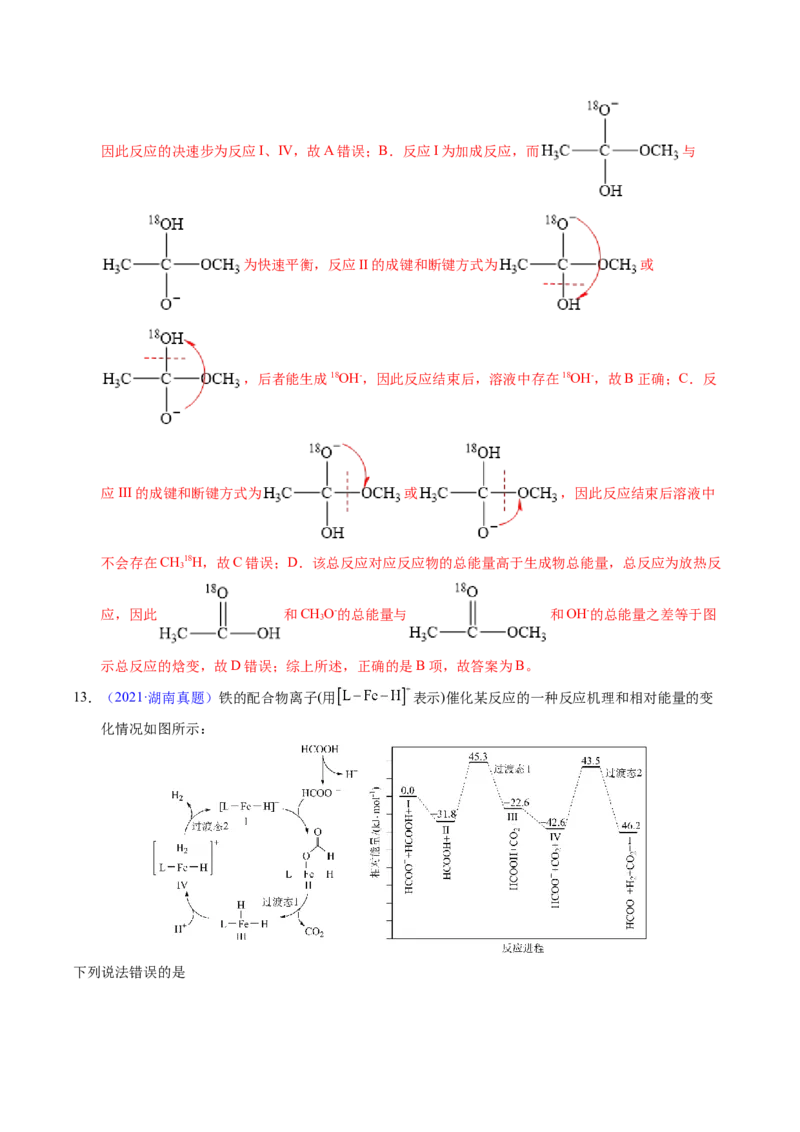
13.(2021·湖南真题)铁的配合物离子(用 表示)催化某反应的一种反应机理和相对能量的变
化情况如图所示:
下列说法错误的是A.该过程的总反应为
B. 浓度过大或者过小,均导致反应速率降低
C.该催化循环中 元素的化合价发生了变化
D.该过程的总反应速率由Ⅱ→Ⅲ步骤决定
【答案】CD
【解析】A.由反应机理可知,HCOOH电离出氢离子后,HCOO-与催化剂结合,放出二氧化碳,然后又
结合氢离子转化为氢气,所以化学方程式为HCOOH CO↑+H ↑,故A正确;B.若氢离子浓度
2 2
过低,则反应Ⅲ→Ⅳ的反应物浓度降低,反应速率减慢,若氢离子浓度过高,则会抑制加酸的电离,
使甲酸根浓度降低,反应Ⅰ→Ⅱ速率减慢,所以氢离子浓度过高或过低,均导致反应速率减慢,故B
正确;C.由反应机理可知,Fe在反应过程中,做催化剂,化合价没有发生变化,故C错误;D.由
反应进程可知,反应Ⅳ→Ⅰ能垒最大,反应速率最慢,对该过程的总反应起决定作用,故D错误;故
选CD。
14.(2020·天津高考真题)理论研究表明,在101kPa和298K下, 异构化反应过程
的能量变化如图所示。下列说法错误的是
A.HCN比HNC稳定
B.该异构化反应的
C.正反应的活化能大于逆反应的活化能
D.使用催化剂,可以改变反应的反应热
【答案】D
【解析】A.根据图中信息得到HCN能量比HNC能量低,再根据能量越低越稳定,因此HCN比HNC稳
定,正确;B.根据焓变等于生成物总能量减去反应物总能量,因此该异构化反应的
,正确;C.根据图中信息得出该反应是吸热反应,因此正
反应的活化能大于逆反应的活化能,正确;D.使用催化剂,不能改变反应的反应热,只改变反应路
径,反应热只与反应物和生成物的总能量有关,错误。综上所述,答案为D。
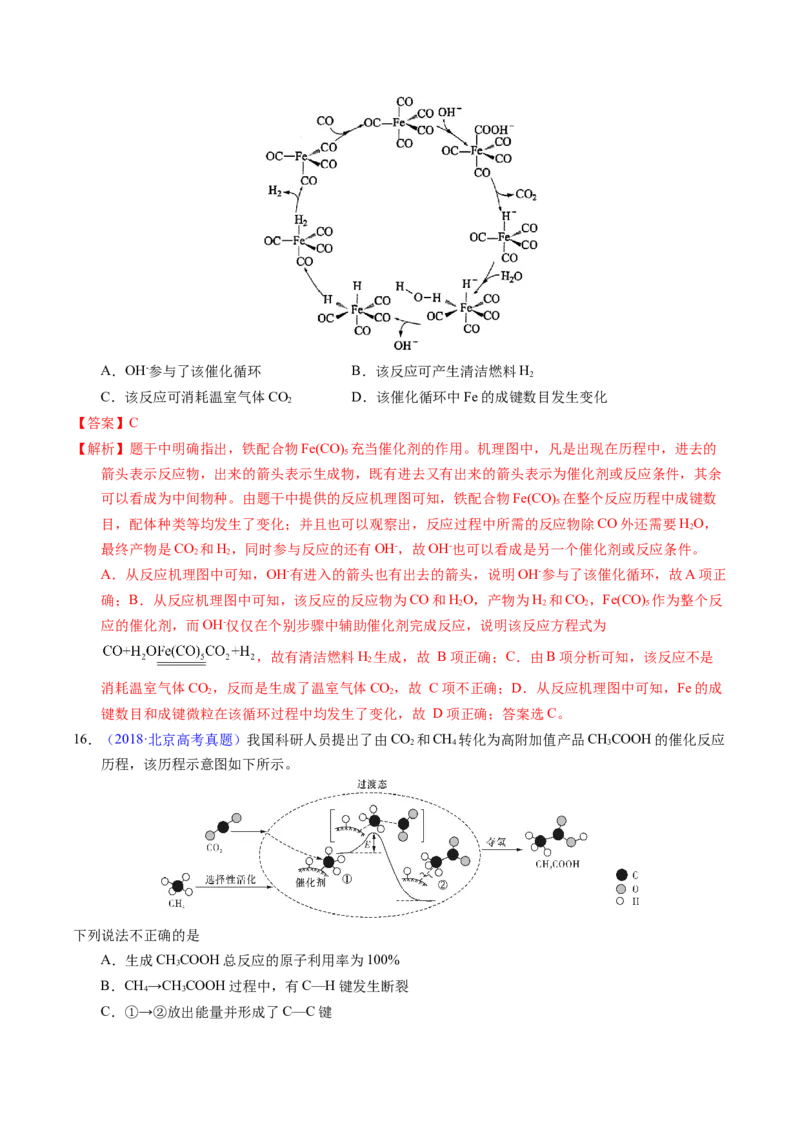
15.(2020·全国高考真题)据文献报道:Fe(CO) 催化某反应的一种反应机理如下图所示。下列叙述错误
5
的是A.OH-参与了该催化循环 B.该反应可产生清洁燃料H
2
C.该反应可消耗温室气体CO D.该催化循环中Fe的成键数目发生变化
2
【答案】C
【解析】题干中明确指出,铁配合物Fe(CO) 充当催化剂的作用。机理图中,凡是出现在历程中,进去的
5
箭头表示反应物,出来的箭头表示生成物,既有进去又有出来的箭头表示为催化剂或反应条件,其余
可以看成为中间物种。由题干中提供的反应机理图可知,铁配合物Fe(CO) 在整个反应历程中成键数
5
目,配体种类等均发生了变化;并且也可以观察出,反应过程中所需的反应物除CO外还需要HO,
2
最终产物是CO 和H,同时参与反应的还有OH-,故OH-也可以看成是另一个催化剂或反应条件。
2 2
A.从反应机理图中可知,OH-有进入的箭头也有出去的箭头,说明OH-参与了该催化循环,故A项正
确;B.从反应机理图中可知,该反应的反应物为CO和HO,产物为H 和CO,Fe(CO) 作为整个反
2 2 2 5
应的催化剂,而OH-仅仅在个别步骤中辅助催化剂完成反应,说明该反应方程式为
,故有清洁燃料H 生成,故 B项正确;C.由B项分析可知,该反应不是
2
消耗温室气体CO,反而是生成了温室气体CO,故 C项不正确;D.从反应机理图中可知,Fe的成
2 2
键数目和成键微粒在该循环过程中均发生了变化,故 D项正确;答案选C。
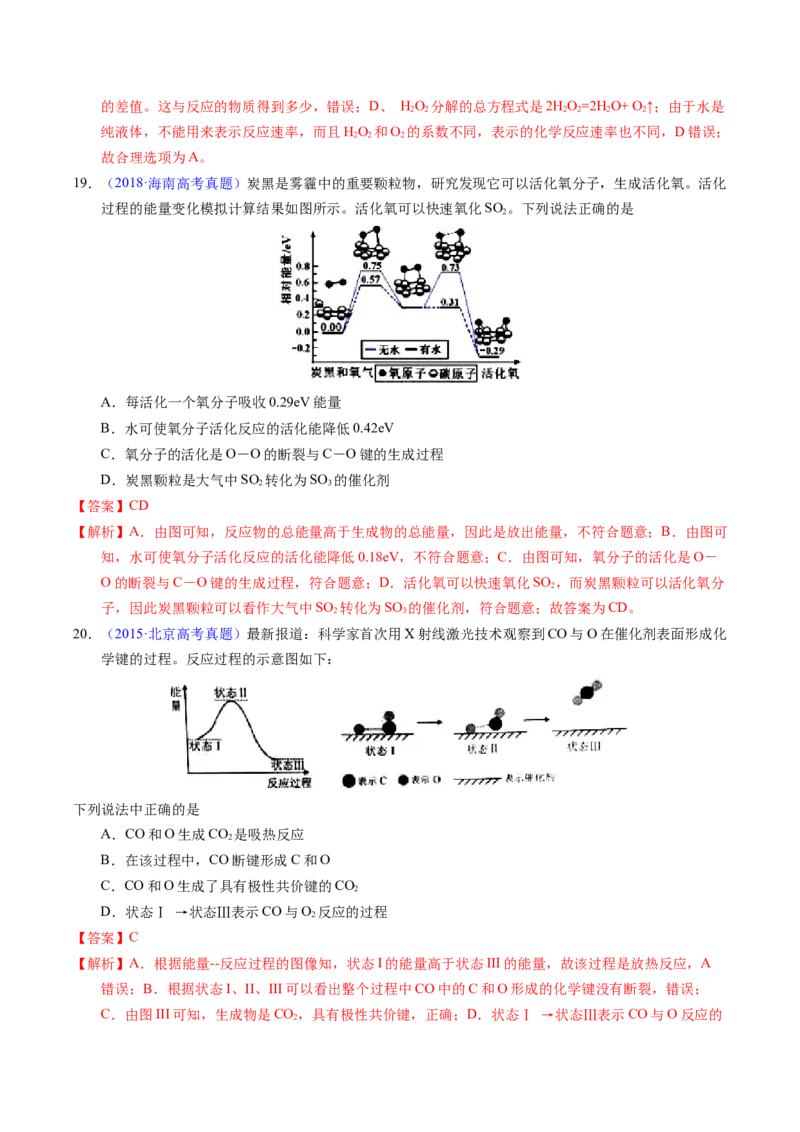
16.(2018·北京高考真题)我国科研人员提出了由CO 和CH 转化为高附加值产品CHCOOH的催化反应
2 4 3
历程,该历程示意图如下所示。
下列说法不正确的是
A.生成CHCOOH总反应的原子利用率为100%
3
B.CH→CHCOOH过程中,有C—H键发生断裂
4 3
C.①→②放出能量并形成了C—C键D.该催化剂可有效提高反应物的平衡转化率
【答案】D
【详解】A.根据图示CH 与CO 在催化剂存在时生成CHCOOH,总反应为CH+CO CHCOOH,
4 2 3 4 2 3
只有CHCOOH一种生成物,原子利用率为100%,A项正确;B.CH 选择性活化变为①过程中,有
3 4
1个C-H键发生断裂,B项正确;C.根据图示,①的总能量高于②的总能量,①→②放出能量,对比
①和②,①→②形成C-C键,C项正确;D.催化剂只影响化学反应速率,不影响化学平衡,不能提
高反应物的平衡转化率,D项错误;答案选D。
17.(2020·北京高考真题)硫酸盐(含SO 、HSO )气溶胶是PM 的成分之一。近期科研人员提出了雾
2.5
霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如图:
下列说法不正确的是
A.该过程有HO参与 B.NO 是生成硫酸盐的氧化剂
2 2
C.硫酸盐气溶胶呈酸性 D.该过程没有生成硫氧键
【答案】D
【详解】A.根据图示中各微粒的构造可知,该过程有HO参与,故A正确;B.根据图示的转化过程,
2
NO 转化为HNO,N元素的化合价由+4价变为+3价,化合价降低,得电子被还原,做氧化剂,则
2 2
NO 的是生成硫酸盐的氧化剂,故B正确;C.硫酸盐(含SO 、HSO )气溶胶中含有HSO ,转化过
2
程有水参与,则HSO 在水中可电离生成H+和SO ,则硫酸盐气溶胶呈酸性,故C正确;D.根据图
示转化过程中,由SO 转化为HSO ,根据图示对照,有硫氧键生成,故D错误;答案选D。
18.(2014·全国高考真题)已知分解1mol HO 放出热量98kJ,在含少量I-的溶液中,HO 的分解机理为:
2 2 2 2
HO+I-→HO+IO- 慢,HO+IO-→HO+O+I- 快;下列有关反应的说法正确的是
2 2 2 2 2 2 2
A.反应的速率与I-的浓度有关 B.IO-也是该反应的催化剂
C.反应活化能等于98kJ·mol-1 D.v(H O)=v(HO)=v(O )
2 2 2 2
【答案】A
【解析】A、根据反应机理可知I-是HO 分解的催化剂,碘离子浓度大,产生的IO-就多反应速率就快,A
2 2
正确;B、IO-不是该反应的催化剂,B错误;C、反应的活化能是反应物的总能量与生成物的总能量的差值。这与反应的物质得到多少,错误;D、 HO 分解的总方程式是2HO=2H O+ O ↑;由于水是
2 2 2 2 2 2
纯液体,不能用来表示反应速率,而且HO 和O 的系数不同,表示的化学反应速率也不同,D错误;
2 2 2
故合理选项为A。
19.(2018·海南高考真题)炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧。活化
过程的能量变化模拟计算结果如图所示。活化氧可以快速氧化SO 。下列说法正确的是
2
A.每活化一个氧分子吸收0.29eV能量
B.水可使氧分子活化反应的活化能降低0.42eV
C.氧分子的活化是O-O的断裂与C-O键的生成过程
D.炭黑颗粒是大气中SO 转化为SO 的催化剂
2 3
【答案】CD
【解析】A.由图可知,反应物的总能量高于生成物的总能量,因此是放出能量,不符合题意;B.由图可
知,水可使氧分子活化反应的活化能降低0.18eV,不符合题意;C.由图可知,氧分子的活化是O-
O的断裂与C-O键的生成过程,符合题意;D.活化氧可以快速氧化SO ,而炭黑颗粒可以活化氧分
2
子,因此炭黑颗粒可以看作大气中SO 转化为SO 的催化剂,符合题意;故答案为CD。
2 3
20.(2015·北京高考真题)最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化
学键的过程。反应过程的示意图如下:
下列说法中正确的是
A.CO和O生成CO 是吸热反应
2
B.在该过程中,CO断键形成C和O
C.CO和O生成了具有极性共价键的CO
2
D.状态Ⅰ →状态Ⅲ表示CO与O 反应的过程
2
【答案】C
【解析】A.根据能量--反应过程的图像知,状态I的能量高于状态III的能量,故该过程是放热反应,A
错误;B.根据状态I、II、III可以看出整个过程中CO中的C和O形成的化学键没有断裂,错误;
C.由图III可知,生成物是CO,具有极性共价键,正确;D.状态Ⅰ →状态Ⅲ表示CO与O反应的
2过程,错误。故选C。
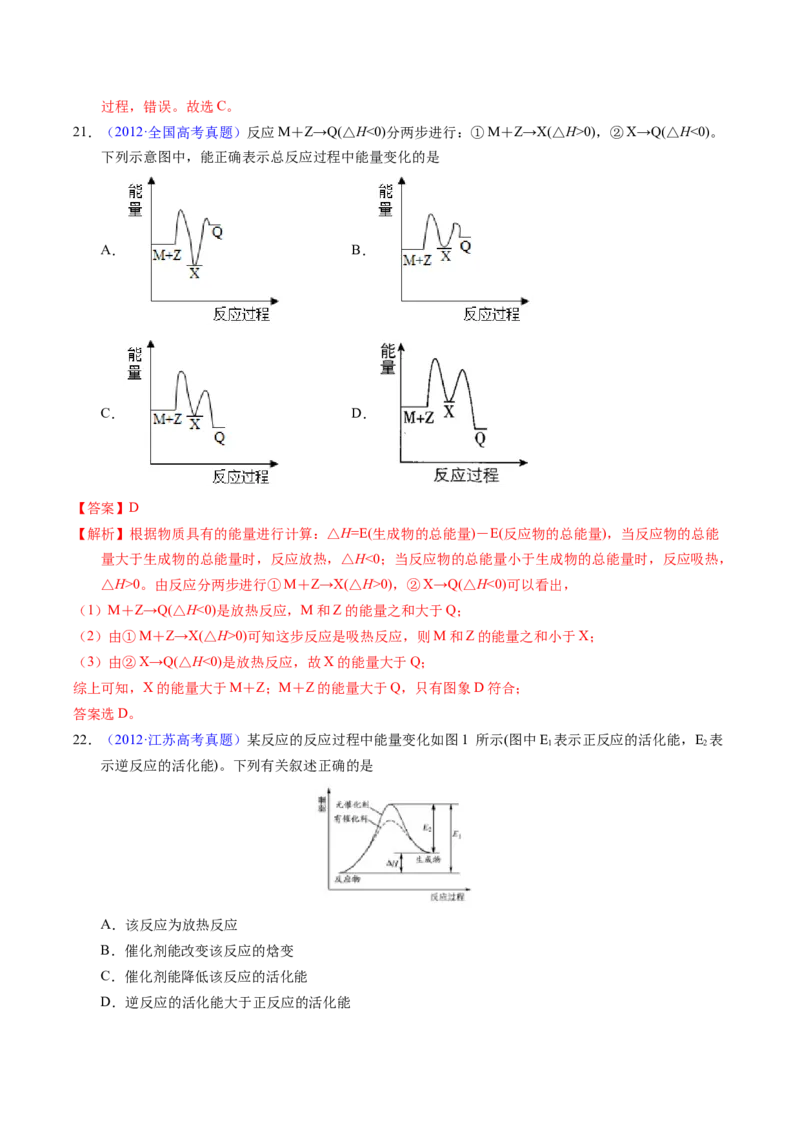
21.(2012·全国高考真题)反应M+Z→Q(△H<0)分两步进行:①M+Z→X(△H>0),②X→Q(△H<0)。
下列示意图中,能正确表示总反应过程中能量变化的是
A. B.
C. D.
【答案】D
【解析】根据物质具有的能量进行计算:△H=E(生成物的总能量)-E(反应物的总能量),当反应物的总能
量大于生成物的总能量时,反应放热,△H<0;当反应物的总能量小于生成物的总能量时,反应吸热,
△H>0。由反应分两步进行①M+Z→X(△H>0),②X→Q(△H<0)可以看出,
(1)M+Z→Q(△H<0)是放热反应,M和Z的能量之和大于Q;
(2)由①M+Z→X(△H>0)可知这步反应是吸热反应,则M和Z的能量之和小于X;
(3)由②X→Q(△H<0)是放热反应,故X的能量大于Q;
综上可知,X的能量大于M+Z;M+Z的能量大于Q,只有图象D符合;
答案选D。
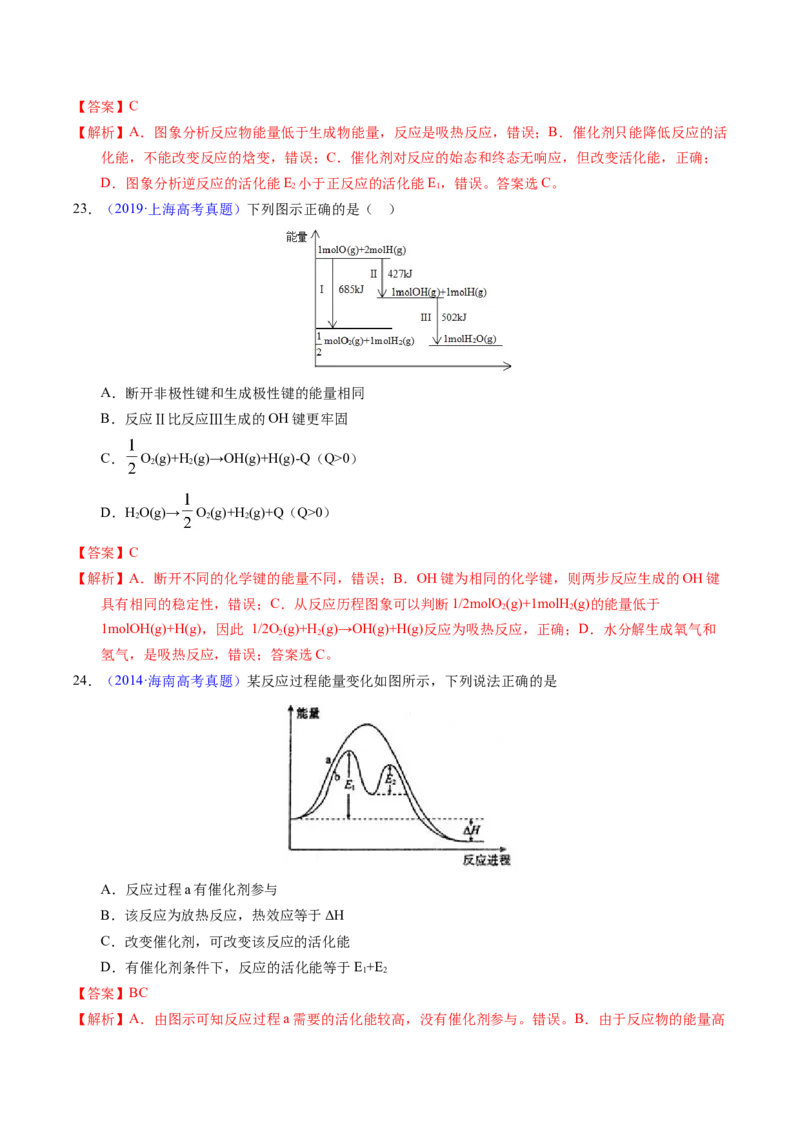
22.(2012·江苏高考真题)某反应的反应过程中能量变化如图1 所示(图中E 表示正反应的活化能,E 表
1 2
示逆反应的活化能)。下列有关叙述正确的是
A.该反应为放热反应
B.催化剂能改变该反应的焓变
C.催化剂能降低该反应的活化能
D.逆反应的活化能大于正反应的活化能【答案】C
【解析】A.图象分析反应物能量低于生成物能量,反应是吸热反应,错误;B.催化剂只能降低反应的活
化能,不能改变反应的焓变,错误;C.催化剂对反应的始态和终态无响应,但改变活化能,正确;
D.图象分析逆反应的活化能E 小于正反应的活化能E,错误。答案选C。
2 1
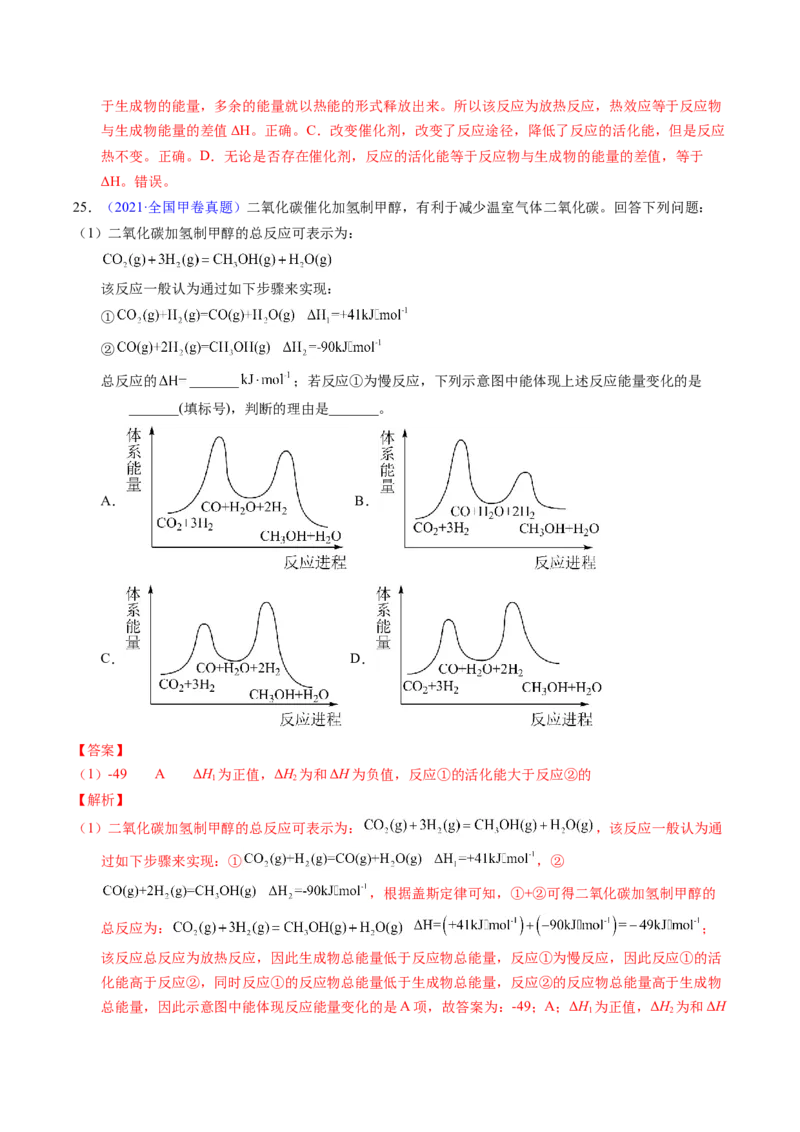
23.(2019·上海高考真题)下列图示正确的是( )
A.断开非极性键和生成极性键的能量相同
B.反应Ⅱ比反应Ⅲ生成的OH键更牢固
C. O(g)+H(g)→OH(g)+H(g)-Q(Q>0)
2 2
D.HO(g)→ O(g)+H(g)+Q(Q>0)
2 2 2
【答案】C
【解析】A.断开不同的化学键的能量不同,错误;B.OH键为相同的化学键,则两步反应生成的OH键
具有相同的稳定性,错误;C.从反应历程图象可以判断1/2molO(g)+1molH (g)的能量低于
2 2
1molOH(g)+H(g),因此 1/2O (g)+H(g)→OH(g)+H(g)反应为吸热反应,正确;D.水分解生成氧气和
2 2
氢气,是吸热反应,错误;答案选C。
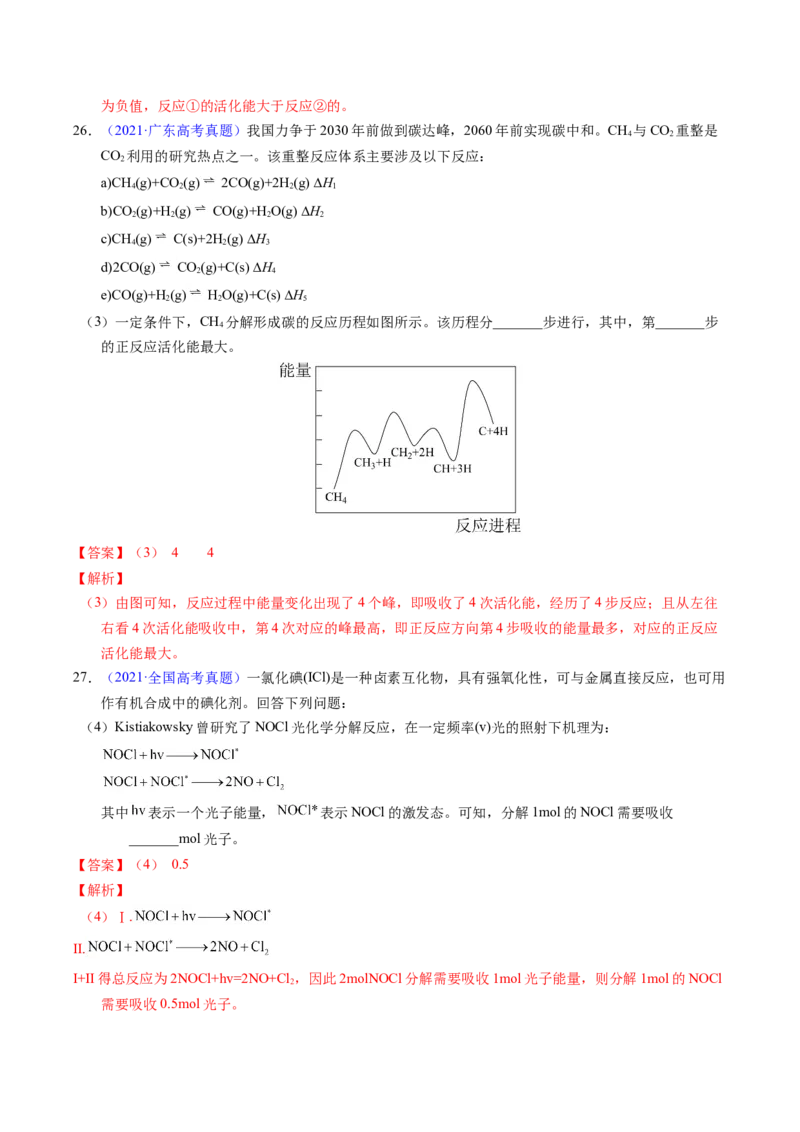
24.(2014·海南高考真题)某反应过程能量变化如图所示,下列说法正确的是
A.反应过程a有催化剂参与
B.该反应为放热反应,热效应等于ΔH
C.改变催化剂,可改变该反应的活化能
D.有催化剂条件下,反应的活化能等于E+E
1 2
【答案】BC
【解析】A.由图示可知反应过程a需要的活化能较高,没有催化剂参与。错误。B.由于反应物的能量高于生成物的能量,多余的能量就以热能的形式释放出来。所以该反应为放热反应,热效应等于反应物
与生成物能量的差值ΔH。正确。C.改变催化剂,改变了反应途径,降低了反应的活化能,但是反应
热不变。正确。D.无论是否存在催化剂,反应的活化能等于反应物与生成物的能量的差值,等于
ΔH。错误。
25.(2021·全国甲卷真题)二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为:
该反应一般认为通过如下步骤来实现:
①
②
总反应的 _______ ;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是
_______(填标号),判断的理由是_______。
A. B.
C. D.
【答案】
(1)-49 A ΔH 为正值,ΔH 为和ΔH为负值,反应①的活化能大于反应②的
1 2
【解析】
(1)二氧化碳加氢制甲醇的总反应可表示为: ,该反应一般认为通
过如下步骤来实现:① ,②
,根据盖斯定律可知,①+②可得二氧化碳加氢制甲醇的
总反应为: ;
该反应总反应为放热反应,因此生成物总能量低于反应物总能量,反应①为慢反应,因此反应①的活
化能高于反应②,同时反应①的反应物总能量低于生成物总能量,反应②的反应物总能量高于生成物
总能量,因此示意图中能体现反应能量变化的是A项,故答案为:-49;A;ΔH 为正值,ΔH 为和ΔH
1 2为负值,反应①的活化能大于反应②的。
26.(2021·广东高考真题)我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH 与CO 重整是
4 2
CO 利用的研究热点之一。该重整反应体系主要涉及以下反应:
2
a)CH(g)+CO (g) 2CO(g)+2H(g) ∆H
4 2 2 1
b)CO(g)+H(g) CO(g)+HO(g) ∆H
2 2 2 2
c)CH(g) C(s)+2H(g) ∆H
4 2 3
d)2CO(g) CO(g)+C(s) ∆H
2 4
e)CO(g)+H(g) HO(g)+C(s) ∆H
2 2 5
(3)一定条件下,CH 分解形成碳的反应历程如图所示。该历程分_______步进行,其中,第_______步
4
的正反应活化能最大。
【答案】(3) 4 4
【解析】
(3)由图可知,反应过程中能量变化出现了4个峰,即吸收了4次活化能,经历了4步反应;且从左往
右看4次活化能吸收中,第4次对应的峰最高,即正反应方向第4步吸收的能量最多,对应的正反应
活化能最大。
27.(2021·全国高考真题)一氯化碘(ICl)是一种卤素互化物,具有强氧化性,可与金属直接反应,也可用
作有机合成中的碘化剂。回答下列问题:
(4)Kistiakowsky曾研究了NOCl光化学分解反应,在一定频率(v)光的照射下机理为:
其中 表示一个光子能量, 表示NOCl的激发态。可知,分解1mol的NOCl需要吸收
_______mol光子。
【答案】(4) 0.5
【解析】
(4)Ⅰ.
Ⅱ.
Ⅰ+Ⅱ得总反应为2NOCl+hv=2NO+Cl ,因此2molNOCl分解需要吸收1mol光子能量,则分解1mol的NOCl
2
需要吸收0.5mol光子。28.(2015·广东高考真题)用O 将HCl转化为Cl,可提高效益,减少污染,
2 2
(1)传统上该转化通过如图所示的催化剂循环实现,
其中,反应①为:2HCl(g) + CuO(s) HO(g)+CuCl (g) △H
2 2 1
反应②生成1molCl (g)的反应热为△H,则总反应的热化学方程式为___________(反应热用△H 和
2 2 1
△H 表示)。
2
【答案】(1)2HCl(g) + 1/2O(g) HO(g)+Cl(g) △H=△H+△H
2 2 2 1 2
【解析】
(1)根据图像信息,箭头指向的是生成物可写出反应②的热化学方程式:CuCl (g)+1/2O (g)
2 2
CuO(s) +Cl(g) △H,则①+②可得总反应;
2 2