文档内容
重庆八中 2024——2025 学年度(下)高三年级入学适应性训练
化 学 试 题
考试时间:75分钟 满分:100分
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5
Fe-56 Co-59 Sb-122
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只
有一项是符合题目要求的。
1.2023年10月26日,神舟十七号成功发射。下列说法正确的是
A.重庆造“神十七”关键铝材超六成,铝属于金属材料
B.载人飞船返回舱表面层使用的玻璃纤维属于天然高分子材料
C.“神十七”使用了砷化镓太阳能电池板,砷化镓属于复合材料
D.“神十七”使用的耐辐照光学石英玻璃属于有机合成材料
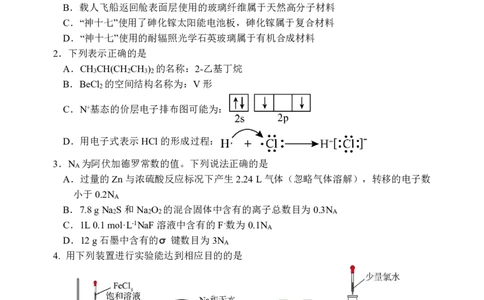
2.下列表示正确的是
A.CH CH(CH CH ) 的名称:2-乙基丁烷
3 2 3 2
B.BeCl 的空间结构名称为:V形
2
C.N+基态的价层电子排布图可能为:
D.用电子式表示HCl的形成过程:
3.N 为阿伏加德罗常数的值。下列说法正确的是
A
A.过量的Zn与浓硫酸反应标况下产生2.24L气体(忽略气体溶解),转移的电子数
小于0.2N
A
B.7.8gNa S和Na O 的混合固体中含有的离子总数目为0.3N
2 2 2 A
C.1L0.1mol·L-1NaF溶液中含有的F-数为0.1N
A
D.12g石墨中含有的σ 键数目为3N
A
4. 用下列装置进行实验能达到相应目的的是
A.用图①装置制备Fe(OH) 胶体
3
B.用图②装置制取Ti单质
C.用图③装置干燥二氧化碳
D.用图④装置探究Fe2+与I-还原性强弱
试卷第1页,共10页5. 下列离子方程式书写正确的是
A. 将FeSO 溶液与过量NH HCO 混合溶液反应,生成FeCO 沉淀:
4 4 3 3
Fe2++2HCO-=FeCO +CO +H O
3 3 2 2
B. 向FeCl 溶液中加入过量的Na S溶液:2Fe3++S2-=2Fe2++S↓
3 2
C. 向明矾溶液中滴加氢氧化钡至沉淀质量最大:
2Al3++3SO2-+3Ba2++6OH-=3BaSO +2Al OH
4 4 3
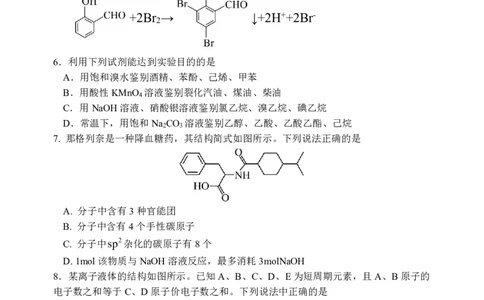
D. 邻羟基苯甲醛中加入足量浓溴水:
+2Br → ↓+2H++2Br-
2
6.利用下列试剂能达到实验目的的是
A.用饱和溴水鉴别酒精、苯酚、己烯、甲苯
B.用酸性KMnO 溶液鉴别裂化汽油、煤油、柴油
4
C.用NaOH溶液、硝酸银溶液鉴别氯乙烷、溴乙烷、碘乙烷
D.常温下,用饱和Na CO 溶液鉴别乙醇、乙酸、乙酸乙酯、己烷
2 3
7. 那格列奈是一种降血糖药,其结构简式如图所示。下列说法正确的是
A. 分子中含有3种官能团
B. 分子中含有4个手性碳原子
C. 分子中sp2杂化的碳原子有8个
D.1mol该物质与NaOH溶液反应,最多消耗3molNaOH
8.某离子液体的结构如图所示。已知A、B、C、D、E为短周期元素,且A、B原子的
电子数之和等于C、D原子价电子数之和。下列说法中正确的是
A.简单氢化物的极性:A>B
B.第一电离能:D>C>B
C.EC 中E原子为sp2杂化
2
D.阴离子中所有原子均满足8e-结构
试卷第2页,共10页9.根据下列实验操作和现象所得到的结论正确的是
选
实验操作和现象 实验结论
项
A
某溶液中滴加K [Fe(CN) ]溶液,产生蓝色沉淀 原溶液中有Fe2+,无Fe3+
3 6
向久置的Na SO 溶液中加入足量BaCl 溶液,出现白色
2 3 2
B Na 2 SO 3 部分被氧化
沉淀;再加入足量稀盐酸,沉淀部分溶解
取2ml淀粉溶液,加入少量稀硫酸,加热2~3min,冷
C 淀粉已经完全水解
却后加入NaOH溶液至碱性,再滴加碘水,溶液未变蓝
D 常温下,将铁片浸入足量浓硫酸中,无明显现象 常温下,铁与浓硫酸不反应
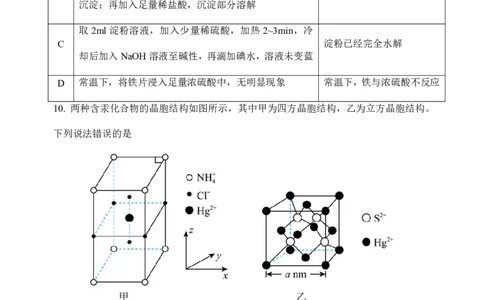
10. 两种含汞化合物的晶胞结构如图所示,其中甲为四方晶胞结构,乙为立方晶胞结构。
下列说法错误的是
A. 甲的化学式为NH HgCl
4 3
B. 甲中Hg2+的配位数为6
1
C. 将乙晶胞沿x轴方向平移 a 后,S2-位于立方体的棱上和体内
2
3
D. 乙中相邻的Hg2+和S2-之间的距离为 a nm
4
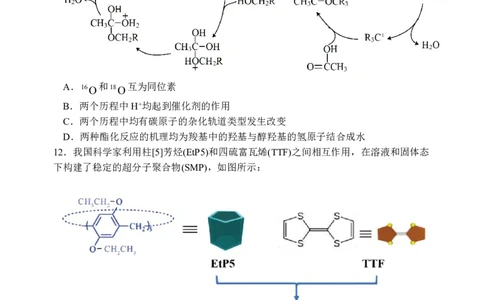
试卷第3页,共10页11.伯醇(记为RCH OH)和叔醇(记为R COH)发生酯化反应的机理如下图所示。下列说法
2 3
错误的是
A.
16O
和
18O
互为同位素
B.两个历程中H+均起到催化剂的作用
C.两个历程中均有碳原子的杂化轨道类型发生改变
D.两种酯化反应的机理均为羧基中的羟基与醇羟基的氢原子结合成水
12.我国科学家利用柱[5]芳烃(EtP5)和四硫富瓦烯(TTF)之间相互作用,在溶液和固体态
下构建了稳定的超分子聚合物(SMP),如图所示:
下列说法正确的是( )
A.EtP5分子间存在氢键
B.TTF分子中核磁共振氢谱有2组峰
C.EtP5与TTF通过分子间作用力形成SMP
D.EtP5和EtP10互为同系物,且EtP10与TTF形成的SMP稳定性强于EtP5
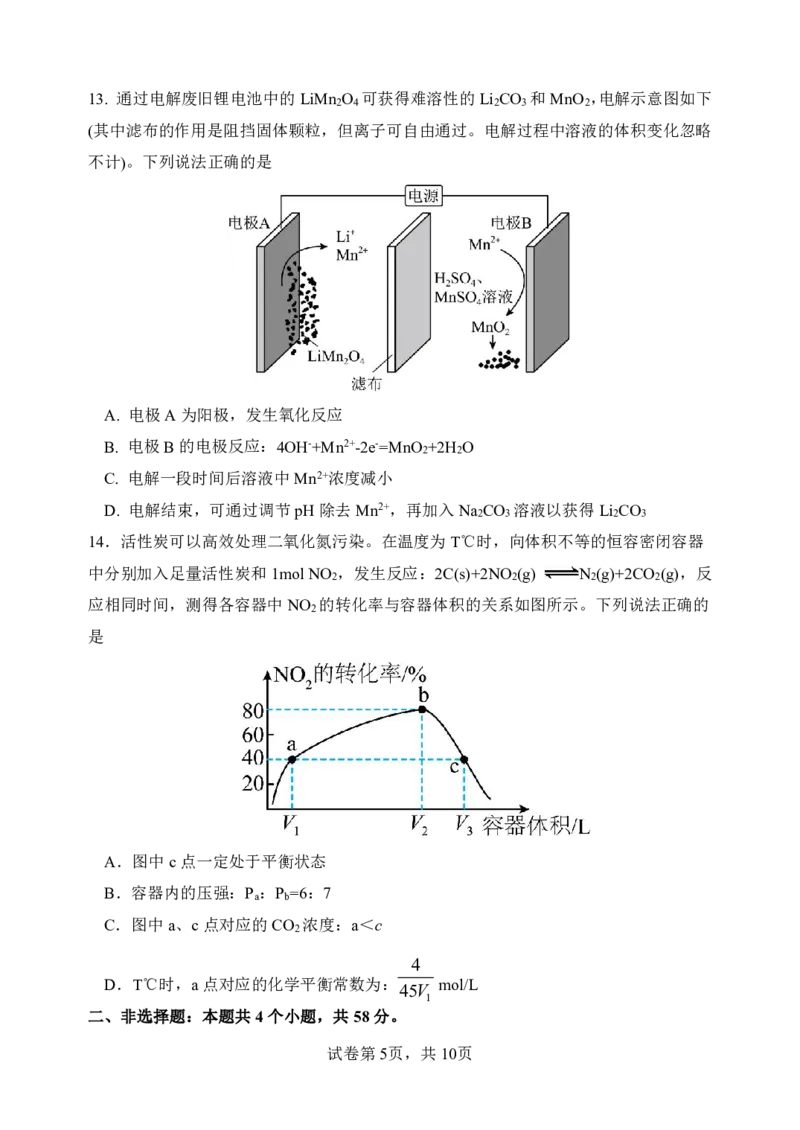
试卷第4页,共10页13. 通过电解废旧锂电池中的LiMn O 可获得难溶性的Li CO 和MnO ,电解示意图如下
2 4 2 3 2
(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略
不计)。下列说法正确的是
A. 电极A为阳极,发生氧化反应
B. 电极B的电极反应:4OH-+Mn2+-2e-=MnO +2H O
2 2
C. 电解一段时间后溶液中Mn2+浓度减小
D. 电解结束,可通过调节pH除去Mn2+,再加入Na CO 溶液以获得Li CO
2 3 2 3
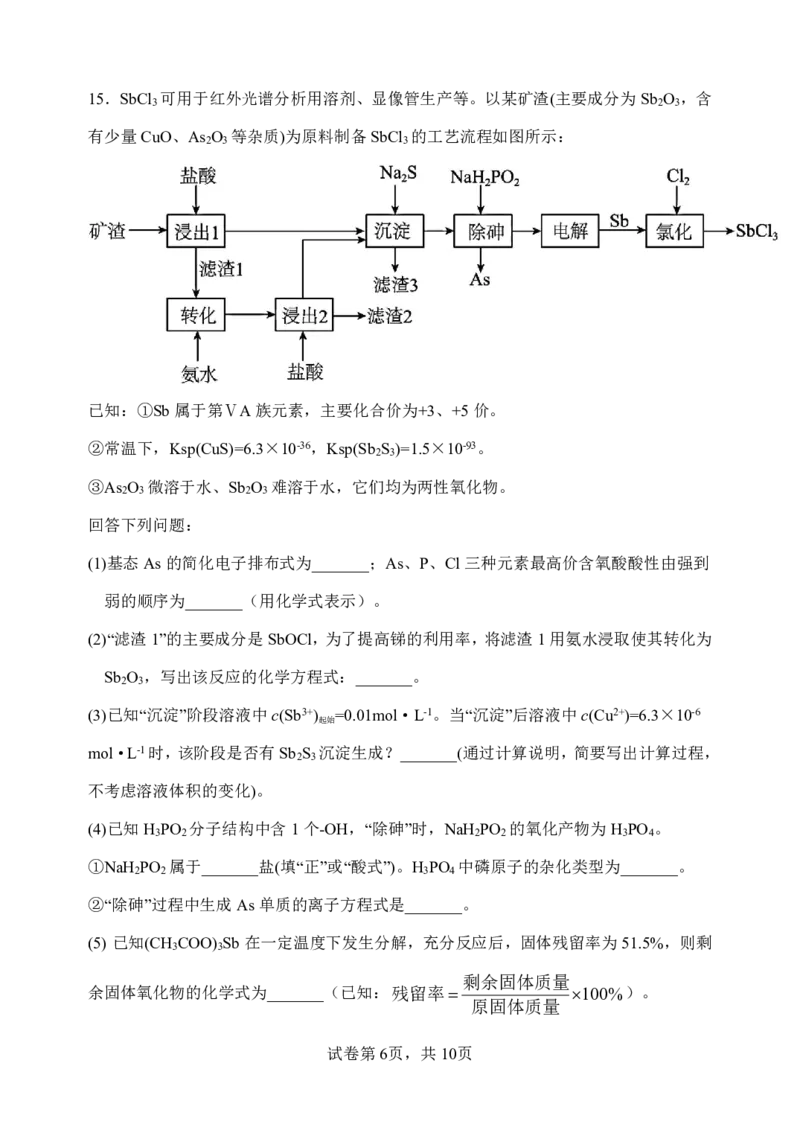
14.活性炭可以高效处理二氧化氮污染。在温度为T℃时,向体积不等的恒容密闭容器
中分别加入足量活性炭和1molNO ,发生反应:2C(s)+2NO (g) N (g)+2CO (g),反
2 2 2 2
应相同时间,测得各容器中NO 的转化率与容器体积的关系如图所示。下列说法正确的
2
是
A.图中c点一定处于平衡状态
B.容器内的压强:P :P =6:7
a b
C.图中a、c点对应的CO 浓度:a<c
2
4
D.T℃时,a点对应的化学平衡常数为: mol/L
45V
1
二、非选择题:本题共4个小题,共58分。
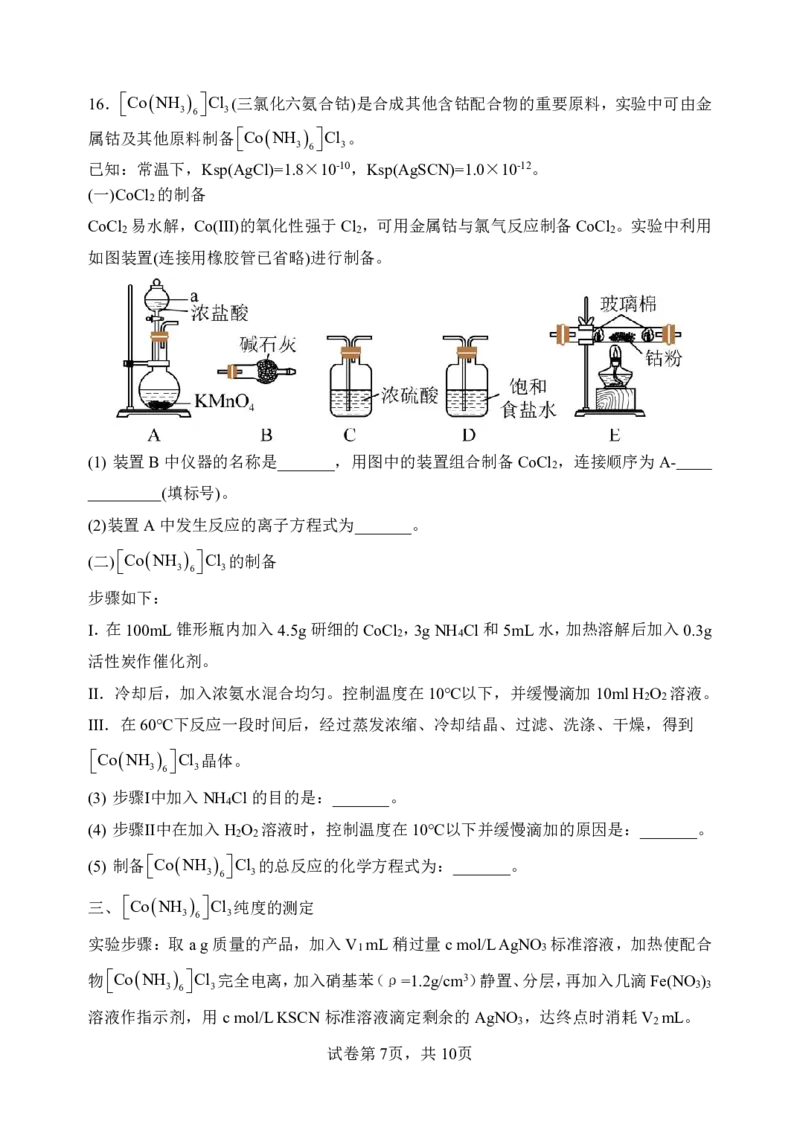
试卷第5页,共10页15.SbCl 可用于红外光谱分析用溶剂、显像管生产等。以某矿渣(主要成分为Sb O ,含
3 2 3
有少量CuO、As O 等杂质)为原料制备SbCl 的工艺流程如图所示:
2 3 3
已知:①Sb属于第ⅤA族元素,主要化合价为+3、+5价。
②常温下,Ksp(CuS)=6.3×10-36,Ksp(Sb S )=1.5×10-93。
2 3
③As O 微溶于水、Sb O 难溶于水,它们均为两性氧化物。
2 3 2 3
回答下列问题:
(1)基态As的简化电子排布式为_______;As、P、Cl三种元素最高价含氧酸酸性由强到
弱的顺序为_______(用化学式表示)。
(2)“滤渣1”的主要成分是SbOCl,为了提高锑的利用率,将滤渣1用氨水浸取使其转化为
Sb O ,写出该反应的化学方程式:_______。
2 3
(3)已知“沉淀”阶段溶液中c(Sb3+) =0.01mol·L-1。当“沉淀”后溶液中c(Cu2+)=6.3×10-6
起始
mol·L-1时,该阶段是否有Sb S 沉淀生成?_______(通过计算说明,简要写出计算过程,
2 3
不考虑溶液体积的变化)。
(4)已知H PO 分子结构中含1个-OH,“除砷”时,NaH PO 的氧化产物为H PO 。
3 2 2 2 3 4
①NaH PO 属于_______盐(填“正”或“酸式”)。H PO 中磷原子的杂化类型为_______。
2 2 3 4
②“除砷”过程中生成As单质的离子方程式是_______。
(5) 已知(CH COO) Sb在一定温度下发生分解,充分反应后,固体残留率为51.5%,则剩
3 3
剩余固体质量
余固体氧化物的化学式为_______(已知:残留率 100%)。
原固体质量
试卷第6页,共10页16.
CoNH
3
6
Cl
3
(三氯化六氨合钴)是合成其他含钴配合物的重要原料,实验中可由金
属钴及其他原料制备CoNH Cl 。
3 6 3
已知:常温下,Ksp(AgCl)=1.8×10-10,Ksp(AgSCN)=1.0×10-12。
(一)CoCl 的制备
2
CoCl 易水解,Co(Ⅲ)的氧化性强于Cl ,可用金属钴与氯气反应制备CoCl 。实验中利用
2 2 2
如图装置(连接用橡胶管已省略)进行制备。
(1) 装置B中仪器的名称是_______,用图中的装置组合制备CoCl ,连接顺序为A-
2
(填标号)。
(2)装置A中发生反应的离子方程式为_______。
(二)
CoNH
3
6
Cl
3
的制备
步骤如下:
Ⅰ.在100mL锥形瓶内加入4.5g研细的CoCl ,3gNH Cl和5mL水,加热溶解后加入0.3g
2 4
活性炭作催化剂。
Ⅱ.冷却后,加入浓氨水混合均匀。控制温度在10℃以下,并缓慢滴加10mlH O 溶液。
2 2
Ⅲ.在60℃下反应一段时间后,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到
CoNH Cl 晶体。
3 6 3
(3) 步骤Ⅰ中加入NH Cl的目的是:_______。
4
(4) 步骤Ⅱ中在加入H O 溶液时,控制温度在10℃以下并缓慢滴加的原因是:_______。
2 2
(5) 制备 CoNH 3 6 Cl 3 的总反应的化学方程式为:_______。
三、CoNH Cl 纯度的测定
3 6 3
实验步骤:取ag质量的产品,加入V mL稍过量cmol/LAgNO 标准溶液,加热使配合
1 3
物 CoNH 3 6 Cl 3 完全电离,加入硝基苯(ρ=1.2g/cm3)静置、分层,再加入几滴Fe(NO 3 ) 3
溶液作指示剂,用cmol/LKSCN标准溶液滴定剩余的AgNO ,达终点时消耗V mL。
3 2
试卷第7页,共10页(6)、下列操作会导致测定结果偏低的是______(填序号),该配合物的纯度为_______
(含a、c、V 、V 的计算式表示)。
1 2
A. 滴定管使用前未用待测液润洗
B. 滴定前锥形瓶未干燥
C. 未加入硝基苯
17.丁二烯(C H )是生产合成橡胶的重要原料,其用量占全部合成橡胶原料消耗的60%
4 6
以上,工业上可通过多种催化方法生产丁二烯。回答下列问题:
(1)已知:丁烷(C H )脱氢:C H (g) C H (g)+2H (g) △H=+234kJ/mol
4 10 4 10 4 6 2
丁烯(C H )脱氢:C H (g) C H (g)+H (g) △H=+118kJ/mol
4 8 4 8 4 6 2
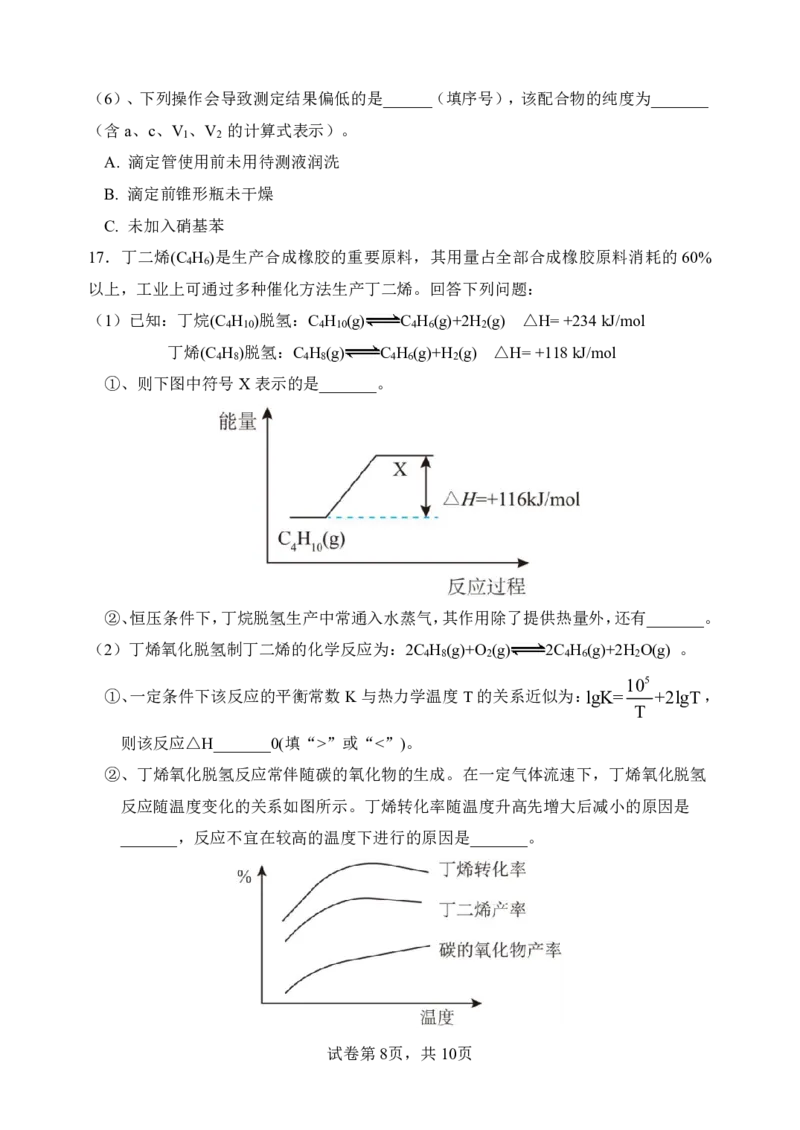
①、则下图中符号X表示的是_______。
②、恒压条件下,丁烷脱氢生产中常通入水蒸气,其作用除了提供热量外,还有_______。
(2)丁烯氧化脱氢制丁二烯的化学反应为:2C H (g)+O (g) 2C H (g)+2H O(g) 。
4 8 2 4 6 2
105
①、一定条件下该反应的平衡常数K与热力学温度T的关系近似为:lgK= +2lgT,
T
则该反应△H_______0(填“>”或“<”)。
②、丁烯氧化脱氢反应常伴随碳的氧化物的生成。在一定气体流速下,丁烯氧化脱氢
反应随温度变化的关系如图所示。丁烯转化率随温度升高先增大后减小的原因是
_______,反应不宜在较高的温度下进行的原因是_______。
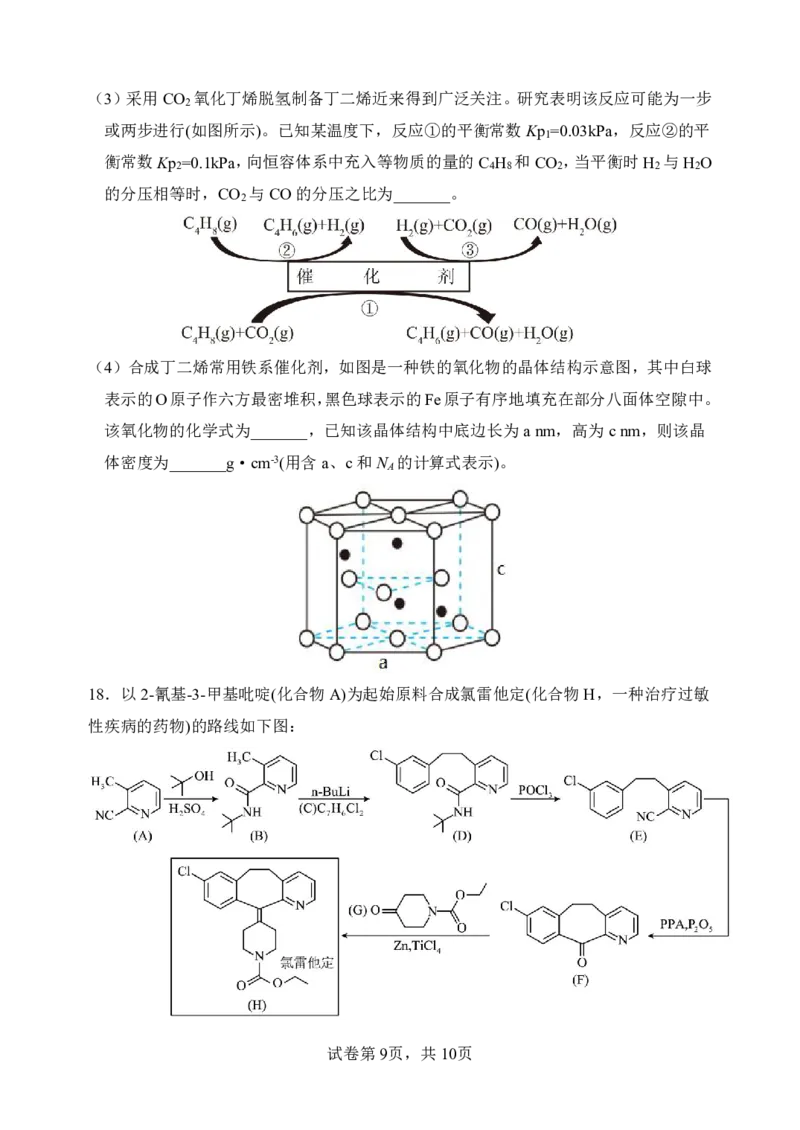
试卷第8页,共10页(3)采用CO 氧化丁烯脱氢制备丁二烯近来得到广泛关注。研究表明该反应可能为一步
2
或两步进行(如图所示)。已知某温度下,反应①的平衡常数Kp =0.03kPa,反应②的平
1
衡常数Kp =0.1kPa,向恒容体系中充入等物质的量的C H 和CO ,当平衡时H 与H O
2 4 8 2 2 2
的分压相等时,CO 与CO的分压之比为_______。
2
(4)合成丁二烯常用铁系催化剂,如图是一种铁的氧化物的晶体结构示意图,其中白球
表示的O原子作六方最密堆积,黑色球表示的Fe原子有序地填充在部分八面体空隙中。
该氧化物的化学式为_______,已知该晶体结构中底边长为anm,高为cnm,则该晶
体密度为_______g·cm-3(用含a、c和N 的计算式表示)。
A
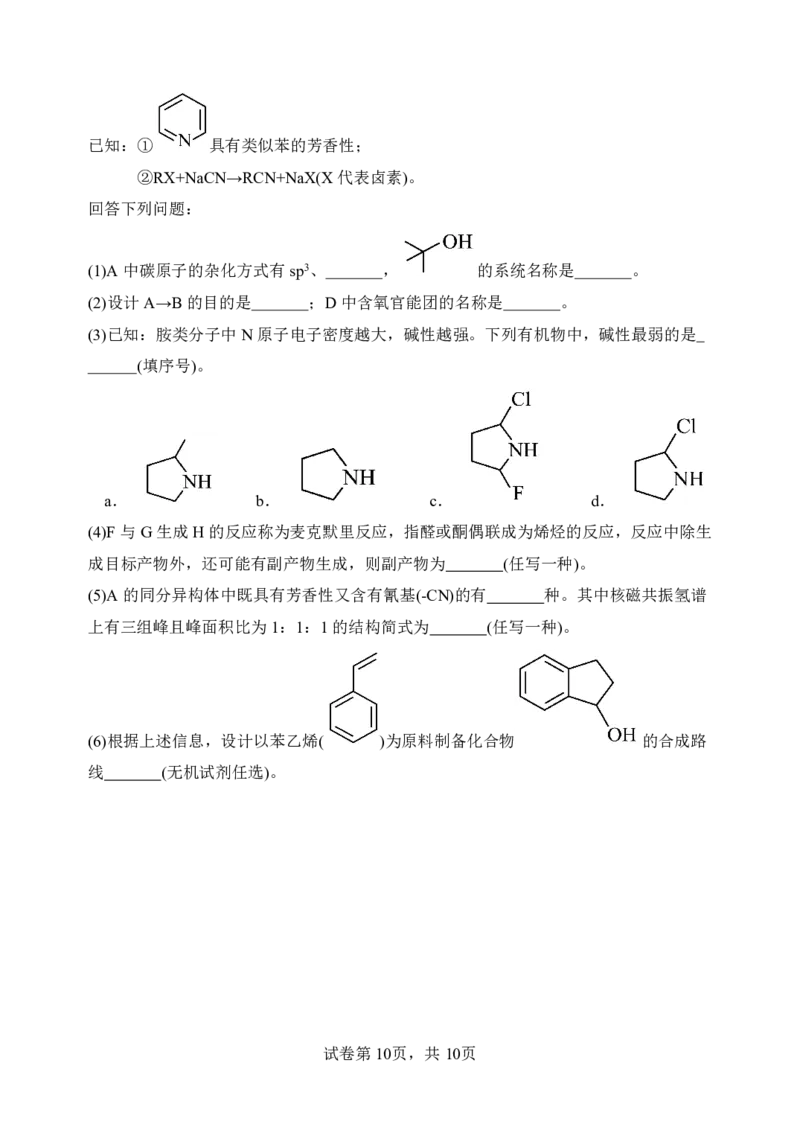
18.以2-氰基-3-甲基吡啶(化合物A)为起始原料合成氯雷他定(化合物H,一种治疗过敏
性疾病的药物)的路线如下图:
试卷第9页,共10页已知:① 具有类似苯的芳香性;
②RX+NaCN→RCN+NaX(X代表卤素)。
回答下列问题:
(1)A中碳原子的杂化方式有sp3、 , 的系统名称是 。
(2)设计A→B的目的是 ;D中含氧官能团的名称是 。
(3)已知:胺类分子中N原子电子密度越大,碱性越强。下列有机物中,碱性最弱的是
(填序号)。
a. b. c. d.
(4)F与G生成H的反应称为麦克默里反应,指醛或酮偶联成为烯烃的反应,反应中除生
成目标产物外,还可能有副产物生成,则副产物为 (任写一种)。
(5)A的同分异构体中既具有芳香性又含有氰基(-CN)的有 种。其中核磁共振氢谱
上有三组峰且峰面积比为1:1:1的结构简式为 (任写一种)。
(6)根据上述信息,设计以苯乙烯( )为原料制备化合物 的合成路
线 (无机试剂任选)。
试卷第10页,共10页