文档内容
重庆八中 2024——2025 学年度(下)高三年级入学适应性训练
参考答案
1.【答案】A
【解析】A.金属材料包括金属单质和合金,A正确;
B.玻璃纤维属于合成无机非金属材料,不是天然材料,B错误;
C.砷化镓属于半导体材料,无机非金属材料,C错误;
D.光学石英玻璃主要成分为SiO ,属于传统无机非金属材料,D错误;
2
2.【答案】C
【解析】A.CH CHCH CH 的名称:3-甲基戊烷,故A错误;
3 2 3 2
B.BeCl 中的Be形成2个σ键,无孤电子对,空间结构名称为:直线形,故B错误;
2
C.N原子序数为7,N 的价层电子排布式为2s22p2,N 能量最低时的价层电子排布图可能为:
,故C正确;
D.用电子式表示HCl的形成过程: ,故D错误;
3.【答案】B
【解析】A.标准状况下,2.24L气体为0.1mol,无论气体是SO 还是H ,均转移0.2mol电子,
2 2
故转移的电子数为0.2N ,A错误;
A
B.Na S、Na O 的摩尔质量均为78g⋅ mol1,1mol Na S含有2mol阳离子和1mol阴离子,1
2 2 2 2
mol Na O 也含有2mol阳离子和1mol阴离子(过氧根离子),7.8g Na S和1 Na O 的混合物的
2 2 2 2 2
物质的量为0.1mol,含有的离子数为0.3N ,B正确;
A
C.NaF溶液中存在水解平衡F H O HFOH,故1L0.1mol⋅ L1 NaF溶液中含有的F数
2
小于0.1N ,C错误;
A
D.12g石墨含有1mol碳原子,每个碳原子与周围的3个碳原子形成σ 键,所以平均每个碳原子
形成1.5个σ 键,故12g金刚石中含有的σ 键数为1.5N ,D错误。
A
4. 【答案】D
【解析】A.制备制备Fe(OH) 胶体不能使用NaOH溶液,A错误;
3
B.在坩埚中加热,Na与空气中的氧气反应,B错误;
C.U形管除杂不能选用液体除杂试剂,C错误;
D.根据上层液体不变色,下层液体变为紫色来判断还原性I->Fe2+,D正确。
5. 【答案】A
【 解 析 】 A . FeSO 溶 液 与 NH HCO 反 应 , 生 成 FeCO 沉 淀 , 离 子 方 程 式 为 :
4 4 3 3
Fe2++HCO+NH H O=FeCO +NH++H O,故A错误;
3 3 2 3 4 2
B.Fe3+与过量的Na S先发生氧化还原反应,然后生成FeS沉淀。离子方程为:2Fe3++3S2-=2FeS↓+S↓,
2
故B错误;
C.向明矾溶液中滴加氢氧化钡至沉淀质量最大时,是产生沉淀只有硫酸钡沉淀,反应的离子方程
式为:Al3 2SO2 2Ba2 4OH=2BaSO Al(OH) ,故C错误;
4 4 4
D.醛基具有强还原性、能被溴水氧化,邻羟基苯甲醛中加入足量浓溴水,生成 ,离子方程式为: ,故D错误。
6.【答案】A
【解析】A.溴水与酒精不反应,但是可以混溶;苯酚与溴水反应生成白色沉淀;乙烯与溴水发生
加成反应使溴水褪色;甲苯与溴水萃取,可以鉴别,A正确;
B.汽油能使酸性高锰酸钾溶液褪色,煤油和柴油均不能使酸性高锰酸钾溶液褪色,B错误;
C.氯乙烷、溴乙烷和碘乙烷在碱性条件下可水解,应先加入酸中和碱后再加入硝酸银,进行卤素
离子的检验,C错误;
D.乙醇溶于饱和Na CO 溶液,乙醛不与饱和Na CO 溶液反应,但可与饱和Na CO 溶液互溶,
2 3 2 3 2 3
乙酸与饱和Na CO 溶液反应有气泡冒出,常温下,乙酸乙酯不溶于饱和Na CO 溶液分层,不能
2 3 2 3
鉴别,D错误;
7.【答案】C
【解析】A.由结构可知该物质中含有酰胺基和羧基2种官能团,A错误;
B.手性碳原子是与四个不同的原子或原子团相连的碳原子,由结构可知羧基直接相连的碳为手性
碳原子,因此只有1个手性碳原子,B错误;
C.苯环上的碳原子为sp2杂化,酰胺基和羧基上碳原子为sp2杂化,因此分子中sp2杂化的碳原子
有8个,C正确;
D.与盐酸反应会发生酰胺基的水解反应,与NaOH溶液反应同时发生酰胺基的水解反应和羧酸
的中和反应,D错误;
8.【答案】C
【解析】A.A的简单氢化物为CH ,为非极性分子,B为NH ,非极性分子,A错误;
4 3
B.元素的第一电离能:F>N>O,B错误;
C.SO 中,S原子的价电子对数为2,原子为sp2杂化,C正确;
2
D.S原子不满足8e-结构,D错误;
9.【答案】B
【解析】A.可以证明溶液中含有Fe2+,不能证明是否含有Fe3+,A错误;
B.沉淀部分溶解,证明原溶液中含有Na SO 和Na SO ,所以Na SO 部分变质,B错误;
2 3 2 4 2 3
C.因为I 也可以与NaOH反应而被消耗,C错误;
2
D.常温下,Fe与浓硫酸会发生钝化而使反应停止,钝化属于化学变化,D错误。
10. 【答案】C
【解析】A.根据均摊法计算可得 ,A正确;
B.Hg2+周围有6个Cl-,所以配位数为6,B项正确;
C.乙晶胞平移后,S2-应该只位于体内,C项错误;
D.乙晶胞中相邻的Hg2+和S2-距离为面对角线长度的1/4,D项正确。
11.【答案】D
【详解】A.
16O
和 18O质子数相等,中子数不等的原子,故A正确;
B.根据两个历程可以分析出H均先被消耗、后生成,均起到催化剂的作用,故B正确;
C.两个历程中都有碳原子的杂化类型从sp3变为sp2,故C正确;
D.两种酯化反应的机理,前者是羧基中的羟基与醇羟基的氢原子结合成水,后者是醇中羟基与酸
中羟基上的氢结合成水,不同,故D错误。
12.【答案】C
【解析】A项,EtP5分子间不存在氢键;A错误;
B项,TTF的结构对称,只有一种氢原子,核磁共振氢谱中含有1组峰,B错误;C项,超分子是由两种或两种以上分子通过分子间相互作用形成的分子聚集体,由题目给出信息
可知,SMP是由科学家已构建成功的超分子聚合物,故EtP5和TTF可通过分子间作用力自组装
得到超分子聚合物SMP,C正确;
D项,EtP5和EtP10官能团数目不同,所以EtP5和EtP10不是同系物,若用EtP10替换EtP5,碳
环变大,分子间距离变大,分子间作用力变弱,D错误。
13.【答案】D
【解析】A.由分析可知,电极B为阳极,发生氧化反应,A错误;
B.电极B为阳极,电解质呈酸性,电极反应式为2H O+Mn2+-2e-=MnO +4H+,B错误;
2 2
电解
C.电解的总反应方程式为2LiMn O +4H+ 2Li++Mn2++3MnO +2H O,反应生成了Mn2+,电
2 4 2 2
解一段时间后,溶液中Mn2+浓度增大,C错误;
电解
D.电解的总反应方程式为2LiMn O +4H+ 2Li++Mn2++3MnO +2H O,电解结束后,可通过调
2 4 2 2
节溶液pH将锰离子转化为沉淀除去,然后再加入碳酸钠溶液,从而获得碳酸锂,D正确。
14.【答案】D
【解析】A选项c点对应的容器体积最大,压强最小,反应速率最小,c点不是平衡状态,A错误;
B.a点反应三段式为:
2C(s) + 2NO (g) N (g) + 2CO (g)
2 2 2
起始/mol 1 0 0
转化/mol 0.4 0.2 0.4
平衡/mol 0.6 0.2 0.4
b点反应三段式为:
2C(s) + 2NO (g) N (g) + 2CO (g)
2 2 2
起始/mol 1 0 0
转化/mol 0.8 0.4 0.8
平衡/mol 0.2 0.4 0.8
根据a点反应三段式、b点反应三段式和PV=nRT可知,PV =1.2RT,P V =1.4RT,由于V >V ,
a 1 b 2 2 1
所以容器内的压强:p :p 6:7,故B错误;
a b
C.图中a点、c点NO 的转化率相同,生成的CO 的物质的量相同,但a点容器体积小于c
2 2
点容器体积,则对应CO 的浓度:c CO c CO ,故C错误;
2 a 2 c 2
D.由于a点为平衡点,此时NO 的转化率为40%,a点反应三段式为:
2
2C(s) + 2NO (g) N (g) + 2CO (g)
2 2 2
起始/mol 1 0 0
转化/mol 0.4 0.2 0.4
平衡/mol 0.6 0.2 0.4
0.6 0.2 0.4
各物质平衡浓度为c(NO )= mol/L、c(N )= mol/L、c(CO )= mol/L,T℃时,该反应
2 V 2 V 2 V
1 1 1
0.2 0.4
( )2
c(N )c2(CO ) V V 4
的化学平衡常数K= 2 2 1 1 ,故D正确。
c2(NO ) 0.6 45V
2 ( )2 1
V
1
15.【答案】(1)[Ar]3d104s24p3 HClO >H PO >H AsO
4 3 4 3 4
(2)2SbOCl+2NH ∙H O=Sb O +2NH Cl+H O
3 2 2 3 4 2
(3)根据K (CuS)=6.3×10-36,当c(Cu2+)=6.3×10-6mol/L时,c(S2-)= =1.0×10-30mol/L,此时
sp
Ksp CuS
2+
c Cuc2(Sb3+)·c3(S2-)=(0.01mol/L)2·(1.0×10-30mol/L)3=1.0×10-94<1.5×10-93,故无Sb S 沉淀生成
2 3
(4)正(1分) sp3 (1分) 4As3++3H PO -+6H O=4As↓+3H PO +9H+
2 2 2 3 4
(5) O
2
【分析】以某矿渣(主要成分为 ,含有少量 、 等杂质)为原料制备SbCl ,矿渣用盐
3
酸浸Sb出,Sb O 、CuO、As O 分别与盐酸反应生成SbCl 、CuCl 、AsCl ,过滤除去难溶性杂质,
2 3 2 3 3 2 3
Sb2O3 CuO As2O3
滤液中加入Na S,沉淀Cu2+,过滤得到滤渣3为CuS,滤液中加入NaH PO 除去AsCl ,发生氧
2 2 2 3
化还原反应生成As单质和磷酸,电解SbCl 制得金属Sb,用氯气氯化Sb制得SbCl ;
3 3
【详解】(1)As的原子序数为33,则核外电子数为33,简化电子排布式为[Ar]3d104s24p3;As
位于第VA族,同周期元素自左到右,非金属性逐渐增大,同主族元素,从上到下,非金属性逐
渐减小,As、P、Cl三种元素的非金属性从大到小的顺序为Cl>P>As, 、 、 三种元素最高价
含氧酸酸性从大到小的顺序为HClO >H PO >H AsO ;
4 3 4 3 4
As P Cl
(2)“滤渣1”的主要成分是SbOCl,将滤渣1用氨水浸取使SbOCl转化为Sb O ,即SbOCl和
2 3
NH ∙H O反应生成Sb O 、NH Cl和H O,离子方程式为:2SbOCl+2NH ∙H O=
3 2 2 3 4 2 3 2
Sb O +2 +2Cl-+H O;
2 3 2
(3)根据K + (CuS)=6.3×10-36,当c(Cu2+)=6.3×10-6mol/L时,c(S2-)= =1.0×10-30mol/L,此时
NH4sp
Ksp CuS
c2(Sb3+)·c3(S2-)=(0.01mol/L)2·(1.0×10-30mol/L)3=1.0×10-94<1.5×10-93,故无2S+b S 沉淀生成;
c Cu 2 3
(4)①次磷酸为一元中强酸,NaH PO 的化学名称为次磷酸钠,属于正盐,H PO 中磷原子的价
2 2 3 4
层电子对数为4+ =4,磷原子的杂化类型为sp3;
②“除砷”过程中A 5+ s 3 C − l 2×和4 NaH PO 反应生成As, 的氧化产物为 ,P元素化合价升
3 2 2
2
高,As元素化合价降低,根据得失电子守恒和原子守恒配平化学方程式为:
NaH2PO2 H3PO4
4AsCl +3NaH PO +6H O=4As↓+3H PO +9HCl+3NaCl;
3 2 2 2 3 4
(5)(CH COO) Sb相对分子质量为299,固体残留率为51.5%,故剩余固体的分子量为299×
3 3
51.5%=154。分子式中氧原子数为:(154-122)÷16=2。故氧化物的化学式为 O 。
2
16【. 答案】(1)球形干燥管(1分) D→C→E→B (2)2Mn +16H++10 =2Mn2++5Cl ↑+8H O
2 2
Sb
(3)抑制Co2+水解,提供Cl-形成配合物 − −
O4 Cl
(4)防止温度过高使 和 分解,减慢(控制)反应速率
活性炭
(5) H2O2 NH3⋅H2O
(6)2CCoCl2+2NH4Cl+10N%H3⋅H2O+H2O2 2 Co NH3 6 Cl3+12H2O
【详解】(6)26 A .75 . ( 滴 1定− 管2)使用前未用待测液 6 润 0 洗 ℃ ,导致KSCN标准溶液浓度偏高,因此标准液消
3
耗的体积V 偏小,计算所得纯度偏高;
2
B. 滴定前锥形瓶未干燥,不影响所消耗的标准液体积,故不影响计算纯度。
C. 硝基苯密度大于水,因此可以覆盖第一步生成的AgCl沉淀,防止滴定时与KSCN反应发生沉
淀转化。当未加入硝基苯时,AgCl沉淀可与KSCN反应发生沉淀转化,导致V 偏大,计算所得
2
纯度偏低;
由于AgNO 标准溶液先后与样品和KSCN反应,因此根据关系式: ~3AgNO 、
3 3
KSCN~AgNO ,可计算出 的物质的量为 ×10-3mol,因此样品的纯度为:
3 Co NH3 6 Cl3
( 1− 2)
×100%= Co NH3 6 C%l3。 3
−3
267.5( 1− 2)×10 26.75( 1− 2)
17. 【答案】(1)① ②该反应为气体分子数增大的反应,通入水蒸气可增大
3 3
容器体积减小体系分压,有利于反应正向进行,提高丁二烯的产率
(2) ①<(1分)
C4H
②
8
温
g
度
+
升
H
高
2
速
g
率加快,转化率增大;温度过高催化剂活性下降,速率减小,
转化率下降(或较高温度下反应已达平衡,由于反应放热,升高温度平衡逆向移动,转化率下降)
丁二烯产率下降,碳的氧化物产率上升(1分)
(3)10:3 (4)Fe O
2 3
320
3 3 2 −21
2 a c⋅10 ⋅ A【分析】白球表示的O原子作六方最密堆积,均摊为: ,灰色球表示的Fe
原子有序地填充在部分八面体空隙中,均摊为4个,据此回答1。1
12×6+2×2+3= 6
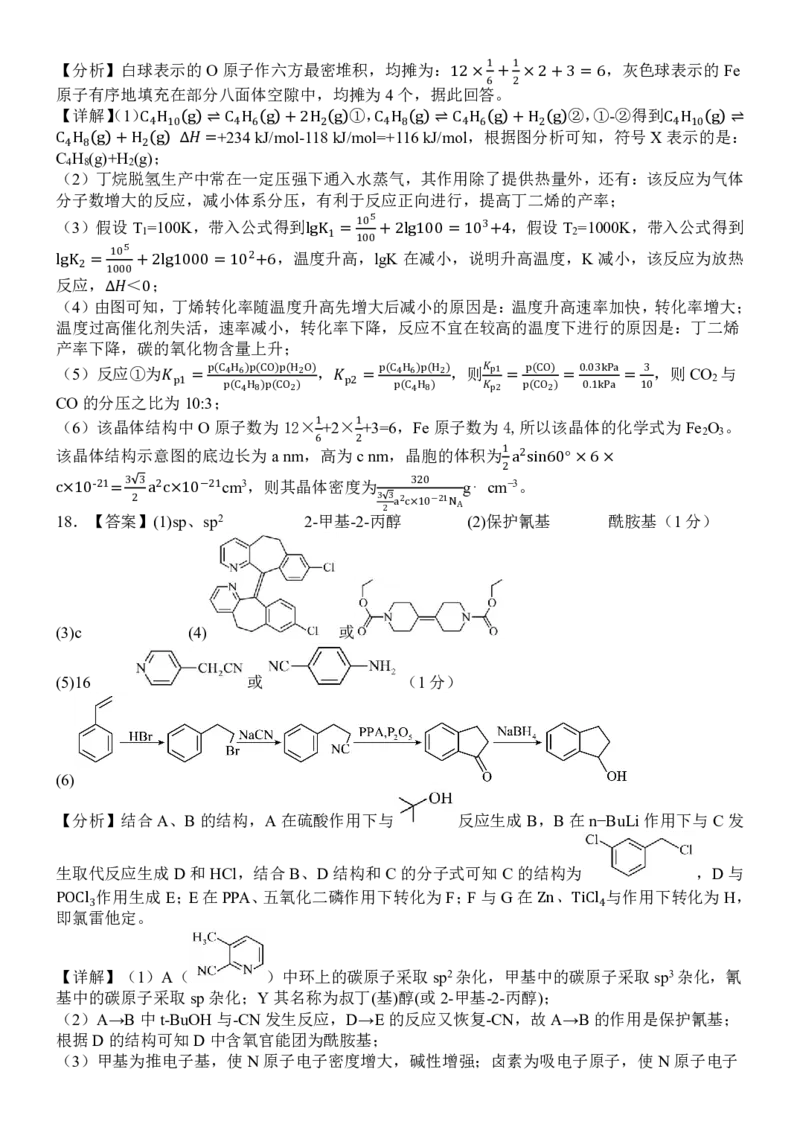
【详解】(1) ①, ②,①-②得到
+234kJ/mol-118kJ/mol=+116kJ/mol,根据图分析可知,符号X表示的是:
C4H10 g ⇌C4H6 g +2H2 g C4H8 g ⇌C4H6 g +H2 g C4H10 g ⇌
C H (g)+H (g);
4 8 2
C4H8 g +H2 g Δ =
(2)丁烷脱氢生产中常在一定压强下通入水蒸气,其作用除了提供热量外,还有:该反应为气体
分子数增大的反应,减小体系分压,有利于反应正向进行,提高丁二烯的产率;
(3)假设T =100K,带入公式得到 ,假设T =1000K,带入公式得到
1 2
5
10 3
,温 l 度 gK 升1 = 高 1 , 00 lg+K2 在 lg1 减 00 小 = , 1 说 0 明 + 升 4 高温度,K减小,该反应为放热
5
反应, 10 < ; 2
lgK2 =1000+2lg1000 =10 +6
(4)由图可知,丁烯转化率随温度升高先增大后减小的原因是:温度升高速率加快,转化率增大;
温度过高Δ 催化0剂失活,速率减小,转化率下降,反应不宜在较高的温度下进行的原因是:丁二烯
产率下降,碳的氧化物含量上升;
(5)反应①为 , ,则 ,则CO 与
2
p(C4H6)p(CO)p(H2O) p(C4H6)p(H2) p1 p(CO) 0.03kPa 3
CO的分压之比 为 p11 = 0:3; p(C4H8)p(CO2) p2 = p(C4H8) p2 =p(CO2)= 0.1kPa =10
(6)该晶体结构中O原子数为12× +2× +3=6,Fe原子数为4,所以该晶体的化学式为Fe O 。
2 3
1 1
该晶体结构示意图的底边长为anm,高为cnm,晶胞的体积为
6 2
1 2
cm3,则其晶体密度为 g⋅ cm 2 − a 3。 sin60°×6×
-21 3 3 2 −21 320
c1×8.10【答=案2】a(1c)×sp1、0sp2 2-甲基-2-丙3
2
醇3
a
2
c×10
−21
NA
(2)保护氰基 酰胺基(1分)
(3)c (4) 或
(5)16 或 (1分)
(6)
【分析】结合A、B的结构,A在硫酸作用下与 反应生成B,B在n−BuLi作用下与C发
生取代反应生成D和HCl,结合B、D结构和C的分子式可知C的结构为 ,D与
作用生成E;E在PPA、五氧化二磷作用下转化为F;F与G在 、 与作用下转化为H,
即氯雷他定。
POCl3 Zn TiCl4
【详解】(1)A( )中环上的碳原子采取sp2杂化,甲基中的碳原子采取sp3杂化,氰
基中的碳原子采取sp杂化;Y其名称为叔丁(基)醇(或2-甲基-2-丙醇);
(2)A→B中t-BuOH与-CN发生反应,D→E的反应又恢复-CN,故A→B的作用是保护氰基;
根据D的结构可知D中含氧官能团为酰胺基;
(3)甲基为推电子基,使N原子电子密度增大,碱性增强;卤素为吸电子原子,使N原子电子密度减小,碱性减弱;氟的电负性大于氯,因此碱性最弱的是c;
(4)由题意知该反应是醛或酮偶联成为烯烃的反应,则可能的副产物为 或
;
(5)同分异构体分两类:第1类:含苯环结构。取代基可能是-NHCN(1种);-NH 、-CN(3种)。
2
第2类:含吡啶环( )结构。①含1个取代基:-CH CN(3种);②含2个取代基: 、
2
、 再取代甲基:(a)有3种(除本身外);(b)有4种;(c)有2种;符合条件的
同分异构体有16种;其中,在核磁共振氢谱上有三组峰且峰的面积比为1:1:1,符合条件的结
构简式为 或 ;
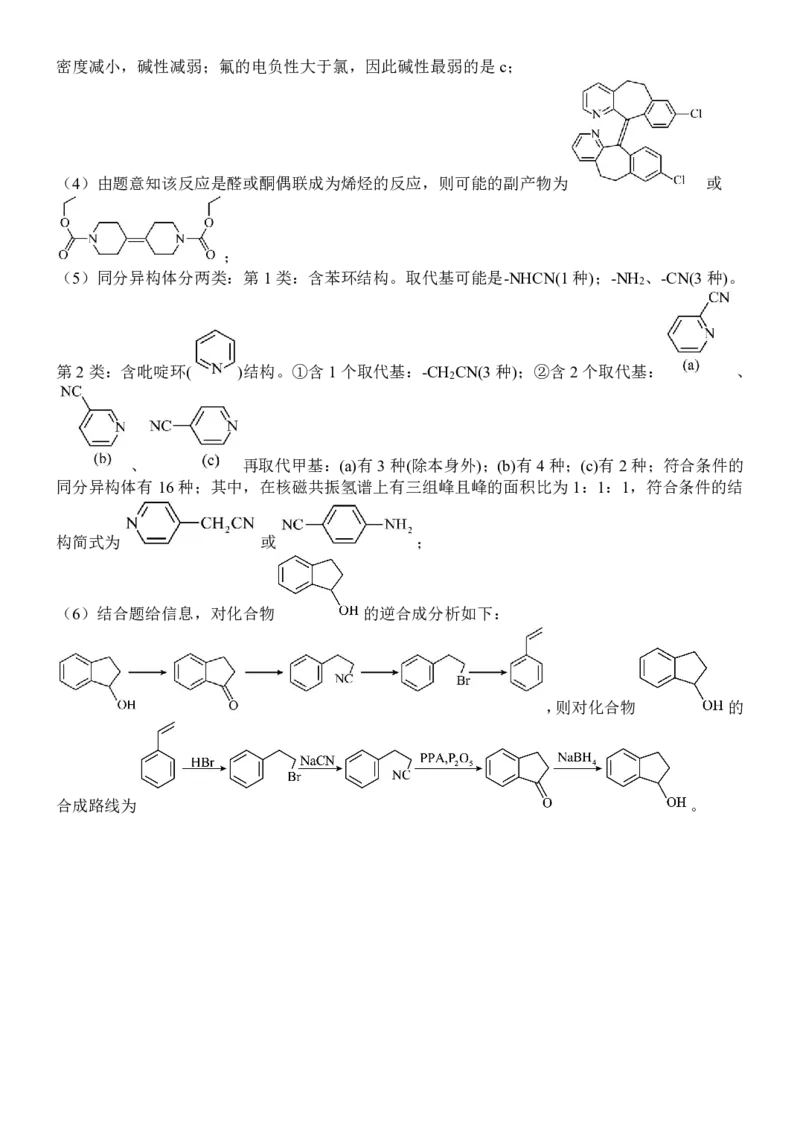
(6)结合题给信息,对化合物 的逆合成分析如下:
,则对化合物 的
合成路线为 。