文档内容
B.①中用NaOH作强碱性介质
长春外国语学校 2023-2024 学年第一学期第一次月考高三年级
C.②中K MnO 只体现氧化性
2 4
化学试卷
D.MnO
2
转化为KMnO
4
的理论转化率约为66.7%
4.某白色粉末样品,可能含有Na SO 、Na SO 、Na S O 和Na CO 。取少量样品进
出题人:王丽秋 审题人:杨春娜 2 4 2 3 2 2 3 2 3
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共8页。考试结束后, 行如下实验:
将答题卡交回。 ①溶于水,得到无色透明溶液
注意事项: ②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
1.答题前,考生先将自己的姓名、准考证号填写清楚,将条形码准确粘贴在考生信 ③取②的上层清液,向其中滴加BaCl 溶液有沉淀生成。
2
息条形码粘贴区。 该样品中确定存在的是( )
2.选择题必须使用2B铅笔填涂;非选择题必须使用0.5毫米黑色字迹的签字笔书
A.Na SO、Na S O B.Na SO、Na S O
写,字体工整、笔迹清楚。 2 4 2 2 3 2 3 2 2 3
3.请按照题号顺序在各题目的答题区域内作答,超出答题区域书写的答案无效;
B.C.Na SO、Na CO D.Na SO、Na CO
在草稿纸、试题卷上答题无效。 2 4 2 3 2 3 2 3
4.作图可先使用铅笔画出,确定后必须用黑色字迹的签字笔描黑。 5.下列实验现象描述及有关离子方程式书写都合理的是
5.保持卡面清洁,不要折叠,不要弄破、弄皱,不准使用涂改液、修正带、刮纸刀。
A.向Ba(OH) 溶液中加入NaHSO 至溶液呈中性的离子方程式:
可能用到的相对原子质量:H-1 D-2 C-12 O-16 Mn-55 2 4
第Ⅰ卷 Ba2 OHH SO2 BaSO H O
4 4 2
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只
B.向含有淀粉的FeNO 溶液中滴入HI溶液,溶液变为蓝色:
有一项是符合题目要求的。 3 2
1.我国提出争取在2030年前实现碳达峰,2060年实现碳中和,这对于改善环境,实现
2Fe3 2I 2Fe2 I
绿色发展至关重要。碳中和是指CO 的排放总量和减少总量相当。下列措施中能促进 2
2
碳中和最直接有效的是( )
C.向Na SO :Na S1:2的溶液中滴加稀盐酸:SO22S26H 3S3H O
A.将重质油裂解为轻质油作为燃料 2 3 2 3 2
B.大规模开采可燃冰作为新能源
电解
C.通过清洁煤技术减少煤燃烧污染 D.用铁作电极电解饱和食盐水:2Cl2H O Cl H 2OH
2 2 2
D.研发催化剂将CO 还原为甲醇
2
2.关于反应Na S O +H SO =Na SO +S+SO +H O,下列说法正确的是( )
2 2 3 2 4 2 4 2 2 6.KIO 常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步反应为
A.H SO 发生还原反应 3
2 4
B.Na S O 既是氧化剂又是还原剂 Δ
2 2 3 6I +11KClO +3H O 6KH IO +5KCl+3Cl 。下列说法错误的是( )
C.氧化产物与还原产物的物质的量之比为2∶1 2 3 2 3 2 2
D.1mol Na S O 发生反应,转移4mol电子 A.产生22.4L(标准状况)Cl 时,反应中转移10mole
2 2 3 2
3.实验室制备KMnO 过程为:①高温下在熔融强碱性介质中用KClO 氧化MnO 制备 B.反应中氧化剂和还原剂的物质的量之比为11:6
4 3 2
K MnO ;②水溶后冷却,调溶液pH至弱碱性,K MnO 歧化生成KMnO 和MnO ; C.可用石灰乳吸收反应产生的Cl 制备漂白粉
2 4 2 4 4 2 2
③减压过滤,将滤液蒸发浓缩、冷却结晶,再减压过滤得KMnO 。下列说法正确的是 D.可用酸化的淀粉碘化钾溶液检验食盐中IO的存在
4 3
( ) 7.设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.①中用瓷坩埚作反应器A.在25℃时,1LpH为12的Ba(OH) 2 溶液中含有OH-数目为0.01N A 编
实验目的 实验过程
B.1.8g重水(D O)中所含质子数为N 号
2 A
C.足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 A
A 检验溶液是否含有SO2 取少量该溶液,依次加入稀硝酸和 BaCl 溶液
4 2
D.32g甲醇的分子中含有C—H键的数目为4N
A
8.LiBr溶液可作为替代氟利昂的绿色制冷剂。合成LiBr工艺流程如下:
探究维生素 C 的还原 向盛有2mL 黄色氯化铁溶液的试管中滴加浓的维生素
B
性 C 溶液,观察颜色变化
向稀盐酸中加入锌粒,将生成的气体依次通过浓硫酸、
C 制取干燥纯净的氢气
NaOH 溶液,然后收集
D 制备 Fe(OH) 胶体 将NaOH 浓溶液滴加到饱和 FeCl 溶液中
3 3
下列说法错误的是( )
A.还原工序逸出的Br 用NaOH溶液吸收,吸收液直接返回还原工序 12.下列实验操作或装置能达到目的的是( )
2
B.除杂工序中产生的滤渣可用煤油进行组分分离 A B C D
C.中和工序中的化学反应为Li CO +2HBr=CO +2LiBr+H O
2 3 2 2
D.参与反应的nBr :n(BaS):nH SO 为1∶1∶1
2 2 4
9.阿莫西林是种最常用的抗生素,其结构如图所示。下列说法错误的是( )
A.1mol阿莫西林最多消耗5molH
2
B.1mol阿莫西林最多消耗4molNaOH
混合浓硫酸和乙 配制一定浓度的溶 证明乙炔可使溴水褪
收集NO 气体
C.阿莫西林分子中含有4个手性碳原子 醇 液 2 色
D.阿莫西林能发生取代、加成、氧化、缩聚等反应
13.X、Y、Z、W四种主族元素,原子序数依次增大,且均不大于20,四种元素核电荷
10.利用如图所示的装置(夹持及加热装置略)制备高纯白磷的流程如下:
数之和为46,X、Y两种元素能够形成两种化合物,其中一种化合物被称为生命的源
泉。Z元素是一种重要的“成盐元素”,其形成的一种盐在海水中含量最高,其单质通
下列操作错误的是( ) 过电解该盐溶液获得。下列关于四种元素说法错误的是( )
A.X Y 、ZY 、 W(ZY) 均是常见的杀菌消毒剂,三者作用原理相同
2 2 2 2
A.红磷使用前洗涤以除去表面杂质
B.WX 中X元素的检验方法可以将WX 固体置于氧气流中灼烧并将产物通过无水硫酸
2 2
B.将红磷转入装置,抽真空后加热外管以去除水和氧气
铜
C.从a口通入冷凝水,升温使红磷转化
C.WZ 、WY 两种化合物中阴阳离子个数比均为1 : 2
2 2
D.冷凝管外壁出现白磷,冷却后在氮气氛围下收集
D.可以通过XZY、ZY 等物质中的元素化合价来比较Y、Z两种元素的非金属性强弱
2
14.如图,某课题组设计了一种以 为原料固定CO 的方法。下列说法不正确的
2
是( )
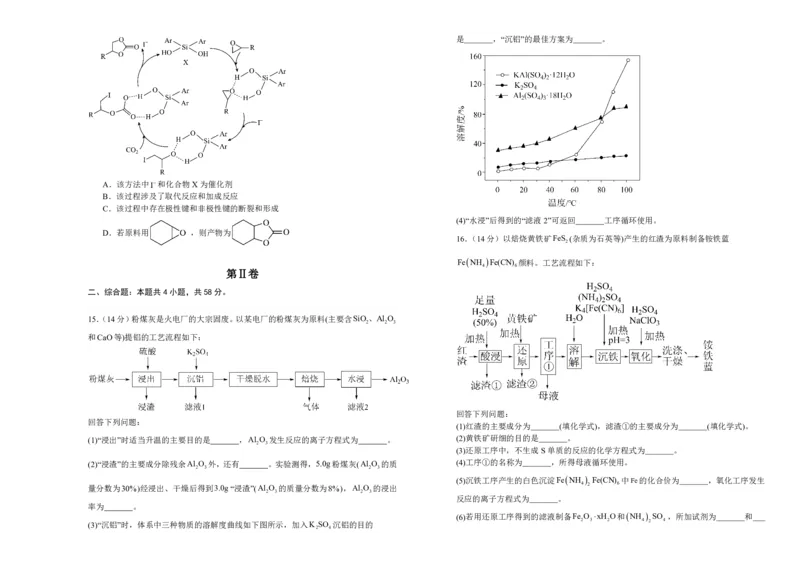
11.下列实验过程可以达到实验目的的是( )是 ,“沉铝”的最佳方案为 。
A.该方法中I和化合物X为催化剂
B.该过程涉及了取代反应和加成反应
C.该过程中存在极性键和非极性键的断裂和形成
(4)“水浸”后得到的“滤液2”可返回 工序循环使用。
D.若原料用 ,则产物为
16.(14分)以焙烧黄铁矿FeS (杂质为石英等)产生的红渣为原料制备铵铁蓝
2
FeNH Fe(CN) 颜料。工艺流程如下:
4 6
第Ⅱ卷
二、综合题:本题共4小题,共58分。
15.(14分)粉煤灰是火电厂的大宗固废。以某电厂的粉煤灰为原料(主要含SiO、Al O
2 2 3
和CaO等)提铝的工艺流程如下:
回答下列问题:
回答下列问题:
(1)红渣的主要成分为 (填化学式),滤渣①的主要成分为 (填化学式)。
(1)“浸出”时适当升温的主要目的是 ,Al O 发生反应的离子方程式为 。 (2)黄铁矿研细的目的是 。
2 3
(3)还原工序中,不生成S单质的反应的化学方程式为 。
(2)“浸渣”的主要成分除残余Al O 外,还有 。实验测得,5.0g粉煤灰(Al O 的质 (4)工序①的名称为 ,所得母液循环使用。
2 3 2 3
(5)沉铁工序产生的白色沉淀FeNH Fe(CN) 中Fe的化合价为 ,氧化工序发生
量分数为30%)经浸出、干燥后得到3.0g“浸渣”(Al O 的质量分数为8%),Al O 的浸出 4 2 6
2 3 2 3
反应的离子方程式为 。
率为 。
(6)若用还原工序得到的滤液制备Fe O xH O和NH SO ,所加试剂为 和
(3)“沉铝”时,体系中三种物质的溶解度曲线如下图所示,加入K SO 沉铝的目的 2 3 2 4 2 4
2 4(填化学式,不引入杂质)
的合成路线(部分反应条件略去)如图所示。
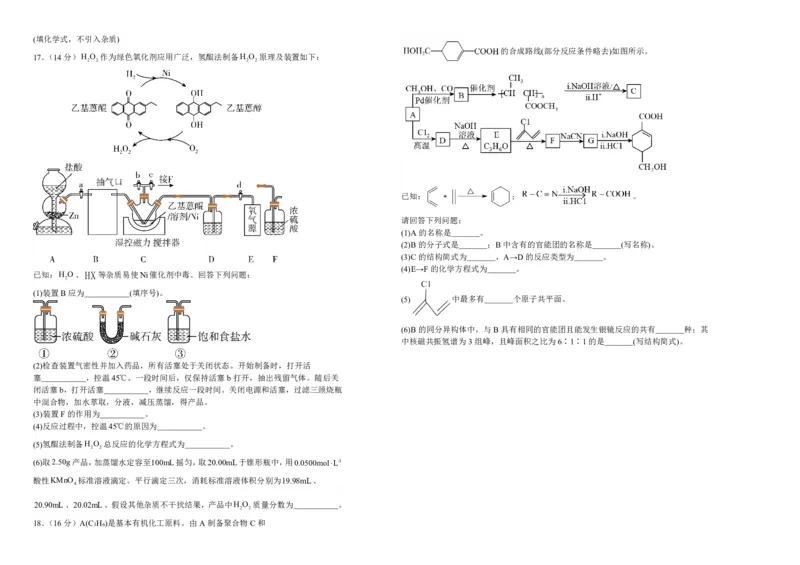
17.(14分)H O 作为绿色氧化剂应用广泛,氢醌法制备H O 原理及装置如下:
2 2 2 2
已知: ; 。
请回答下列问题:
(1)A的名称是 。
(2)B的分子式是 ;B中含有的官能团的名称是 (写名称)。
(3)C的结构简式为 ,A→D的反应类型为 。
(4)E→F的化学方程式为 。
已知:H O、HX等杂质易使Ni催化剂中毒。回答下列问题:
2
(1)装置B应为 (填序号)。
(5) 中最多有 个原子共平面。
(6)B的同分异构体中,与B具有相同的官能团且能发生银镜反应的共有 种;其
中核磁共振氢谱为3组峰,且峰面积之比为6∶1∶1的是 (写结构简式)。
(2)检查装置气密性并加入药品,所有活塞处于关闭状态。开始制备时,打开活
塞 ,控温45℃。一段时间后,仅保持活塞b打开,抽出残留气体。随后关
闭活塞b,打开活塞 ,继续反应一段时间。关闭电源和活塞,过滤三颈烧瓶
中混合物,加水萃取,分液,减压蒸馏,得产品。
(3)装置F的作用为 。
(4)反应过程中,控温45℃的原因为 。
(5)氢醌法制备H O 总反应的化学方程式为 。
2 2
(6)取2.50g产品,加蒸馏水定容至100mL摇匀,取20.00mL于锥形瓶中,用0.0500molL-1
酸性KMnO 标准溶液滴定。平行滴定三次,消耗标准溶液体积分别为19.98mL、
4
20.90mL、20.02mL。假设其他杂质不干扰结果,产品中H O 质量分数为 。
2 2
18.(16分)A(C H )是基本有机化工原料。由A制备聚合物C和
3 6答案 (2) C H O 碳碳双键、酯基
5 8 2
第Ⅰ卷
(3) 取代反应(或水解反应)
一、选择题
(4)
1-5 DBDAC 6-10 AAAAC 11-14 BBCC
第Ⅱ卷 (5)10
二、综合题
(6) 8
15.(1) 提高浸出率(或提高浸出速率) Al O 6H 2Al3 3H O
2 3 2
(2) SiO 和CaSO 84%
2 4
(3) 使更多的铝元素转化为晶体析出,同时保证晶体纯度 高温溶解再冷却结晶
(4)沉铝
16.(1) Fe O SiO
2 3 2
(2)增大固液接触面积,加快反应速率,提高黄铁矿的利用率
(3)7Fe (SO ) +FeS +8H O=15FeSO +8H SO
2 4 3 2 2 4 2 4
(4)蒸发浓缩、冷却结晶、过滤洗涤
(5) +2; 6Fe(NH
4
)
2
Fe(CN)
6
+ClO
3
+6H+=6Fe(NH
4
)Fe(CN)
6
+3H
2
O+Cl-+6NH+
4
(6) H O NH ·H O
2 2 3 2
17.(1)②或③①
(2) a、c c、d
(3)防止外界水蒸气进入C中使催化剂中毒
(4)适当升温加快反应速率,同时防止温度过高H O 分解
2 2
Ni
(5)H +O H O
2 2乙基蒽醌 2 2
(6)17%
18.(1)丙烯