文档内容
2024 北京朝阳高三一模
化 学
2024.3
(考试时间 90分钟 满分100分)
可能用到的相对原子质量:H 1 B 11 C 12 N 14 O 16 Na 23 Mn 55 Fe 56
第一部分
本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的一项。
1.最近,中国科学家成功采用“变压吸附+膜分离+精制纯化”方法成功分离氢氦制得高纯氦。下列说法不
.
正确的是
..
A.H的第一电离能小于He的
B.H 分子间存在共价键,He分子间存在范德华力
2
C.也可以利用沸点不同对H 和He进行分离
2
D.利用原子光谱可以鉴定He元素和H元素
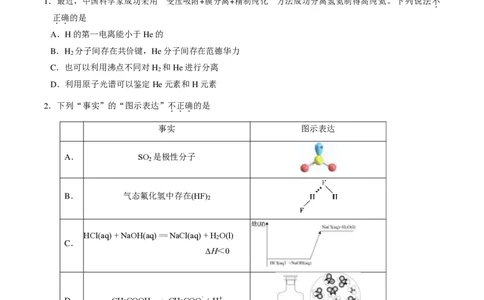
2.下列“事实”的“图示表达”不正确的是
...
事实 图示表达
A. SO 是极性分子
2
B. 气态氟化氢中存在(HF)
2
HCl(aq) + NaOH(aq) == NaCl(aq) + H O(l)
2
C.
<
D. CH COOH CH COO- + H+
3 3
3.下列比较正确的是
A.离子半径:S2- > Cl- > K+ B.键角:CH < NH PH > HF D.酸性:HNO < H PO < H SiO
3 3 3 3 4 2 3
4.下列事实与水解反应无关的是
..
第1页/共12页A.油脂在碱性溶液中进行皂化反应
B.葡萄糖与银氨溶液发生银镜反应
C.核酸在酶的作用下转化为核苷和磷酸
D.四氯化钛与大量水在加热条件下制备二氧化钛
5.下列方程式与所给事实不相符的是
...
A.Al溶于NaOH溶液产生无色气体:2Al + 2OH- + 2H O == 2AlO - + 3H ↑
2 2 2
B.用CuSO
4
溶液除去乙炔中的H
2
S产生黑色沉淀:Cu2+ + S2- == CuS↓
C.Fe(OH) 在空气中放置最终变为红褐色:4Fe(OH) + O + 2H O == 4Fe(OH)
2 2 2 2 3
D.乙醛与新制的Cu(OH) 在加热条件下产生砖红色沉淀:
2
CH CHO + 2Cu(OH) + NaOH
→△
C H COONa + Cu O↓+ 3H O
3 2 3 2 2
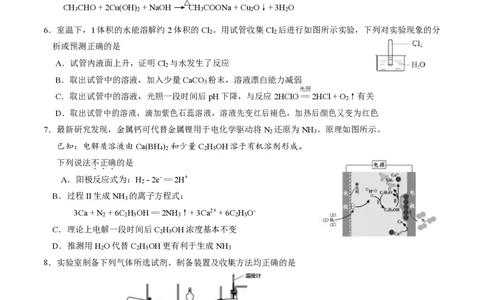
6.室温下,1体积的水能溶解约2体积的Cl 。用试管收集Cl 后进行如图所示实验,下列对实验现象的分
2 2
析或预测正确的是
A.试管内液面上升,证明Cl 与水发生了反应
2
B.取出试管中的溶液,加入少量CaCO 粉末,溶液漂白能力减弱
3
光照
C.取出试管中的溶液,光照一段时间后pH下降,与反应2HClO == 2HCl + O ↑有关
2
D.取出试管中的溶液,滴加紫色石蕊溶液,溶液先变红后褪色,加热后颜色又变为红色
7.最新研究发现,金属钙可代替金属锂用于电化学驱动将N 还原为NH 。原理如图所示。
2 3
已知:电解质溶液由Ca(BH ) 和少量C H OH溶于有机溶剂形成。
4 2 2 5
下列说法不正确的是
...
A.阳极反应式为:H - 2e- == 2H+
2
B.过程II生成NH 的离子方程式:
3
3Ca + N + 6C H OH == 2NH ↑+ 3Ca2+ + 6C H O-
2 2 5 3 2 5
C.理论上电解一段时间后C H OH浓度基本不变
2 5
D.推测用H O代替C H OH更有利于生成NH
2 2 5 3
8.实验室制备下列气体所选试剂、制备装置及收集方法均正确的是
气体 试剂 制备装 收集方
A. CH 2 =CH 2 C 2 H 5 OH + 浓硫酸 置 c 法 f
B. NH
3
NH
4
Cl a e
C. CO 2 石灰石 + 稀硫酸 b d
第2页/共12页D. NO 2 Cu + 浓硝酸 b f
9.研究人员提出利用热化学硫碘循环实现硫化氢分解联产氢气和硫黄,转化过程如下,其中 Y、Z代表 I
2
或HI中的一种。下列说法不正确的是
...
A.Y在Z溶液中比在H SO 溶液中易溶
2 4
B.反应I中X的浓度与硫黄的产率无关
C.反应Ⅱ的化学方程式为 SO + 2H O + I == H SO + 2HI
2 2 2 2 4
D.等压条件下,反应Ⅰ、Ⅱ、Ⅲ的反应热之和等于硫化氢直接分解的反应热
10.某同学进行如下实验:
① 将H O 溶液与KI溶液混合,产生大量气泡,溶液颜色变黄;
2 2
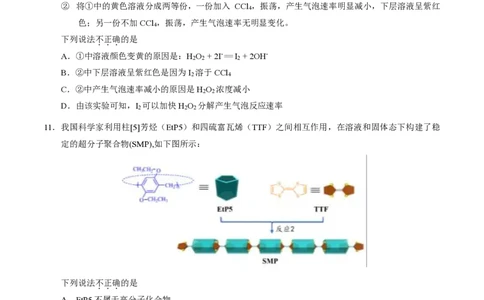
② 将①中的黄色溶液分成两等份,一份加入 CCl ,振荡,产生气泡速率明显减小,下层溶液呈紫红
4
色;另一份不加CCl ,振荡,产生气泡速率无明显变化。
4
下列说法不正确的是
...
A.①中溶液颜色变黄的原因是:H O + 2I- == I + 2OH-
2 2 2
B.②中下层溶液呈紫红色是因为I 溶于CCl
2 4
C.②中产生气泡速率减小的原因是H O 浓度减小
2 2
D.由该实验可知,I 可以加快H O 分解产生气泡反应速率
2 2 2
11.我国科学家利用柱[5]芳烃(EtP5)和四硫富瓦烯(TTF)之间相互作用,在溶液和固体态下构建了稳
定的超分子聚合物(SMP),如下图所示:
SMP
下列说法不正确的是
...
A.EtP5不属于高分子化合物
B.TTF的核磁共振氢谱中含有1组峰
C.EtP5和TTF可通过分子间作用力自组装得到SMP
D.若用EtP10替换 EtP5可形成更稳定的SMP
12.常温下,用0.20 mol·L-1盐酸滴定25.00 mL 0.20 mol·L-1 NH ·H O溶
3 2
液,所得溶液的pH、NH +和NH ·H O的物质的量分数(x)与滴加盐
4 3 2
酸体积的关系如图所示。
下列说法不正确的是
...
第3页/共12页A.曲线①代表x(NH ·H O)
3 2
B.当溶液显中性时,滴入盐酸的体积小于25.00 mL
C.NH ·H O的电离常数约为1×10-9.26
3 2
D.a点的溶液中存在c(NH +)=c(NH ·H O)>c (Cl-)
4 3 2
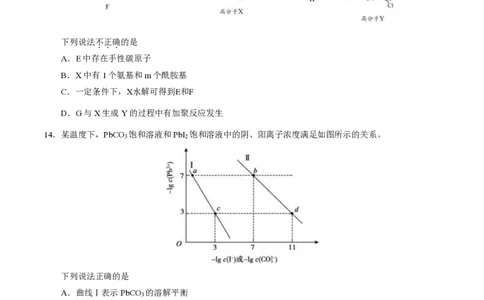
13.高分子Y是一种人工合成的温敏性聚肽高分子,其合成路线如下:
H
H
下列说法不正确的是
...
A.E中存在手性碳原子
B.X中有1个氨基和m个酰胺基
C.一定条件下,X水解可得到E和F
D.G与X生成Y的过程中有加聚反应发生
14.某温度下,PbCO 饱和溶液和 PbI 饱和溶液中的阴、阳离子浓度满足如图所示的关系。
3 2
下列说法正确的是
A.曲线Ⅰ表示PbCO 的溶解平衡
3
B.该温度下K (PbI ) : K (PbCO ) =108
sp 2 sp 3
C.曲线Ⅱ上的b 点可通过改变温度移动至d 点
D.向PbI 的悬浊液中加入Na CO 浓溶液,可以将其转化成PbCO
2 2 3 3
第二部分
本部分共5题,共58分。
15.(10分)硼及其化合物在科研、工业等方面有许多用途。
(1)基态B原子价层电子排布式是 。
第4页/共12页(2)六方氮化硼晶体也被称为“白石墨”,具有和石墨晶体相似的层状结构,如图所示。
① 比较B和N的电负性大小,并从原子结构角度说明理由: 。
② 分析六方氮化硼晶体层间是否存在化学键并说明依据: 。
(3)氮化硼量子点(粒径大小为2~10 nm)可用于检测金属离子,如Fe2+或Fe3+的检测原理如下图。
① 图2所示的微粒中Fe与O之间存在的相互作用力类型为 。
② n = (填数字)。
(4)NaBH 是一种重要的储氢材料,其晶胞结构由I、II
4
两部分组成,如图所示。
① I不是晶胞,从结构角度说明原因: 。
② 已知阿伏加德罗常数为N ,该晶体的密度
A
为 g·cm-3 。(1 nm =10- 7 cm)
16.(12分)CO 再生为“零碳甲醇”是实现碳中和的一种方式。
2
(1)CO 催化加氢可生成甲醇。
2
已知:i. 2H (g) + O (g) == 2H O (g) ΔH = a kJ·mol-1
2 2 2
ii. 2CH OH(g) + 3O (g) 2CO (g) + 4H O(g) ΔH= b kJ·mol-1
3 2 2 2
① CO 和H 生成CH OH和H O的热化学方程式是 。
2 2 3 2
② 合成过程中选择高压条件的原因: 。
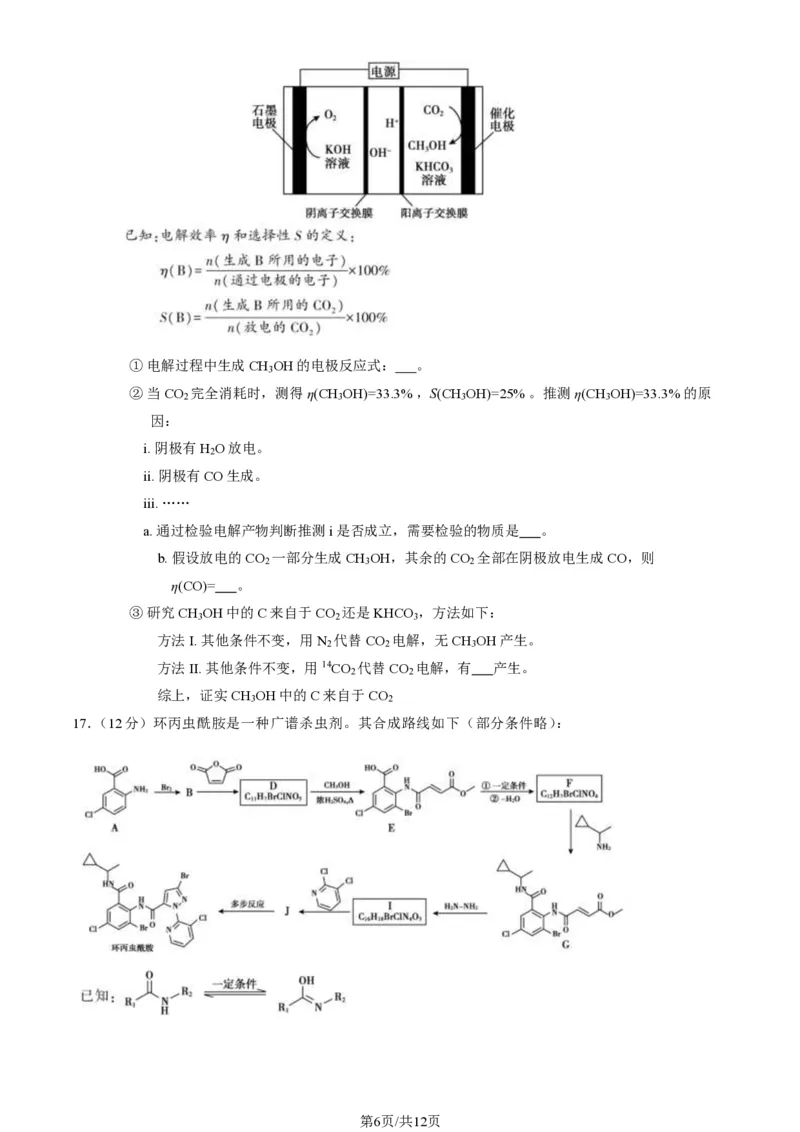
(2)电解还原法将CO 转化为甲醇的装置如图。
2
第5页/共12页① 电解过程中生成CH OH的电极反应式: 。
3
② 当CO 完全消耗时,测得η(CH OH)=33.3% ,S(CH OH)=25% 。推测η(CH OH)=33.3% 的原
2 3 3 3
因:
i. 阴极有H O放电。
2
ii. 阴极有CO生成。
iii. ……
a. 通过检验电解产物判断推测i是否成立,需要检验的物质是 。
b. 假设放电的CO 一部分生成CH OH,其余的CO 全部在阴极放电生成CO,则
2 3 2
η(CO)= 。
③ 研究CH OH中的C来自于CO 还是KHCO ,方法如下:
3 2 3
方法I. 其他条件不变,用N 代替CO 电解,无CH OH产生。
2 2 3
方法II. 其他条件不变,用14CO 代替CO 电解,有 产生。
2 2
综上,证实CH OH中的C来自于CO
3 2
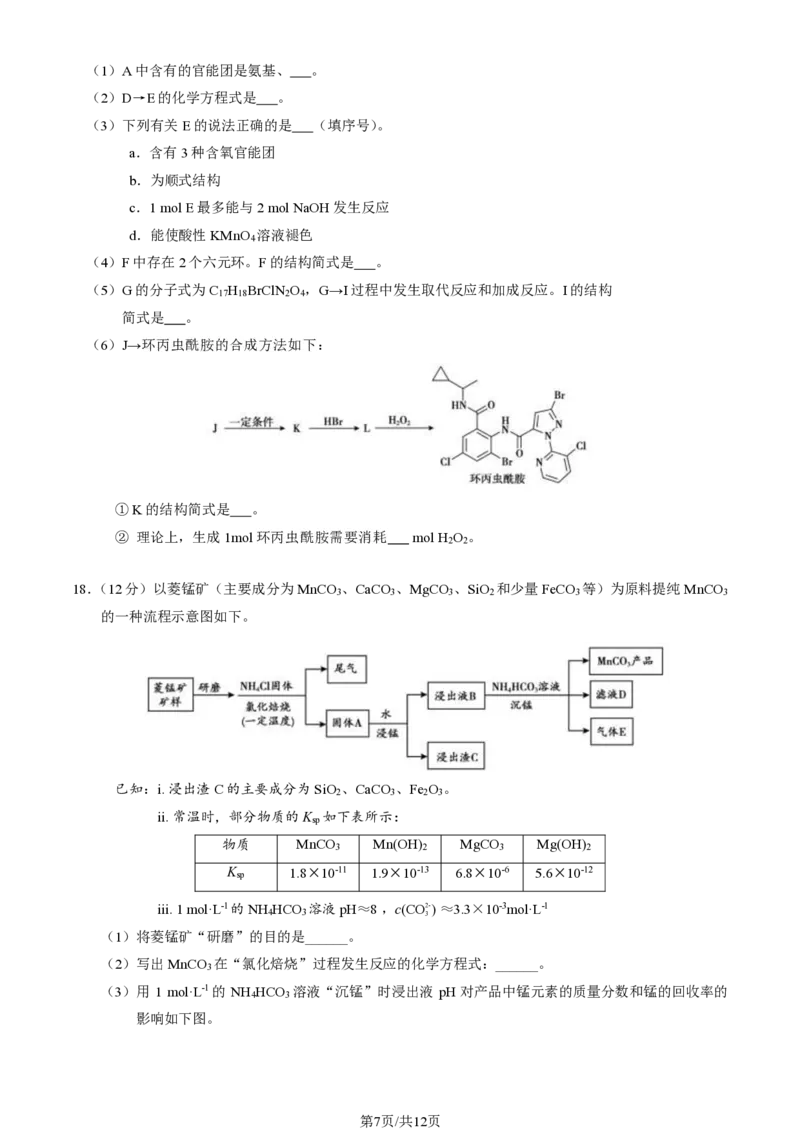
17.(12分)环丙虫酰胺是一种广谱杀虫剂。其合成路线如下(部分条件略):
第6页/共12页(1)A中含有的官能团是氨基、 。
(2)D→E的化学方程式是 。
(3)下列有关E的说法正确的是 (填序号)。
a.含有3种含氧官能团
b.为顺式结构
c.1 mol E最多能与2 mol NaOH 发生反应
d.能使酸性KMnO 溶液褪色
4
(4)F中存在2个六元环。F的结构简式是 。
(5)G的分子式为C H BrClN O ,G→I过程中发生取代反应和加成反应。I的结构
17 18 2 4
简式是 。
(6)J→环丙虫酰胺的合成方法如下:
① K的结构简式是 。
② 理论上,生成1mol环丙虫酰胺需要消耗 mol H O 。
2 2
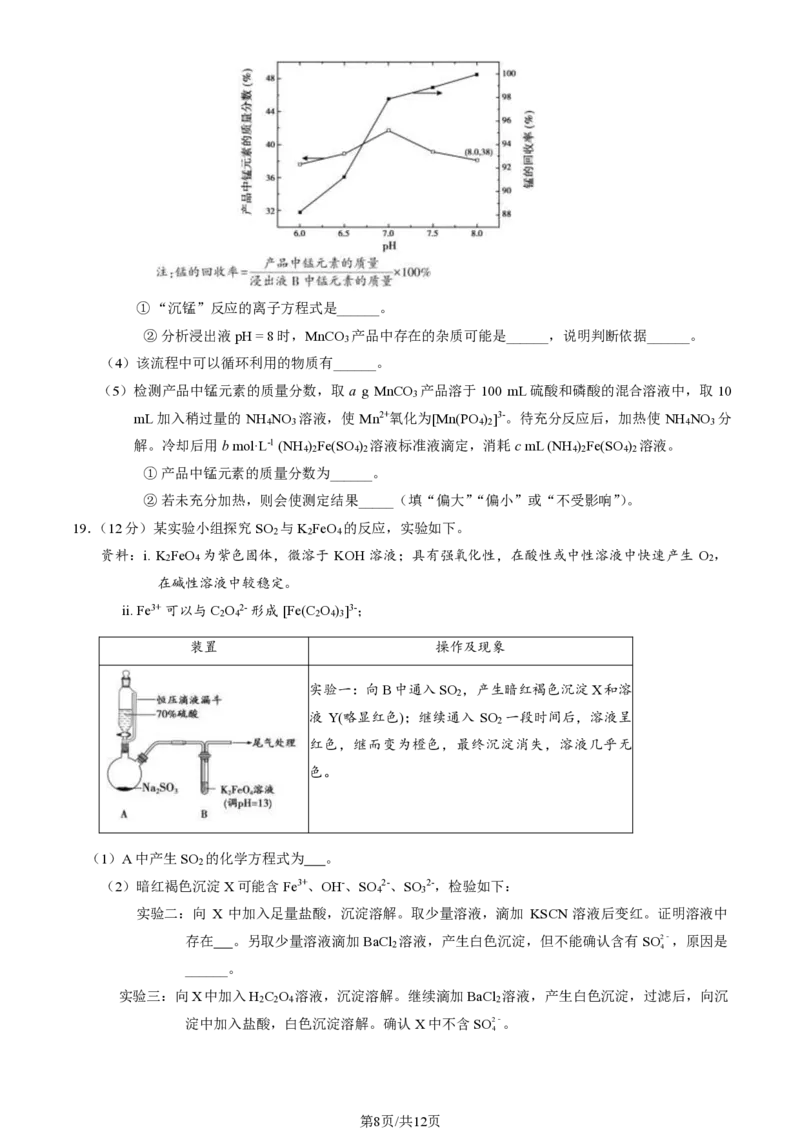
18.(12分)以菱锰矿(主要成分为MnCO 、CaCO 、MgCO 、SiO 和少量FeCO 等)为原料提纯MnCO
3 3 3 2 3 3
的一种流程示意图如下。
已知:i. 浸出渣C的主要成分为SiO 、CaCO 、Fe O 。
2 3 2 3
ii. 常温时,部分物质的K 如下表所示:
sp
物质 MnCO
3
Mn(OH)
2
MgCO
3
Mg(OH)
2
K
sp
1.8×10-11 1.9×10-13 6.8×10-6 5.6×10-12
iii. 1 mol·L-1的NH HCO 溶液pH≈8 ,c(CO2- ) ≈3.3×10-3mol·L-1
4 3 3
(1)将菱锰矿“研磨”的目的是______。
(2)写出MnCO 在“氯化焙烧”过程发生反应的化学方程式:______。
3
(3)用 1 mol·L-1的 NH HCO 溶液“沉锰”时浸出液 pH对产品中锰元素的质量分数和锰的回收率的
4 3
影响如下图。
第7页/共12页① “沉锰”反应的离子方程式是______。
② 分析浸出液pH = 8时,MnCO 产品中存在的杂质可能是______,说明判断依据______。
3
(4)该流程中可以循环利用的物质有______。
(5)检测产品中锰元素的质量分数,取 a g MnCO 产品溶于 100 mL硫酸和磷酸的混合溶液中,取 10
3
mL加入稍过量的 NH NO 溶液,使 Mn2+氧化为[Mn(PO ) ]3-。待充分反应后,加热使 NH NO 分
4 3 4 2 4 3
解。冷却后用b mol·L-1 (NH ) Fe(SO ) 溶液标准液滴定,消耗c mL (NH ) Fe(SO ) 溶液。
4 2 4 2 4 2 4 2
① 产品中锰元素的质量分数为______。
② 若未充分加热,则会使测定结果_____(填“偏大”“偏小”或“不受影响”)。
19.(12分)某实验小组探究SO 与K FeO 的反应,实验如下。
2 2 4
资料:i. K FeO 为紫色固体,微溶于 KOH 溶液;具有强氧化性,在酸性或中性溶液中快速产生 O ,
2 4 2
在碱性溶液中较稳定。
ii. Fe3+ 可以与C O 2- 形成 [Fe(C O ) ]3-;
2 4 2 4 3
装置 操作及现象
实验一:向B中通入SO ,产生暗红褐色沉淀X和溶
2
液 Y(略显红色);继续通入 SO 一段时间后,溶液呈
2
红色,继而变为橙色,最终沉淀消失,溶液几乎无
色。
(1)A中产生SO 的化学方程式为 。
2
(2)暗红褐色沉淀X可能含Fe3+、OH-、SO 2-、SO 2-,检验如下:
4 3
实验二:向 X 中加入足量盐酸,沉淀溶解。取少量溶液,滴加 KSCN 溶液后变红。证明溶液中
存在 。另取少量溶液滴加BaCl 溶液,产生白色沉淀,但不能确认含有SO2﹣,原因是
2 4
______。
实验三:向X中加入H C O 溶液,沉淀溶解。继续滴加BaCl 溶液,产生白色沉淀,过滤后,向沉
2 2 4 2
淀中加入盐酸,白色沉淀溶解。确认X中不含SO2﹣。
4
第8页/共12页实验三中用H C O 溶液溶解沉淀的目的是:______。
2 2 4
实验四:向 X中加入足量盐酸,沉淀溶解。加入几滴碘水(含淀粉),蓝色立即褪去。静置,一段
时间后蓝色复现,振荡,不褪色。
结合离子方程式解释沉淀溶解后的现象: 。
(3)查阅资料:a. Fe3+、SO2﹣、H O(或OH﹣)会形成配合物HOFeOSO 。
3 2 2
① 向溶液 Y中滴加 2滴 KSCN溶液,未见红色;再加几滴 6 mol·L-1盐酸,溶液变红。溶液 Y中存
在Fe(III),但直接滴加KSCN溶液未见红色的原因是_____。
② 取出部分实验一中的橙色溶液,久置不褪色。结合资料a中过程ii分析实验一中溶液最终“几乎无
色”的原因: 。
总结:SO 与K FeO 发生了氧化还原反应和复分解反应,并且遵循化学反应速率和限度规律。
2 2 4
第9页/共12页参考答案
第一部分
本部分共14小题,每小题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的一项。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 B C A B B C D A B C D C C D
第二部分
15.(10分)
(1)2s22p1
(2)① 电负性:B < N
B和N电子层数相同,核电核数 B<N,原子半径B>N,原子核对键合电子的吸引作用B<
N
② 层内B原子与N原子的核间距为145pm,层间距离为333pm,说明层间没有化学键相连
(3)① 配位键
② 3
(4)① I中8个顶角不完全相同,三套各两个平行面不完全相同
②
16.(12分)
(1)① CO (g) + 3H (g) CH OH(g) + H O(g) ΔH = (1.5a-0.5b) kJ·mol-1
2 2 3 2
② 加快反应速率,促进反应正向进行,提高甲醇的产率
(2)① CO + 6HCO- + 6e- == CH OH + H O + 6CO2-
2 3 3 2 3
(7CO + 6e- + 5H O == CH OH + 6HCO -)
2 2 3 3
② a. H
2
1
b. 33.3% (或 )
3
③ 14CH OH
3
17.(12分)
(1)羧基、碳氯键
(2)
(3)a、d
(4)
第10页/共12页(5)
(6)①
② 1
18.(12分)
(1)增大接触面积,加快反应速率,使反应充分进行
焙烧
(2)MnCO 3 + 2NH 4 Cl = = = = MnCl 2 + H 2 O + CO 2 ↑+ 2NH 3 ↑
(3)① Mn2+ + 2HCO - == MnCO ↓+ H O + CO ↑
3 3 2 2
② MgCO (其他合理给分);MnCO 和 Mn(OH) 中锰元素的质量分数均大于 38%,推知必有含
3 3 2
镁难溶杂质
(4)CO 、NH 、NH Cl
2 3 4
(5)①
② 偏大
19.(12分)
(1)Na SO + H SO == Na SO + H O + SO ↑
2 3 2 4 2 4 2 2
(2)实验二:Fe3+
Fe3+可能将+4价含硫物质氧化
实验三:H C O 溶液溶解沉淀并形成 [Fe(C O ) ]3-;使c(Fe3+)降低,氧化性减弱,不能将+4价含硫
2 2 4 2 4 3
物质氧化
实验四:反应i:SO + 2H O + I == H SO + 2HI
2 2 2 2 4
反应ii:2Fe3+ + 2I- == 2Fe2+ + I
2
(或反应ii:O + 4I- + 4H+ == 2I + 2H O)
2 2 2
反应i速率快于反应ii,当SO 消耗完全,I-被Fe3+或O 氧化为I
2 2 2
第11页/共12页(3)① Fe3+与SO2﹣、H O(或OH﹣)形成配合物的稳定性强于Fe(SCN)
3 2 3
② 持续通入SO 一段时间后,溶液酸性增强,生成的H SO 将橙色溶液中的HOFeOSO 氧化
2 2 5 2
第12页/共12页