文档内容
1.2.1 盖斯定律 练习(原卷版)
1.以下反应可表示获得乙醇并用作汽车燃料的过程,下列有关说法正确的是( )
6CO (g)+6H O(1)═C H O (s)+6O (g)△H
2 2 6 12 6 2 1
①C
6
H
12
O
6
(s)═2C
2
H
5
OH(1)+2CO
2
(g)△H
2
②C
2
H
5
OH(1)+3O
2
(g)═2CO
2
(g)+3H
2
O(1)△H
3
③A.2△H
3
=﹣△H
1
﹣△H
2
B.△H 、△H 、△H 均为△H<0
3 1 2
C.在不同油耗汽车中发生反应 ,△H 会不同
3
D.植物的光合作用通过反应 ③将热能转化为化学能
2.2018年,NASA宣布将发起“①CO
2
转化挑战赛“,这项研究有助于解决在火星上的生存问题。
下列说法不正确的是( )
A.△H =﹣(△H +△H +△H )
1 2 3 4
B.用工业催化剂代替微生物发酵,△H 不变
5
C.葡萄糖的燃烧热为﹣△H
1
D.“人造转化器”所起的作用就是催化剂
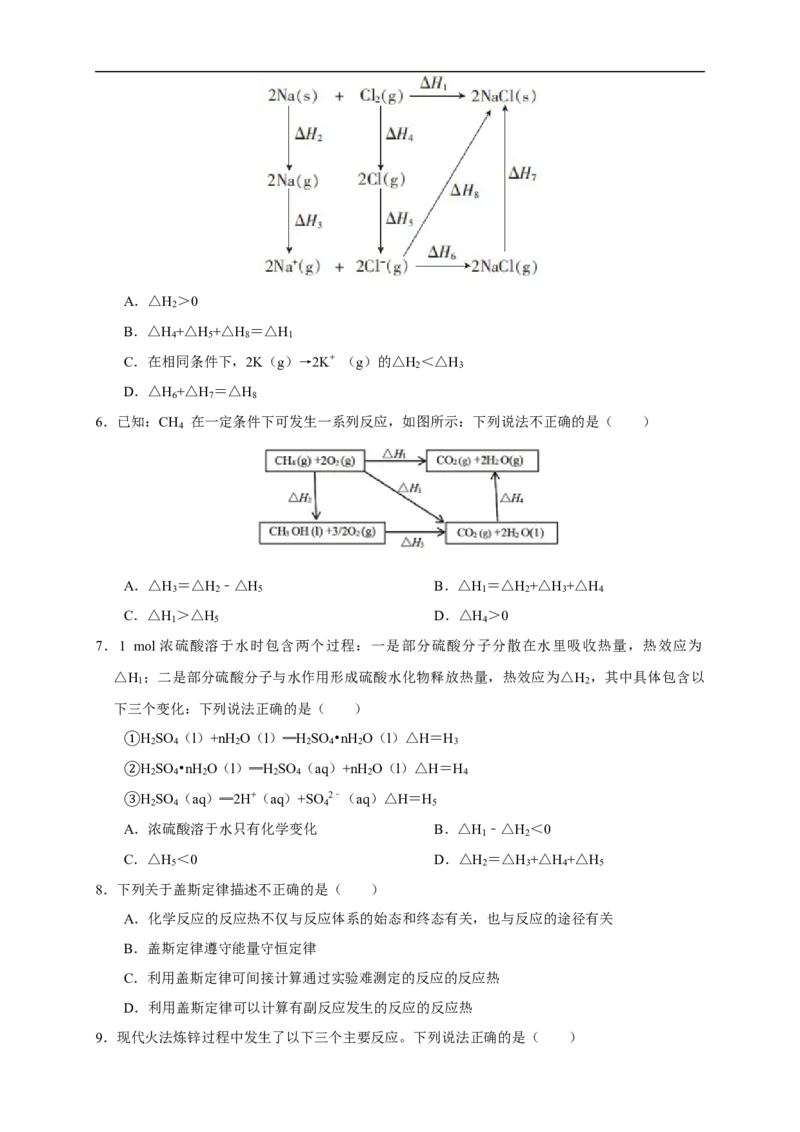
4.2mol金属钠和1mol氯气反应的能量关系如图所示,下列说法不正确的是( )
A.△H >0
2
B.△H +△H +△H =△H
4 5 8 1
C.在相同条件下,2K(g)→2K+(g)的△H ′<△H
3 3
D.△H +△H =△H
6 7 8
5.2mol金属钠和1mol氯气反应的能量关系如图所示,下列说法不正确的是( )A.△H >0
2
B.△H +△H +△H =△H
4 5 8 1
C.在相同条件下,2K(g)→2K+ (g)的△H <△H
2 3
D.△H +△H =△H
6 7 8
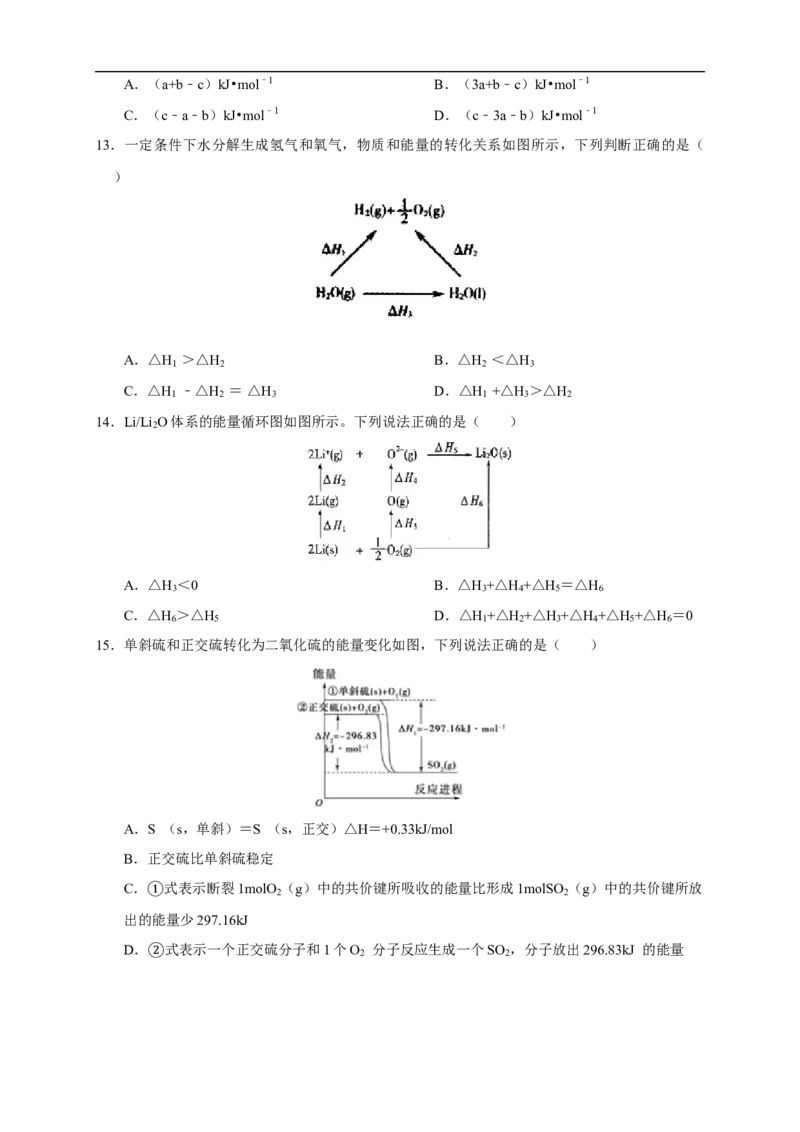
6.已知:CH 在一定条件下可发生一系列反应,如图所示:下列说法不正确的是( )
4
A.△H =△H ﹣△H B.△H =△H +△H +△H
3 2 5 1 2 3 4
C.△H >△H D.△H >0
1 5 4
7.1 mol浓硫酸溶于水时包含两个过程:一是部分硫酸分子分散在水里吸收热量,热效应为
△H ;二是部分硫酸分子与水作用形成硫酸水化物释放热量,热效应为△H ,其中具体包含以
1 2
下三个变化:下列说法正确的是( )
H SO (l)+nH O(l)═H SO •nH O(l)△H=H
2 4 2 2 4 2 3
①H
2
SO
4
•nH
2
O(l)═H
2
SO
4
(aq)+nH
2
O(l)△H=H
4
②H SO (aq)═2H+(aq)+SO 2﹣(aq)△H=H
2 4 4 5
③A.浓硫酸溶于水只有化学变化 B.△H
1
﹣△H
2
<0
C.△H <0 D.△H =△H +△H +△H
5 2 3 4 5
8.下列关于盖斯定律描述不正确的是( )
A.化学反应的反应热不仅与反应体系的始态和终态有关,也与反应的途径有关
B.盖斯定律遵守能量守恒定律
C.利用盖斯定律可间接计算通过实验难测定的反应的反应热
D.利用盖斯定律可以计算有副反应发生的反应的反应热
9.现代火法炼锌过程中发生了以下三个主要反应。下列说法正确的是( )2ZnS(s)+3O (g)=2ZnO(s)+2SO (g)△H =a kJ•mol﹣1
2 2 1
①2C(s)+O (g)=2CO(g)△H =b kJ•mol﹣1
2 2
②ZnO(s)+CO(g)=Zn(g)+CO (g)△H =c kJ•mol﹣1
2 3
③A.以上三个反应中,只有 是放热反应
B.反应 的作用是仅为反①应 提供还原剂
② ③
C.反应 ZnS(s)+C(s)+2O (g)=Zn(g)+SO (g)+CO (g)的△H= (a+b+2c)
2 2 2
kJ•mol﹣1
D.碳的燃烧热为 b kJ•mol﹣1
10.对下列有关反应的说法正确的是( )
NH HCO (s)═NH (g)+H O(g)+CO (g)△H=+185.6kJ•mol﹣1
4 3 3 2 2
①2H O(l)═2H (g)+O (g)△H =+571.6kJ•mol﹣1
2 2 2 2
②CH (g)+H O(g)═CO(g)+3H (g)△H =+206.1kJ•mol﹣1
4 2 2 3
③A.反应 均为吸热反应,均需在高温下进行
B.2 mo①l H②2 完③全燃烧生成气态水时,放出的热量为571.6kJ
C.若反应 中使用不同的催化剂,△H 会发生改变
3
D.1mol N③H
4
HCO
3
(s)的总能量低于1 mol NH
3
(g)、1 mol H
2
O(g)与1 mol CO
2
(g)
的总能量
11.已知:2H (g)+O (g)═2H O(g)△H
2 2 2 1
3H (g)+Fe O (s)═2Fe(s)+3H O(g)△H
2 2 3 2 2
2Fe(s)+ O (g)═Fe O (s)△H
2 2 3 3
2Al(s)+ O (g)═Al O (s)△H
2 2 3 4
2Al(s)+Fe O (s)═Al O (s)+2Fe(s)△H
2 3 2 3 5
下列关于上述反应焓变的判断正确的是( )
A.△H <0,△H >0 B.△H <0,△H <△H
1 3 5 4 3
C.△H =△H +△H D.△H =△H +△H
1 2 3 3 4 5
12.已知: C(s)+O (g)=CO (g)△H =akJ•mol﹣1
2 2 1
S(s①)+2K(s)=K S(s)△H =bkJ•mol﹣1
2 2
②2K(s)+N (g)+3O (g)=2KNO (s)△H =ckJ•mol﹣1
2 2 3 3
③则S(s)+2KNO
3
(s)+3C(s)=K
2
S(s)+N
2
(g)+3CO
2
(g)的热效应△H为 ( )A.(a+b﹣c)kJ•mol﹣1 B.(3a+b﹣c)kJ•mol﹣1
C.(c﹣a﹣b)kJ•mol﹣1 D.(c﹣3a﹣b)kJ•mol﹣1
13.一定条件下水分解生成氢气和氧气,物质和能量的转化关系如图所示,下列判断正确的是(
)
A.△H
1
>△H
2
B.△H
2
<△H
3
C.△H
1
﹣△H
2
= △H
3
D.△H
1
+△H
3
>△H
2
14.Li/Li O体系的能量循环图如图所示。下列说法正确的是( )
2
A.△H <0 B.△H +△H +△H =△H
3 3 4 5 6
C.△H >△H D.△H +△H +△H +△H +△H +△H =0
6 5 1 2 3 4 5 6
15.单斜硫和正交硫转化为二氧化硫的能量变化如图,下列说法正确的是( )
A.S (s,单斜)=S (s,正交)△H=+0.33kJ/mol
B.正交硫比单斜硫稳定
C. 式表示断裂1molO (g)中的共价键所吸收的能量比形成1molSO (g)中的共价键所放
2 2
出的①能量少297.16kJ
D. 式表示一个正交硫分子和1个O 分子反应生成一个SO ,分子放出296.83kJ 的能量
2 2
②