文档内容
第三章 晶体结构与性质
第一节 物质的聚集状态与晶体的常识
培优第一阶——基础过关练
1.(2022·黑龙江·鸡西市英桥高级中学高二期中)下列物质中,属于晶体的是
A.玻璃 B.石蜡和沥青 C.塑料 D.干冰
2.(2022·广东清远·高二期末)下列关于晶体的说法中正确的是
A.自然形成的水晶柱是晶体,从水晶柱上切削下来的粉末不是晶体
B.晶胞中任何一个粒子都属于该晶胞
C.玻璃制成的弹珠具有规则的几何外形,所以玻璃弹珠是晶体
D.缺角的NaCl晶体在饱和NaCl溶液中慢慢变为完美的立方体块,体现了晶体的自范性
3.(2022·四川·遂宁中学高二阶段练习)现有四种晶体,其构成粒子(均为单原子核粒子)排列方式如下图
所示,其化学式正确的是
A. B.
C. D.
4.(2021·浙江·海亮高级中学高二期中)下列叙述中,正确的是
A.石英玻璃和水晶都是晶体
B.具有各向异性的固体可能是晶体
C.粉末状的固体肯定不是晶体
D.晶体与非晶体的根本区别在于固体是否具有规则的几何外形
5.(2022·福建省泉州实验中学高二期中)晶体内微粒总是按周期性规律重复排列,反映其结构特点的基
本重复单位为晶胞,晶体可视为晶胞经平移无隙并置而成。以下是某些晶体的局部结构,可做为晶胞的是
A. (都在顶点) B. (在顶点和面心)C. (在顶点和面心) D. (在顶点和体心)
6.(2022·福建·莆田砺志学校高二期中)有下列离子晶体的空间结构示意图。图中●和化学式中M分别
代表阳离子,图中○和化学式中N分别代表阴离子,则化学式为MN的晶体结构为
A.A B.B C.C D.D
7.(2022·广东广州·高二期末)下列结构示意图中,表示晶胞的是
A. B.
C. D.
8.(2022·浙江丽水·高二期末)下列关于晶体和非晶体的说法不正确的是
A.破损的NaCl晶体能在饱和NaCl溶液中自动变成规则的立方体
B.晶体某些物理性质的各向异性反映了晶体内部质点排列的有序性
C.导电性可用于区别晶体和玻璃体
D.固体 可能是晶体,也可能是非晶体
9.(2022·广东·佛山一中高二期中)某晶体是一种性能良好的非线性光学材料,晶胞中K、I、O分别处于
顶角、体心、面心位置,该晶体的化学式应为
A.KIO B.KIO C.KIO D.KIO
2 3 4
10.(2022·四川·遂宁中学高二阶段练习)金属玻璃是由金属元素或金属元素为主要成分的熔体通过快速冷却得到的具有非晶态结构的金属固体。以下关于金属玻璃的说法正确的是
A.金属玻璃能自发呈现多面体外形
B.金属玻璃具有固定的熔点
C.鉴别金属玻璃是否为晶体最可靠的科学方法为X射线衍射实验
D.金属玻璃是金属与二氧化硅的混合物
11.(2022·辽宁丹东·高二期末)如图分别为物质I和物质Ⅱ的微观结构示意图,下列说法错误的是
A.物质I具有能自发地呈现多面体外形的性质
B.物质I形成的固体有固定的熔、沸点
C.物质II形成的固体物理性质有各向异性
D.二者的X-射线衍射图谱不相同
培优第二阶——拓展培优练
12.(2022·重庆市清华中学校高二阶段练习)根据图中相关信息,判断下列说法不正确的是
A.在NaCl晶体中,距离Na+最近的Cl-形成正八面体
B.该气态团簇分子的分子式为EF 或FE
4 4 4 4
C.1个Zn的晶胞中含有2个Zn原子
D.KO 晶体中每个K+周围有6个紧邻的K+,每个 周围有6个紧邻的
2
13.(2022·新疆·柯坪湖州国庆中学高二期末)如图表示一个晶胞,该晶胞为正方体,结构粒子位于正方
体的顶点和面心。下列说法正确的是A.若是一个不完整的 晶胞,已知 中 的配位数为8,则图中实心球表示
B.若是一个不完整的金刚石晶胞,则晶胞中缺失碳原子位于8个小立方体的中心
C.若是一个不完整的 晶胞,顶点和面心的粒子表示 ,则晶胞中 位置均在12条棱边的中心
D.若是一个分子晶体的晶胞,其可表示干冰、冰
14.(2022·湖南·益阳平高学校高二期末)铜的晶胞结构如图所示,下列关于其晶胞的说法中错误的是
A.若晶胞的边长为a,则最近的两个铜原子的距离为
B.每个晶胞中含有4个铜原子
C.铜原子的配位数为12
D.晶胞的空间利用率为
15.(2022·湖北·鄂州市教学研究室高二期末)某钙钛矿型氧化物的晶胞结构如图所示,其中A为镧系金
属离子,B为过渡金属离子,C为氧离子。下列说法正确的是
A.镧系元素位于元素周期表中IB族
B.该化合物的化学式为
C.1个基态氧原子有2个未成对电子
D.1个A离子周围最近的A离子有12个
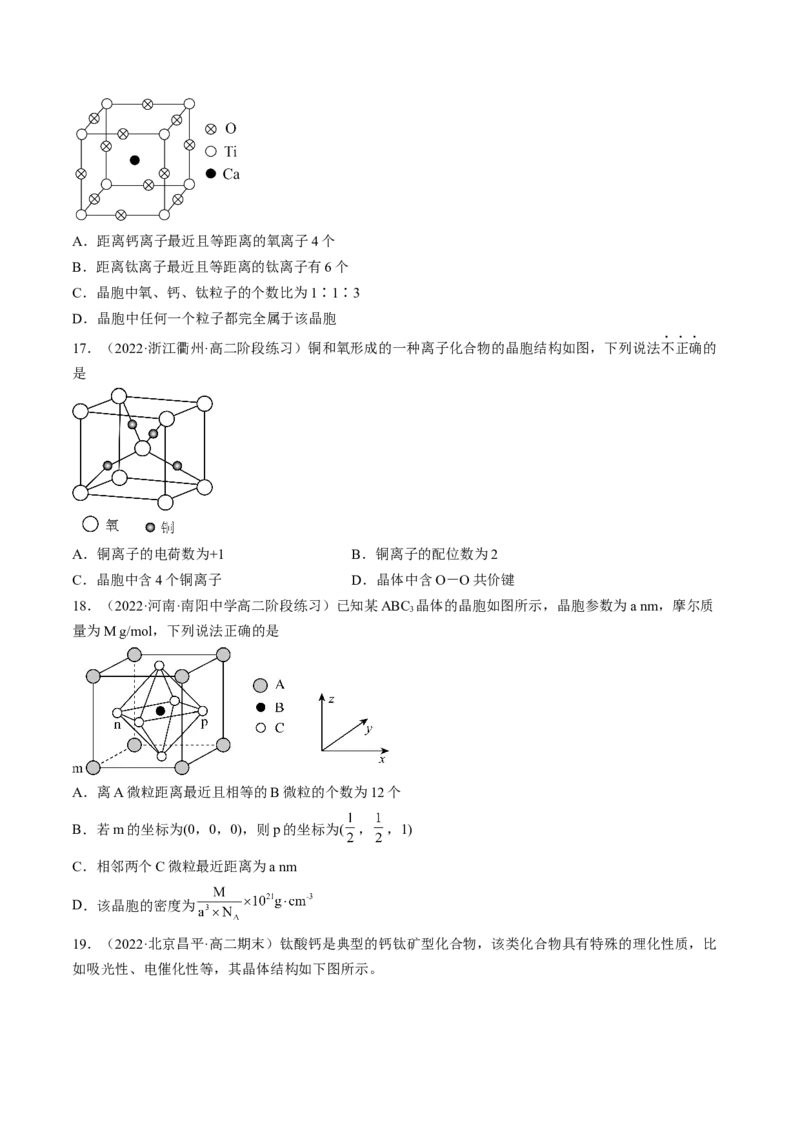
16.(2022·浙江宁波·高二期末)钙钛矿可用于高温超导领域,其晶胞结构如图所示,下列说法正确的是A.距离钙离子最近且等距离的氧离子4个
B.距离钛离子最近且等距离的钛离子有6个
C.晶胞中氧、钙、钛粒子的个数比为1∶1∶3
D.晶胞中任何一个粒子都完全属于该晶胞
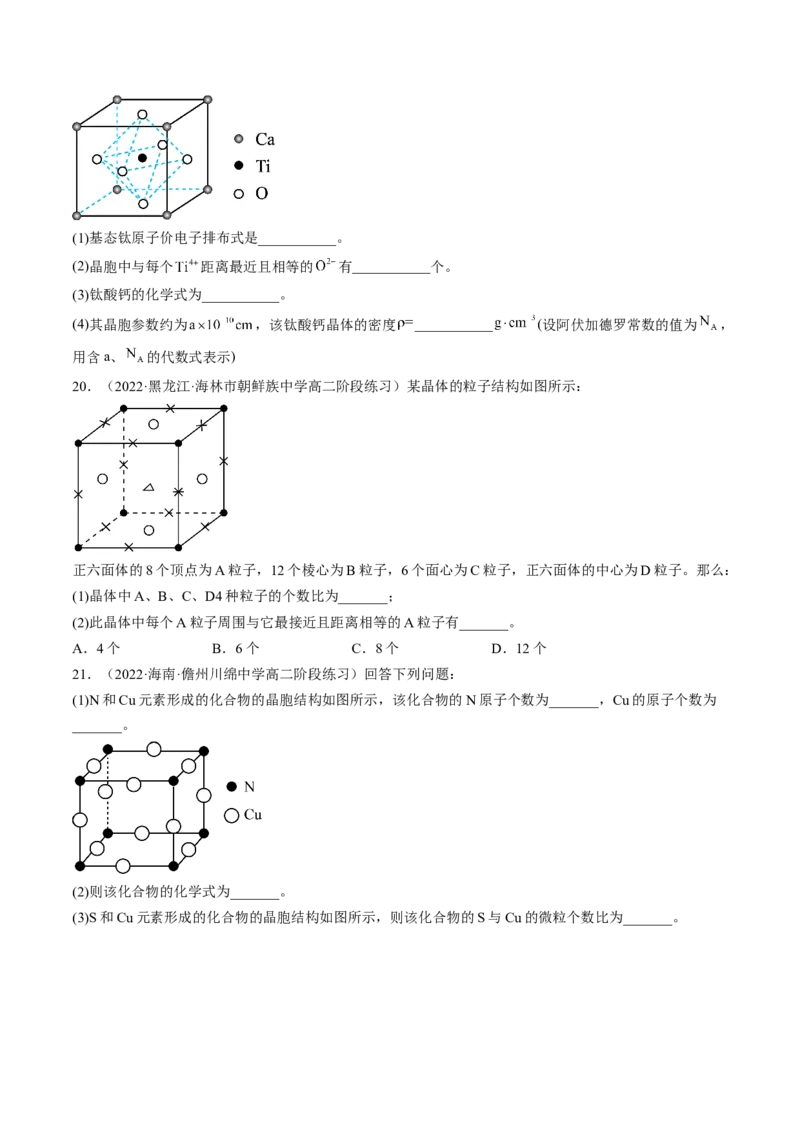
17.(2022·浙江衢州·高二阶段练习)铜和氧形成的一种离子化合物的晶胞结构如图,下列说法不正确的
是
A.铜离子的电荷数为+1 B.铜离子的配位数为2
C.晶胞中含4个铜离子 D.晶体中含O-O共价键
18.(2022·河南·南阳中学高二阶段练习)已知某ABC 晶体的晶胞如图所示,晶胞参数为a nm,摩尔质
3
量为M g/mol,下列说法正确的是
A.离A微粒距离最近且相等的B微粒的个数为12个
B.若m的坐标为(0,0,0),则p的坐标为( , ,1)
C.相邻两个C微粒最近距离为a nm
D.该晶胞的密度为
19.(2022·北京昌平·高二期末)钛酸钙是典型的钙钛矿型化合物,该类化合物具有特殊的理化性质,比
如吸光性、电催化性等,其晶体结构如下图所示。(1)基态钛原子价电子排布式是___________。
(2)晶胞中与每个 距离最近且相等的 有___________个。
(3)钛酸钙的化学式为___________。
(4)其晶胞参数约为 ,该钛酸钙晶体的密度 ___________ (设阿伏加德罗常数的值为 ,
用含a、 的代数式表示)
20.(2022·黑龙江·海林市朝鲜族中学高二阶段练习)某晶体的粒子结构如图所示:
正六面体的8个顶点为A粒子,12个棱心为B粒子,6个面心为C粒子,正六面体的中心为D粒子。那么:
(1)晶体中A、B、C、D4种粒子的个数比为_______;
(2)此晶体中每个A粒子周围与它最接近且距离相等的A粒子有_______。
A.4个 B.6个 C.8个 D.12个
21.(2022·海南·儋州川绵中学高二阶段练习)回答下列问题:
(1)N和Cu元素形成的化合物的晶胞结构如图所示,该化合物的N原子个数为_______,Cu的原子个数为
_______。
(2)则该化合物的化学式为_______。
(3)S和Cu元素形成的化合物的晶胞结构如图所示,则该化合物的S与Cu的微粒个数比为_______。(4)价电子排布式为3d54s2的原子,其原子元素符号为_______。
(5)CuSn S 中Cu元素有+1和+2两种价态,从结构上分析基态Cu+、Cu2+中_______更稳定,原因是_______;
a b c
22.(2021·新疆伊犁·高二阶段练习)(1)一种Pt、Co金属间化合物可作为质子交换膜燃料电池的催化剂,
其晶胞结构如图1所示,该金属间化合物的中Pt与Co的个数比为___________。
(2)室温下,[Cu(NH )](NO ),与液氨混合并加入Cu可制得一种黑绿色晶体。黑绿色晶体的晶胞如图2所
3 4 3 2
示,写出该晶体的化学式___________。
(3)如图3所示的是金红石的晶胞,则每个晶胞拥有___________个Ti4+、___________个O2-。