文档内容
第一节 化学反应与能量变化--课时训练 2022-2023学年高
一下学期化学人教版(2019)必修第二册
学校:___________姓名:___________班级:___________考号:___________
一、单选题
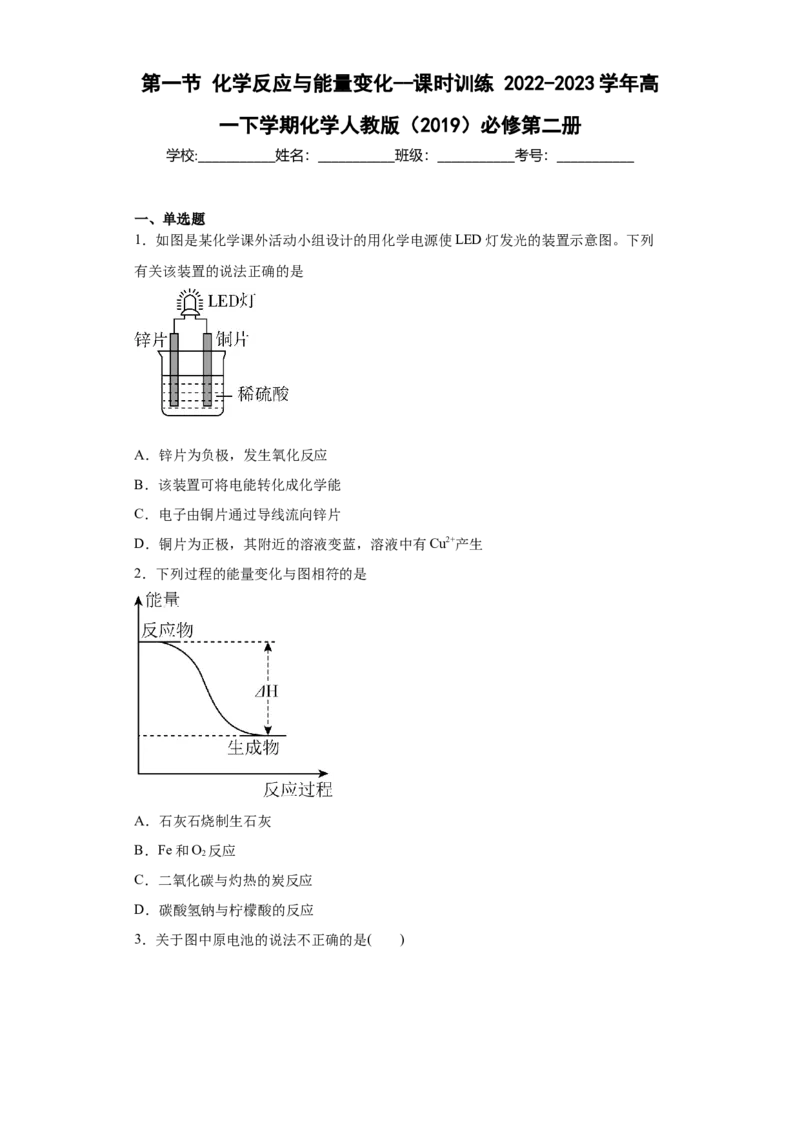
1.如图是某化学课外活动小组设计的用化学电源使LED灯发光的装置示意图。下列
有关该装置的说法正确的是
A.锌片为负极,发生氧化反应
B.该装置可将电能转化成化学能
C.电子由铜片通过导线流向锌片
D.铜片为正极,其附近的溶液变蓝,溶液中有Cu2+产生
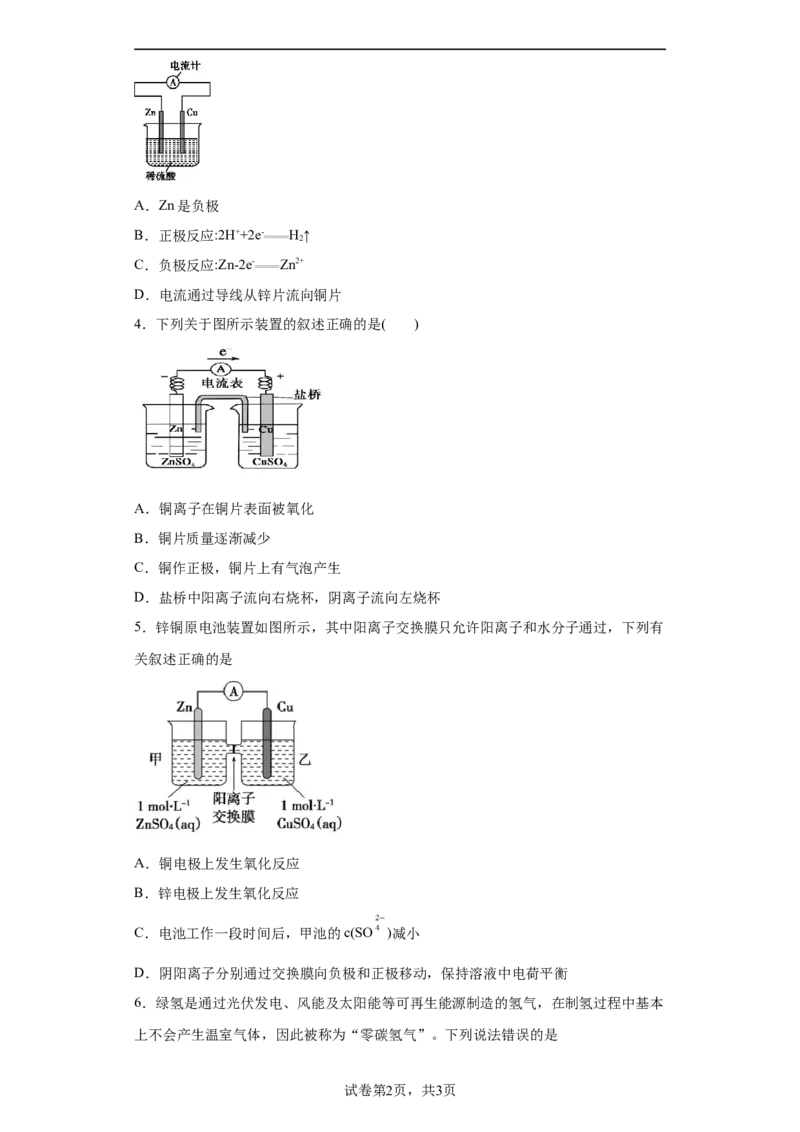
2.下列过程的能量变化与图相符的是
A.石灰石烧制生石灰
B.Fe和O 反应
2
C.二氧化碳与灼热的炭反应
D.碳酸氢钠与柠檬酸的反应
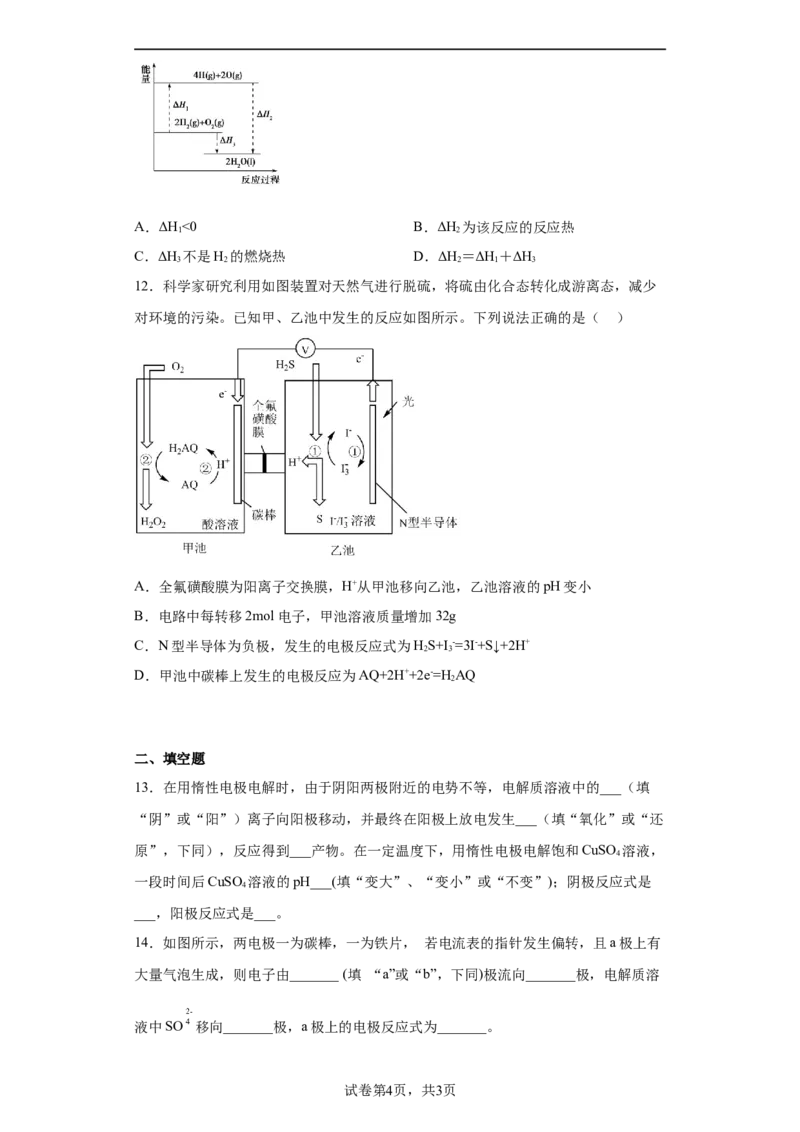
3.关于图中原电池的说法不正确的是( )A.Zn是负极
B.正极反应:2H++2e- H↑
2
C.负极反应:Zn-2e- Zn2+
D.电流通过导线从锌片流向铜片
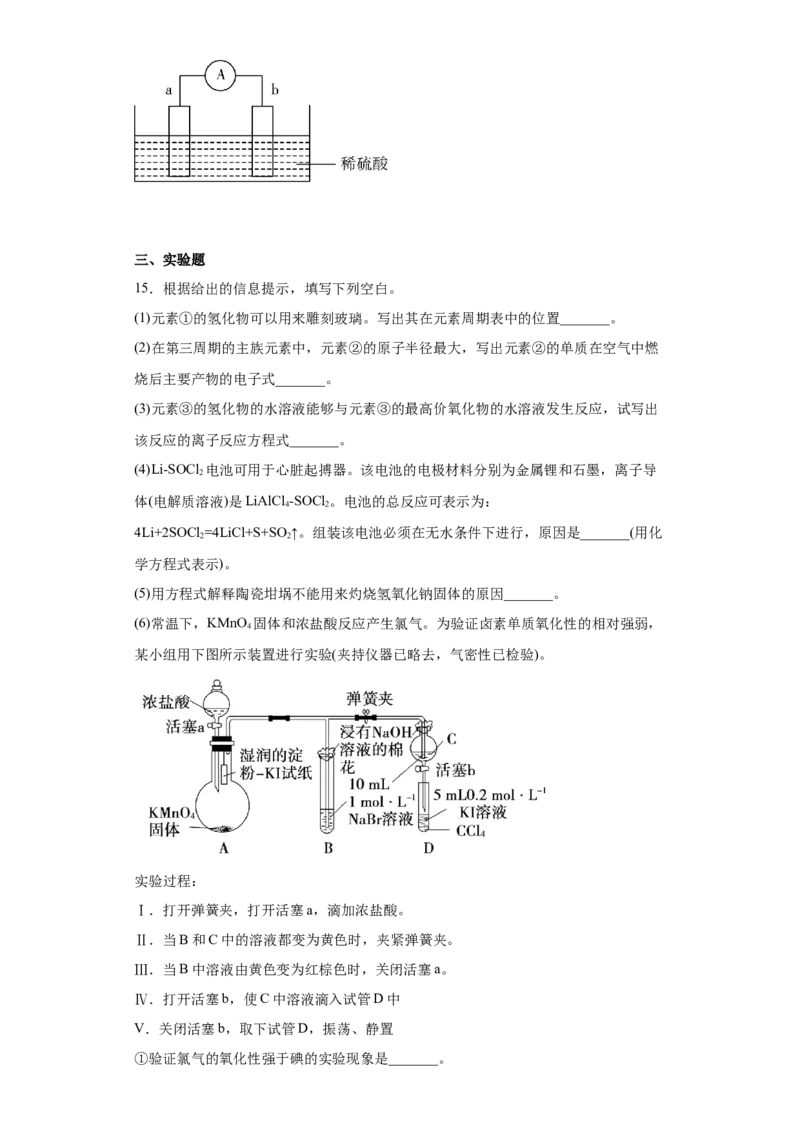
4.下列关于图所示装置的叙述正确的是( )
A.铜离子在铜片表面被氧化
B.铜片质量逐渐减少
C.铜作正极,铜片上有气泡产生
D.盐桥中阳离子流向右烧杯,阴离子流向左烧杯
5.锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有
关叙述正确的是
A.铜电极上发生氧化反应
B.锌电极上发生氧化反应
C.电池工作一段时间后,甲池的c(SO )减小
D.阴阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
6.绿氢是通过光伏发电、风能及太阳能等可再生能源制造的氢气,在制氢过程中基本
上不会产生温室气体,因此被称为“零碳氢气”。下列说法错误的是
试卷第2页,共3页A.氢气是清洁能源、燃烧产物对环境友好
B.氢气是高效燃料,燃烧的火焰呈淡蓝色
C.北京冬奥会火炬的“微火”体现低碳理念
D.利用太阳能分解水制备绿氢是放热反应
7.对于反应2NaO+2H O = 4NaOH+O ↑中化学键的变化判断正确的是
2 2 2 2
A.只有离子键的断裂和形成
B.只有共价键的断裂和形成
C.既有离子键和共价键的断裂,又有离子键和共价键的形成
D.既有离子键和极性键的断裂,又有离子键和极性键的形成
8.下列反应中既是氧化还原反应,能量变化情况又符合如图的是
A.铝片与稀盐酸的反应 B.碳和水蒸气的反应
C.NH Cl和Ba(OH) ·8H O的反应 D.H 的燃烧反应
4 2 2 2
9.能量通常包括热能、电能、光能、机械能、化学能等,下列有关能量转化关系的判
断错误的是
A.甲烷燃烧:化学能转化为热能和光能
B.植物进行光合作用:太阳能转化为化学能
C.二次电池放电:电能转化为化学能
D.风力发电:风能转化为机械能,机械能转化为电能
10.对于锌-铜-稀硫酸组成的原电池装置中,当导线中有0.1mol电子通过时,理论上
的两极变化是( )
①锌片溶解了3.25g ②锌片增重3.25g
③铜片上析出0.1g H ④铜片上析出0.1mol H
2 2
A.①和③ B.①和④ C.②和③ D.②和④
11.反应2H(g)+O(g)=2HO(l)过程中的能量变化如图所示,下列有关说法中正确的
2 2 2
是( )A.ΔH<0 B.ΔH 为该反应的反应热
1 2
C.ΔH 不是H 的燃烧热 D.ΔH=ΔH+ΔH
3 2 2 1 3
12.科学家研究利用如图装置对天然气进行脱硫,将硫由化合态转化成游离态,减少
对环境的污染。已知甲、乙池中发生的反应如图所示。下列说法正确的是( )
A.全氟磺酸膜为阳离子交换膜,H+从甲池移向乙池,乙池溶液的pH变小
B.电路中每转移2mol电子,甲池溶液质量增加32g
C.N型半导体为负极,发生的电极反应式为HS+I -=3I-+S↓+2H+
2 3
D.甲池中碳棒上发生的电极反应为AQ+2H++2e-=H AQ
2
二、填空题
13.在用惰性电极电解时,由于阴阳两极附近的电势不等,电解质溶液中的___(填
“阴”或“阳”)离子向阳极移动,并最终在阳极上放电发生___(填“氧化”或“还
原”,下同),反应得到___产物。在一定温度下,用惰性电极电解饱和CuSO 溶液,
4
一段时间后CuSO 溶液的pH___(填“变大”、“变小”或“不变”);阴极反应式是
4
___,阳极反应式是___。
14.如图所示,两电极一为碳棒,一为铁片, 若电流表的指针发生偏转,且a极上有
大量气泡生成,则电子由_______ (填 “a”或“b”,下同)极流向_______极,电解质溶
液中SO 移向_______极,a极上的电极反应式为_______。
试卷第4页,共3页三、实验题
15.根据给出的信息提示,填写下列空白。
(1)元素①的氢化物可以用来雕刻玻璃。写出其在元素周期表中的位置_______。
(2)在第三周期的主族元素中,元素②的原子半径最大,写出元素②的单质在空气中燃
烧后主要产物的电子式_______。
(3)元素③的氢化物的水溶液能够与元素③的最高价氧化物的水溶液发生反应,试写出
该反应的离子反应方程式_______。
(4)Li-SOCl 电池可用于心脏起搏器。该电池的电极材料分别为金属锂和石墨,离子导
2
体(电解质溶液)是LiAlCl -SOCl 。电池的总反应可表示为:
4 2
4Li+2SOCl =4LiCl+S+SO ↑。组装该电池必须在无水条件下进行,原因是_______(用化
2 2
学方程式表示)。
(5)用方程式解释陶瓷坩埚不能用来灼烧氢氧化钠固体的原因_______。
(6)常温下,KMnO 固体和浓盐酸反应产生氯气。为验证卤素单质氧化性的相对强弱,
4
某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.打开活塞b,使C中溶液滴入试管D中
V.关闭活塞b,取下试管D,振荡、静置
①验证氯气的氧化性强于碘的实验现象是_______。②B中溶液发生反应的离子方程式是_______。
③该实验_______(填“能”或“不能”)证明溴的氧化性强于碘,原因是_______。
试卷第6页,共3页参考答案:
1.A
【详解】A.锌活动性大于铜,为原电池负极,失去电子发生氧化反应生成锌离子,A正
确;
B.该装置为原电池,可将化学能转化成电能,B错误;
C.锌为负极,电子由锌片通过导线流向铜片,C错误;
D.铜片为正极,溶液中氢离子在铜极放电生成氢气,D错误;
故选A。
2.B
【分析】由图知,该反应为放热反应;
【详解】A.石灰石烧制生石灰属于吸热反应,A错误;
B.Fe和O 反应属于放热反应,B正确;
2
C.二氧化碳与灼热的炭反应属于吸热反应,C错误;
D.碳酸氢钠与柠檬酸的反应属于吸热反应,D错误;
故答案为B。
3.D
【详解】A. Zn活泼性强,与稀硫酸反应,锌是负极,故A正确;
B. 正极反应:2H++2e- H↑,故B正确;
2
C. 负极反应:Zn−2e- Zn2+,故C正确;
D. 电流通过导线从铜片流向锌片,故D错误。
综上所述,答案为D。
4.D
【详解】A.铜为正极,发生还原反应,故A错误;
B.铜作正极,铜片上有Cu产生,铜片质量增加,故B错误;
C.铜为正极,铜离子得电子生成铜,无气泡产生,故C错误;
D.右烧杯中铜离子减少,要保持溶液的电中性,所以盐桥中阳离子流向右烧杯,左烧杯
中生成Zn2+,所以阴离子流向左烧杯,故D正确。
故选D。
5.B
【详解】A.铜锌原电池,锌作负极,铜作正极,铜电极上发生还原反应,故A错误;
B.铜锌原电池,锌作负极,锌失去电子被氧化转变为锌离子,B正确;
C.原电池工作时,锌离子透过阳离子交换膜向乙池移动,甲池的c(SO 2-)不参加反应、且
4就在甲池内,故浓度不变,故C错误;
D. 由于中间存在阳离子交换膜,只有阳离子能通过,即锌离子通过阳离子交换膜进入乙
池,阴离子不能通过,故D错误;
答案为B。
6.D
【详解】A.氢气燃烧产物是水,对环境无污染,故氢气是清洁能源,故A正确;
B.氢气燃烧火焰呈淡蓝色,故B正确;
C.氢气燃烧不会产生二氧化碳,体现了低碳理念,故C正确;
D.利用太阳能分解水制备氢气是吸热反应,故D错误;
故选:D。
7.C
【详解】对于反应2NaO+2H O = 4NaOH+O ↑,NaO 中含有离子键和非极性键,HO中
2 2 2 2 2 2 2
含有极性键,在发生化学反应时都发生了断裂,新形成了NaOH中的离子键和极性键、O
2
中的非极性键,所以该反应中既有离子键和共价键的断裂,又有离子键和共价键的形成,
故答案选C。
8.B
【分析】从图中可以看出,反应物的总能量低于生成物的总能量,所以为吸热反应。
【详解】A.铝片与稀盐酸发生置换反应,生成氯化铝和氢气,并能释放能量,属于放热
反应,A不符合题意;
B.碳和水蒸气在高温下反应,生成一氧化碳和氢气,需要不断地提供能量,属于吸热反
应,反应中C、H元素的价态发生改变,属于氧化还原反应,B符合题意;
C.NH Cl和Ba(OH) ·8H O发生复分解反应,通过从周围环境中吸收热量,维持反应的不
4 2 2
断进行,属于吸热反应,但不含有价态变化的元素,属于非氧化还原反应,C不符合题意;
D.H 燃烧能释放大量的热,属于放热反应,D不符合题意;
2
故选B。
9.C
【详解】A.甲烷在氧气中剧烈燃烧,产生淡蓝色火焰,放出大量的热,所以该过程中除
了将化学能转化为热能外,还有一部分化学能转化为光能,故A正确;
B.光合作用是植物把接收到的光能转化为化学能贮存起来,故B正确;
C.二次电池放电,化学能转化为电能,故C错误;
D.风力发电主要是将风能转化为风轮的机械能,再通过发电机转化为电能,故D正确;
答案第2页,共2页选C。
10.A
【详解】锌-铜-稀硫酸组成的原电池装置中Zn为负极,电极反应式为Zn-2e-=Zn2+,Cu为
正极,电极反应式为2H++2e-=H ↑,则导线中有0.1mol电子通过时,溶解Zn的质量为
2
65g/mol× =3.25g,生成H 的质量为2g/mol× =0.1g,选项①和③正确,故答案
2
为A。
11.C
【详解】A.△H 是分子拆成原子的过程,需吸收能量,△H>0,故A错误;
1 1
B.△H 是该反应的反应热,△H 只是原子结合成分子时释放的能量,故B错误;
3 2
C.燃烧热是指1mol可燃物燃烧放出的热量,△H 是2mol氢气燃烧放出的热量,故C正确;
3
D.一个反应的△H应是拆开反应物的化学键吸收的能量与形成新的化学键释放的能量之差,
从反应过程分析,△H=△H +△H ,故D错误;
3 1 2
答案选C。
12.D
【分析】甲池中,发生两步反应,HAQ+O = H O+AQ,AQ+2H++2e-=H AQ,HAQ是催
2 2 2 2 2 2
化剂,总反应为2H++O +2e-=H O,O元素化合价由0价升高到−1价,碳棒作正极,正极
2 2 2
上的电极反应为AQ+2H++2e-=H AQ,乙池中,N型半导体为负极,负极的电极反应式为
2
3I--2e-= I-,乙池的总反应为HS-2e-=2H++S↓。
3 2
【详解】A.全氟磺酸膜为阳离子交换膜,由图可知,H+从乙池移向甲池,乙池虽然产生
了H+,但是其向甲池迁移,电子转移的数目与H+的数目相同,故乙池的pH不变,故A错
误;
B.H+从乙池移向甲池,甲池的总反应为2H++O +2e-=H O,电路中每转移2mol电子,溶
2 2 2
液增加的是1mol氧气的质量和由乙池转移2mol H+的质量,2mol氢离子的质量
m=nM=2mol×1g/mol=2g,所以甲池溶液质量增加32g+2g=34g,故B错误;
C.N型半导体为负极,负极的电极反应式为3I--2e-= I-,乙池的总反应为HS-2e-=2H+
3 2
+S↓,故C错误;
D.根据分析可知,甲池中碳棒上发生的电极反应为AQ+2H++2e-=H AQ,故D正确;
2
答案选D。
【点睛】本题的难点是电池中的两极在两个池中,判断出HAQ是催化剂,可能学生在判
2
断正负极时会遇到困难,可以从电子的流向判断出正负极,能根据氧化还原反应原理写出电极反应式是解本题的关键。
13. 阴 氧化 氧化 变小 Cu2++2e-=Cu
4OH--4e-=2H O+O↑
2 2
【详解】在用惰性电极电解时,“异性相吸”即电解质溶液中的阴离子向阳极移动,并最
终在阳极上放电发生氧化,反应得到氧化产物;在一定温度下,用惰性电极电解饱和
CuSO 溶液,阳极生成氧气,剩余氢离子,阴极生成铜单质,因此一段时间后CuSO 溶液
4 4
的pH变小,阴极生成铜单质,其电极反应式是Cu2++2e-=Cu,阳极反应式是4OH--4e-
=2H O+O↑。
2 2
14. b a b 2H++2e-=H ↑
2
【分析】在铁、碳、稀硫酸组成的原电池中,有气体产生的一极为正极,故a极为正极,b
极为负极,据此分析解题。
【详解】a极上有大量气泡生成,则a极为正极(碳棒),b极为负极(铁片),电子由负极流向
正极,即由b极流向a极,电解质溶液中,阴离子向负极移动,即SO 移向b极,a极上
的H+得电子生成H,a电极反应式为2H++2e-=H ↑。
2 2
15. 第二周期VIIA族
NH ·H O+H+= +H O 2Li+2HO=2LiOH+H ↑ SiO+2NaOH NaSiO+H O A中湿
3 2 2 2 2 2 2 3 2
润的淀粉碘化钾试纸变蓝 Cl+2Br-=Br +2Cl- 能 由步骤II、III可知,
2 2
C中的Br-过量,溶液中除生成的Br 之外,不存在多余的Cl
2 2
【详解】(1)氢氟酸能够与SiO 发生反应产生SiF 和水,因此氢氟酸能够腐蚀玻璃,氢氟酸
2 4
是HF的水溶液,故元素①是F元素,F元素原子序数是9,原子核外电子排布是2、7,因
此在元素周期表中位于第二周期第VIIA;
(2)同一周期元素的原子半径随原子序数的增大而减小。元素②是第三周期主族元素,原子
半径最大,则元素②是Na元素,金属Na与空气中的O 在点燃反应产生NaO,该物质是
2 2 2
离子化合物,Na+与 通过离子键结合,在 中2个O原子通过共价键结合,故其电子
答案第4页,共2页式为: ;
(3)元素③的氢化物的水溶液能够与元素③的最高价氧化物的水溶液发生反应,则该元素是
N元素,其氢化物是NH ,NH 溶于水反应得到NH ·H O,其最高价氧化物对应的水化物
3 3 3 2
是HNO,二者反应产生NH NO ,该反应的离子反应方程式为:NH ·H O+H+=
3 4 3 3 2
+H O;
2
(4)Li-SOCl 电池可用于心脏起搏器。该电池的电极材料分别为金属锂和石墨,离子导体(电
2
解质溶液)是LiAlCl -SOCl 。电池的总反应可表示为:4Li+2SOCl =4LiCl+S+SO ↑。由于Li
4 2 2 2
是比较活泼的金属,能够与水发生化学反应,产生LiOH、H,该反应方程式为:
2
2Li+2HO=2LiOH+H ↑,所以组装该电池必须在无水条件下进行;
2 2
(5)陶瓷中含有SiO,SiO 是酸性氧化物,能够与碱NaOH发生反应:SiO+2NaOH
2 2 2
=Na SiO+H O,所以陶瓷坩埚不能用来灼烧氢氧化钠固体;
2 3 2
(6)①若Cl 的氧化性比I 强,则在A试管的湿润的淀粉-KI中试纸上会发生反应:
2 2
Cl+2KI=2KCl+I ,I 遇淀粉溶液变为蓝色,故氯气的氧化性强于碘的实验现象是:A中湿
2 2 2
润的淀粉碘化钾试纸变蓝;
②在B试管中Cl 与NaBr发生置换反应产生Br ,使溶液变为橙色,反应的离子方程式为:
2 2
Cl+2Br-=Br +2Cl-;
2 2
③Cl、Br 都具有强氧化性,能够与KI发生置换反应产生I,由步骤II、III可知,C中的
2 2 2
Br-过量,溶液中除生成的Br 之外,不存在多余的Cl,因此能够说明溴的氧化性强于碘。
2 2答案第6页,共2页