文档内容
第六章 化学反应与能量
第一节 化学反应与能量变化
(第2课时 化学反应与电能)
一、选择题
1.如图所示,电流计G发生偏转,同时A极逐渐变细,B极逐渐变粗,C为电解质溶液,则A、B、C应
是下列各组中的
A.A是Zn、B是Cu、C为稀硫酸
B.A是Cu、B是Al、C为CuSO 溶液
4
C.A是Zn、B是石墨、C为AgNO 溶液
3
D.A是石墨、B是Fe、C为FeCl 溶液
3
【答案】C
【解析】
原电池中负极的活泼性大于正极的活泼性,负极上金属失电子变成离子进入溶液,质量减少,正极上得电
子发生还原反应,正极上析出物质,若析出的物质是金属,则正极质量增加,A极逐渐变细则A为负极,
B极逐渐变粗则B为正极;
A.Zn的金属性比Cu活泼,与稀硫酸组成原电池时Zn做负极,失电子生成锌离子,A极变细,由于得电
子能力:H+>Cu2+,B极产生氢气,B极不变粗,A错误;
B.Al的金属性比Cu活泼,A为正极,铜离子得电子生成铜,A极变粗,B为负极,B极变细,B错误;
C.石墨是惰性电极,B为正极,银离子得电子生成Ag,B极变粗,A为负极,Zn失电子生成锌离子,A
极变细,C正确;
D.Fe与FeCl 溶液反应生成FeCl ,A是石墨为正极,质量不变,B是Fe为负极,Fe失电子生成亚铁离子,
3 2
B极变细,D错误;
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司故选:C。
2.将铜片和锌片用导线和电流计连接后,浸入一定浓度的稀硫酸中,如图所示,下面有关说法正确的是
A.Zn是正极,Cu是负极
B.电子从Cu片经导线流向Zn片
C.Zn极有铜析出
D.Cu极上有气泡产生
【答案】D
【解析】
A.将铜片和锌片用导线和电流计连接后,浸入一定浓度的稀硫酸中构成原电池,由于金属性Zn>Cu,则
Zn是负极,Cu是正极,A错误;
B.Zn是负极,Cu是正极,电子从Zn片经导线流向Cu片,B错误;
C.Zn是负极,Zn溶解,没有铜析出,C错误;
D.Cu是正极,正极上氢离子放电,则Cu极上有气泡产生,D正确;
答案选D。
3.(2021·上海静安·高一期末)下图为铜锌原电池示意图,下列说法中不正确的是
A.锌为阴极,铜为阳极
B.电子由锌片通过导线流向铜片
C.锌片质量逐渐减少,溶液的质量逐渐增加
D.该装置能把化学能转化为电能
【答案】A
【解析】
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司由图中的铜锌原电池可知,Zn较活泼,则Zn作负极,Cu作正极,电池总反应式为
Zn+H SO ═ZnSO +H ↑,负极反应式为Zn-2e-=Zn2+,正极反应式为2H++2e-=H ↑,电子由负极经导线流向正
2 4 4 2 2
极,该装置可将化学能转变为电能,据此解答。
A.用锌片、铜片和稀硫酸组成的原电池装置中,锌片的活泼性大于铜片的活泼性,所以锌片作负极,铜
片作正极,A项错误;
B.电子由负极(锌片)通过导线流向正极(铜片),B项正确;
C.锌、铜和稀硫酸构成的原电池中,锌易失电子生成锌离子进入溶液而质量逐渐减少,铜电极上氢离子
得电子生成氢气而产生气泡,根据Zn+H SO ═ZnSO +H ↑,溶液的质量逐渐增加,C项正确;
2 4 4 2
D.该装置是把化学能转化为电能,D项正确;
答案选A。
4.(2022·全国·高一)图1是原电池示意图,图2中x轴表示实验时流入正极的电子的物质的量,y轴表
示
A.溶液的质量 B. C. D.锌棒的质量
【答案】A
【解析】
A.图1发生反应Zn+CuSO = ZnSO+Cu,随转移电子的物质的量增多,溶液质量增大,故选A;
4 4
B.图1发生反应Zn+CuSO = ZnSO+Cu,随转移电子的物质的量增多,溶液中 由0逐渐增大,故
4 4
不选B;
C.图1发生反应Zn+CuSO = ZnSO+Cu,随转移电子的物质的量增多,溶液中 逐渐减小,故不选
4 4
C;
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司D.图1发生反应Zn+CuSO = ZnSO+Cu,随转移电子的物质的量增多,锌棒的质量减小,故不选D;
4 4
选A。
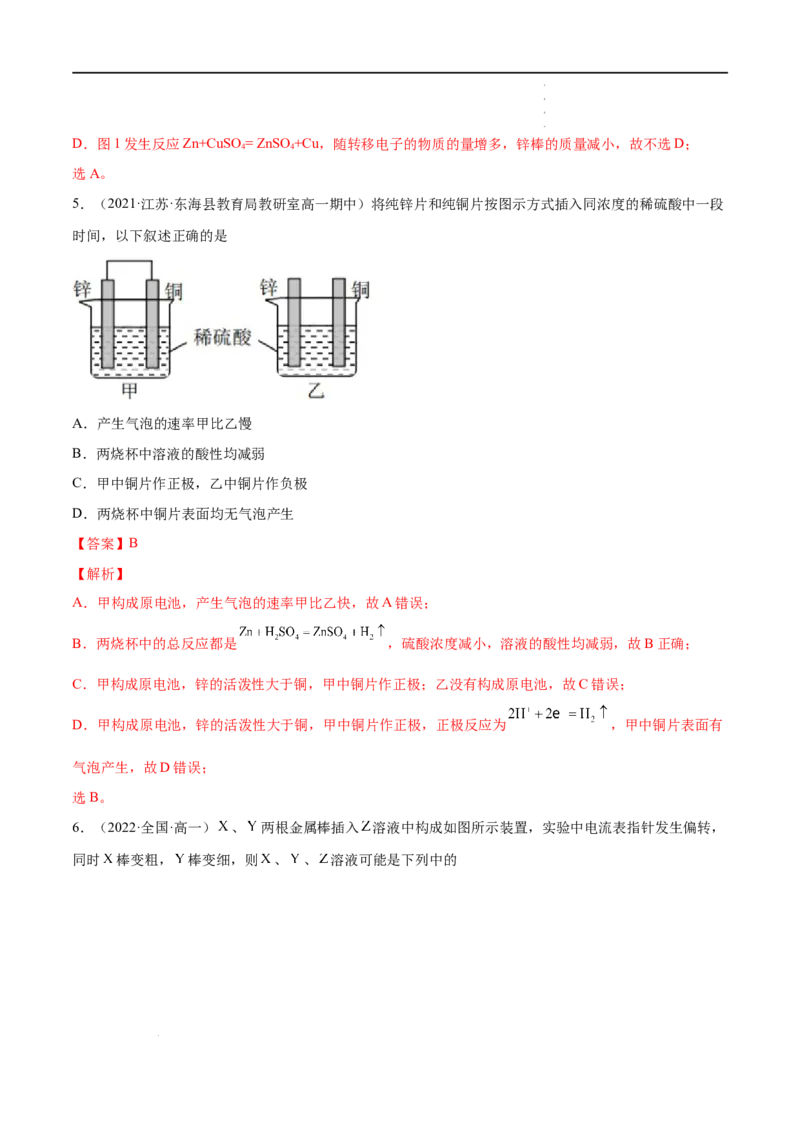
5.(2021·江苏·东海县教育局教研室高一期中)将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段
时间,以下叙述正确的是
A.产生气泡的速率甲比乙慢
B.两烧杯中溶液的酸性均减弱
C.甲中铜片作正极,乙中铜片作负极
D.两烧杯中铜片表面均无气泡产生
【答案】B
【解析】
A.甲构成原电池,产生气泡的速率甲比乙快,故A错误;
B.两烧杯中的总反应都是 ,硫酸浓度减小,溶液的酸性均减弱,故B正确;
C.甲构成原电池,锌的活泼性大于铜,甲中铜片作正极;乙没有构成原电池,故C错误;
D.甲构成原电池,锌的活泼性大于铜,甲中铜片作正极,正极反应为 ,甲中铜片表面有
气泡产生,故D错误;
选B。
6.(2022·全国·高一) 、 两根金属棒插入 溶液中构成如图所示装置,实验中电流表指针发生偏转,
同时 棒变粗, 棒变细,则 、 、 溶液可能是下列中的
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司编号 溶液
A 稀硫酸
B 硝酸银溶液
C 硫酸铜溶液
D 稀硫酸
A.A B.B C.C D.D
【答案】B
【解析】
A.锌、铜在稀硫酸中构成原电池,X棒为活泼金属锌,做原电池的负极,失去电子发生氧化反应生成锌
离子,X棒变细,故A不符合题意;
B.锌、银在硝酸银溶液中构成原电池,X棒为不活泼金属银,做原电池的正极,银离子在正极得到电子
发生还原反应生成银,X棒变粗,Y棒为活泼金属锌,做原电池的负极,失去电子发生氧化反应生成锌离
子,Y棒变细,故B符合题意;
C.铜、银在硫酸铜溶液中构成原电池,铜的金属性强于银,X棒为金属铜,做原电池的负极,失去电子
发生氧化反应生成铜离子,X棒变细,故C不符合题意;
D.锌、铜在稀硫酸中构成原电池,X棒为不活泼金属铜,做原电池的正极,氢离子在正极得到电子发生
还原反应生成氢气,X棒没有变化,故D不符合题意;
故选B。
7.碱性电池具有容量、放电电流大的特点。锌锰碱性电池以氢氧化钾溶液为电解质,电池总反应式为
Zn(s)+2MnO(s)+HO(l)=Zn(OH) (s)+Mn O(s)。下列说法不正确的是
2 2 2 2 3
A.该电池属于一次电池,已使用过的电池需放到专门的电池回收箱中
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司B.原电池工作时,正极的极反应式为:2MnO (s)+HO(l)+2e-=Mn O(s)+2OH-(aq)
2 2 2 3
C.电池工作时,电解质氢氧化钾溶液中阳离子迁移到电池的正极
D.电池工作时,Zn为负极,负极区pH变大
【答案】D
【解析】
电池总反应式为Zn(s)+2MnO(s)+HO(l)=Zn(OH) (s)+Mn O(s),据此分析,锌被氧化,为原电池的负极,
2 2 2 2 3
极反应式为:Zn-2e-+2OH-= Zn(OH) ,总反应减去负极反应式可得正极的极反应式为:2MnO (s)+HO(l)
2 2 2
+2e-=Mn O(s)+2OH-(aq),据以上分析解答。
2 3
A.该电池属于一次电池,用完之后无法充电,其内部的氧化还原反应是不可逆的;已使用过的电池需放
到专门的电池回收箱中,故A正确;
B.结合以上分析可知,电池正极的电极反应式为2MnO (s)+HO(l)+2e-=Mn O(s)+2OH-(aq),故B正确;
2 2 2 3
C.原电池工作时,阳离子向正极移动,因此电解质氢氧化钾溶液中阳离子迁移到电池的正极,故C正确;
D.电池工作时,Zn为负极,极反应式为:Zn-2e-+2OH-= Zn(OH) ,氢氧根离子浓度减小,负极区pH变小,
2
故D错误;
故选D。
8.锌一铜西红柿电池装置示意图如图所示,下列说法不正确的是
A.铜片为正极,发生还原反应
B.锌片上发生氧化反应:Zn-2e-=Zn2+
C.可将西红柿替换成盛装酒精的装置
D.电子由锌片沿导线流向铜极
【答案】C
【解析】
A.该原电池工作时,Zn为负极,Cu为正极,正极发生还原反应,A项正确;
B.Zn为负极,发生氧化反应,电极反应式为Zn-2e-=Zn2+,B项正确;
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司C.酒精是非电解质,不能导电,若将西红柿替换成盛装酒精的装置,则不能形成闭合回路,不能构成原
电池,C项错误;
D.电子由负极经导线流向正极,即电子由锌片沿导线流向铜极,D项正确;
答案选C。
9.(2021·湖南·双峰县第八中学高一期中)下列说法正确的是( )
A.镍镉电池、锂电池和锌锰电池都是二次电池
B.燃料电池是一种高效但是会污染环境的新型电池
C.化学电池的反应原理是氧化还原反应
D.铅蓄电池放电时正极是Pb,负极是PbO
2
【答案】C
【解析】
A.镍氢电池、锂离子电池为二次电池,碱性锌锰干电池为一次电池,故A错误;
B.燃料电池有氢氧燃料电池、甲烷燃料电池、乙醇燃料电池等,产物多为CO、HO等,不污染环境,
2 2
故B错误;
C.化学电池是将化学能转变为电能的装置,有电子的得失,实质为氧化还原反应,故C正确;
D.铅蓄电池放电的时候,Pb被氧化,为原电池的负极;PbO 被还原,为原电池的正极,故D错误。
2
答案选C。
10.(2021·广东梅州·)如图为某锌-铜原电池示意图,下列说法正确的是
A.该装置能将化学能完全转变为电能
B.电子由锌片通过导线流向铜片
C.锌片为负极,且发生还原反应
D.正极的电极反应式:
【答案】B
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司【解析】
锌-铜原电池,铜的活泼性小于锌,锌做负极,发生氧化反应,铜做正极,发生还原反应,铜离子在此极得
电子生成铜。
A.原电池是把化学能转化为电能的装置,但原电池在工作中会发热,故不能将化学能全部转化为电能,
故A错误;
B.原电池中电子由负极流经导线进入正极,即电子由锌片通过导线流向铜片,故B正确;
C.锌为负极,失电子发生氧化反应,故C错误;
D.铜做正极,铜离子在此极得电子,发生还原反应,电极反应式:Cu2++2e-=Cu,故D错误;
故选B。
11.已知空气—锌电池的电极反应为:锌片:Zn+2OH--2e-=ZnO+H O;碳棒: O+H O+2e- =2OH- ,据此
2 2 2
判断,锌片是
A.负极,被氧化 B.正极,被氧化
C.负极,被还原 D.正极,被还原
【答案】A
【解析】
在空气—锌电池中锌片发生的反应为:Zn+2OH--2e-=ZnO+H O,则锌的化合价升高,发生氧化反应,原电
2
池中负极发生氧化反应,所以在空气—锌电池中锌为负极被氧化,故A正确,
故选A。
12.(2021·河南商丘·高一期末)金属镁和铝设计成如图所示的原电池。下列说法正确的是
A.铝作该原电池的负极 B.溶液中 向 极移动
C. 电极的电极反应式为 D.电流方向为 A
【答案】D
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司【解析】
根据原电池构成条件,Mg比Al活泼,因此Mg为负极,Al为正极,据此分析;
A.Mg比Al活泼,且Mg能与硫酸反应,因此Mg为负极,Al为正极,故A错误;
B.根据原电池工作原理,阴离子向负极移动,阳离子向正极移动,即 向Mg极移动,故B错误;
C.根据上述分析,Mg为负极,电极反应式为Mg-2e-=Mg2+,故C错误;
D.电流方向是正电荷定向移动方向,从正极流出,因此电流方向是Al→A→Mg,故D正确;
答案为D。
13.(2021·全国·高一课时练习)将铜片和锌片用导线和电流计连接后,浸入一定浓度的稀硫酸中,如图
所示,下面有关说法正确的是
A.Zn是正极,Cu是负极
B.电子从Cu片经导线流向Zn片
C.Zn极有铜析出
D.Cu极上有气泡产生
【答案】D
【解析】
A.将铜片和锌片用导线和电流计连接后,浸入一定浓度的稀硫酸中构成原电池,由于金属性Zn>Cu,则
Zn是负极,Cu是正极,A错误;
B.Zn是负极,Cu是正极,电子从Zn片经导线流向Cu片,B错误;
C.Zn是负极,Zn溶解,没有铜析出,C错误;
D.Cu是正极,正极上氢离子放电,则Cu极上有气泡产生,D正确;
答案选D。
14.(2021·江苏省前黄高级中学高一期末)某新能源汽车电池中含有LiFePO ,放电过程中,LiFePO 转
4 4
化为FePO ,下列说法正确的是
4
A.LiFePO 中P为+5价,则Fe为+3价
4
B.该过程铁元素被还原
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司C.该过程得到电子
D.将FePO 溶于稀硫酸后,可以用硫氰化钾溶液检验其中所含的铁元素
4
【答案】D
【解析】
A.磷酸根离子中P为+5价,故LiFePO 中P为+5价,Li为+1价,则Fe为+2价,A错误;
4
B.LiFePO 转化为FePO ,Fe由+2价转化为+3价,化合价升高,被氧化,B错误;
4 4
C.LiFePO 转化为FePO ,Fe由+2价转化为+3价,化合价升高,被氧化,失电子,C错误;
4 4
D.将FePO 溶于稀硫酸得到硫酸铁和磷酸,硫酸铁完全电离得到Fe3+,故可以用硫氰化钾溶液检验其中所
4
含的铁元素,D正确;
15.(2021·河南·高一期末)18世纪末伏打用锌片与铜片夹以盐水浸湿的纸片叠成电堆产生了电流,制造
了最初的电池。某兴趣小组依据反应 探究原电池的工作原理,将质量相等的铁片
和碳棒用导线相连后浸入硫酸铜溶液中构成如图所示装置,当两电极质量相差 时,通过导线转移的电
子的物质的量为
A. B. C. D.
【答案】B
【解析】
根据总反应式为Fe+Cu2+═Fe2++Cu,负极铁逐渐溶解,Fe-2e-=Fe2+,正极逐渐析出铜,Cu2++2e-=Cu,结合两
电极质量差分析计算。
总反应式为Fe+Cu2+═Fe2++Cu,一段时间后,两电极质量相差18g,负极铁逐渐溶解,正极逐渐析出铜,若
转移2mol电子,两极质量差为56g+64g=120g,则两电极质量相差18g时,通过导线转移的电子的物质的
量为 ×2mol=0.3mol,故选B。
二、非选择题
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司16.原电池是一种可将___________直接转化为___________的装置,其中发生的化学反应属于
___________。原电池的必要组成部分有___________。
【答案】 化学能 电能 氧化还原反应 两个活泼性不同的电极、电解质溶液和形成闭合
回路
【解析】
原电池是一种将化学能直接转化为电能的装置,原电池反应中存在电子转移,则化学反应属于氧化还原反
应;原电池的必要组成部分有两个活泼性不同的电极、电解质溶液和形成闭合回路。
17.为了验证a、b、c三种金属的活动性顺序进行如下实验:①将金属片a、b插入稀硫酸中,用导线将它
们与电流表相连,发现a是负极;②用金属片b、c替换a、b后重复上述实验,发现c是正极。则a、b、c
三种金属的活动性由强到弱的顺序为___________。
【答案】a>b>c
【解析】
原电池中金属活动性较强的金属作原电池负极,不活泼金属做正极。
将金属片a、b插入稀硫酸中,用导线将它们与电流表相连,发现a是负极,则a的金属性强于b;用金属
片b、c替换a、b后重复上述实验,发现c是正极,则b的金属性强于c,所以a、b、c三种金属的活动性
由强到弱的顺序为a>b>c,故答案为:a>b>c。
18.写出下列原电池的电极反应和总反应(属于离子反应的,用离子方程式表示)。
负极 正极 电解质溶液
(1) 铁 铜 稀硫酸
(2) 铜 银 AgNO 溶液
3
(1)负极:___________;正极:___________;总反应式:___________。
(2)负极:___________;正极:___________;总反应式:___________。
【答案】
(1) Fe-2e-=Fe2+ 2H++2e-=H ↑ Fe+2H+=Fe2++H↑
2 2
(2) Cu-2e-=Cu2+ 2Ag++2e-=2Ag Cu+2Ag+=Cu2++2Ag
【解析】
(1)金属性铁强于铜,构成的原电池中铁是负极,反应是为Fe-2e-=Fe2+,铜是正极,溶液中的氢离子放电,
电极反应式为2H++2e-=H ↑,总反应是为Fe+2H+=Fe2++H↑。
2 2
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司(2)金属性铜强于银,构成的原电池中铜是负极,反应是为Cu-2e-=Cu2+,银是正极,溶液中的银离子放电,
反应是为2Ag++2e-=2Ag,因此总反应式为Cu+2Ag+=Cu2++2Ag。
19.(2021·云南·玉溪第二中学高一期中)以Zn、Cu为两电极,稀硫酸为电解质溶液的原电池。
(1)原电池:化学能能转化为___________能的装置。
(2)正负电极的判断:负极___________电子,发生___________反应,一般为活泼___________;
(3)正极___________电子,发生___________反应,一般为不活泼_______或非金属单质;
(4)电子流向___________,电流流向___________。
(5)电极反应式及总反应式的书写:负极___________;正极___________;
【答案】(1)电
(2) 失去 氧化 金属
(3) 得到 还原 金属
(4) 由负极流向正极 由正极流向负极
(5) Zn-2e-=Zn2+ 2H++2e- =H ↑
2
【解析】
(1)原电池是将化学能能转化为电能的装置;
(2)负极失去电子,发生氧化反应,一般为活泼金属;
(3)正极得到电子,发生还原反应,一般为不活泼金属或非金属单质;
(4)电子负极流向正极,电流由正极流向负极;
(5)该原电池负极的电极反应式为Zn-2e-=Zn2+;正极的电极反应式为2H++2e- =H ↑。
2
20.(2021·山东聊城·高一期末)探究原电池原理并应用原电池原理制作多种电池,对现实生活具有重要
的意义。
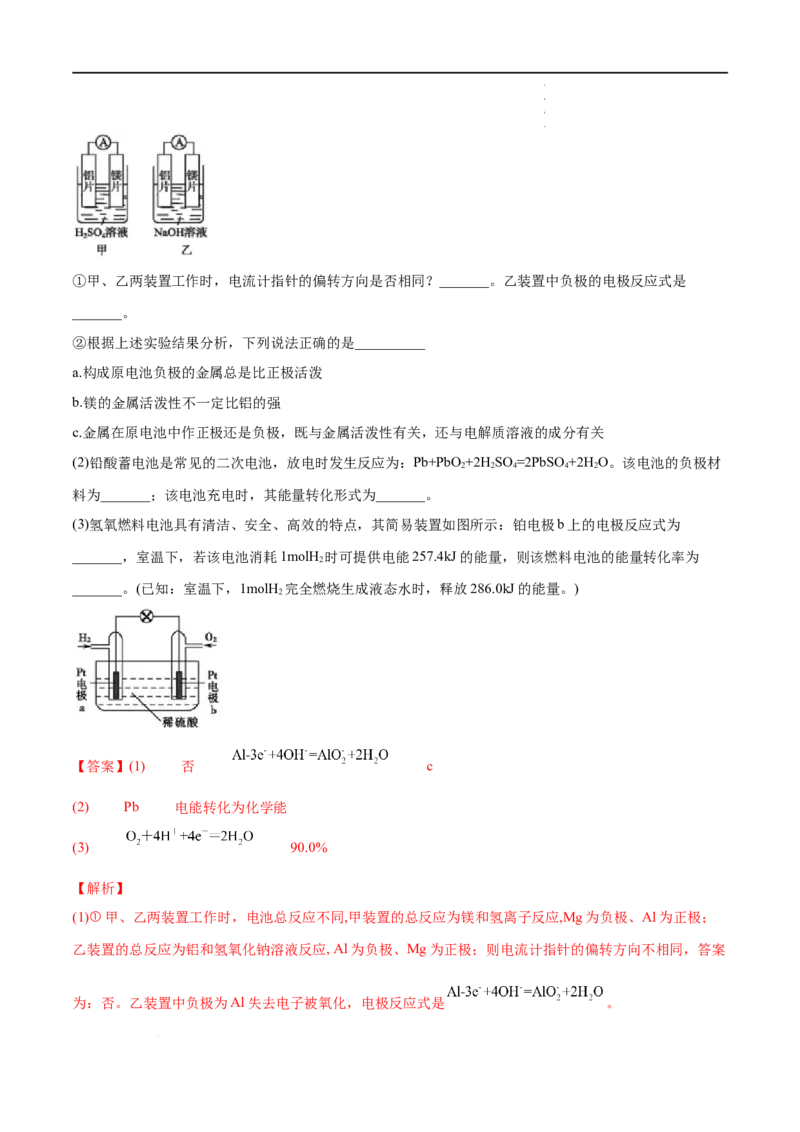
(1)某化学兴趣小组为了探究铝电极在原电池中的作用时,设计了如下实验:
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司①甲、乙两装置工作时,电流计指针的偏转方向是否相同?_______。乙装置中负极的电极反应式是
_______。
②根据上述实验结果分析,下列说法正确的是__________
a.构成原电池负极的金属总是比正极活泼
b.镁的金属活泼性不一定比铝的强
c.金属在原电池中作正极还是负极,既与金属活泼性有关,还与电解质溶液的成分有关
(2)铅酸蓄电池是常见的二次电池,放电时发生反应为:Pb+PbO+2H SO =2PbSO+2H O。该电池的负极材
2 2 4 4 2
料为_______;该电池充电时,其能量转化形式为_______。
(3)氢氧燃料电池具有清洁、安全、高效的特点,其简易装置如图所示:铂电极b上的电极反应式为
_______,室温下,若该电池消耗1molH 时可提供电能257.4kJ的能量,则该燃料电池的能量转化率为
2
_______。(已知:室温下,1molH 完全燃烧生成液态水时,释放286.0kJ的能量。)
2
【答案】(1) 否 c
(2) Pb 电能转化为化学能
(3) 90.0%
【解析】
(1)①甲、乙两装置工作时,电池总反应不同,甲装置的总反应为镁和氢离子反应,Mg为负极、Al为正极;
乙装置的总反应为铝和氢氧化钠溶液反应, Al为负极、Mg为正极;则电流计指针的偏转方向不相同,答案
为:否。乙装置中负极为Al失去电子被氧化,电极反应式是 。
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司②a.原电池工作时发生氧化还原反应,负极上发生氧化反应,而构成原电池负极的金属不一定比正极活泼,
因为反应电极跟电解质的性质有关,a错误;
b.镁的金属活泼性一定比铝的强,但镁不一定作原电池的负极,b错误;
c.由①可知,金属在原电池中作正极还是负极,既与金属活泼性有关,还与电解质溶液的成分有关,c正
确;
则说法正确的是c。
(2)原电池工作时,还原剂在负极上发生氧化反应。已知铅酸蓄电池放电时发生反应为:
Pb+PbO+2H SO =2PbSO+2H O。则该电池的负极材料为Pb;该电池充电时,为电解池,其能量转化形式
2 2 4 4 2
为电能转化为化学能。
(3)在图示的氢氧酸式燃料电池中,铂电极b为正极,b上氧气得电子被还原,电极反应式为
,已知:室温下,1molH 完全燃烧生成液态水时,释放286.0kJ的能量。室温下,若
2
该电池消耗1molH 时可提供电能257.4kJ的能量,则该燃料电池的能量转化率为 。
2
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司