文档内容
2024 年广州市普通高中毕业班冲刺训练题(一)
化学
本试卷共8页,20小题,满分100分。考试用时75分钟。
可能用到的相对原子质量: H 1 C 12 N 14 O 16
一、单项选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。
每小题只有一个选项符合题意。
1. 文房四宝是中国独有的书法绘画工具。下列文房四宝中主要由硅酸盐材料组成的是
A.湖州的“湖笔” B.黄山的“徽墨” C.宣城的“宣纸” D.肇庆的“端砚”
2. 从科技前沿到人类的日常生活,化学无处不在。下列说法不正确的是
A.国产大型飞机C919用到的氮化硅陶瓷是新型无机非金属材料
B.光化学烟雾、臭氧层空洞、白色污染的形成都与氮氧化合物有关
C.漂粉精既可作棉麻织物漂白剂,又可用作环境的消毒剂
D.粒子直径为1nm~100nm的铁粉材料,不属于胶体
3. 化学在科技强国中发挥着重要作用。下列有关叙述正确的是
A.铝合金中硬铝密度小,强度高,常用于制造飞机外壳
B.二氧化硅广泛用于航天器太阳能电池板
C.液氧甲烷运载火箭中的甲烷是烃的衍生物
D.医用无纺布防护服中常用聚乙烯作原料,聚乙烯属于天然纤维
4. 下列化学用语表示正确的是
A.溴的简化电子排布式:
化学试题 第 1 页 (共 11 页)
A r 4 s 2 4 p 5
B.1-丁醇的键线式:
C.反-2-丁烯分子的球棍模型:
D.水的VSEPR模型:5. 下列有关反应的离子方程式正确的是
A.食醋和84消毒液混合:Cl- + ClO- + 2H+ = Cl ↑+ H O
2 2
B.用惰性电极电解饱和
化学试题 第 2 页 (共 11 页)
M g C l 2 溶液: 2 C l - + 2 H
2
O
通 电
C l
2
+ H
2
+ 2 O H -
C. C u S O
4
溶液中加入过量浓氨水: C u 2 + + 2 N H
3
H
2
O = C u ( O H )
2
+ 2 N H +4
D.向Ba(HCO ) 溶液中滴入
3 2
N a H S O
4
溶液使 B a 2 + 恰好完全沉淀:
B a 2 + + H C O −3 + H + + S O 24 − = B a S O
4
+ C O
2
+ H
2
O
6. 下列叙述Ⅰ和叙述Ⅱ均正确,且有因果关系的是
选项 叙述Ⅰ 叙述Ⅱ
A 石墨能导电且化学性质不活泼 阴极电保护法中可用石墨作辅助阳极
B 煤中含有苯、甲苯等芳香烃 通过煤的干馏可获得苯、甲苯等芳香烃
C 医护人员利用酒精消毒 乙醇具有强氧化性
D 断裂氨分子中的化学键需要吸收热量 工业上用液氨作制冷剂
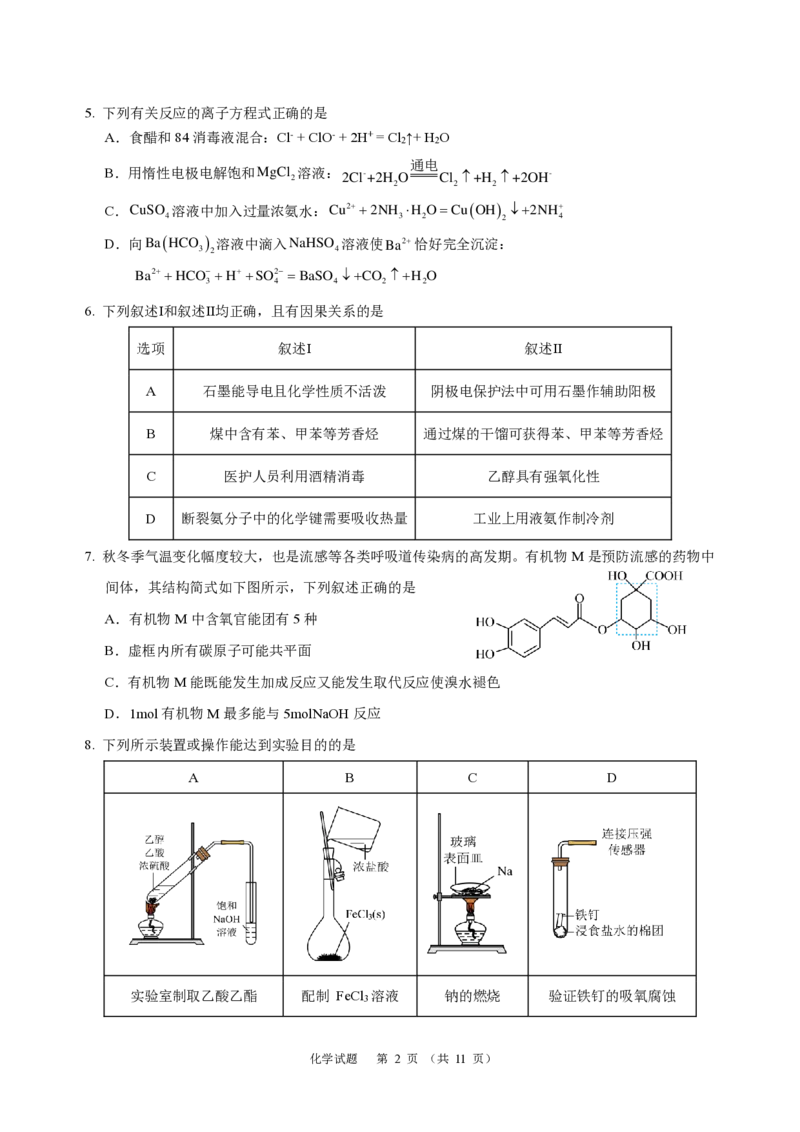
7. 秋冬季气温变化幅度较大,也是流感等各类呼吸道传染病的高发期。有机物M是预防流感的药物中
间体,其结构简式如下图所示,下列叙述正确的是
A.有机物M中含氧官能团有5种
B.虚框内所有碳原子可能共平面
C.有机物M能既能发生加成反应又能发生取代反应使溴水褪色
D.1mol有机物M最多能与5molNaOH反应
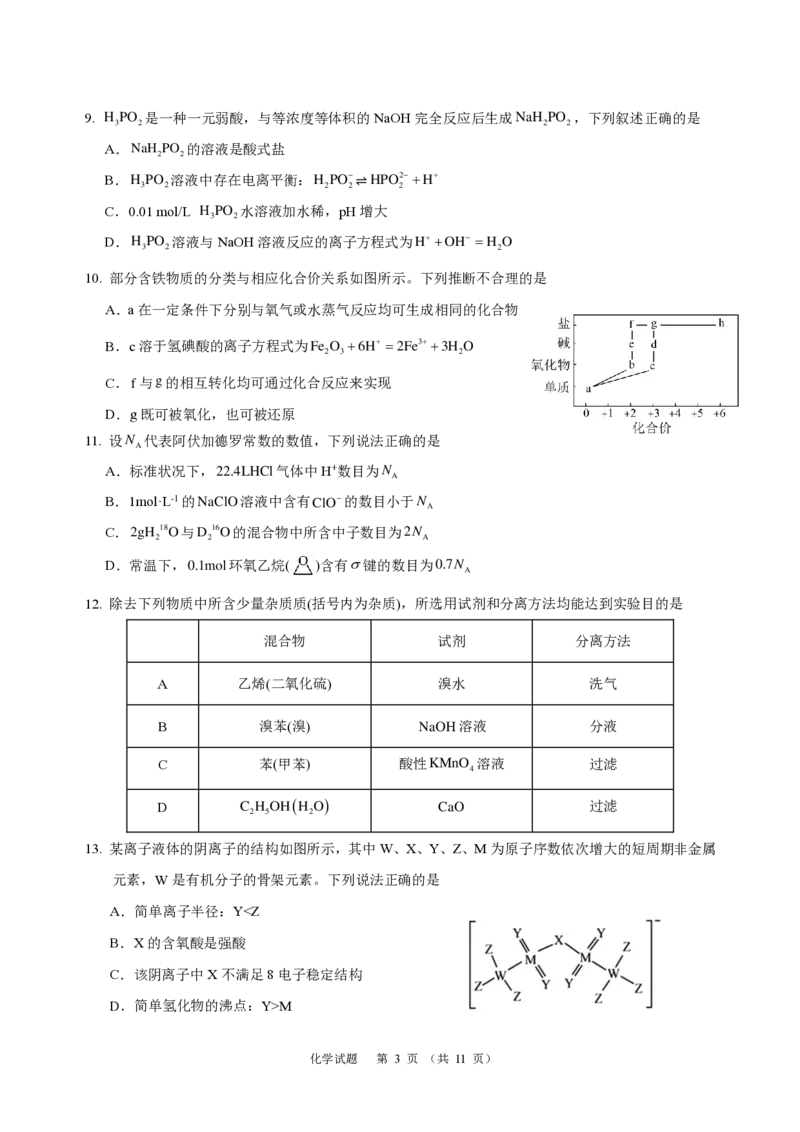
8. 下列所示装置或操作能达到实验目的的是
A B C D
实验室制取乙酸乙酯 配制 FeCl 溶液 钠的燃烧 验证铁钉的吸氧腐蚀
39.
化学试题 第 3 页 (共 11 页)
H
3
P O
2
是一种一元弱酸,与等浓度等体积的NaOH完全反应后生成 N a H
2
P O
2
,下列叙述正确的是
A. N a H
2
P O
2
的溶液是酸式盐
B. H
3
P O
2
溶液中存在电离平衡:HHPPOO−−⇌HHPPOO2−2−++HH+ +
22 22 22
C.0.01 mol/L H PO 水溶液加水稀,pH增大
3 2
D. H
3
P O
2
溶液与NaOH溶液反应的离子方程式为 H + + O H − = H
2
O
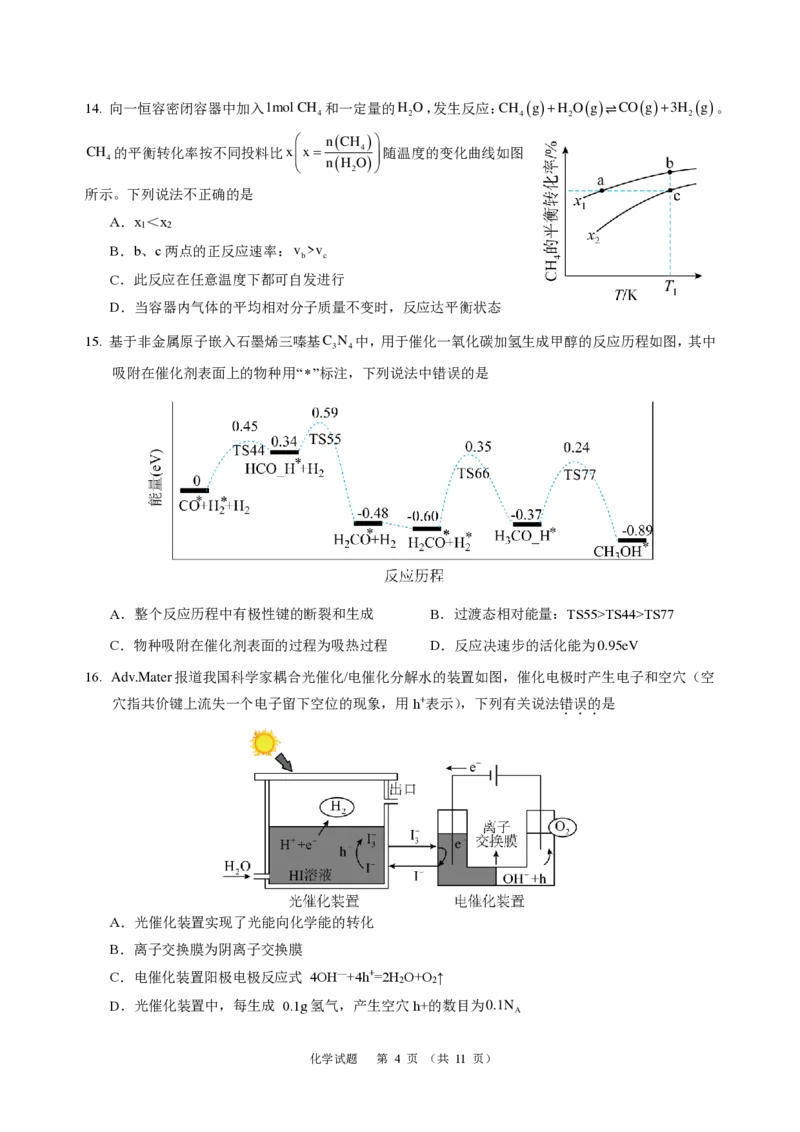
10. 部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是
A.a在一定条件下分别与氧气或水蒸气反应均可生成相同的化合物
B.c溶于氢碘酸的离子方程式为 F e
2
O
3
+ 6 H + = 2 F e 3 + + 3 H
2
O
C. f 与 g 的相互转化均可通过化合反应来实现
D.g既可被氧化,也可被还原
11. 设 N
A
代表阿伏加德罗常数的数值,下列说法正确的是
A.标准状况下, 2 2 .4 L H C l 气体中H+数目为N
A
B.1mol·L-1的 N a C lO 溶液中含有 C lO − 的数目小于 N
A
C. 2 g H 12 8 O 与 D 12 6 O 的混合物中所含中子数目为 2 N
A
D.常温下, 0 .1 m o l 环氧乙烷( )含有键的数目为 0 .7 N
A
12. 除去下列物质中所含少量杂质质(括号内为杂质),所选用试剂和分离方法均能达到实验目的是
混合物 试剂 分离方法
A 乙烯(二氧化硫) 溴水 洗气
B 溴苯(溴) N a O H 溶液 分液
C 苯(甲苯) 酸性 K M n O
4
溶液 过滤
D C
2
H
5
O H ( H
2
O ) CaO 过滤
13. 某离子液体的阴离子的结构如图所示,其中W、X、Y、Z、M为原子序数依次增大的短周期非金属
元素,W是有机分子的骨架元素。下列说法正确的是
A.简单离子半径:YM14. 向一恒容密闭容器中加入
化学试题 第 4 页 (共 11 页)
1 m o l C H
4
和一定量的 H
2
O ,发生反应: C H
4
( g ) + H
2
O ( g ) C O ( g ) + 3 H
2
( g ) ⇌ C H
4
( g ) + H
2
O ( g ) C O ( g ) + 3 H
2
( g ) 。
C H
4
的平衡转化率按不同投料比 x
x =
n
n
(( C
H
H
2
O
4
))
随温度的变化曲线如图
所示。下列说法不正确的是
A.x <x
1 2
B.b、c两点的正反应速率: v
b
> v
c
C.此反应在任意温度下都可自发进行
D.当容器内气体的平均相对分子质量不变时,反应达平衡状态
15. 基于非金属原子嵌入石墨烯三嗪基 C
3
N
4
中,用于催化一氧化碳加氢生成甲醇的反应历程如图,其中
吸附在催化剂表面上的物种用“”标注,下列说法中错误的是
A.整个反应历程中有极性键的断裂和生成 B.过渡态相对能量:TS55>TS44>TS77
C.物种吸附在催化剂表面的过程为吸热过程 D.反应决速步的活化能为 0 .9 5 e V
16. A d v .M a te r 报道我国科学家耦合光催化/电催化分解水的装置如图,催化电极时产生电子和空穴(空
穴指共价键上流失一个电子留下空位的现象,用h+表示),下列有关说法错误的是
...
A.光催化装置实现了光能向化学能的转化
B.离子交换膜为阴离子交换膜
C.电催化装置阳极电极反应式 4OH—+4h+=2H O+O ↑
2 2
D.光催化装置中,每生成 0.1g氢气,产生空穴h+的数目为0.1N
A二、非选择题:56分。
17. (14分)某小组研究Cu与浓硝酸反应时发现如下现象:
装置与试剂 现象
Cu片完全溶解,反应放热,产生红棕色气体,得到绿色
溶液A,该溶液长时间放置后得到蓝色溶液B。反应后溶
液体积几乎不变。
(1)Cu与浓硝酸反应的离子方程式为 。
(2)甲同学猜测溶液A不是蓝色而呈绿色与溶解了NO 有关,于是向溶液B中通入NO ,然后再持续
2 2
通入一段时间N ,观察到现象: ,
2
证实猜测合理。
甲同学为深入研究溶液A呈绿色的原因,查得如下资料并提出了新的假设:
资料i:NO 溶于水部分发生歧化反应:2NO +H O⇌HNO +HNO
2 2 2 2 3
资料ii:NO
化学试题 第 5 页 (共 11 页)
−2 能与Cu2+络合:Cu2+(蓝色)+4NO −2 ⇌Cu(NO )
2
24 − (绿色)
资料iii:HNO 是弱酸,加热或遇强酸发生分解3HNO =HNO +2NO↑+H O
2 2 3 2
假设一:A中形成了Cu(NO )
2
24 − 使溶液呈绿色。
为了验证假设一的合理性,甲同学进行了如下实验:
【实验一】
操作 现象
①向20.0mL0.5mol·L-1Cu(NO ) 蓝色溶液中通入少量NO 气体 溶液呈绿色
3 2 2
②向20.0mL水中通入与①中等量的NO 气体 溶液呈无色
2
(3)操作②的目的是 。
(4)乙同学向①所得溶液中滴加浓硫酸,使溶液中c(H+)达约8mol·L-1,观察到有无色气体放出(遇空
气变为红棕色),溶液很快变回蓝色。利用平衡移动原理解释溶液变蓝的原因: 。
(5)综合甲乙两位同学的实验,假设一不成立。请说明理由: 。
乙同学查得如下资料并提出来另一种假设:
资料iv:浓硝酸中溶有NO 时呈黄色;水或稀硝酸中通入少量NO 时呈无色
2 2
假设二:A中浓硝酸溶解了NO 所得黄色溶液与Cu2+的蓝色复合形成的绿色。
2
为验证假设二的合理性,乙同学进行了如下实验:【实验二】
操作 现象
①配制与溶液A等pH的HNO 溶液,取20.0mL,通入NO 气体 溶液呈黄色
3 2
②加入 溶液变为绿色
③ 溶液立即变回蓝色
(6)操作②中加入的试剂为 ,操作③进一步证明了假设二的合理性,写出该操
作: 。溶液变回蓝色可能的原因是 (用
化学方程式表示)。
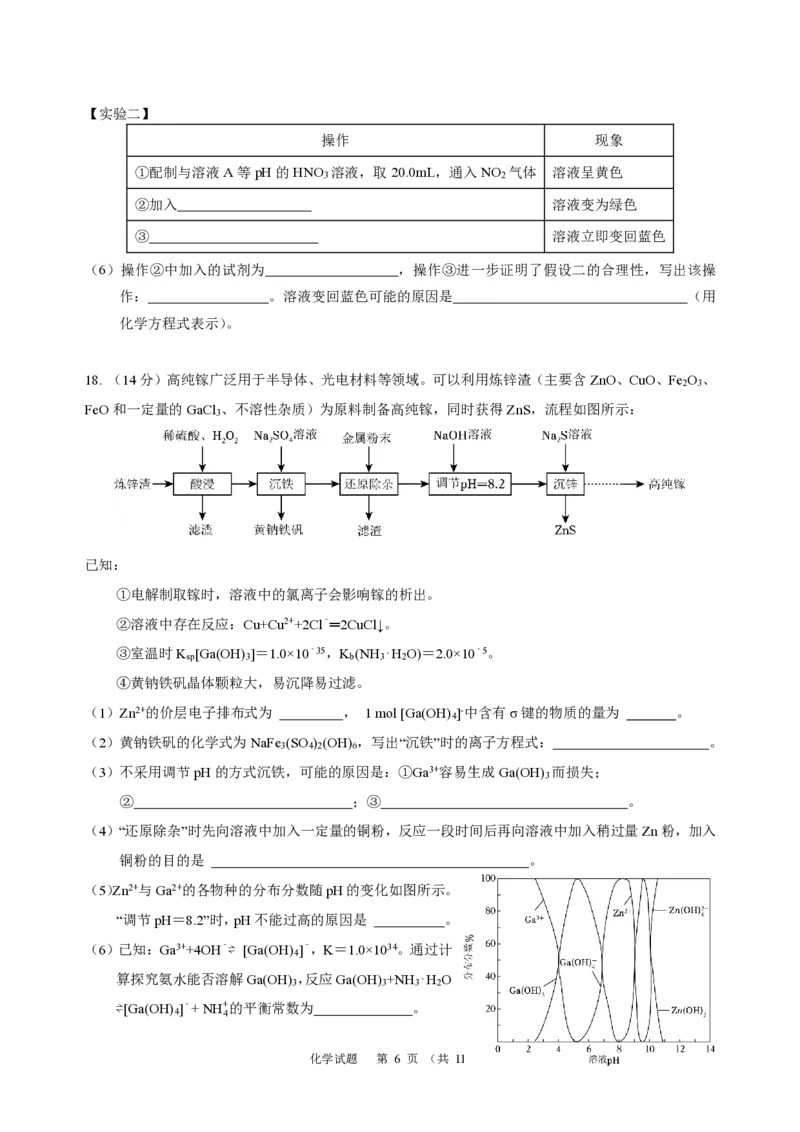
18. (14分)高纯镓广泛用于半导体、光电材料等领域。可以利用炼锌渣(主要含ZnO、CuO、Fe O 、
2 3
FeO和一定量的GaCl 、不溶性杂质)为原料制备高纯镓,同时获得ZnS,流程如图所示:
3
已知:
①电解制取镓时,溶液中的氯离子会影响镓的析出。
②溶液中存在反应:Cu+Cu2++2Cl﹣═2CuCl↓。
③室温时K [Ga(OH) ]=1.0×10﹣35,K (NH ⋅H O)=2.0×10﹣5。
sp 3 b 3 2
④黄钠铁矾晶体颗粒大,易沉降易过滤。
(1)Zn2+的价层电子排布式为 , 1 mol [Ga(OH) ]-中含有σ键的物质的量为 。
4
(2)黄钠铁矾的化学式为NaFe (SO ) (OH) ,写出“沉铁”时的离子方程式: 。
3 4 2 6
(3)不采用调节pH的方式沉铁,可能的原因是:①Ga3+容易生成Ga(OH) 而损失;
3
② ;③ 。
(4)“还原除杂”时先向溶液中加入一定量的铜粉,反应一段时间后再向溶液中加入稍过量Zn粉,加入
铜粉的目的是 。
(5)Zn2+与Ga2+的各物种的分布分数随pH的变化如图所示。
“调节pH=8.2”时,pH不能过高的原因是 。
(6)已知:Ga3++4OH﹣⇌ [Ga(OH) ]﹣,K=1.0×1034。通过计
4
算探究氨水能否溶解Ga(OH) ,反应Ga(OH) +NH ⋅H O
3 3 3 2
⇌[Ga(OH) ]﹣+ NH+的平衡常数为 。
4 4
化学试题 第 6 页 (共 11 页)(7)在沉铁前可以加入铁氰化钾检验 Fe2+是否被完全氧化,若有 Fe2+则会
观察到蓝色沉淀。该蓝色沉淀是一种铁的配合物KFe [Fe (CN) ](其摩尔质
6
量为M g⋅mol﹣1),其晶胞的 1 如下图[K+未标出,占据四个互不相邻的小立方
8
体(晶胞的 1 部分)的体心]。若该晶体的密度为ρ g⋅cm﹣3,则Fe3+和Fe2+的
8
最短距离为 cm(设N 为阿伏加德罗常数的值)。
A
19.(14分)CO 转化成可利用的化学能源的“负碳”研究对解决环境、能源问题意义重大。
2
以CO 、H 为原料合成CH OH涉及的反应如下:
2 2 3
反应i:CO (g) + 3H (g) ⇌ CH OH(g) + H O(g) △H
2 2 3 2 1
反应ii:CO (g) + H (g) ⇌ CO(g) + H O(g) △H = +41.2 kJ·mol-1
2 2 2 2
反应iii:CO(g) + 2H (g) ⇌ CH OH(g) △H = -90.0 kJ·mol-1
2 3 3
(1)计算反应i的△H = 。
1
(2)关于反应i、ⅱ、iii的说法正确的是 。
a.升高温度能使反应i的反应速率增大,平衡常数增大
b.当甲醇的分压不再改变时,体系达到平衡
c.低温、高压有利于CO 催化加氢制取CH OH
2 3
d. 在恒压密闭容器中充入Ar,反应ⅱ速率不变
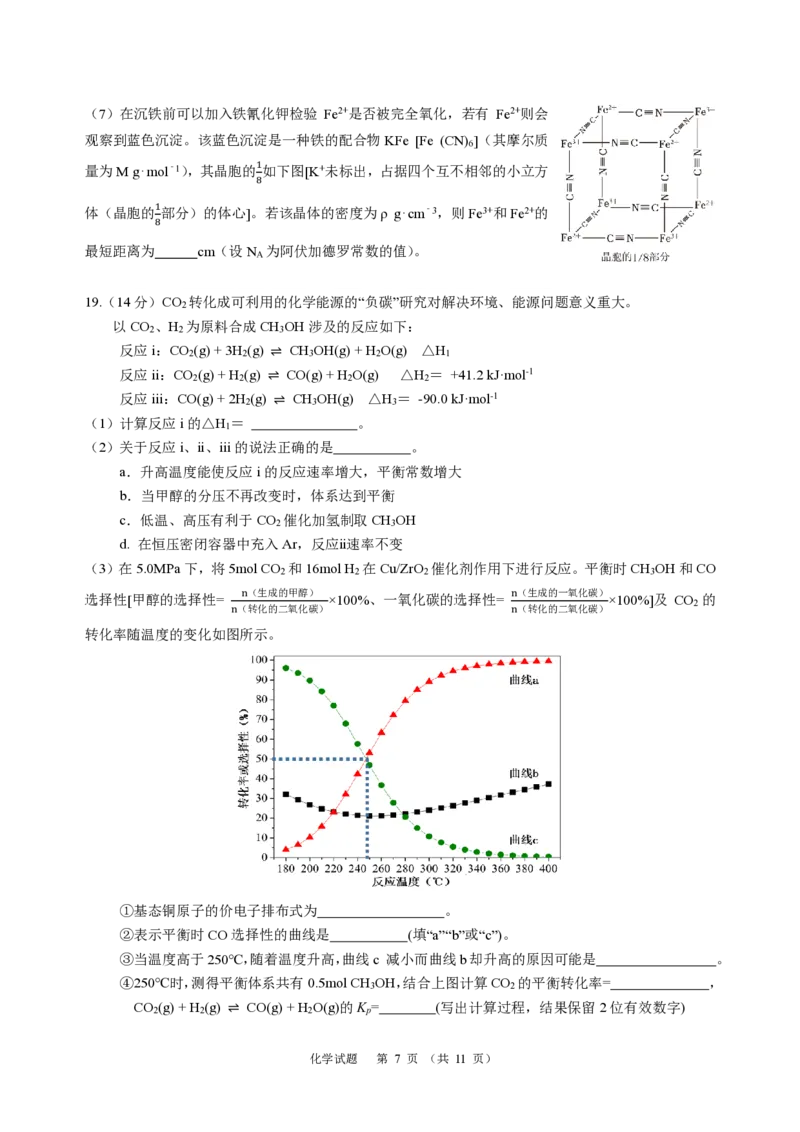
(3)在5.0MPa下,将5mol CO 和16mol H 在Cu/ZrO 催化剂作用下进行反应。平衡时CH OH和CO
2 2 2 3
n(生成的甲醇) n(生成的一氧化碳)
选择性[甲醇的选择性= ×100%、一氧化碳的选择性= ×100%]及 CO 的
2
n(转化的二氧化碳) n(转化的二氧化碳)
转化率随温度的变化如图所示。
①基态铜原子的价电子排布式为 。
②表示平衡时CO选择性的曲线是 (填“a”“b”或“c”)。
③当温度高于250℃,随着温度升高,曲线c 减小而曲线b却升高的原因可能是 。
④250℃时,测得平衡体系共有0.5mol CH OH,结合上图计算CO 的平衡转化率= ,
3 2
CO (g) + H (g) ⇌ CO(g) + H O(g)的K = (写出计算过程,结果保留2位有效数字)
2 2 2 p
化学试题 第 7 页 (共 11 页)O O
20.(14 分) (1,3-环己二酮)常用作医药中间体,用于有机合成。如作为除草剂磺草酮、硝
磺酮的中间体。下列是合成1,3-环己二酮一种方法。
Br OHC
O O
[1] C 6 H 10 3 O O CHSCH CrO 3 O COOH
CH 3 CH 3 3 CH 3 [2] H 3 C
甲 3 乙 [3]
O
HSO CHCHOH
2 4 3 2
HO OH O O [4]
LiAlH 4 丙
CHONa
HO 2 5
2 CHCOOH
3
回答下列问题:
(1)写出甲的分子式 ,乙中含有的还原性官能团的名称是 。
(2) 的沸点
化学试题 第 8 页 (共 11 页)
O O
的沸点(填“高于”,“低于”,“等于”或者“不确定”)。
(3)反应[3]是在浓硫酸催化作用下,和乙醇共加热制备丙,写出丙的结构简式 。
(4)反应[1]的产物C H 的系统名称为1-甲基环戊烯,请写出该反应的化学方程式: 。
6 10
(5)1,3—环己二醇( )具有多种化学性质,请按照要求填写下表
序号 反应物和反应条件 产物的结构 反应类型
1 CuO,加热 _______________ ____________
2 取代反应
_______________
(6)
O O
的同分异构体较多,一部分同分异构满足下列条件
① 核磁共振氢谱有二种吸收峰
② 在加热条件下和新制氢氧化铜反应生成砖红色沉淀
③ 链状脂肪化合物
请写出符合上述条件的同分异构体的结构简式 (写出一种即可)。
O OH OH
(7)根据上述设计方法,以H 3 C CH 3(丙酮)、乙醇、乙酸制备H 3 C CH 3(2,4-戊二醇)
条件 条件
设计反应流程如下: A B C。
O H
O H
O H
O H
B r
B r2024 年广州市普通高中毕业班冲刺训练题(一)
化学 参考答案
一、单项选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。
1 2 3 4 5 6 7 8
D B A D D A C D
9 10 11 12 13 14 15 16
C B D B D C C B
17. (14分)
(1)Cu+4H++2
化学试题 第 9 页 (共 11 页)
N O -3 =Cu2++2H O+2NO ↑ (2分)
2 2
(2)通入NO 后溶液呈绿色,通入一段N 后变蓝 (2分)
2 2
(3)证明NO 溶于水时没有颜色变化,排除这一因素在①中的干扰 (2分)
2
(4)加入浓硫酸后,温度升高且c(H+)增大,HNO 分解导致c(HNO )下降,均引起平衡HNO
2 2 2
N O -2
+H+逆向移动,c( N O -2 )下降,Cu2+(蓝色)+4 N O -2 ⇌Cu(NO )
2
24 − (绿色)逆向移动,溶液颜色由绿色变为蓝色
(2分)
(5)加酸且升温后,溶液变为蓝色,说明酸性较强的热溶液A中 N O -2 不能大量存在,因此Cu(NO )2−
2 4
也不能大量存在,不是溶液A呈绿色的主要原因 (2分)
(6)0.01molCu(NO ) (1分) 加水稀释 (1分) 3NO +H O=2HNO +NO (2分)
3 2 2 2 3
18. (14分)(1)3d10 (1分); 8mol (1分);
(2)3Fe3++2SO
4
2-+Na++6H2O=NaFe3(SO4)2(OH)6↓+6H+ (2分)
(3)②直接调pH沉铁易生成Fe(OH) 胶体,不容易过滤 (1分),③Fe(OH) 胶体同时容易吸附Zn2+
3 3
而造成ZnS损失 (1分)
(4)可除去Cl﹣,发生的反应为Cu+Cu2++2Cl﹣=2CuCl↓,CuCl难溶于水和稀酸,避免Cl﹣影响镓的析
出 (2分)
(5)当pH过高时,Zn2+将转化为Zn(OH)2 或Zn(OH)4 2﹣,Zn(OH)4 2﹣较稳定不利于ZnS生成,Zn(OH)2
直接沉淀,导致产品中的ZnS中混有Zn(OH)2 (2分)
(6)2.0×10﹣6 (2分)
(7)√ 3 M (2分)
2ρ𝑁𝐴19. (14分)
(1)-48.8 kJ·mol-1 (2分)
(2)bc (2分)
(3)①3d104s1 (1分) ②a (2分)
③生成甲醇的反应为放热反应,升温时平衡逆向移动,甲醇选择性降低;反应ⅱ是吸热反应,升温
平衡正向移动,且反应ⅱ占主导作用。 (2分)
④20% (2分)
250℃时,测得平衡体系共有 0.5molCH OH,结变化图可知,甲醇、一氧化碳选择性都为 50%,
3
即n (CH OH)=n (CO)=0.5mol
平 3 平
CO (g) + 3H (g) ⇌ CH OH(g) + H O(g)
2 2 3 2
n (mol) 5 16 0 0
o
△n(mol) 0.5 0.5 0.5 0.5
n (mol) 4 14 0.5 1
平
CO (g) + H (g) ⇌ CO(g) + H O(g)
2 2 2
n (mol) 5 16 0 0
o
△n(mol) 0.5 0.5 0.5 0.5
n (mol) 4 14 0.5 1
平
0.5×1
K = = 8.9×10-3 (3分)
p
4×14
20. (14分)
(1) C H O (1分) ,醛基 (1分)
6 10 3
(2) 高于 (1分)
O O
C H
2 5
H C O
(3) 3 (1分)
(4)
化学试题 第 10 页 (共 11 页)
C H
B
3
r
+ N a O H
C H2
5
O H
C H
+
3
N a B r + H
2
O
(2分)
(5)各1分,共3分
序号 反应物和反应条件 产物的结构 反应类型
1 氧化反应
2 浓氢溴酸,加热
O
OH C CH
3 3
(6)OHC CHO 或 (2分)
(7)
化学试题 第 11 页 (共 11 页)
C H
3
C O O H C
H
H
2
3
S
C
O
H
4
2 O H C H
3
C O O C H
2
C H
3
C 2 H 5
H
O
3
N
C
a
O
C
C
H
H
3
3
C O O H O O L iA
H
2
lH
O
4 O H O H
(3分)