文档内容
昆明一中 2024 届高三第 8 次联考
化学参考答案
7 8 9 10 11 12 13
D C A B B B D
7.【答案】D
【解析】葡萄酒中添加SO 的主要目的是杀菌和抗氧化,A项错误;食盐中添加KIO 的主要目的是补充
2 3
微量元素碘,B项错误;在钢铁制品表面喷涂油漆的主要目的是防止锈蚀,C项错误;生香蕉喷洒乙烯利
的主要目的就是利用释放出的乙烯催熟果实,D项正确。
8.【答案】C
【解析】甲中含酮羰基,不含醛基,不能用新制氢氧化铜检验甲是否反应完全,A项错误;乙中的饱和
碳原子结合的4个原子位于四面体的顶点,不可能全部共面,B项错误;甲与乙先发生加成反应生成
O O
OH
HN N
,再发生消去反应生成中间体丁 ,C项正确;1 mol丙与5
O O
*
* N
mol氢气反应的产物为 ,含手性碳原子(用*标注),D项错误。
O
9.【答案】A
【解析】FeI 溶液中滴加少量溴水,还原性较强的碘离子被氧化,A项符合题意;氯化银悬浊液中加入硫
2
化钠溶液,可发生沉淀转化,B项不符合题意;硝酸钡溶液中通入少量SO ,溶液呈酸性,硝酸根离子将
2
四价硫氧化为六价,生成硫酸钡沉淀,C项不符合题意;苏打水中滴加少量硫酸铝溶液,铝离子与碳酸根
离子互相促进水解,由于铝离子少量,碳酸根离子水解生成碳酸氢根离子,D项不符合题意。
10.【答案】B
【解析】焰色试验的载体为铂丝或光洁无锈的铁丝,铜灼烧时焰色呈现绿色,有干扰,不能用铜丝作焰
色试验的载体,A项不符合题意;探究SO是否被氧化变质,先用足量盐酸排除SO干扰,再用氯化钡溶
液检验是否存在SO,B项符合题意;探究SO是否具有氧化性,用具有还原性的硫离子,并且在酸性条
件下两者可发生氧化还原反应,在碱性条件下则不发生氧化还原反应,C项不符合题意;亚硫酸钾为强碱
弱酸盐,亚硫酸根离子水解使溶液呈碱性,由于甲基橙在弱酸性、中性及碱性条件下均呈现黄色,故不
能用甲基橙检测,D项不符合题意。
11.【答案】B
【解析】根据信息可推知W、X、Y、Z分别为氢、碳、氮、氧元素。碳、氮、氧的简单氢化物中,水最
稳定,A项错误;四种元素中氮的第一电离能最大,氧的电负性最大,B项正确;氢、碳、氮、氧四种元
素可形成碳酸铵等离子化合物,C项错误;该高分子结构中的苯环及五元环中双键、单键、双键的部分存
在大π键,D项错误。
12.【答案】B
【解析】原电池放电时,负极、正极分别发生氧化、还原反应,可推知放电时的总反应为2NiOOH+H AQ=
2
2Ni(OH) +AQ,放电时的反应自发,则 ΔG<0,A项错误;充电时,阴极发生还原反应,电极反应式为:
2
AQ+2H++2e−=HAQ,B项正确;正极的电势高于负极的电势,放电时,正极与负极的电势差会衰减,C
2
项错误;放电时,正极NiOOH→Ni(OH) ,质量增大,负极HAQ→AQ,质量减小,则正极与负极的质量
2 2
差(m -m )逐渐增大,D项错误。
正 负
1
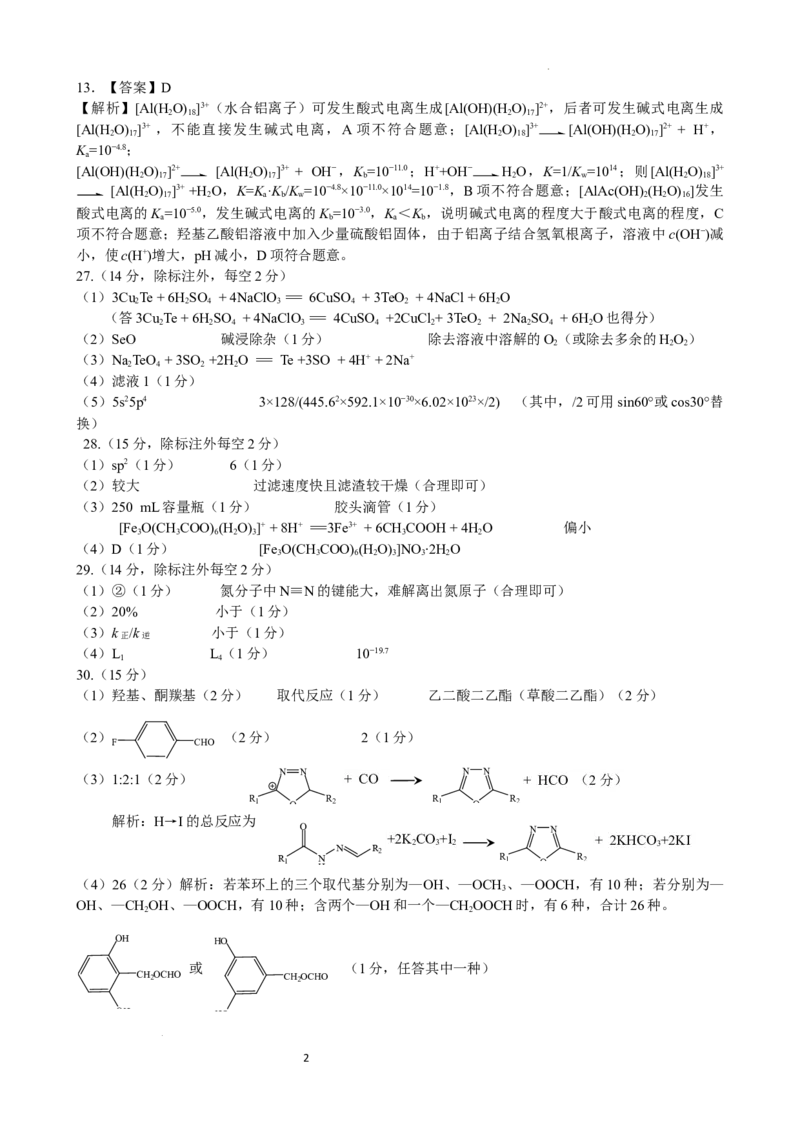
学科网(北京)股份有限公司13.【答案】D
【解析】[Al(H O) ]3+(水合铝离子)可发生酸式电离生成[Al(OH)(H O) ]2+,后者可发生碱式电离生成
2 18 2 17
[Al(H O) ]3+ ,不能直接发生碱式电离,A 项不符合题意;[Al(H O) ]3+ [Al(OH)(H O) ]2+ + H+,
2 17 2 18 2 17
K=10−4.8;
a
[Al(OH)(H O) ]2+ [Al(H O) ]3+ + OH−,K =10−11.0;H++OH− HO,K=1/K =1014;则[Al(H O) ]3+
2 17 2 17 b 2 w 2 18
[Al(H O) ]3+ +H O,K=K·K /K =10−4.8×10−11.0×1014=10−1.8,B项不符合题意;[AlAc(OH) (H O) ]发生
2 17 2 a b w 2 2 16
酸式电离的K=10−5.0,发生碱式电离的K =10−3.0,K<K ,说明碱式电离的程度大于酸式电离的程度,C
a b a b
项不符合题意;羟基乙酸铝溶液中加入少量硫酸铝固体,由于铝离子结合氢氧根离子,溶液中c(OH−)减
小,使c(H+)增大,pH减小,D项符合题意。
27.(14分,除标注外,每空2分)
(1)3Cu Te + 6HSO + 4NaClO = 6CuSO + 3TeO + 4NaCl + 6H O
2 2 4 3 4 2 2
(答3Cu Te + 6HSO + 4NaClO = 4CuSO +2CuCl+ 3TeO + 2NaSO + 6H O也得分)
2 2 4 3 4 2 2 2 4 2
(2)SeO 碱浸除杂(1分) 除去溶液中溶解的O(或除去多余的HO)
2 2 2
(3)NaTeO + 3SO +2H O = Te +3SO + 4H+ + 2Na+
2 4 2 2
(4)滤液1(1分)
(5)5s25p4 3×128/(445.62×592.1×10−30×6.02×1023×/2) (其中,/2可用sin60°或cos30°替
换)
28.(15分,除标注外每空2分)
(1)sp2(1分) 6(1分)
(2)较大 过滤速度快且滤渣较干燥(合理即可)
(3)250 mL容量瓶(1分) 胶头滴管(1分)
[Fe O(CH COO) (H O) ]+ + 8H+ =3Fe3+ + 6CHCOOH + 4H O 偏小
3 3 6 2 3 3 2
(4)D(1分) [Fe O(CH COO) (H O) ]NO ∙2HO
3 3 6 2 3 3 2
29.(14分,除标注外每空2分)
(1)②(1分) 氮分子中N≡N的键能大,难解离出氮原子(合理即可)
(2)20% 小于(1分)
(3)k /k 小于(1分)
正 逆
(4)L L(1分) 10−19.7
1 4
30.(15分)
(1)羟基、酮羰基(2分) 取代反应(1分) 乙二酸二乙酯(草酸二乙酯)(2分)
(2) (2分) 2(1分)
F CHO
(3)1:2:1(2分)
N N
+ CO
N N
+ HCO (2分)
R1
O
R2 R1
O
R2
解析:H→I的总反应为
O N N
+2KCO+I + 2KHCO +2KI
N R2 2 3 2 3
R1 N R1 O R2
H
(4)26(2分)解析:若苯环上的三个取代基分别为—OH、—OCH 、—OOCH,有10种;若分别为—
3
OH、—CHOH、—OOCH,有10种;含两个—OH和一个—CHOOCH时,有6种,合计26种。
2 2
OH HO
或 (1分,任答其中一种)
CH2OCHO CH2OCHO
OH HO
2
学科网(北京)股份有限公司